Vaskemidler og Kemikalier pĺ offentlige og private vaskerier
Miljř- og sundhedsvurdering
Bilag 4 Blegemidler
B.4.1 Natriumhypochlorit
B.4.2 Natriumdichloroisocyanurat
B.4.3 Peroxid
B.4.4 Hydrogenperoxid (brintoverilte)
B.4.5 Pereddikesyre
B.4.6 Eddikesyre
B.4.7 Diskussion
B.4.8 Konklusion
B.4.9 Referencer
Det har som tidligere omtalt ikke vćret projektets formĺl at gĺ i dybden med tensidernes eller de řvrige indholdsstoffers specifikke miljřmćssige egenskaber. Chlorblegemidlerne har imidlertid givet specielle problemer, da de med deres hřje toksicitet ikke har kunnet indplaceres i scoringsmodellen, idet konsekvensen ville vćre, at alle vaskerecepter, hvor chlor indgĺr, ville falde udenfor rammerne af de opstillede kriterier. Det ville umuliggřre den relative vurdering af de řvrige faktorer alene pĺ grund af et enkelt stof. De chlorbaserede blegemidler er derfor holdt udenfor scoringsmodelvurderingerne og i stedet peget ud, nĺr de indgik.
Chlorblegemidlerne indtager desuden en speciel status. Nogle vaskerier mener, at visse třjtyper krćver chlorblegning for at opnĺ et tilfredsstillende blegningsresultat (f.eks. restaurationstřj).
Graden af den opnĺelige blegeeffekt er afhćngig af en rćkke faktorer sĺsom hvilket blegemiddel, dets koncentration i procesvandet og třjets opholdstid i vaske- eller renseprocessen, vandets temperatur, typen af snavs samt typen af tekstil.
Chlorblegemidlerne har andre effekter i vaskeprocesserne end blegning, der gřr, at de lřser visse problemer, der ellers kunne opstĺ, idet de virker som desinfektionsmidler, der hćmmer/hindrer en uhensigtsmćssig opvćkst af mikroorganismer (f.eks. bakterier, mug), holder maskineriet rent, osv.
Blegemidler
De vigtigste oxidative blegemidler i industrien er
| Natriumhypochlorit | |
| Kaliumhypochlorit | |
| Kalciumhypochlorit | |
| Chlor | |
| Hydrogenperoxid og dets derivater (f.eks. pereddikesyre, natriumperborat) | |
| Ozon | |
| Nitrogendioxid |
Tekstilblegning
I Danmark er chlorblegemidler de mest anvendte. I Sverige er det primćrt hydrogenperoxid (brintoverilte) baserede midler.
Chlorblegemidler
Hypochlorit
I alkalisk medium omdannes hypochlorit blegemidler til den aktive hypochlorit anion:
HOCl + OH- « ClO- + H2O
Til blegning anvendes i vaskerierne normalt en vandig oplřsning af natriumhypochlorit (NaOCl) som hypochlorit kilde.
B.4.1 Natriumhypochlorit
Natriumhypochlorit ("klorbleg"), NaOCl, er det mest anvendte chlorblegemiddel. Den oxiderende effekt af et iltatom er ćkvivalent med effekten af to chloratomer. Natriumhypochlorit et letoplřseligt i vand med en vandoplřselighed pĺ 294 g/l ved 0oC. I vand omdannes natriumhypochlorit hurtigt til natriumchlorid og oxygen:
NaOCl ® NaCl + [O]
Natriumhypochlorit er ustabilt i vand ved tilstedevćrelse af organisk materiale. I kloakvand kan udvikles chloraminer, som giver en karakteristisk klorlugt (IUCLID).
Řkotoksicitet
Tabel B4-1
Toksicitet overfor vandlevende organismer (IUCLID, 1995).
Toxicity towards aquatic organisms (IUCLID, 1995).
| Organisme | Art | Effekt | mg/l | Bemćrkninger |
| Fisk | Pimephales promelas | EC50 , 96t | 0,22-0,62 | F, ferskvandsorg. |
| Alburnus alburnus | EC50 , 96 t | 32-37 | F, brakvand.7 0000 salt,8-12% Cl | |
| Dafnier | Ceriodaphnia sp. | EC50 , 24 t | 0,006 | som hypochlorit-ion |
| Daphnia magna* | EC50 , 24 t | 0,07-0,7 | 12.7% Cl2 oplřsning. | |
| Algae | Phaeodactylum tricornutum | NOEC, 72h | 0,2 | Static, ECETOC 56 |
| Dunaliella primolecta | EC50 ,72 t NOEC, 72 t |
0,4 0,1 |
Static, ECETOC 56 | |
| Pavlowa lutheri | NOEC, 72 t | 3,0 | Static, ECETOC 56 |
* Toksiciteten af omdannelsesprodukterne i samme oplřsning var for monochloramin 0,016 mg/l og for dichloramin 0,027 mg/l ogsĺ udtrykt som hypochlorit-ion.
Med den givne giftighed overfor vandlevende organismer vil en klassifikation af stoffet forventes at vćre: N; R50
B.4.2 Natriumdichloroisocyanurat
Organiske klorholdige midler som f.eks. natriumdichloroisocyanurat, som hydrolyseres til hypochlorit i alkalisk medium, anvendes ogsĺ til tekstilblegning i industrielle erhvervsvaskerier.
Natriumdichloroisocyanurat er et hypochlorit-baseret produkt, og det betyder, at der dannes hypochlorit, nĺr stoffet bringes i vandig oplřsning. Vandoplřseligheden er 250 g/l (IUCLID, 1995, Sax). Hypochlorit omdannes i vand hovedsagelig til natriumchlorid.
 |
Řkotoksicitet
Tabel B4-2
Řkotoksicitet for vandlevende organismer (IUCLID, 1995).
Ecotoxicity towards aquatic organisms (IULID, 1995).
| Organisme | Art | Effekt | mg/l | Bemćrkninger |
| Fisk | Salmo gairdneri | LC50 ,96 t | 0,13 | ferskvandsorg, IUCLID |
| Lepomis macrochirus | LC50 , 96 t | 0,28 0,46 |
ferskvandsorg, to referencer i IUCLID | |
| Dafnier | Daphnia magna | EC50 , 48 t | 0,28 | IUCLID |
| Alger | ingen resultater fundet |
Med den givne giftighed overfor vandlevende organismer vil en klassifikation af stoffet forventes at vćre: N; R50.
B.4.3 Peroxid
Peroxid baseret blegning sker primćrt med hydrogenperoxid (brintoverilte, H2O2), men ogsĺ andre peroxider kan/bliver anvendt, perborater, pereddikesyre, osv. Perborater anvendes normalt ikke i industrielle erhvervsvaskerier men kan indgĺ i husholdningsvaskemidler. Ved peroxid forstĺs forbindelser indeholdende to til hinanden bundne iltatomer (R- O- O- R), altsĺ derivater af hydrogenperoxid. Denne stoftype reprćsenterer et sćrligt oksidationstrin, hvor stofferne er meget reaktionsdygtige og reagerer som udprćgede oxidationsmidler.
B.4.4 Hydrogenperoxid (brintoverilte)
Hydrogenperoxid bliver i alkalisk medium omdannet til det aktive mellemstof: hydrogenperoxid-anion.
H2O2 + OH- Ű H2O + HO2-
Koncentrationen af det blegeaktive hydrogenperoxid anion řges med stigende pH og temperatur. Det vil sige, at til hydrogenperoxid blegning anvendes let til stćrkt alkaliske betingelser eventuelt ved tilsćtning af alkali (f.eks. natriummetasilikat) for at řge blegeeffekten. Natriumhydroxid er mindre anvendeligt, da det let giver for hřj pH og en ukontrolleret blegning.
Anvendes natriumhydroxid som alkalikilde fĺs reaktionen:
HOOH + OH- Ţ HOO- + H2O
Řkotoksiciteten er ikke omtalt, da stoffet er vurderet og indgĺr i DID-databasen (bilag 5).
B.4.5 Pereddikesyre
Organiske persyrer (R- CO- O- OH) som f.eks. pereddikesyre, CH3COOOH, har ogsĺ oxiderende egenskaber og kan anvendes som blegemiddel og desinfektionsmiddel. Da pereddikesyre er et kemisk reaktivt stof, kan det forventes at ville reagere med organisk materiale, metal-ioner og komplekser, der eksisterer i vandigt miljř. Organiske peroxysyrer anses for ustabile, og pereddikesyre forventes at hydrolyseres langsomt til eddikesyre og hydrogen peroxid:
CH3COOOH +H2O ® CH3COOH + H2O2
Pereddikesyre er dog ikke let bionedbrydeligt (inherent). Med en pKa pĺ 8.2 ved 25oC kan pereddieksyre eksistere i bĺde ioniseret og ikke-ioniseret form i vandmiljř, hvor procenten af ionisering afhćnger af pH med 50% ionisering ved pH 8.2. Log Kow er estimeret at vćre omkring -1, og derudfra kan Koc estimeres til ca. 7.5 for ikke ioniseret materiale det vil sige lav adsorption. Adsorptionen af ioniseret materiale kan ikke estimeres, men ville krćve et undersřgelse.
Řkotoksicitet
Tabel B4-3
Řkotoksicitetsdata.
Data on ecotoxocity.
| Organisme | Art | Effekt | mg/l | Bemćrkninger | |
| Fisk | Pleuronectes platessa | LC50 , 96 t | 89,1 | marin, mĺlt konc.* | |
| Salmo gairdneri | LC50 , 96 t | 13 | semistatisk, mĺlt konc.* | ||
| Dafnier | Daphnia magna | EC50 , 48 t | 3,3 | semistatisk, mĺlt konc.* | |
| Alger | ssp (flere arter) | EC50 , 72-96 t | 0,7-16 | ||
* 15% PAA, 15% H2O2, 25% HOAc
B.4.6 Eddikesyre
Eddikesyre anvendes ikke som blegemiddel, men er omtalt som nedbrydningsprodukt af pereddikesyre. Eddikesyre er let bionedbrydeligt, og giftigheden overfor vandlevende organismer er vćsentlig lavere end for pereddikesyre.
Řkotoksicitet
Tabel B4-4
Řkotoksicitet for vandlevende organismer (IUCLID 1995, Nikunen).
Ecotoxicty for aquatic organisms (IULID, 1995, Nikunen).
| Organisme | Art | Effekt | mg/l | Bemćrkninger |
| Fisk | Pimephales promelas | LC50 , 96 t | 88 | statisk, iuclid |
| Lepomis macrochirus | LC50 , 96 t | 75 | ferskvandsorg, iuclid | |
| Dafnier | Daphnia magna | EC50 , 24 t | 47 | |
| Alger | Scenedesmus quadricauda | LOEC | 4000 | reprod, 7 d (Nik) |
| Microcystis aeruginosa | LOEC | 90 | reprod, 8 d (Nik) |
B.4.7 Diskussion
I vaskeprocesser, hvor chlorblegemidler er anvendt, findes, afhćngig af pH, en blanding af dissocierede og udissocierede chlorforbindelser som f.eks. fri chlor (Cl2), chlor-anion (Cl-), hypochlorsyre (HClO), hypochlorit (ClO-), chloraminer, trichlormetan (chloroform), forskellige salte (chlorider) samt chlorerede aromatiske stoffer.
Pĺ grund af de mange mulige stoffer analyserer man ikke for de enkelte stoffer separat men ved en samlet metode for adsorberbare organiske halider (AOX), som er den totale mćngde af organisk bundet chlor, som tilbageholdes af en carbon adsorbent. Mĺlingen giver dog ingen oplysninger om strukturer eller art af de organiske stoffer, som chlor er bundet til.
Hypochlorit frigiver chlor i vandig oplřsning. Chlor er giftigt for vandlevende organismer i overfladevand og isćr for ferskvandsorganismer. Chlor forventes dog ikke at nĺ frem til rensningsanlćgget i form af frit chlor (Cl2) men "nedbrydes" (neutraliseres), mens det endnu befinder sig i kloaksystemet ved kemiske reaktioner med andre kemiske stoffer som f.eks. ammonium og forskellige organiske stoffer, som allerede er oxiderede eller chlorerede. Chlor er et meget reaktivt stof og vil vćsentligt optrćde som chlorider. Dannelsen af mange forskellige uorganiske og organiske chlorforbindelser i kloaksystemet er derfor mulig. Mange af de mulige organiske chlorforbindelser er vurderet til at vćre skadelige for vandlevende organismer i overfladevand og/eller svćrt nedbrydelige. En del af disse stoffer er optaget pĺ EUs liste over kemiske stoffer, der er farlige for vandmiljřet (Direktiv 76/464/EEC, Bro-Rasmussen et al. 1994). Eksempler pĺ mulige kemiske omdannelsesprodukter er vist i tabel B4-5 med de anbefalede vandkvalitetsvćrdier (WQO-vćrdier), som anses for at ville opfylde betingelserne i Rĺdets Direktiv 76/464 (EEC 1976).
B.4.8 Konklusion
Anvendelsen af klorblegemidler er ud fra et řkotoksikologisk synspunkt ikke řnskvćrdig, da reaktionen mellem chlor og organisk stof kan fřre til dannelse af uřnskede (giftige og/eller svćrt nedbrydelige) organiske chlorforbindelser. Pĺ grund af omdannelserne i aflřbssystemet forventes den direkte giftighed af chlorholdige blegemidler at vćre lavere end de resultater, der er fundet i laboratorietests. Men indholdet af andre chlorerede forbindelser i aflřbssystemet og muligheden for dannelse af hřjere chlorerede organiske forbindelser eller andre skadelige chlorforbindelser anses chloblegemidlerne for potentielt miljřskadelige. Hvor det er muligt, vil det derfor vćre anbefalelsesvćrdigt ud fra et miljřsynspunkt at anvende peroxidbaserede blegemidler i vaskerierne.
Tabel B4-5
Eksempler pĺ chlorreaktionsprodukter optaget pĺ EU liste 1 (Bro-Rasmussen).
Examples on products reacting on chloric which have been introduced on the EU list 1 (Bro-Rasmussen.
| EC76/464 Liste 1 Nr. |
CAS Nr. | Kemisk navn | Molekylformel | Struktur | WQO value * |
| 14 | 302-17-0 | chloral hydrate | C2HCl3O.H2O |  |
|
| 16 | 79-11-8 | chloroacetic acid | C2H3ClO2 |  |
|
| 23 | 67-66-3 | chloroform | CHCl3 |  |
10 µg/l |
| 58 | 75-34-3 | 1,1-dichloroethane | C2H4Cl2 |  |
|
| 59 | 107-06-2 | 1,2-dichloroethane | C2H4Cl2 | 10 µg/l | |
| 62 | 75-09-2 | dichloromethane | CH2CL2 | 10 µg/l | |
| 20 | 108-90-7 | monochlorobenzene | C6H5Cl |  |
1 µg/l |
| 53 54 55 |
95-50-1 541-73-1 106-46-7 |
1,2-, 1,3-, 1,4-dichlorbenzene |
C6H4Cl2 |  |
10 µg/l |
| 117 | 3 isomere | trichlorbenzenes | C6H3Cl3 |  |
0,1 µg/l |
| 33 34 35 |
95-57-8 108-43-0 106-48-9 |
2-, 3-, 4-, mono-chlorphenol |
C6H5ClO | 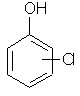 |
|
| 64 | 120-83-2 | 2,4-dichlorphenol | C6H4Cl2O |  |
10 µg/l |
| 122 | 95-95-4 88-06-2 |
2,4,5-, 2,4,6-trichlorphenol |
 |
1 µg/l | |
| 121 | 79-01-6 | trichlorethylene | C2HCl3 |  |
10 µg/l |
WQO: recommended water quality objectives
B.4.9 Referencer
Bro-Rasmussen F, Calow P, Canton JH, Chambers PL, fernandes AS, Hoffmann L, Jouany JM, Klein W, Persoone G, Scoullos M, Tarazona JV Vighi M (1994): EEC water quality objectives for chemicals dangerous to the aquatic environments (List 1). Rev. Envir. Contam. Toxicol. Vol. 137.
EEC 1976: Council Directive 76/464. Official Journal of the European Communities No. L 129 of 18 May 1976, p.23.
Nikunen E, Leinonen R, Kultamaa A (1990): Environmental properties of chemicals. research Report 91/1990. Ministry of the Environment. VAPK-Publishing, Helsinki.