|
GEOPROC - edb program til vurdering af geokemiske processer 2 Grundlæggende grundvandskemi2.1 Danmarks kvartære geologi - betydning for grundvandskemi og jordforureningDet danske landskabs overflade er primært formet i den kvartære periode under og foran gletschere i flere kolde perioder (istider) afbrudt af varmere mellemistider. Med undtagelse af bakkeøerne der ligger i landskabet foran den sidste istids maksimale gletscherfremstød (vest for hovedstilstandslinien ) har de øverste jordlag indtil for ca. 10.000 år siden været rodet godt og grundigt igennem. Der er selvfølgelig regionale forskelle i disse sedimentære bjergarters indhold af mineraler (silikater, kalk/kridt, oxider m.fl.), men specielt kan de mekaniske egenskaber og indhold af sten, grus, sand, silt og ler variere meget på alle skalaer fra regionale til mikro forhold. Som et resultat af de dannede landskabselementer er der i de sidste 10.000 år udviklet naturlige hydrologiske systemer, som fører overskuddet af nedbør (nettonedbør) bort og ud til havet i vandløb og som grundvand. I de øvre jordlag har dette givet anledning til fysiske, kemiske og biologiske processer, som har ført til dannelse af rødler, udvaskning af kalk, jordflydning, sprækker, oxidering af organisk stof osv. Et kendskab til og beskrivelse af disse processer på en lokal skala vil være afgørende for forståelsen af udbredelsen og varigheden af en jord.- eller grundvandsforurening. Jord- og grundvandsforureninger forekommer ofte i højtliggende grundvands.magasiner med kompliceret geologi og dårligt beskrevne hydrauliske forhold. De geologiske og hydrologiske forhold varierer typisk på en meget lokal skala og er samtidigt under indflydelse af sæsonmæssige variationer i nettonedbør og vandspejl – man omtaler dette som geologisk heterogenitet. I modsætning til dette vil sedimenternes geokemiske egenskaber overordnet ofte være mere sammenlignelige. Dette muliggør en bredere fortolkning og anvendelse af de geokemiske data som man er i stand til at indsamle. Mange af de biogeokemiske processer der er af betydning for omsætningen af miljøfremmede stoffer involverer kemiske og fysiske reaktioner med de tilstedeværende bjergarter. Et særkende for danske forhold er rigelige mængder af kalksten/kridt i de fleste grundvandsmagasiner, hvilket har haft væsentlig betydning for de beregninger det er blevet valgt at man skal kunne udføre på grundvandskemien med GEOPROC. Det vestlige Jylland var ikke isdækket under den sidste istid og der er derfor kalkfattige grundvandsmagasiner der har vandtyper med såkaldt aggressiv kulsyre. Tilsvarende er der på Bornholm (af andre grunde) aggressive vandtyper, hvor grundvandet ikke er i ligevægt med kalkspat (CaCO3). Et andet særkende er en tilsyneladende ulogisk blanding af reducerede og oxiderede mineraler som f.eks. pyrit og jernoxider. Dette skyldes gletschernes ovenfor nævnte ”blendereffekt” der har eroderet, transporteret og opblandet reducerede mineraler som pyrit fra dybereliggende aflejringer. Samtidigt har mange af de glaciale aflejringsmiljøer været oxiderede og derfor optræder mere stabile jernoxider som hematit (α-Fe2O3) hyppigt som en belægning på ler, silt og sandpartikler i grundvandsmiljøer der i dag er reducerede. Som hovedregel er det sedimenternes indhold af reducerede eller oxiderede forbindelser der bestemmer ”miljøet”, men en kraftig forurening med organisk stof kan alligevel godt lave et lokalt område i grundvandsmagasinet med reducerede forhold og reducerede mineraler i et ellers oxideret miljø. Man er derfor nødt til at skele til de oprindelige naturgivne forhold som har haft et tidsrum på 10.000 år at virke i selvom det der lige nu og her dominerer grundvandskemien er resultatet af en jordforurening. Dette vil ofte gøre det muligt at opdele jordsøjlen i oxiderede og reducerede jordlag, hvor sammensætningen af mineraler er forskellig. En mulig fremgangsmåde kan være at anvende geokemiske indikatorparametre til karakterisering af de forskellige jordlag som vist i nedenstående Tabel 1. På baggrund af en sådan karakterisering er det muligt at forudsige væsentlige forhold omkring mobilitet og nedbrydning af miljøfremmede stoffer. Ved at sammenligne reducerede og oxiderede sedimenter kan man få en ide om hvor stort indholdet af redoxaktive stoffer er, da der sandsynligvis også forekommer mineraler der er inerte eller som er indkapslede og dermed ikke er tilgængelige for redoxprocesser. Tabel 1. Middelværdier for geokemiske parametre i undersøgelse ved Odense /8/
2.2 Grundvandskemi og areal anvendelsenDet grundvand der dannes i dag er under stærk indflydelse af menneskets arealanvendelse på overfladen, hvilket både har betydning for de mængder af grund.vand der dannes og opholdstiden i grundvandsmagasinerne, såvel som sammensætningen af det unge grundvand. Det er derfor afgørende at karakterisere arealanvendelsen og de grundlæggende hydrologiske forhold, hvis man forsøger at beskrive den naturlige baggrundssammensætning af grundvandskemien. I byerne – hvor mange punktforureningskilder i sagens natur befinder sig – giver de befæstede områder en begrænset grundvandsdannelse. Her kan en række stofkilder få relativ stor betydning – f.eks. saltning og ukrudtsbekæmpelse på befæstede, brolagte og flisebelagte arealer. I byområder er udbredt dræning normalt forekommende, hvilket kan give anledning til iltning af pyrit og dermed væsentlige sulfatindhold (se også afsnit 2.3). Til gengæld er nitrat indholdet som regel begrænset. I landzonen er grundvandsdannelsen normalt større og sammensætning som regel betinget af landbrugsdriften. I nogle områder strømmer vand fra land.områder ind under byerne og det er selvfølgelig væsentligt for grundvands.kemien under de forhold. Tabel 2. Typiske parameterintervaller i ungt grundvand /9/, /10/ (samt upubl. materiale)
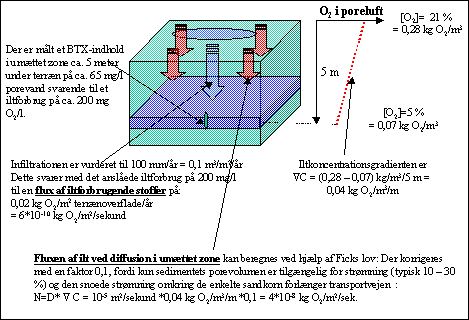
I Tabel 2 er der illustreret eksempler på typiske værdier for nogle parametre der har betydning for den biogeokemiske nedbrydning af miljøfremmede stoffer og som ofte er forskellige i by og landområder. I praksis er variationsmulighederne i princippet ubegrænsede og grundvandets sammensætning på de enkelte lokaliteter vil afspejle de mangeartede forhold man møder under realistiske forhold. 2.3 Grundvandskemi i den umættede zoneOverskuddet af nedbøren (nettonedbør) vil sive ned i gennem de øverste meter af jordsøjlen under varierende fysiske og geokemiske forhold. I den øverste del af jordsøjlen er der som regel en situation hvor ikke alle af jordskelettets porer er vandfyldte – den umættede zone. Der er ikke en skarp grænse til den mættede zone – f.eks. kan der i finkornede sedimenter som moræneler eller kridt være en i praksis mættet matrix pga. overfladekræfternes sugende virkning samtidigt med tørre sprækker hvor transport af luft og vand kan foregå. I sand/grus sedimenter vil overgangen fra umættede til mættede forhold være mere markant fordi overfladekræfterne har mindre betydning i disse sedimentets større porestruktur. Udveksling af stof mellem poreluft, vandfase og sediment er af betydning for en række biogeokemiske processer. Mens sedimentet bliver hvor det er, kan både luft og vand bevæge sig og på denne måde styre hvilke processer der forløber. Poreluften kan udveksle med atmosfæren gennem advektiv transport – f.eks. hvor der opstår trykforskellige mellem poreluft og atmosfære som følge af naturlige trykvariationer i atmosfæren (barometerånding). Denne type fænomener er beskrevet i to nye projekter udført med støtte fra Miljøstyrelsen (Vandfonden og Teknologi udviklingsprogrammet) /11/, /12/. Udveksling med atmosfæren kan også foregå ved diffusion som er en væsentlig langsommere proces end advektion, men samtidigt kan diffussion være effektiv nok set ud fra en massebalancevurdering. Hvis transporten af stofferne i poreluften sker ved diffusion kan Ficks lov anvendes til at vurdere det diffusive bidrag til massetransporten: (1) N=D*ΔC N: Flux af stof igennem et tværsnit f.eks. terrænoverflade (kg/m²/sek) Dette er illustreret i Figur 1, hvor der er diskuteret et tænkt eksempel med en olieforurening i de øverste 5 meter af et umættet sandmagasin. Der er beregnet en flux af iltforbrugende stoffer på grundlag af indholdet af BTX. Det fremgår at den beregnede flux af atmosfærisk ilt i det umættede sandmagasin alligevel er størrelsesordner større end det beregnede iltforbrug fra en forholdsvis markant BTX forurening. Diffusion kan på denne måde være en væsentlig faktor i gasudvekslingen mellem atmosfære og poreluft og dermed for oprensning af forureninger.
Figur 1. Illustrering af betydningen af diffusion for transport af ilt i umættet zone En række geokemiske processer i den umættede zone er af stor betydning for grundvandets sammensætning. Dette gælder f.eks. produktionen af kuldioxid fra omsætning af organisk stof der fører til opløsning af kalk: (2) CH2O + O2(g) ↔ CO2 (g) + H2O ↔ H2CO3 (3) H2CO3 + CaCO3 ↔ Ca2+ + 2HCO3- Opløsningen af kuldioxid fører sammen med opløsning af kalk til dannelsen af grundvandets vigtigste syre-base buffersystem kulsyresystemet, der består af (4) CO2 – H2CO3* – HCO3- – CO32- . I den umættede zone kan det infiltrerende grundvand frit udveksle gasarter med poreluften, fordi der på denne måde opstår en væske/gas grænseflade henover hvilken massetransporten kan foregå – et åbent system. Man kan i den slags systemer antage at kuldioxid trykket i poreluft og grundvand er tilnærmelsesvist i ligevægt. Dette kan udtrykkes ved hjælp af følgende ligning: (5) [H2CO3*] = KH*PCO2 hvor [H2CO3*]: Koncentration af kulsyre + opløst kuldioxid [mol/l] PCO2 : Partialtryk af kuldioxid i poreluften [atm] KH: Henrys konstant (10-1,25 mol/l/atm ved 9 °C) Under naturlige forhold vil CO2 trykket ligge i intervallet 0,5 – 2 % svarende til 12 – 50 mg/l opløst CO2. Imidlertid kan en kraftig biologiske omsætning af olie- og benzinstoffer eller blandet organisk affald (jf. ligning (2)) give væsentligt højere CO2-tryk (5 – 20 %) svarende til op imod 500 mg CO2/l. Det er væsentligt at undgå at forveksle opløst CO2 med aggressiv kulsyre som er en regneteknisk størrelse og ikke et egentligt stof. Opløsningen af kalkspat fører som beskrevet ovenfor i ligning(3) til dannelse af bikarbonat (HCO3-), der sammen med indholdet af opløst CO2 rent faktisk bestemmer grundvandets pH: (6) pH = -log(K1)+ log([HCO3-]/[CO2]) ≈ 6,45 + log([HCO3-]/[CO2]) hvor K1 Kulsyresystemets 1. dissociationsligevægtskonstant [10-6,45 M] Tilførsel af ilt kan også føre til iltning af reducerede mineraler i sedimentet hvor oxidation af pyrit [FeS2] vel nok er den iltningsproces, som har den kraftigste effekt på kvaliteten af grundvandet. Processen giver en kraftig syreproduktion og kan føre til meget hårde vandtyper, hvis der er kalk til stede i sedimentet og ellers meget blødt og aggressivt vand: (7) FeS2 + 15/4 O2 + 5/2H2O ↔ FeOOH + 2SO42- + 4H+ Hvis der er kalk til stede i sedimentet opløses kalken: (8) H+ + CaCO3 ↔ Ca2+ + HCO3- Effekten af pyritoxidation er overordnet at CO2 – trykket stiger pga. opløsningen af kalk – en effekt som altså til forveksling ligner resultatet af en forurening. Typiske intervaller for de parametre der primært berøres af pyritoxidation og CO2 – opløsning er vist i nedenstående Tabel 3. Tabel 3. Typiske værdier for udvalgte parametre i naturligt og forurenet vand baseret på erfaringstal
En anden vigtig proces i den umættede zone er iltningen af ammonium til nitrat (nitrifikation) som typisk foregår i de allerøverste cm (muldlaget). Denne proces er også forsurende og er medvirkende til at grundvand under landområder er temmelig hårdt hvis der er kalk naturligt tilstede eller ved kunstig tilsætning. (9) NH4+ + 2O2 ↔ NO3- + H2O +2H+ De stoffer som omsættes i den umættede zone i forbindelse med jord- og grundvandsforureninger forureninger kan både være de primære forurenings.komponenter såvel som nedbrydnings.produkterne. F.eks. kan metan – der er produceret ved redoxprocesser i de områder af en forureningskilde hvor ilt er opbrugt – transporteres ved afdampning fra grundvandet, diffusion og advektion til de dele af den umættede zone hvor ilt er tilgængeligt. Her kan metan blive oxideret af metanoxiderende bakterier: (10) CH4 + 2O2 ↔ CO2 + 2H2O 2.4 Grundvandskemi i den mættede zoneNår porevandet fra den umættede zone når ned til ”vandspejlet” ved grænsen til den mættede zone bliver tilførslen af ilt begrænset til den mængde som kan være opløst i grundvandet (ca. 11 mg O2/l ved 9 °C). Det betyder, at de biogeokemiske redox processer der involverer opløst ilt – som f.eks. ligning (2) – vil få en begrænset betydning i den mættede zone af grundvandsmagasinerne – grundvandet bliver anaerobt. Imidlertid er der redoxprocesser som kan give anledning til omsætning af organisk stof , hvor andre såkaldte elektronacceptorer er aktive og alle disse processer kan have betydning i den mættede zone (se Tabel 4). Observationer af udviklingen af naturlig grundvandskemi i den mættede zone, viser at energi.udbyttet ved overførslen af elektroner (se Tabel 4) er en vigtig faktor, der er med til at bestemme hvor og hvornår en given reaktion forløber. Redoxprocesser er jo kemiske reaktioner, hvor der flyttes elektroner fra den ene forbindelse til den anden. I Tabel 4 er de redoxprocesser, som forekommer almindeligt i naturen med organisk stof, ordnet efter energiudbyttet pr. overflyttet elektron. Det største energiudbytte fås af processer der involvere ilt og nitrat og det ringeste i forbindelse med sulfatreduktion og methanogenese. Energiudbyttet afhænger også af typen af organisk stof – der vil være mere energi i toluen end i det naturlige organiske stof der er anvendt som modelstof her. Tabel 4. Typiske redoxreaktioner med organisk stof ved standardforhold med termo.dynamiske data fra /13/ (pH=7, aktiviteter for elektronacceptor/ -donor = 1 dog {Fe2+} = 10-6 og {Mn2+} = 10-6) ordnet efter energi frigivelse pr. elektronoverførsel (kcal/ekv).
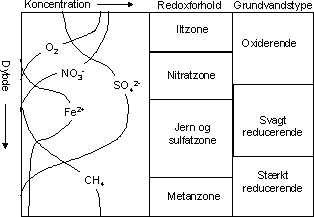
Energiudbyttet har betydning for de biogeokemiske processer dvs. for de mikroorganismer der udnytter redoxprocesserne vist i Tabel 4. Dette er illustreret i Figur 2, hvor der er en skematisk gengivelse af hvilke redoxprocesser, der har betydning i forskellige ”dybder” som her skal forstås som vandets bevægelse langs en strømlinie ned gennem den mættede zone. Indholdet af ilt, nitrat og sulfat stammer typisk fra input og omsætning i muldjorden og den umættede zone. Da både sulfat og nitrat er væsentlig mere opløselige end ilt er dannelse af store mængder af nitrat og sulfat i den umættede zone en effektiv måde for naturen at transportere iltningsmiddel ned under grundvandsspejlet hvor opløseligheden af ilt er begrænset til 10 – 11 mg/l.
Figur 2. Skematisk forløb af redoxaktive komponenter under naturlig grundvands..dannelse i mættet zone (modificeret efter /14/) Sulfat kan desuden dannes under grundvandsspejlet ved pyritoxidation med nitrat (se ligning(11)). Meningen med at vise at indholdet af sulfat stadig stiger når opløst ilt er opbrugt på Figur 2 er således at illustrere nedenstående reaktion, der ofte har betydning for nitrats mobilitet. Dette er væsentligt når man vurderer årsagerne til at nitrat fjernes langs en strømlinie – det behøver ikke at være nitratreduktion som følge af organisk stof som i Tabel 4 – det kunne være pyritoxidation ved nitrat reduktion: (11) FeS2 + 3NO3- + H2O ↔ FeOOH + 2SO42- + 3/2N2 + H+ På grundlag af den skitserede udvikling af grundvandets sammensætning langs en strømlinie vist på Figur 2 kan man inddele grundvandet i typer som reflekterer, hvor langs denne teoretiske udviklingslinie grundvandet befinder sig. Dette er vist i Tabel 5 med en inddeling foreslået af Miljøstyrelsen og GEUS og med kriterier for indholdet af udvalgte redoxparametre. Tabel 5. Inddeling af grundvand i typer som foreslået i /15/
Metoden i Tabel 5 har imidlertid den ulempe at man ofte ser blandede vandtyper i vandforsyningsboringer og undersøgelsesboringer. Dette gør det svært at vurdere præcist, hvilken kategori man skal placere en vandprøve i – f.eks. vandprøver med samtidigt indhold af opløst jern (Fe2+) og nitrat (NO3-). Den foreslåede inddeling i Tabel 5 og Figur 2 afspejler, at der er en stor mængde fri energi til rådighed i oxiderede vandtyper og en lille mængde i reducerede vandtyper. Samtidigt er der i oxiderede vandtyper kun forbrugt en lille mængde fri energi, mens den forbrugte mængde fri energi er stor i reducerede vandtyper. Ved blanding af forskellige vandtyper udviskes disse forskelle og det bliver svært at vurdere om grundvandstypen er oxideret eller reduceret. For at løse dette problem er der med GEOPROC indført et nyt redoxindeks R som er uafhængigt af blandingsforhold. Det vil sige at redoxindekset R giver en meningsfuld værdi, selvom vandprøvens sammensætning er opstået ved en blanding af stærkt reduceret og oxideret grundvand. Redoxindekset som får enheden (cal/l) er baseret på en lineær karakterisering af den fri energi der samlet er til rådighed fratrukket den fri energi der samlet allerede er frigivet. Som grundlag for energi.beregningerne er der anvendt en opdeling i de redoxreaktioner der er vist i Tabel 4 med de tilhørende værdier for frigivelse af fri energi ved reaktion med standard organisk stof CH2O (se ligning(12)). (12) R =Σ ΔG°(W)*ne*Cpot - Σ ΔG°(W)*ne*Cfor (cal/l) hvor Σ ΔG°(W) Standard fri energi ændring ved redox reaktion; se tabel 4 (kcal/ekv) ne Antal overførte elektroner pr mol elektronacceptor; se tabel 4 (ekv/mol) Cpot Koncentration af elektronacceptorer der potentielt kan medvirke i en redoxreaktion med organisk stof (mol/l) Cfor Koncentration af elektronacceptorer der allerede har medvirket i en redoxreaktion med organisk stof (mol/l) Den absolutte værdi af redoxindekset R vil ikke være fuldstændig korrekt i en situation hvor der omsættes olie og benzinstoffer, fordi de værdier af standard fri energi ændringer (Σ ΔG°(W)) som man skulle anvende er forskellige i forhold til reaktioner med standard organisk stof (CH2O). Det vil imidlertid kun give en relativ forskydning af nulpunktet for R – en sammenligning indenfor den samme ”situation” er stadigvæk meningsfuld. Derimod skal man ikke forsøge at lave universelle sammenligninger på tværs af forskellige typer af organisk stof med udtrykket i ligning(12). For at kunne gennemføre bredere sammenligninger kan man gennemføre en mere almen beregning af R der er forholdsvis simpel, men som dog falder uden for det snævre formål vi har opstillet her. Typiske værdier for R vil ligge omkring 100 cal/l i oxiderede vandtyper og omkring – 50 cal/l i stærkt reducerede vandtyper. Ved at anvende ligningerne og de oplyste værdier i Tabel 4 kan man udspecificere ligning(12) til: (13) R = +29,8*4*[O2]/32 + 28,4*5*[NO3-]/62 + 5,9*7*[SO42-]/96 R: Lineært redoxindeks eller fri energi indeks målt i (cal/l) Redoxindekset R udtrykker således i hvilken udstrækning grundvandet har været i kontakt med reaktivt organisk stof eller andre reducerende forbindelser som f.eks. pyrit. Den ovenfor diskuterede reaktion mellem pyrit og nitrat der fører til sulfat dannelse (se ligning(11)) vil formindske redoxindekset. Fjernelse af 62 mg/l nitrat (1 mmol/l) vil føre til dannelse af 64 mg/l sulfat og vil samtidigt få redoxindekset til at falde med 114 cal/l (du kan selv kontrollere ved at anvende ovenstående udtryk for R sammen med ligning(11)). Det betyder ikke at det samlede potentiale for at oxidere det organiske stof er væsentligt formindsket, fordi elektronerne kan jo stadig flyttes fra det organiske stof ved sulfat.reduktion og jernreduktion. Men energiudbyttet er blevet formindsket og dermed formentlig også den hastighed hvormed biogeokemiske processer kan forløbe 2.5 Mere om biogeokemiNår redoxprocesserne beskrevet i Tabel 4 forløber sker desuden ændringer i grundvandets indhold af uorganisk kulstof – der frigives således CO2 fra oxidationen af det organiske kulstof. Derfor påvirker redoxprocesserne også grundvandets væsentligste buffersystem – kulsyresystemet (se ligning(4)). Samtidigt vil de processer hvor der produceres eller forbruges elektrisk ladede komponenter (f.eks. Fe2+ eller SO42-) forskubbe ladningsbalancen og føre til ændringer i grundvandets alkalinitet. I de ferske vandtyper som er hovedsigtet med beregningerne i GEOPROC vil alkaliniteten næsten udelukkende være bestemt af kulsyresystemets alkalinitet: (14) ALK = [HCO3-] – 2[CO32-] + [OH-] – [H+] hvor ALK Kulsyresystemets alkalinitet (ekv/l eller mekv/l) De forskellige redoxprocesser i Tabel 4 vil således efterlade et fingeraftryk på grundvandets sammensætning som omfatter
Redox reaktionernes produktionen af alkalinitet vil typisk give anledning til en stigning i grundvandets indhold af bikarbonat (ved pH < 9). Et eksempel baseret på de forskellige redox reaktioners biogeokemiske fingeraftryk med toluen som modelstof er samlet i en oversigt i Tabel 6. Talstørrelserne i Tabel 6 er selvfølgelig afhængige af hvilket modelstof man anvender, således at jo mere reduceret det organiske stof er desto mindre omsætning og produktion af CO2 målt pr. gram eller mol elektron.acceptor. Derimod er produktionen af alkalinitet primært en funktion af ladningen af elektron.acceptor med mindre det organiske stof er elektrisk ladet (f.eks. en organisk syre). Tabel 6. Støkiometri for redoxreaktioner med toluen som modelstof. Tabellen viser hvor meget toluen der omsættes, og hvor meget CO2 og alkalinitet (som HCO3-) der produceres pr mg elektronacceptor
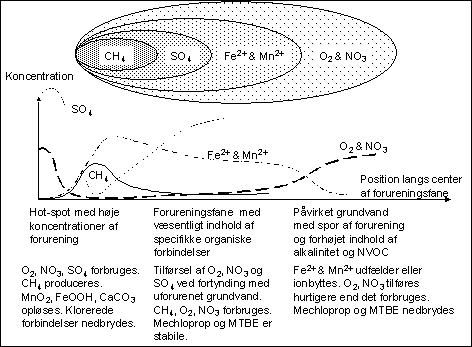
Imidlertid vil det kun være i de færreste tilfælde at disse fingeraftryk beskrevet i Tabel 4 og Tabel 6 slår fuldt igennem i grundvandskemien. I Tabel 4 er der for sulfatreduktion (se også ligning(15)) vist en alkalinitet produktion på 1 ekv/mol ved neutral pH samtidgt med dannelsen af opløst hydrogensulfid. Imidlertid er det kun sjældent man måler ækvivalente mængder af opløst svovlbrinte – selv ved ret store reduktioner af grundvandets sulfatindhold. i forbindelse med forureningssager. Hvor bliver svovlbrinten af ? Opløsning af jernoxider er formentlig den væsentligste årsag til dette forhold. Dette skyldes både at jernoxider ikke er stabile når der er væsentlige indhold af opløst svovlbrinte samt at jernoxider også deltager i redoxreaktioner med organisk stof. Derfor produceres der store mængder af opløst jern der virker som en effektiv udfældningsmekanisme for opløst svovlbrinte (ligning(16)). I Tabel 6 er der således anvendt en alkalinitetsproduktion på 2 ekv/mol reduceret sulfat ud fra en antagelse om dannelsen af et neutralt slutprodukt (FeS eller FeS2). (15) SO42- + 2CH2O + H+ ↔ 2CO2 + HS- + 2H2O (16) S2- + Fe2+ ↔ FeS Da der både produceres høje koncentrationer af opløst jern (Fe2+) samt alkalinitet kunne man også som hypotese antage udfældning af mineralet siderit (FeCO3: ligning(17)). Imidlertid viser de fleste beregninger (som også kan udføres med GEOPROC) at opløselighedsproduktet ofte er kraftig overskredet i opløsning. Samtidigt er siderit termodynamisk ustabilt i opløsninger der er overmættet mht. jernsulfid og pyrit og derfor vil udfældning af siderit næppe forekomme så længe sulfat.reduktion er betydningsfuld. (17) 2HCO3- + Fe2+ ↔ FeCO3 + H2CO3 Det fulde gennemslag af de biogeokemiske fingeraftryk på grundvandets sammensætning modvirkes også af buffersystemet bestående af kulsyresystemet koblet med ligevægt til mineralet kalkspat beskrevet i ligning(3)-(6). Fuldt gennemslag kan kun forventes i bløde vandtyper som man finder i områder uden kalk i jorden (f.eks. i vestlige Jylland). I de fleste øvrige tilfælde vil udfældning og opløsning af kalk(spat) virke som en begrænsende buffer på de stigninger i grundvandets indhold af uorganisk kulstof og alkalinitet som redoxreaktionerne ellers ville føre til. For at vurdere resultatet af disse påvirkninger er det som regel nødvendigt at gennemføre numeriske beregninger – hvilket er et af hovedformålene med udviklingen af GEOPROC. Sammenligning af målte data med de forventede biogeokemiske fingeraftryk beregnet med en modelbeskrivelse er en af de bedste metoder til at analysere ændringer af grundvandskemien og dette er muligt med GEOPROC. Et typisk geokemisk problem er at der i forhold til de forventede processer er for meget opløst kuldioxid i grundvandet, hvorimod alkalinitets ændringerne stemmer nogenlunde. Dette skyldes ofte at man har overset processer hvor der er udveksling med poreluft i den umættede zone som typisk vil bidrage med CO2 og ikke alkalinitet (aerob iltning og methanogenese). Vurdering af dette problem vil blive beskrevet i et praktisk gennemgang i afsnit 3. I forbindelse med de redoxprocesser der kommer som følge af en forurening vil grundvandets sammensætning af kationer som ammonium (NH4), ferro-jern (Fe2+), calcium (Ca2+) osv. blive ændret. Disse ændringer bliver modvirket af sedimenternes ionbytningskapacitet (ofte målt som CEC; cation exchange capacity mekv/g sediment) og man vil næppe kunne se bort fra betydningen de mineraler der bidrager til denne type buffer. Det er også muligt at lave simple beregninger med ionbytning i GEOPROC – dog kun ionbytning mellem natrium og calcium som beskrevet nedenfor (18) 2X-Na+ + Ca2+ ↔ X=Ca2+ + 2Na+ hvor X-, X= overfladeplads ledig for ionbytning (f.eks. på lermineraler) 2.6 Kildeområde og forureningsfanerNår grundvand passerer under en forureningskilde hvor der foregår omsætning af organisk stof udvikler der sig zoner i grundvandsmagasinet der ofte er karakteriseret ved den dominerende tilstedeværelse at en eller flere forskellige typer af elektronacceptorer – se Figur 3. Grundvandet i Figur 3 er oprindeligt iltholdigt, men bliver pga. omsætningen af det af organisk stof hurtigt iltfrit. Der udvikler sig herefter mere eller mindre klart definerede zoner domineret af forskellige typer redoxreaktioner (redoxzoner). Man kan få informationer om de forskellige redoxprocesser ud fra geokemiske data – f.eks. formindsket indhold af ilt, nitrat og sulfat eller forhøjet indhold af uorganisk kulstof, metan, jern og mangan.
Figur 3 Skematisk rumlig fordeling af indholdet af elektronacceptorer og reaktionsprodukter i en forureningsfane med organiske stoffer Den påviste udvikling af redoxzoner formodes at skyldes konkurrence mellem forskellige typer af mikroorganismer, hvor de mest effektive mikroorganismer med det højeste energiudbytte (aerobe og denitrificerende organismer jf. Tabel 4) udkonkurrerer de øvrige. Fortolkningen af disse zoner er dog ikke nær så ligefrem, som de redoxzoner, der udvikler sig ved grundvandets naturlige dannelse (se 3). Dette skyldes at opblanding og dispersion har større betydning for udviklingen af geokemien i forureningsfaner. Hverken sulfat, nitrat eller ilt kan således ”opstå” i den nedstrøms liggende del af forureningsfanen, men må nødvendigvis transporteres ind til kernen af forureningsfanen ved dispersion og diffusion. En konklusion der omtaler f.eks. denitrificerende forhold baseret på et reduceret indhold af nitrat kan således skyldes, at man fejlfortolker vandprøver af blandingsvand bestående af reduceret grundvand fra forureningsfanen på den ene side og oxideret upåvirket grundvand med nitrat på den anden side Fortynding pga. en uhensigtsmæssig placering af prøvetagningsfiltre i undersøgelsesboringer er mere reglen end undtagelsen. Dette kan give anledning til fejlfortolkninger og i værste fald forkerte konklusioner vedr. f.eks. omfanget af naturlig nedbrydning. Det er i en række tilfælde muligt at vurdere fortyndingen ud fra ændringer i grundvandets alkalinitet og denne mulighed er indbygget i GEOPROC. Alkaliniteten er en konservativ parameter ligesom f.eks. klorid og den resulterende alkalinitet ved blanding af forskellige vandtyper kan derfor beregnes ved simpel forholdsregning. CO2 – afgasning eller opløsning har ikke direkte betydning for alkaliniteten, men kan få indirekte betydning ved udfældning eller opløsning af kalk (CaCO3) som har betydning for alkaliniteten. Kraftige stigninger i grundvandets alkalinitet opstår som følge af omsætning af organisk stof, hvilket primært vil sige i kildeområdet. Typisk ses stigninger svarende til intervallet 300 – 1000 mg HCO3/l (60 – 200 mg C/l) i hotspot området ved olie/benzin forurening, ukontrollerede lossepladser o.l. Den kraftige omsætning i kildeområdet og dertil hørende alkalinitets ændring vil ofte fuldstændigt overskygge de ændringer som sker i forureningsfanens alkalinitet pga. biogeokemiske processer. Også selvom en forureningsfaner indeholder ret høje koncentrationer af organisk stof (1.000 – 10.000 µg organisk kulstof pr. liter). Derfor kan man i en del tilfælde anvende forureningsfanen af alkalinitet fra kildeområdet som en konservativ markør for opblanding. Man skal måle alkaliniteten i kildeområdet (hotspot), opstrøm for hotspot og i den blandede vandprøve udtaget i forureningsfanen nedstrøm for hotspot. Herefter kan blandingsforholdet mellem grundvand fra kildeområdet og uforurenet baggrund bestemmes som: (19) ALK = α*ALKHOTSPOT + (1-α)ALKBAGGRUND (20) α = (ALK – ALKBAGGRUND)/(ALKHOTSPOT – ALKBAGGRUND) hvor α Fraktion af forurenet grundvand fra hotspot i blandingsprøve [0 - 1] Opblanding af forureningsfanens kerne med omgivende uforurenet grundvand vil give anledning til transiente ændringer af forureningsfanens form og størrelse. Selvom en forureningskilde giver en tilnærmelsesvis konstant belastning vil f.eks. omfanget af jernreduktion ændres efterhånden som reaktivt jernoxid opbruges i sedimentet. Imidlertid vil dette opløste jern blive reoxideret og genudfælde hvor der sker opblandingsprocesser – typisk i randen af forureningsfanen. Forureningsfanen skubber således en stedse stigende pulje af jernoxider foran sig, imens kernen af forureningsfanen formentlig forøger sin udbredelse i de områder hvor jernoxid er blevet udvasket. Når man beskriver udviklingen i forureningsfanens sammensætning er det derfor væsentligt at vurdere om de ofte observerede fald i indholdet af reducerede komponenter som jern, mangan og metan skyldes oxidation eller simpel opblanding Tilsvarende gælder for indholdet af selve forureningskomponenterne som drøftet ovenfor. Ofte kan en vurdering af hvorledes disse stoffer ”forsvinder” i en forureningsfane gennemføres med en 1. orden model: (21) C = CHOT* exp(k1*t) hvor C Målt forureningskoncentration på prøvested (mg/l eller µg/l) Hvis man kan bestemme k1 med rimelig sikkerhed har man en model til at forudsige hvor langt forureningen vil brede sig. Bestemmelsen af k1 er imidlertid særdeles følsom overfor opblanding med uforurenet grundvand der vil føre til for store k1-værdier og dermed for optimistiske vurdering af fjernelsen af forureningen, fordi opblanding formindsker koncentrationerne i forureningsfanen. I GEOPROC er der indbygget 1. ordens model til at vurdere nedbrydningen hvor det er muligt at få fortyndingskorrigerede værdier ud fra alkalinitets ændringerne. 2.7 Nogle praktiske forhold omkring datagrundlagetDe anvendte metoder til indsamling af data, dvs. boreteknik, prøvetagning og analyser er under stadig udvikling, men dette er ikke nogen garanti for at fejlfrekvensen formindskes. Det er derfor væsentligt at vurdere de indsamlede data før de anvendes til en egentlig analyse. Dette har betydning for udformning af undersøgelsesboringer, hvor der kan foregå opblanding i filteret, utilstrækkelig eller overdreven forpumpning, feltmålinger med for høje iltindhold, sedimenter i prøveflasker, tab af metan osv. Vurderingen kan ikke blive bedre end de indsamlede data og i selve vurderingsfasen er det nødvendigt at gennemføre en kritisk vurdering af de indsamlede data. Det sker ofte at tvivlsomme data alligevel får lov til at slippe igennem til den endelige rapport. Dette er uhensigtsmæssigt – det er bedre med en tom plads eller indikation af tvivlsom datakvalitet. Undersøgelsesboringer er ofte af tvivlsom karakter eller ikke reproducerbare (eks. direct-push metoder som GEOPROBE). Tab af flygtige stoffer omfatter ikke alene de miljøfremmede stoffer men også CO2 og CH4 som indgår med stor vægt i vurderingerne og sådanne prøvetagningsbetingelser giver også mulighed for en uhensigtsmæssig iltning af prøven. Derfor er bevidste valg omkring prøvetagningsteknik og feltmålinger et uundværligt kvalitetssikringsværktøj. GEOPROC har en kvalitetskontrol som giver en intern test af de anvendte data ved at sammenligne afvigelserne mellem den samlede ladning af kationer og anioner. Det kan kun anbefales at gennemføre så fuldstændige vandanalyser som muligt – dvs. svarende til de stoffer der har betydning for grundvandets ionstyrke jf. GEOPROCs inddatablok i næste afsnit. Den mere fuldstændige beskrivelse af grundvandskemien bør også omfatte en måling af grundvandet indhold af ikke flygtigt organisk kulstof (NVOC). Sammen vil disse data give et grundlag der som regel kan udpege misforhold ved prøvetagning, opblanding eller andre typiske fejlkilder – så disse ekstraomkostninger vil ofte være givet godt ud.
|