Bekæmpelsesmiddelforskning fra Miljøstyrelsen nr. 109, 2007
Hudoptagelse af pesticider - betydning af lag-time og reservoir-effekt
Indholdsfortegnelse
- 1.1 Baggrund
- 1.2 Metode
- 1.3 In vitro model
- 1.4 Eksperimentelt design
- 1.5 Variabilitet og statistik
- 1.6 Kemiske analyser
- 1.7 Delstudier
- 1.8 Relevans
- 1.9 Internationale samarbejdspartnere
- 2.1 Betydning af stoffers opløselighed for absorptionsmængde og hastighed
- 2.2 Betydning af afvaskning og let hudbeskadigelse for penetration
- 3.1 Hovedobservationer og diskussion
- 3.2 Betydning af stoffers opløselighed for absorptionsmængde og hastighed
- 3.3 Betydning af afvaskning og let hudbeskadigelse for penetration
Forord
Hudeksponering er fortsat den dominerende eksponeringsvej for bekæmpelsesmidler. Tiltagende begrænsninger i brug, bedre uddannelse, hensigtsmæssig anvendelse af værnemidler har nedsat udsættelsen for bekæmpelsesmidler i Danmark, ligesom de mest toksiske midler efterhånden fjernes fra markedet. Blandt de arbejdstagere der ikke selv udbringer bekæmpelsesmidlerne pågår imidlertid fortsat en relevant eksponering, ligesom brugen af bekæmpelsesmidler i Danmark ikke afspejler den globale situation, hvor der fortsat ses betydelig anvendelse og human eksponering.
Den fortsatte udvikling af nye produkter stiller løbende krav til myndigheder om godkendelse og regulering af brugen af bekæmpelsesmidler. Den hastige nyudvikling har afstedkommet et ønske om undersøgelser af muligheden for på basis af fysisk-kemiske forhold at modellere sig frem til en risikoprofil i forhold til dermal penetration hos arbejdstagere – arbejdstagere der næppe altid har en fuldt duelig barrierefunktion i huden.
Nærværende projekt har ved anvendelse af en række modelstoffer undersøgt betydningen af fysisk-kemiske forhold for hudoptagelsen, ligesom betydningen af afvaskning af huden efter endt eksponering samt betydningen af en lettere beskadiget hud for den dermale absorption af modelstoffer er belyst.
Undersøgelsen er finansieret af Miljøstyrelsens program for bekæmpelsesmiddelforskning og nærværende rapportering gælder projektet ’Hudoptagelse af pesticider – betydning af lag-time og reservoir-effekt’.
Der har til projektet været knyttet en af Miljøstyrelsen nedsat følgegruppe, og forfatterne er taknemlige for de konstruktive kommentarer fra repræsentanter fra Miljøstyrelsen (Susanne Hougaard, Jørn Kirkegaard), Arbejdsmiljøinstituttet (Mari-Ann Flyvholm) samt Dansk Toksikologi Center (Karl-Heinz Cohr).
Endelig skal laborant Franziska Lind takkes for professionel gennemførelse af undersøgelsens eksperimentelle dele.
Den 28. december 2006
Jesper Bo Nielsen, Institut for Sundhedstjenesteforskning, Syddansk Universitet
Flemming Nielsen, Institut for Sundhedstjenesteforskning,Syddansk Universitet
Jens Ahm Sørensen, Odense Universitetshospital
Sammenfatning
Projektet havde følgende overordnede formål:
- Gennem anvendelse af en række modelstoffer at fastlægge et interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes.
- At beskrive den betydning den midlertidige ophobning i huden (reservoir-effekten) har i forhold til en forsinket absorption efter eksponeringsophør.
- At vurdere hvorvidt man ved afvaskning efter endt eksponering kan fjerne en del af det på huden deponerede pesticid eller, om det fortsat skal henregnes som absorberet.
- At vurdere den betydning en lettere beskadiget hud har for såvel absorption som midlertidig ophobning i huden.
Som modelstoffer udvalgtes ni stoffer, hvoraf 8 var bekæmpelsesmidler med anvendelse i Danmark på undersøgelsestidspunktet. Modelstofferne udvalgtes med baggrund i ønsket om at dække et bredt opløseligheds- og molvægts-spektrum. De anvendte bekæmpelsesmidler var glyphosat, dimethoat, pirimicarb, malathion, paclobutrazol, methiocarb, og prochloraz, medens de to andre modelstoffer var kaffein og benzosyre. Fire af stofferne blev anvendt som radioaktive isotoper og kunne kvantiteres som sådan, medens de resterende fem modelstoffer blev kvantiteret ved hjælp af HPLC. Som eksperimentel model anvendtes statiske diffusionsceller med human hud og en fremgangsmåde, der levede op til gældende OECD guideline for undersøgelser af dermal penetration af fremmedstoffer.
De planlagte eksperimentelle undersøgelser er gennemført, og de vurderes generelt at leve op til internationale OECD guidelines for denne type undersøgelser. For et enkelt modelstof, malathion, faldt de opnåede resultater klart ved siden af det forventede. Der er ikke fundet validerbare årsager til denne observation. Overordnet set er det imidlertid vurderingen, at de opnåede resultater muliggør diskussion og konklusion vedrørende de initialt opstillede mål, hvilket er sammenfattet i nedenstående afsnit.
Fastlæggelse af interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes:
- Resultaterne indikerer generelt en U-formet sammenhæng mellem Kp og logPow, således at hurtigst penetration opnås ved en logPow værdi mellem 1½ og cirka 4. Et enkelt af de ni modelstoffer (malathion) falder udenfor denne generalisering.
- Der var ingen umiddelbar sammenhæng mellem molvægt og penetrationshastighed udtrykt som Kp.
- For de i dette studie anvendte modelstoffer gælder, at den korteste lag-time kan forventes af stoffer med en vandopløselighed mellem 3g/L og godt 20 g/L.
- Med stigende molvægt øgedes lag-time. Således var lag-time for det mindste modelstof med en molvægt på 122 gram nede på omkring 1½ time, medens lag-time ved molvægt over 350 gram oversteg 20 timer, hvilket er en ganske markant forskel, der også influerer på den mængde stof, der i løbet af en begrænset periode vil kunne absorberes dermalt. Igen adskiller malathion sig fra de øvrige modelstoffer.
- For dermis ses en klart større relativ deponering af de lipofile stoffer, hvilket også var ventet, givet at dermis er et overvejende lipofilt matrix.
Delstudiet af hvorvidt en midlertidig ophobning af fremmedstof i huden (reservoir effekt) kan give anledning til forsinket absorption efter eksponeringsophør konkluderede:
- Undersøgelsen viser, at absorption fra huden og ud i receptordelen fortsætter efter endt eksponering. For visse stoffer i over et døgn efter endt eksponering.
- Der er derfor ingen tvivl om, at en vis del af den i huden deponerede mængde modelstof senere vil absorberes.
- For et modelstof med en lang lag-time og en begrænset affinitet for den mere lipofile hudkompartment kan man ikke forvente nogen målbar absorption gennem huden efter kortere tids eksponering (i dette tilfælde under en tredjedel af lag-time), ligesom en midlertidig ophobning i huden heller ikke ses.
- For de hydrofile stoffer kan nærværende data ikke give fyldestgørende svar på problemstillingen omkring betydningen af midlertidig ophobning i huden.
- For de lipofile stoffer indikerer de nærværende, om end begrænsede data, at den nuværende anvendelse af data ved regelsætning for dermal absorption baseret på guideline-forsøg i en vis grad overestimerer den reelle absorberbare mængde fremmedstof ved at indregne alt stof ikke genfundet i donor som absorberet. Overestimatet er dog ikke voldsomt stort, og for de lipofile stoffers vedkommende synes den hidtil anvendte procedure pragmatisk anvendelig.
Undersøgelsen af hvorvidt afvaskning af huden efter endt eksponering fjerner en del af det på huden eller i stratum corneum deponerede pesticid gav følgende konklusioner:
- En afvaskning efter 6 timer fjerner den altovervejende del af den administrerede mængde modelstof og nedsætter derved muligheden for senere huddeponering og absorption.
- For de mest vandopløselige modelstoffer (glyphosat og caffein) nedsætter en afvaskning af huden efter 6 timers eksponering huddeponeringen med 80-90 %, medens reduktionen for de mere lipofile stoffer såsom malathion og methiocarb er omkring 35 %.
- Den nedsatte mængde modelstof i huden betyder en mindre koncentrationsgradient mellem hud og receptorkammer, hvilket resulterer i en nedsat flux af modelstof.
- Samlet kan det konkluderes, at en afvaskning efter endt eksponering signifikant nedsætter den samlede absorption. For de mest vandopløselige stoffer med omkring 67 % og for de mere lipofile modelstoffer med lidt mindre. Det er således muligt ved almindelig let afvaskning at fjerne ikke alene resterende fremmedstof på huden, men også en del af den stofmængde, der er trængt ind i huden.
- Denne observation har klare forebyggelsesmæssige implikationer, og dokumenterer betydningen af afvask med sæbeopløsning efter endt arbejde, der har indebåret dermal kontakt til fremmedstoffer.
På basis af undersøgelsen af betydningen af en lettere beskadiget hud for fremmedstoffers dermale absorption og midlertidige ophobning i huden kunne følgende konkluderes:
- En lettere beskadiget hud resulterer i en generel forøget penetrationshastighed for alle stoffer.
- Forøgelsen er marginal for de stoffer, der allerede ved den intakte hud har gode penetrationsegenskaber.
- Forøgelsen er signifikant for de mere lipofile stoffer, men den klart største effekt observeres ved eksponering for hydrofile modelstoffer.
- Imidlertid vil en afvaskning af den beskadigede hud efter endt eksponering i meget høj grad kunne reducere den forøgede absorption såvel som huddeponering – dog kun til et niveau, der mængdemæssigt stadig er signifikant højere end efter afvaskning af intakt hud.
- Den kraftigt forøgede penetration af specielt de mere hydrofile modelstoffer gennem lettere beskadiget hud kan have den konsekvens, at man reguleringsmæssigt er nødt til at forholde sig til, at den reelle situation blandt en stor del af ansatte med dermal eksponering og ikke-intakt hud er, at de absorberer ganske meget mere dermalt, end de traditionelle in vitro guideline-forsøg indikerer.
Summary
This project had four primary aims:
- Through the use of a range of model compounds, to identify an interval in relation to lipophilicity, where the most effective dermal absorption would be expected.
- To describe the importance of temporary deposition in the skin (reservoir effect) in relation to delayed absorption after end of exposure.
- To assess whether washing skin after exposure might remove part of the pesticide deposited on or within the upper stratum corneum, and whether regulators should continue seeing this fraction as de facto absorbed.
- To assess the importance of slightly damaged skin for dermal absorption as well as temporary deposition in the skin.
Among the nine model compounds selected for this study, eight where pesticides in use in Denmark at the time the study was initiated. The model compounds were chosen to cover a wide spectrum of solubilities and molecular weights. The pesticides included were glyphosate, dimethoate, pirimicarb, malathion, paclobutrazol, methiocarb, prochloraz, and benzoic acid, the ninth model compound being caffeine. Four of the model compounds where used as radioactive isotopes and quantified through beta counting, whereas the remaining model compounds were analysed with HPLC. Static diffusion cells mounted with human skin were used as the experimental model, and experiments were carried out in accordance with requirements given in the OECD guideline for experimental studies of dermal penetration.
Results from one of the model compounds (malathion) were clearly at variance with what was expected on the basis of results from the other model compounds as well as the physical-chemical data. No explanation for this deviation from the expected was identified. Generally, however, the data obtained enables discussion and valid conclusions on the primary aims for the project. The main conclusions are summarized in four sections, each comprising five paragraphs.
On identification of an interval in relation to lipophilicity, where the most effective dermal absorption would be expected, the following was concluded:
- Results indicate a general inverted U-shaped relationship between Kp and logPow. Thus, the fastest dermal penetration occurs for compounds with logPow values between 1½ and 4. Malathion does not fit into this generalisation.
- No obvious relationship was observed between molecular weight Kp values.
- The shortest lag-time was observed for model compounds with water solubility between 3 g/L and 20 g/L.
- With increasing molecular weight, lag-time increased. Thus, the lag-time for the smallest model compound with a molecular weight of 122 g was close to 1½ hours, while the lag-time exceeded 20 hours for a model compound with a molecular weight of 377 g. A difference in lag-time of this size inevitably also causes differences in the amounts of compounds able to penetrate the skin within a limited period of time.
- The relative deposition in dermis was highest for the lipophilic model compounds, which was also expected given that dermis is seen as a lipophilic compartment.
On the importance of the temporary deposition in the skin (reservoir effect) in relation to delayed absorption after end of exposure the following was concluded:
- Absorption of model compounds temporarily deposited in the skin compartment continues after exposure is terminated; for certain model compounds for more than 24 hours.
- Thus, a certain fraction of a compound deposited temporarily within the skin compartment will penetrate the skin at a later point and appear as absorbed.
- For a compound with a long lag-time and limited affinity for the lipophilic skin compartment, neither significant temporary skin deposition nor significant dermal penetration through the skin can be expected following short-term exposure (i.e. less than one third of the lag-time).
- The present data does not warrant conclusions on the relationship between temporary skin deposition and later skin penetration for hydrophilic compounds.
- For lipophilic compounds, data indicates that rule setting and administration on use of pesticides based on data generated along the lines of OECD guidelines for experimental studies on dermal penetration to some extent overestimates the actual degree of penetration. However, the overestimated dermal penetration for lipophilic compounds is probably relatively limited. Thus, at least for lipophilic compounds, regulators are advised to continue the pragmatic approach and use the total fraction of an administered compound not recovered in the donor compartment as a measure for the amount potentially available for absorption.
On the assessment of whether washing skin after exposure removes part of the pesticide deposited on or within the upper stratum corneum the following was concluded:
- A skin wash after six hours exposure removes a significant fraction of the pesticide administered on the skin and significantly reduces the amount available for later absorption.
- For the most hydrophilic model compounds (glyphosate and caffeine) a skin wash after 6 hours reduces skin deposition by 80-90 %, while the reduction for the most lipophilic model compounds (malathion and methiocarb) was around 35 %.
- A reduced amount of model compound in the skin reduces the concentration gradient between skin and receptor causing reduced flux of the model compound.
- For the most hydrophilic model compounds, overall skin penetration was reduced by close to 67 % following skin wash, for lipophilic model compounds the effect was slightly less. Gentle washing removes not only what is left on the skin, but also a fraction of what is deposited in the upper part of stratum corneum.
- This observation has clear preventive implications, and documents the importance of washing hands following dermal exposure to chemicals.
On the implications of slight skin damage for dermal absorption as well as temporary deposition in the skin the following was concluded:
- Slightly damaged skin causes general increased dermal penetration for all model compounds.
- The increase is marginal for compounds with good penetration characteristics through uncompromised skin.
- The increased penetration is significant for the more lipophilic compounds, but the largest increase in penetration rate is seen for the more hydrophilic compounds.
- Washing the damaged skin after exposure significantly reduces skin deposition as well as skin penetration though it does not bring deposition and penetration down to a level comparable to uncompromised skin.
- The significantly increased penetration of especially the more hydrophilic compounds through slightly damaged skin may have regulatory consequences. Thus, traditional extrapolation from in vitro guideline studies may significantly underestimate the actual systemic exposure following dermal exposure in people with slightly damaged skin.
1 Indledning
- 1.1 Baggrund
- 1.2 Metode
- 1.3 In vitro model
- 1.4 Eksperimentelt design
- 1.5 Variabilitet og statistik
- 1.6 Kemiske analyser
- 1.7 Delstudier
- 1.8 Relevans
- 1.9 Internationale samarbejdspartnere
Mange års forebyggende indsats for at nedbringe luftvejseksponeringen for bekæmpelsesmidler i gartneri og landbrug betyder, at hudeksponering nu er dominerende (Archibald et al. 1994, Benford et al. 1999), selvom utilsigtet oral eksponering i enkelttilfælde også kan være betydende. Afhængig af pesticid vil aktivstoffet kunne genfindes på planter og jord i kortere eller længere tid efter udbringning. Eksponeringen sker hyppigst under re-entry aktiviteter, hvor planter håndteres kort tid efter, at de er blevet behandlet med pesticider. Selve absorptionen gennem huden er en flertrins passiv diffusions-proces. Nyere undersøgelser med få modelstoffer indikerer, at absorptionshastigheden blandt andet bestemmes af pesticidernes opløselighed, tilstedeværelsen af hjælpestoffer samt hudens beskyttelsesevne (Brand and Mueller 2002, Nielsen 2004, Nielsen et al. 2004). Miljøstyrelsens nuværende forvaltning af godkendelsesprocedurer for pesticider tager ikke højde for ændringer i hjælpestoffer til allerede godkendte salgsprodukter, midlertidig deponering i overhuden eller, at huden hos de eksponerede ikke altid er intakt. Der er derfor ikke alene et grundvidenskabeligt sigte med dette projekt i forhold til afdækning af faktorer af betydning for pesticiders passage af huden, men også klare regulerings- og forebyggelsesmæssige aspekter i forhold til Miljøstyrelsens rådgivning og regelsætning.
Projektet har følgende formål:
- Gennem anvendelse af en række modelstoffer at fastlægge et interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes.
- At beskrive den betydning den midlertidige ophobning i huden (reservoir-effekten) har i forhold til en forsinket absorption efter eksponeringsophør.
- At vurdere hvorvidt man ved afvaskning efter endt eksponering kan fjerne en del af det på huden deponerede pesticid eller, om det fortsat skal henregnes som absorberet.
- At vurdere den betydning en lettere beskadiget hud har for såvel absorption som midlertidig ophobning i huden.
1.1 Baggrund
Viden om pesticiders hudabsorption er fortsat begrænset, og offentligt tilgængelige undersøgelser har hidtil primært fokuseret på udvalgte aktivstoffernes penetrationsevne (Dick et al. 1997, Nielsen and Nielsen 2000, Cnubben et al. 2002, Nielsen et al. 2004). Virkeligheden er imidlertid, at de produkter, som man eksponeres for, er blandingsprodukter, der ud over aktivstoffer indeholder en række bærestoffer, fortykningsmidler, dispergeringsmidler og blødgørere; stoffer der under ét betegnes detergenter eller hjælpestoffer. Som en konsekvens af disse forhold foreskriver de seneste EU-guidelines for evaluering af hudpenetration og dermal toksicitet (EC Directive 91/414) da også testning af såvel aktivstoffer som salgsprodukt.
Et tidligere gennemført forskningsprojekt ved Miljømedicin i Odense har dokumenteret betydningen af disse hjælpestoffer for hudpenetrationen af aktivstoffer (Nielsen 2004). Således øges den samlede absorption for to undersøgte pesticider, når de administreres i deres salgsformuleringer. Mest betydende er dog den markante nedsættelse af lag-time, hvilket er tiden fra eksponeringsstart til at man kan måle pesticidet på undersiden af huden. Betydningen af lag-time kan illustreres ved nedenstående figur (Figur 1), der viser penetrationen af et modelstof i to forskellige formuleringer (forskellige hjælpestoffer) med samme totale penetration men klart forskellige lag-time og flux.
Manglende kendskab til lag-time vanskeliggør en relevant rådgivning i forhold til biologisk monitorering med blodprøver, hvor man risikerer at underestimere eller helt overse en igangværende eller nylig eksponering. En lag-time på fx 4 timer er således ikke et udtryk for, at stoffet sidder på hudoverfladen i 4 timer, før diffusionen gennem huden begynder, men et udtryk for at absorptionsprocessen gennem huden tager tid og er stofafhængig. Den passive absorption er således en flertrins-proces, hvor man initialt vil se en absorption fra den ofte hydrofile donorfase over huden, efterfulgt af en diffusion gennem huden med mulig midlertidig deponering (en reservoir-effekt) og afsluttende med en diffusion ud af huden til en receptor.
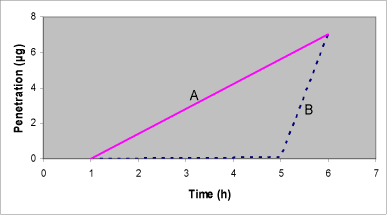
Figur 1. Teoretiske penetrationskurver for to stoffer med identisk totalpenetration efter 6 timer, men forskellig lag-time og flux.
Den passive diffusion fra den oftest hydrofile donor og ind i huden begunstiges af en vis grad af lipofilicitet. Dette er vist i et netop afsluttet EU-projekt ved Miljømedicin i Odense (Nielsen et al. 2004). Her observeredes for det meget hydrofile pesticid dimethoat kun en meget begrænset penetration, medens hovedparten af den administrerede dimethoat genfindes i donorvæsken ved forsøgsafslutning. Når et stof er trængt ind i huden, skal det videre til den generelle cirkulation, hvilket indebærer diffusion fra et lipofilt miljø i huden til en overvejende hydrofil modtager. I den eksperimentelle model svarer det til diffusionen fra huden og ned i receptorvæsken. Denne diffusion faciliteres af en ikke for høj lipofilicitet, idet en sådan vil betinge, at stoffet vil have en klar præference for at blive i huden. Det er sandsynligvis denne effekt, der ses ved forsøg med pesticidet prochloraz, hvor man trods høj lipofilicitet ikke genfinder betydende mængder pesticid i receptorvæsken (Nielsen 2004). Analog med denne konklusion beskriver også Brand og Mueller (2002), at de i en undersøgelse af tre pesticider observerer, at det mest lipofile pesticid har den dårligste penetration, men den største akkumulering i stratum corneum. De gennemførte undersøgelser indikerer således, at både en for høj og en for lav lipofilicitet begrænser hudpenetrationen af pesticider. Det første delmål i dette projekt bliver gennem anvendelse af en række pesticider/modelstoffer at fastlægge et interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes. Dette vil samtidig indikere, hvilke pesticider der grundet deres lipofilicitet absorberes i mindre grad.
Eksperimenter med lettere beskadiget hud har vist, at beskadigelsen primært har effekt på passagen fra donor og ind i huden (Nielsen 2004). Dette ses tydeligt ved markant ændrede penetrationsforhold for det meget hydrofile pesticid dimethoat (Nielsen 2004). Man må her forholde sig til, at en beskadiget hud potentielt giver anledning til en øget ophobning af stof i huden (reservoir effekt). Reservoir effekten er tidligere blevet diskuteret (Cnubben et al. 2002) og anvendt som en del af forklaringen på det forskellige penetrationsmønster for hydrofile og lipofile stoffer. Betydningen af denne deponering, og hvorvidt den vil lede til en øget men forsinket penetration, er hidtil kun meget sparsomt belyst. En undersøgelse af betydningen af opløselighed for reservoir-effekten indebærer en analyse af den mængde stof, der persisterer i huden ved eksponerings- og forsøgsophør, og som efterfølgende fortsat vil kunne absorberes. En enkelt helt ny undersøgelse i rotter har vist, at man ved testning af 19 forskellige pesticider observerede en fortsat absorption efter, at pesticiderne var vasket af huden for 17 af de 19 stoffer (Zendzian 2003). Den fortsatte penetration af disse stoffer gav imidlertid i kun halvdelen af tilfældene anledning til en forøget systemisk koncentration (Zendzian 2003), hvilket sandsynligvis er betinget af rotters hurtige metabolisme. Da betydelige forskelle eksisterer mellem penetration gennem rottehud og human hud, er der et påtrængende behov for at få denne problemstilling belyst i en eksperimentel human model. Det andet delmål i dette projekt er derfor at beskrive den betydning, som den midlertidige ophobning i huden (reservoir-effekten) har i forhold til en forsinket absorption efter eksponeringsophør. Fokus vil her være kortere eksponeringstider og inddragelse af også lettere beskadiget hud, idet man herved kommer nærmere virkelighedens eksponeringsforhold.
Arbejdsmiljømæssigt har fundene væsentlig betydning, idet hudbarrieren hos mange arbejdstagere og måske gartneriarbejdere mere specifikt ofte er kompromitteret grundet fysisk sår, rifter og/eller vådt arbejde. Det betyder, at regulering på basis af undersøgelser med intakt hud skal overvejes kritisk, idet man risikerer at underestimere den reelle absorption. Det vil her være væsentligt at vide, om det er ved de mest lipofile stoffer eller de mest hydrofile stoffer, at man begår den største fejl ved ikke at tage højde for, at den almindelige arbejdstagers hud sjældent er fuldstændig intakt.
Forebyggelsesmæssigt vil det i den forbindelse være væsentligt at vide, hvorvidt man ved afvaskning af hænderne har mulighed for at fjerne noget af den pesticidmængde der ligger i overfladen af stratum corneum – altså hvorvidt den mængde, der måles i huden ved forsøgsafslutning, faktisk bør henregnes som absorberet, eller hvorvidt en del kan vaskes ud. Guidelines for eksperimentelle undersøgelser af hudpenetration foreskriver, at den mængde, der forefindes i huden ved forsøgsafslutning, henregnes som absorberet. Spørgsmålet er, om det er en holdbar situation, og hvorvidt der er forskelle mellem de hydrofile og de lipofile pesticider i forhold til denne problematik. Det tredje delmål bliver derfor en undersøgelse af, hvorvidt man ved afvaskning efter endt eksponering kan fjerne en del af det på huden deponerede pesticid, eller om det fortsat skal henregnes som absorberet.
1.2 Metode
Projektet gennemføres under anvendelse af en in vitro diffusionscellemodel ved anvendelse af human hud. Den oprindelige model er beskrevet i OECD´s guidelines for undersøgelse af hudpenetration og er særdeles relevant for denne type undersøgelser, idet hudens barrierefunktion overvejende er bestemt af det epidermale lag af døde celler, stratum corneum (Grandjean 1990). Den eksperimentelle model tillader kvantitering og sammenligning af både transport igennem og temporær deposition i huden. Modellen har været anvendt på Miljømedicins laboratorium i en årrække, og laboratoriet har i 2002-2003 deltaget i en EU-finansieret valideringsrunde for modeller til studier af hudpenetration. Modellen har her såvel som i andre sammenhænge vist en god overensstemmelse med in vivo hudpenetrationsforsøg på mennesker (Ramsey et al. 1994, van de Sandt et al. 2004). Modellen er den bedste eksperimentelle mulighed for at tilvejebringe systematisk viden.
Der findes flere teoretiske modeller til beskrivelse af et molekyles transport gennem stratum corneum. En af de første brugbare modeller blev udviklet og visualiseret som ’brick and mortar’ modellen (Elias 1983). Senere er svenskeren Bo Forslind fremkommet med en lidt mere udbygget model (’the domain mosaic model’), der inddrog den seneste viden om stratum corneums opbygning (Forslind et al. 1997). Disse modeller vil danne udgangspunkt for en diskussion af en model for hudoptagelse af pesticider baseret på de i projektet opnåede resultater.

Figur 2. Diffusionscelle af glas til penetrationsforsøg.
1.3 In vitro model
Diffusionscellerne er af håndblæst glas og består af et donorkammer og et receptorkammer (figur 2). Huden, der stammer fra abdominalplastikker eller brystreduktioner foretaget på Odense Universitets-hospitals plastikkirurgiske afdeling, præpareres, monteres på et stålgitter og placeres mellem de to kamre med stratum corneum vendende mod donorkammeret. Udtørring af huden ved fordampning undgås og konstant luftfugtighed sikres ved at dække donorcellen med parafilm. Receptorvæsken (0,9% NaCl, 5% BSA, 0,1% hexamycin i vand), der fylder receptor-kammeret, omrøres konstant (magnetomrøring) for at undgå en koncentrationsgradient mellem top og bund i receptorkammeret. Diffusionscellerne placeres i vandbad (35oC) for at sikre en temperatur på omkring 32oC på hudoverfladen, svarende til normal hudtemperatur. Efter opsætning af huden henstår cellerne 16-18 timer med tomt donorkammer men med receptorvæske, hvorved der sikres en ekvilibrering i forhold til vandindhold i huden. Hudens integritet sikres ved kapacitansmåling før forsøg påbegyndes.
1.4 Eksperimentelt design
Et fast volumen af teststof appliceres på huden i donorkammeret. Der udtages med fastsatte intervaller prøver fra receptorkammeret af de applicerede stoffer. Det udtagne volumen erstattes med frisk receptorvæske, således at receptorvolumen holdes konstant. Koncentrationen af teststof måles i de udtagne prøver. Ved gentagne udtagninger over tid vil fluxen af teststof kunne bestemmes. Under forsøgene er der udtaget prøver efter typisk 4, 6, 8, 10, 12, 24, 30, og 48 timer afhængig af stoffernes forventede lag-time. I disse prøver bestemmes koncentrationen af de relevante teststoffer. Disse koncentrationer danner basis for penetrationskurver ud fra hvilke, den totale penetration over 48 timer samt den maksimale penetrationshastighed (fluxen) bestemmes. Kurveforløbene i nærværende forsøg kan beskrives ved en initiel periode (lag-fase), hvor der endnu ikke kan observeres nogen penetration. Lag-fasens udstrækning er ikke et udtryk for, at der ikke trænger pesticid ind i huden, men et udtryk for hvor lang tid der går, før pesticidet trænger gennem huden. Efter lagfasen observeres en penetration resulterende i stadig stigende koncentration af pesticid i receptorvæsken og dermed i de udtagne prøver. En kurve over penetrationen over tid har et tilnærmelsesvis sigmoidt forløb. Hældningen på den kurve er udtryk for penetrationshastigheden og betegnes fluxen. Da lag-fasens udstrækning varierer både mellem donorer og mellem pesticider, vil det kun sjældent være muligt at udtage prøver præcis ved den første gennemtrængning af hudmembranen. Lag-fasens udstrækning estimeres ved at ekstrapolere den lineære del af penetrationskurverne baglæns. Den rapporterede flux er den maksimale flux observeret gennem forsøgsperioden.
Alle tre mål har relevans i vurderingen af penetrationskarakteristika for et givet stof. Den totale mængde penetreret over en bestemt periodes eksponering, fx 48 timer, anvendes ofte som basis for risikovurdering eller anbefalinger i relation til anvendelse af handsker i arbejdsmiljøsituationer. Tallet bør dog, som det fremgår af figur 1 ikke stå alene, men suppleres med de to kinetiske mål, flux samt lag-time. Figuren viser således, at samme totale penetration kan fremkomme på basis af to helt forskellige penetrationskurver. I arbejdsmiljøsammenhænge vil der således ikke være tvivl om, hvilket stof man ville foretrække ved en eksponeringstid under 4-5 timer, medens anbefalingen muligvis ville ændres ved eksponeringstider omkring 6 timer eller længere.
Til beregning af massebalance bestemmes ved forsøgsafslutning mængden af teststof, der resterer i donorkammeret samt i huden. Resterende donorvæske fjernes fra huden ved opsugning med pipette og overføres til glas med skruelåg. Huden aftørres herefter med 6 cotton swabs pr. celle (4-5 stk. vædet med 50% AcCN, 1-2 stk. tørt), der overføres til et tælleglas; tilsættes 3 ml AcCN, hvorefter swabs henstår til ekstraktion i mindst 72 timer. Donorkammeret vaskes så med 1 ml 50% AcCN (skylles ned langs glas- væggen med pipette); væsken opsamles med pipette og overføres til glas med skruelåg. Glascellen skilles ad; huden forbliver på metalgitteret på receptordelen; epidermis skrabes forsigtigt af med en skalpel i det område, hvor teststoffet har ligget på huden (ca. 2,12 cm²); v.h.a. en pincet overføres epidermis til store tælleglas; huden tages herefter af metalgitteret og den hårde kant klippes af med en saks, den resterende bløde del kommes ligeledes over i store tælleglas. Til både epidermis og dermis sættes 3 ml 100 % AcCN; glassene whirli-mixes i få sekunder og henstår i mindst 72 timer til ekstraktion. Ekstrakter samt opsamlede væsker analyseres herefter for indhold af teststoffer.
1.5 Variabilitet og statistik
Anvendelsen af hud fra forskellige donorer betinger en naturlig heterogenicitet med deraf følgende interindividuel variation, der kan estimeres til omkring 60%. Med en power på 90%, et signifikansniveau på 5% og en standard deviation på 60% kan den krævede gruppestørrelse anslås til 13-15. Den intraindividuelle variation er imidlertid mindre end den interindividuelle og ved at sikre repræsentation af samme donor i både eksperimentel og kontrolgruppe, kan vi opnå valide resultater med gruppestørrelser på 6-8 diffusionsceller per stof (Nielsen and Nielsen 2000, Nielsen 2004, Nielsen et al. 2004) samtidig med at alle eksperimenter gentages to gange. For at illustrere den intereksperimentelle forskel, primært betinget af forskellige donorer, er resultaterne fra det første delstudie præsenteret som individuelle forsøg såvel som samlet. Tidligere forsøg har vist, at huden opretholder normal barrierefunktion i over 72 timer, hvilket muliggør både kortere og længere eksponeringsperioder.
1.6 Kemiske analyser
Udgangspunktet for analyser er enten HPLC (Nielsen and Nielsen 2000, Nielsen 2004, Nielsen et al. 2004) eller betatælling. Måling af mængden af pesticid i en prøve sker ved spektrofotometrisk måling i forhold til en standardkurve efter en primær separation ved hjælp af et HPLC apparatur. Separationen på HPLC sker, ved at stofferne presses gennem en kolonne, hvor stofferne tilbageholdes i forskellig grad afhængig af deres polaritet. I den anvendte opsætning betyder det, at jo mere polært et stof er, jo længere tid tager det om at passere. En del af de anvendte teststoffer forefindes som mærkede stoffer. At et stof er radioaktivt mærket betyder, at man har udskiftet et specificeret atom i molekylet, enten et 12C-atom eller et ²H-atom, med henholdsvis et 13C- eller ³H-atom. Det vil sige, at en fraktion af det samlede antal molekyler teststof udsender beta-stråling. De radioaktive teststoffer kan derfor kvantificeres ved hjælp af betatælling.
Tabel 1. Kemiske karakteristika for de 9 udvalgte modelstoffer.
| Modelstof | CAS-nummer | Mol-vægt (g/mol) |
Log Pow | Opløselighed (g/L vand) |
Retentionstid på HPLC (min) |
| Glyphosat | [1071-83-6] | 170 | -1.7 | 12 | * |
| Caffein | [58-08-2] | 194 | 0.16 | 21.7 | * |
| Dimethoate | [60-51-5] | 229.2 | 0.7 | 23.8 | 3.45 |
| Pirimicarb | [23103-98-2] | 238.3 | 1.7 | 3.0 | 3.41 |
| Benzosyre | [65-85-0] | 122 | 1.83 | 3.0 | * |
| Malathion | [121-75-5] | 330 | 2.75 | 0.15 | * |
| Paclobutrazol | [76738-62-0] | 293.8 | 3.2 | 0.026 | 4.50 |
| Methiocarb | [2032-65-7] | 225.3 | 3.34 | 0.027 | 5.17 |
| Prochloraz | [67747-09-5] | 376.7 | 4.4 | 0.034 | 4.96 |
* - Disse teststoffer forefindes som radioaktive stoffer og kvantiteres ved betatælling.
1.7 Delstudier
1.7.1 Opløselighedskarakteristikas betydning for absorptionen
I dette delstudie anvendes en række modelstoffer for fastlæggelse af et interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes. Tidligere studier har ofte alene målt mængden af stof, der kan genfindes i receptorfasen. I dette delstudie inkluderes måling af den del af dosis, der er deponeret i huden ved eksponeringsophør (reservoir-effekt). Forsøgene gennemføres med 48 timers eksponering og opsamling af prøver fra receptorvæsken på relevante tidspunkter i dette forløb. Ved afslutning bestemmes den mængde, der resterer i donorkammeret, den i huden deponerede mængde, samt den penetrerede mængde, således at der kan opstilles massebalancer ved forsøgene. Der vil i forsøgene blive anvendt infinite dose for at sikre penetrationskurver med mulighed for bestemmelse af maksimal flux. Der anvendes 5 pesticider (pirimicarb, methiocarb, paclobutrazol, dimethoat, prochloraz) som fortsat er i aktuel anvendelse i Danmark (prochloraz er senere fjernet fra listen af bekæmpelsesmidler godkendt til brug i Danamrk), og som kendes fra tidligere undersøgelser (Nielsen 2004). Disse pesticider dækker opløseligheder i vand fra 0.03 g/L til 24 g/L (tabel 1). De fem tidligere anvendte pesticider suppleres med 4 nye modelstoffer for at dække et bredt opløselighedsspektrum og udvælges på basis af resultater opnået med de 5 første stoffer. De 4 nye modelstoffer inkluderet i dette delstudie er 3 pesticider (glyphosat, benzosyre samt malathion) samt caffein. Antallet og arten af stoffer er udvalgt for at sikre data fra en tilstrækkelig bred vifte af opløseligheder og molvægte til at kunne anvendes ved diskussion af model for dermal pesticidoptagelse.
1.7.2 Betydning af afvaskning og let hudbeskadigelse for penetration
I dette delstudie anvendes dels intakt hud dels lettere beskadiget hud for at beskrive den betydning, som den midlertidige ophobning i huden (reservoir-effekten) har i forhold til en forsinket absorption efter eksponeringsophør. Endvidere undersøges, hvorvidt afvaskning efter endt eksponering kan fjerne en del af det på/i huden deponerede pesticid, eller om det kan henregnes som absorberet. Eksperimenter med beskadiget hud inkluderes, idet tidligere undersøgelser har indikeret, at beskadigelsen af stratum corneum kan ændre på deponeringsmønstret (Nielsen 2004).
Forsøgene gennemføres med 6 timers eksponering, hvorefter modelstofferne fjernes fra donorkammeret ved afsugning. For de grupper, hvor der også vaskes er proceduren at modelstoffet fjernes ved afsugning fra donorkammer efterfulgt af afvaskning med bomuldsklud vædet i sæbeopløsning afsluttende med 2 gange vask og afsugning af skyllevæske (samme som modelstoffet er opløst i). Herefter følger 42 timers fortsat måling af penetration fra huden og over til receptorkammeret. Lettere beskadiget hud, der anvendes i halvdelen af grupperne, opnås ved 3 timers forbehandling med en 0,3 % opløsning af SLS (natrium layryl sulfat), hvilket er en metode, der tidligere er anvendt og valideret på laboratoriet (Nielsen 2005). Metoden med SLS foretrækkes frem for eksempelvis tape-stripping, idet man ved en kemisk beskadigelse med SLS kan opnå en kvantiterbar og repeterbar gradueret beskadigelse af huden.
Delstudiet er planlagt til at inkludere 6 modelstoffer udvalgt blandt stoffer anvendt i delstudie 1 med forventet lag-time både over og under eksponeringstiden. Følgende stoffer indgår i delprojekt 2: glyphosat, caffein, dimethoate, benzosyre, malathion, og methiocarb. Der vil blive anvendt rene stoffer såvel som salgsformuleringer af dimethoate og methiocarb. Pesticiderne vil blive appliceret i koncentrationer svarende til de erhvervsmæssigt anvendte.
1.8 Relevans
Projektet tager udgangspunkt i de aktivstoffer, der anvendes i Danmark. De koncentrationer af aktivstoffer, der anvendes i de enkelte delstudier, vil være umiddelbart sammenlignelige med de anbefalede koncentrationer af aktivstof ved anvendelse i gartneri/landbrug. Oplysninger om disse koncentrationer er indhentet dels fra producent og dels fra brugerne af færdigprodukterne. Ved siden af pesticiderne er anvendt en række modelstoffer, der er udvalgt på baggrund af deres opløseligheds-karakteristika. Miljøstyrelsens nuværende forvaltning af godkendelsesprocedurer for pesticider tager ikke specifikt højde for ændringer i hjælpestoffer til allerede godkendte salgsprodukter, midlertidig deponering i overhuden eller at huden hos de eksponerede ikke altid er intakt. De udvalgte pesticider er alle på nær prochloraz i aktuel anvendelse i Danmark. Der er derfor ikke alene et grundvidenskabeligt sigte med dette projekt i forhold til afdækning af faktorer af betydning for pesticiders passage af huden, men også klare regulerings- og forebyggelsesmæssige aspekter i forhold til Miljøstyrelsens nuværende rådgivning og regelsætning.
1.9 Internationale samarbejdspartnere
Projektgruppen har via et netop gennemført EU-projekt knyttet tætte forbindelser til 6 Europæiske laboratorier, der primært foretager hudpenetrationsundersøgelser. Disse laboratorier har ikke pesticider som fokusområde, men arbejder med parallelle problemstillinger. Der planlægges derfor 1-2 korte besøg hos disse laboratorier med henblik på laboratorietekniske erfaringsudvekslinger, specielt i forhold til anvendelse af beskadiget hud.
2 Resultater
- 2.1 Betydning af stoffers opløselighed for absorptionsmængde og hastighed
- 2.2 Betydning af afvaskning og let hudbeskadigelse for penetration
2.1 Betydning af stoffers opløselighed for absorptionsmængde og hastighed
Den dermale absorption begrænses af såvel en for høj lipofilicitet som en for lav lipofilicitet. Det har umiddelbart betydning ved formuleringer af produkter til dermal applicering (typisk farmaka samt kosmetikprodukter) samt ved formulering af for eksempel pesticider, hvor man tilstræber en så effektiv penetration af den ydre membran hos mål-organismen (plante eller skadedyr). Viden om det interval, hvor den største og/eller hurtigste absorption foregår, har imidlertid også betydning for den humane risikovurdering og muligheden for en optimeret forebyggelse. Formålet med dette delstudie var således gennem anvendelse af en række modelstoffer at fastlægge et interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes. Andre faktorer end lipofilicitet har dog også betydning for kemiske stoffers penetration gennem huden, idet den molekylære størrelse både udtrykt som molvægt og stereokemisk kan virke hæmmende og/eller blokerende for hudpenetrataionen. De anvendte modelstoffer repræsenterer derfor et betydeligt interval for opløselighed såvel som et relevant molvægts-interval.
For hvert modelstof præsenteres den maksimale flux, penetrationskoefficienten Kp (Kp er defineret som: maksimal flux divideret med koncentrationen af teststof i donor, hvilket betyder at Kp teoretisk er koncentrationsuafhængig), lag-time, huddeponering (epidermis samt dermis), total penetration samt genfinding, ligesom den resterende og ikke-absorberede mængde modelstof i donorkammeret er bestemt.
2.1.1 Glyphosat
Glyphosat blev påsat i en mængde på 424 µg svarende til en koncentration i donorkammeret på 4 mg/mL. Der observeres en betydelig forskel mellem de to delforsøg, der må tilskrives forskelle donorerne imellem (Tabel 2). Den maksimale flux findes som hældningen på det lineære stykke af penetrationskurven (Figur 3), og beregnes for de samlede data til 23,6 ng/cm²*t (0,139 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 59,0 nm/t (Tabel 2). Den totale mængde glyphosat absorberet over membranen på 2,12 cm² i løbet af 48 timer var 743 ng/cm² (Tabel 2). Lag-time findes til knap 8 timer (Figur 3, Tabel 2).
Tabel 2. Penetration data for Glyphosat. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 05-9 | MST 05-10 | All | |
| N | 7 | 7 | 14 |
| Maximal flux (ng/cm2*h) | 17.8 ± 4.6 | 29.4 ± 11.1 | 23.6 ± 2.7 |
| Kp (nm/h) | 44.5 | 73.5 | 59.0 |
| Lag-time (h) | 8.5 ± 7.4 | 7.7 ± 4.0 | 7.9 ± 1.5 |
| Epidermis deposition (% of dose) | 0.7 ± 0.2 | 0.4 ± 0.2 | 0.5 ± 0.1 |
| Dermis deposition (% of dose) | 0.3 ± 0.2 | 0.1 ± 0.1 | 0.2 ± 0.1 |
| Skin deposition (% of dose) | 0.9 ± 0.3 | 0.5 ± 0.2 | 0.7 ± 0.1 |
| Donor recovery (% of dose) | 81.4 ± 6.2 | 100.5 ± 3.1 | 91.0 ± 2.9 |
| Receptor recovery (% of dose) | 0.3 ± 0.1 | 0.4 ± 0.2 | 0.4 ± 0.1 |
| Overall recovery (µg) | 351 ± 25 | 430 ± 13 | 390 ± 12 |
| Overall recovery (% of dose) | 82.7 ± 6.0 | 101.4 ± 3.0 | 92.0 ± 2.9 |
| Skin penetration (ng/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 3h | 42 ± 37 | 3 ± 9 | 23 ± 9 |
| T = 6h | 44 ± 40 | 40 ± 50 | 42 ± 12 |
| T = 9h | 83 ± 66 | 84 ± 94 | 84 ± 21 |
| T = 12h | 123 ± 87 | 177 ± 118 | 150 ± 28 |
| T = 15h | 153 ± 80 | 253 ± 121 | 203 ± 30 |
| T = 24h | 286 ± 113 | 428 ± 218 | 357 ± 49 |
| T = 30h | 334 ± 175 | 548 ± 293 | 441 ± 69 |
| T = 48h | 603 ± 266 | 883 ± 417 | 743 ± 98 |
Den totale glyphosat-deponering i huden efter 48 timer var 0,7 % af den påsatte mængde, hvilket fordelte sig med 0,5 % i epidermis og 0,2 % i dermis (Tabel 2). Kun en meget begrænset mængde glyphosat absorberedes i løbet af de 48 timer, og langt hovedparten af den påsatte mængde glyphosat var fortsat at finde i donorkammeret ved forsøgets afslutning efter 48 timer (Tabel 2). Der var en utilfredsstillende lav donor recovery i det ene forsøg, hvilket resulterer i en overall genfinding på gennemsnitlig 92 %.
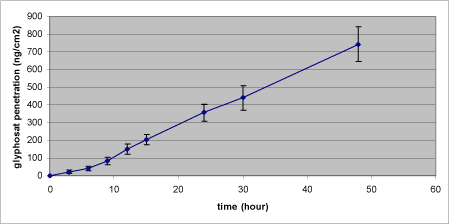
Figur 3. Dermal penetration for glyphosat.
2.1.2 Caffein
Caffein blev påsat i en mængde på 424 µg svarende til en koncentration i donorkammeret på 4 mg/mL. Der observeres en udmærket overensstemmelse mellem de to delforsøg, idet deponeringen i huden dog er klart forskellig (Tabel 3). Den maksimale flux findes som hældningen på det stejleste, lineære stykke af penetrationskurven (Figur 4), og beregnes for de samlede data til 1,51 µg/cm²*t (7,78 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 3,78 µm/t (Tabel 3). Den totale mængde caffein absorberet over membranen på 2,12 cm² i løbet af 48 timer var 37,4 µg/cm² (Tabel 3). Lag-time findes at være knap 7 timer (Figur 4, Tabel 3).
Table 3. Penetration data for Caffein. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 05-9 | MST 05-10 | All | |
| N | 8 | 9 | 17 |
| Maximal flux (µg/cm2*h) | 1.29 ± 0,44 | 1.72 ± 1.27 | 1.51 ± 0.97 |
| Kp (µm/h) | 3,22 | 4.30 | 3.78 |
| Lag-time (h) | 7.0 ± 0.7 | 6.7 ± 2.2 | 6.9 ± 1.7 |
| Epidermis deposition (% of dose) | 5.5 ± 2.3 | 1.5 ± 1.2 | 3.4 ± 2.6 |
| Dermis deposition (% of dose) | 5.3 ± 1.7 | 2.1 ± 0.7 | 3.6 ± 2.1 |
| Skin deposition (% of dose) | 10.8 ± 3.0 | 3.7 ± 1.3 | 7.0 ± 4.3 |
| Donor recovery (% of dose) | 68.9 ± 8.7 | 76.7 ± 10.0 | 72.8 ± 9.9 |
| Receptor recovery (% of dose) | 19.8 ± 7.3 | 19.0 ± 9.6 | 18.7 ± 8.5 |
| Overall recovery (µg) | 422 ± 5 | 423 ± 4 | 422 ± 4 |
| Overall recovery (% of dose) | 99.6 ± 1.1 | 99.7 ± 1.0 | 99.6 ± 1.0 |
| Skin penetration (µg/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 3h | 0.07 ± 0.05 | 0.23 ± 0.32 | 0.15 ± 0.06 |
| T = 6h | 0.85 ± 0.46 | 2.21 ± 2.90 | 1.57 ± 0.53 |
| T = 9h | 2.74 ± 1.30 | 5.99 ± 6.89 | 4.46 ± 1.26 |
| T = 12h | 6.26 ± 2.73 | 10.79 ± 10.68 | 8.66 ± 1.96 |
| T = 15h | 10.08 ± 4.17 | 15.45 ± 13.86 | 12.92 ± 2.55 |
| T = 24h | 21.56 ± 7.69 | 24.55 ± 17.17 | 23.14 ± 3.21 |
| T = 30h | 27.17 ± 9.45 | 28.21 ± 18.19 | 27.72 ± 3.46 |
| T = 48h | 39.68 ± 14.61 | 35.43 ± 19.64 | 37.43 ± 4.13 |
Den totale caffein-deponering i huden efter 48 timer var 7,0 % af den påsatte mængde, hvilket fordelte sig ligeligt med 3,4 % i epidermis og 3,6 % i dermis (Tabel 3). Knap 20 % af den påsatte mængde caffein absorberedes i løbet af de 48 timer, mens hovedparten af den påsatte mængde caffein fortsat var at finde i donorkammeret ved forsøgets afslutning efter 48 timer (Tabel 3). Der var en tilfredsstillende overall genfinding på 100 %.
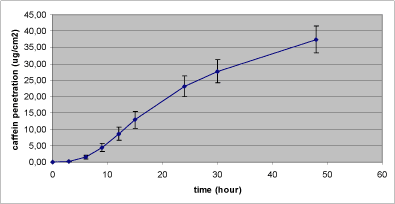
Figur 4. Dermal penetration for caffein.
2.1.3 Dimethoate
Dimethoat blev påsat i en mængde på 137,5 µg svarende til en koncentration i donorkammeret på 229 µg/mL. De to uafhængige forsøg med dimethoat viser udmærket overensstemmelse i forhold til de beregnede penetrationsparametre (Tabel 4). Den maksimale flux findes som hældningen på penetrationskurven mellem 24 og 42 timer (Figur 5), og beregnes for de samlede data til 0,11 µg/cm²*t (0,48 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 4,9 µm/t (Tabel 4). Den totale mængde dimethoat absorberet over membranen på 2,12 cm² i løbet af 42 timer var 2,41 µg/cm² (Tabel 4). Lag-time findes at være godt 22 timer (Figur 5, Tabel 4).
Tabel 4. Penetration data for Dimethoat. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 05-1 | MST 05-2 | All | |
| N | 8 | 6 | 14 |
| Maximal flux (µg/cm2*h) | 0.10 ± 0.06 | 0.13 ± 0.07 | 0.11 ± 0.02 |
| Kp (um/h) | 4.5 | 5.5 | 4.9 |
| Lag-time (h) | 23.3 ± 4.9 | 20.9 ± 3.5 | 22.3 ± 1.2 |
| Epidermis deposition (% of dose) | 0.4 ± 0.3 | 0.5 ± 0.3 | 0.4 ± 0.1 |
| Dermis deposition (% of dose) | 1.3 ± 0.6 | 1.7 ± 0.6 | 1.5 ± 0.2 |
| Skin deposition (% of dose) | 1.7 ± 0.6 | 2.2 ± 0.7 | 1.9 ± 0.2 |
| Donor recovery (% of dose) | 101.2 ± 6.6 | 108.3 ± 5.9 | 104.5 ± 1.7 |
| Receptor recovery (% of dose) | 5.7 ± 3.3 | 4.2 ± 2.6 | 5.1 ± 0.8 |
| Overall recovery (µg) | 149.3 ± 4.8 | 151.9 ± 7.3 | 150.5 ± 1.6 |
| Overall recovery (% of dose) | 108.5 ± 3.5 | 110.5 ± 5.3 | 109.4 ± 1.2 |
| Skin penetration (µg/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 12h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 15h | 0.02 ± 0.06 | 0.0 ± 0.0 | 0.01 ± 0.00 |
| T = 18h | 0.11 ± 0.16 | 0.0 ± 0.0 | 0.06 ± 0.02 |
| T = 24h | 0.32 ± 0.47 | 0.48 ± 0.54 | 0.39 ± 0.10 |
| T = 36h | 1.30 ± 1.08 | 1.90 ± 1.23 | 1.56 ± 0.42 |
| T = 42h | 2.14 ± 1.50 | 2.73 ± 1.68 | 2.40 ± 0.64 |
| T = 60h | 3.70 ± 2.15 | ||
Den totale dimethoat-deponering i huden efter 42 timer var knap 2 % af den påsatte mængde, hvilket fordelte sig med 0,4 % i epidermis og 1,5 % i dermis (Tabel 4). Kun en begrænset mængde dimethoat absorberedes i løbet af de 42 timer, og langt hovedparten af den påsatte mængde dimethoat var fortsat at finde i donorkammeret ved forsøgets afslutning efter 42 timer (Tabel 4). Der var en genfinding på gennemsnitlig 109 %.
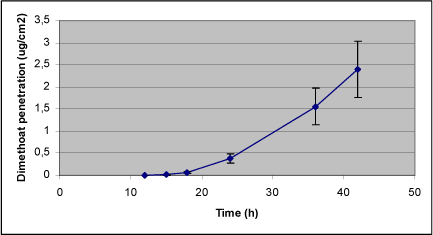
Figur 5. Dermal penetration for Dimethoat.
2.1.4 Pirimicarb
Pirimicarb blev påsat i en mængde af 21,7 µg, svarende til en koncentration i donorkammeret på 36,2 µg/mL. De to uafhængige forsøg med pirimicarb viser en signifikant kortere lag-time (12 timer) i forsøg 04-2.2 i forhold til forsøg 04-1 (19 timer) (Tabel 5) som udtryk for en kortere passagetid og/eller mindre reservoir i huden fra de i forsøg 04-2.2 anvendte donorer. Den maksimale flux findes som hældningen på det lineære stykke af penetrationskurven for de samlede data for pirimicarb (Figur 6), og beregnes til 0,10 µg/cm²*t (0,42 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 27,7 µm/t (Tabel 5).
Tabel 5. Penetration data for Pirimicarb. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 04-1 | MST 04-2.2 | All | |
| N | 8 | 8 | 16 |
| Maximal flux (µg/cm2*h) | 0.09 ± 0.02 | 0.11 ± 0.02 | 0.10 ± 0.01 |
| Kp (um/h) | 24.6 | 30.9 | 27.7 |
| Lag-time (h) | 18.9 ± 1.0 | 11.6 ± 1.9 | 15.2 ± 1.0 |
| Epidermis deposition (% of dose) | 2.5 ± 2.9 | 0.6 ± 0.3 | 1.5 ± 0.6 |
| Dermis deposition (% of dose) | 11.4 ± 6.4 | 8.0 ± 3.3 | 9.7 ± 1.3 |
| Skin deposition (% of dose) | 13.9 ± 5.7 | 8.6 ± 3.5 | 11.2 ± 1.3 |
| Donor recovery (% of dose) | 53.8 ± 13.4 | 51.2 ± 9.2 | 52.5 ± 2.8 |
| Receptor recovery (% of dose) | 25.5 ± 7.4 | 42.7 ± 5.8 | 34.1 ± 2.5 |
| Overall recovery (µg) | 20.2 ± 2.5 | 21.6 ± 0.5 | 20.9 ± 0.5 |
| Overall recovery (% of dose) | 93.1 ± 11.3 | 99.5 ± 2.5 | 96.3 ± 2.1 |
| Skin penetration (µg/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 6h | 0.0 ± 0.0 | 0.11 ± 0.08 | 0.05 ± 0.02 |
| T = 8h | 0.05 ± 0.05 | 0.22 ± 0.16 | 0.14 ± 0.04 |
| T = 12h | 0.14 ± 0.10 | 0.46 ± 0.24 | 0.30 ± 0.06 |
| T = 24h | 0.47 ± 0.18 | 1.53 ± 0.37 | 1.00 ± 0.15 |
| T = 30h | 1.03 ± 0.51 | 2.44 ± 0.53 | 1.73 ± 0.22 |
| T = 48h | 2.61 ± 0.76 | 4.38 ± 0.59 | 3.49 ± 0.28 |
Den kortere lag-time i det ene forsøg betyder også en større totalpenetration over de 48 timer (4,4 versus 2,6 µg/cm², ligesom receptor recovery af samme grund var signifikant højere i forsøg 04-2.2 end i forsøg 04-1 (Table 5). Den totale mængde pirimicarb der gennemsnitligt blev absorberet over membranen på 2,12 cm² i løbet af 48 timer, var 3,5 µg/cm² (Tabel 5). Den totale deponering i huden efter 48 timer var i snit 11 % af den påsatte mængde, hvilket fordelte sig med 1,5 % i epidermis og 10 % i dermis (Tabel 5). Gennemsnitlig en tredjedel af den påsatte mængde pirimicarb absorberedes i løbet af de 48 timer, medens omkring halvdelen af den påsatte mængde pirimicarb var fortsat at finde i donorkammeret ved forsøgets afslutning efter 48 timer (Tabel 5). Der var en genfinding på gennemsnitlig 96 %.
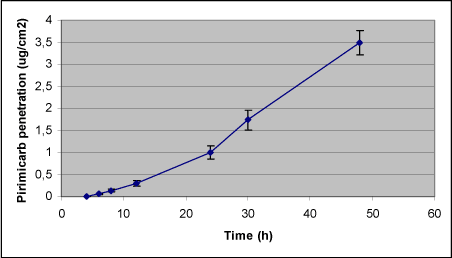
Figur 6. Dermal penetration for Pirimicarb.
2.1.5 Benzosyre
Benzosyre blev påsat i en mængde af 424 µg, svarende til en koncentration i donorkammeret på 4 mg/mL. De to uafhængige forsøg med benzosyre viser udmærket overensstemmelse i forhold til de beregnede penetrationsparametre (Tabel 6). Den maksimale flux findes som hældningen på det initiale lineære stykke af penetrationskurven (Figur 7), og beregnes til 20 µg/cm²*t (0,16 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 50,6 µm/t (Tabel 6). Den totale mængde benzosyre absorberet over membranen på 2,12 cm² i løbet af 48 timer var 187 µg/cm² (Tabel 6). Lag-time findes at være 1,5 timer (Figur 7, Tabel 6).
Tabel 6. Penetration data for Benzosyre. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 04-3 | MST 04-4 | All | |
| N | 8 | 8 | 16 |
| Maximal flux (ug/cm2*h) | 18.9 ± 4.5 | 21.6 ± 4.1 | 20.2 ± 1.1 |
| Kp (um/h) | 47.2 | 54.0 | 50.6 |
| Lag-time (h) | 1.2 ± 1.0 | 1.8 ± 1.1 | 1.5 ± 0.3 |
| Epidermis deposition (% of dose) | 0.3 ± 0.1 | 0.5 ± 0.2 | 0.4 ± 0.1 |
| Dermis deposition (% of dose) | 1.2 ± 0.4 | 1.0 ± 0.2 | 1.1 ± 0.1 |
| Skin deposition (% of dose) | 1.4 ± 0.5 | 1.5 ± 0.3 | 1.5 ± 0.1 |
| Donor recovery (% of dose) | 4.5 ± 2.0 | 3.9 ± 1.0 | 4.2 ± 0.4 |
| Receptor recovery (% of dose) | 93.7 ± 3.2 | 93.0 ± 2.9 | 93.4 ± 0.7 |
| Overall recovery (µg) | 422 + 11 | 417 + 8 | 420 + 10 |
| Overall recovery (% of dose) | 99.6 ± 2.5 | 98.5 ± 2.0 | 99.0 ± 0.6 |
| Skin penetration (ug/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 56.8 ± 29.1 | 51.0 ± 32.6 | 53.9 ± 7.5 |
| T = 6h | 94.5 ± 37.3 | 94.2 ± 39.5 | 94.4 ± 9.3 |
| T = 8h | 118.5 ± 36.7 | 121.7 ± 35.3 | 120.1 ± 8.7 |
| T = 12h | 151.4 ± 26.6 | 152.9 ± 25.2 | 152.1 ± 6.3 |
| T = 24h | 177.7 ± 10.5 | 176.5 ± 11.8 | 177.1 ± 2.7 |
| T = 30h | 180.9 ± 8.0 | 180.4 ± 9.4 | 180.7 ± 2.1 |
| T = 48h | 187.4 ± 6.4 | 186.1 ± 5.9 | 186.7 ± 1.5 |
Den totale benzosyre-deponering i huden efter 48 timer var 1,5 % af den påsatte mængde, hvilket fordelte sig med 0,4 % i epidermis og 1,1 % i dermis (Tabel 6). Kun en begrænset mængde benzosyre var tilbage i donorkammeret (4 %) efter 48 timer, idet langt hovedparten af den påsatte mængde benzosyre var absorberet og kunne findes i receptorkammeret ved forsøgets afslutning efter 48 timer (Tabel 6). Penetrationskurven viser da også den udfladning, der indikerer snarlig ligevægt i den passive diffusion mellem donorkammer og receptorkammer. Der var en genfinding på gennemsnitlig 99 %.
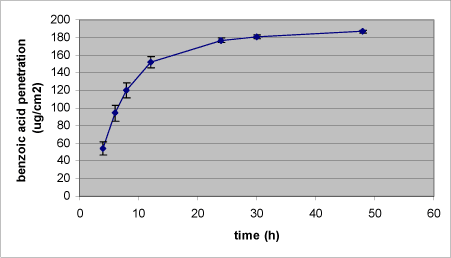
Figur 7. Dermal penetration for benzosyre.
2.1.6 Malathion
Malathion blev påsat i en mængde af 212 µg svarende til en koncentration i donorkammeret på 2 mg/mL. De 18 celler viser udmærket overensstemmelse uden tilstedeværelse af ekstreme celler medførende store spredninger (Tabel 7). Den maksimale flux findes som hældningen på det initiale lineære stykke af penetrationskurven indtil 14 timer (Figur 8), og beregnes til 371 ng/cm²*t (1,12 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 1,85 µm/t (Tabel 7). Den totale mængde malathion absorberet over membranen på 2,12 cm² i løbet af 48 timer var 11,6 µg/cm² (Tabel 7). Lag-time findes at være 2,9 timer (Figur 8, Tabel 7).
Tabel 7. Penetration data for Malathion. Resultaterne er angivet som middelværdi + SEM for det samlede resultat.
| MST 05-13 | |
| N | 18 |
| Maximal flux (ng/cm2*h) | 371 ± 36 |
| Kp (um/h) | 1.85 |
| Lag-time (h) | 2.9 ± 0.3 |
| Epidermis deposition (% of dose) | 2.7 ± 0.2 |
| Dermis deposition (% of dose) | 5.7 ± 0.8 |
| Skin deposition (% of dose) | 8.4 ± 0.9 |
| Donor recovery (% of dose) | 71.4 ± 1.7 |
| Receptor recovery (% of dose) | 11.6 ± 1.0 |
| Overall recovery (µg) | 194 + 2 |
| Overall recovery (% of dose) | 91.4 ± 0.7 |
| Skin penetration (ng/cm2) | |
| T = 0h | 0 ± 0 |
| T= 2h | 60 ± 15 |
| T = 4h | 548 ± 101 |
| T = 6h | 1445 ± 325 |
| T = 8h | 1994 ± 258 |
| T = 12h | 3423 ± 365 |
| T = 14h | 4076 ± 416 |
| T = 24h | 6564 ± 598 |
| T = 30h | 7986 ± 712 |
| T = 48h | 11559 ± 971 |
Den totale malathion-deponering i huden efter 48 timer var 8,4 % af den påsatte mængde, hvilket fordelte sig med 2,7 % i epidermis og 5,7 % i dermis (Tabel 7). En betydelig mængde malathion var tilbage i donorkammeret (71 %) efter 48 timer, medens alene 12 % af den påsatte mængde malathion var absorberet og kunne findes i receptorkammeret ved forsøgets afslutning efter 48 timer (Tabel 7). Penetrationskurven viser udmærket linearitet, idet der dog bemærkes en mindre reduktion i penetrationshastigheden (hældningen) det sidste døgn. Der var en genfinding på gennemsnitlig 91 %.
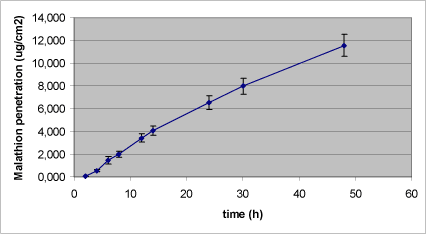
Figur 8. Dermal penetration for malathion.
2.1.7 Methiocarb
Methiocarb blev påsat i en mængde af 18,8 µg svarende til en koncentration i donorkammeret på 31,3 µg/mL. De to uafhængige forsøg med methicarb viser udmærket overensstemmelse i forhold til de beregnede penetrationsparametre (Tabel 8). Den maksimale flux findes som hældningen på det lineære stykke af penetrationskurven (Figur 9), og beregnes til 0,12 µg/cm²*t (0,53 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 38,6 µm/t (Tabel 8). Den totale mængde methiocarb absorberet over membranen på 2,12 cm² i løbet af 48 timer var 4,51 µg/cm² (Tabel 8). Lag-time findes at være knap 12 timer (Figur 9, Tabel 8).
Tabel 8. Penetration data for Methiocarb. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 04-3 | MST 04-4 | All | |
| N | 7 | 7 | 14 |
| Maximal flux (µg/cm2*h) | 0.12 ± 0.04 | 0.12 ± 0.02 | 0.12 ± 0.01 |
| Kp (um/h) | 38.6 | 38.6 | 38.6 |
| Lag-time (h) | 8.6 ± 5.1 | 14.8 ± 5.8 | 11.7 ± 1.6 |
| Epidermis deposition (% of dose) | 2.3 ± 1.3 | 2.6 ± 2.1 | 2.4 ± 0.5 |
| Dermis deposition (% of dose) | 17.8 ± 10.9 | 29.3 ± 11.9 | 23.5 ± 3.3 |
| Skin deposition (% of dose) | 20.0 ± 11.9 | 31.9 ± 13.3 | 26.0 ± 3.6 |
| Donor recovery (% of dose) | 14.3 ± 7.5 | 19.8 ± 9.3 | 17.1 ± 2.3 |
| Receptor recovery (% of dose) | 54.1 ± 12.7 | 47.8 ± 23.5 | 50.9 ± 4.9 |
| Overall recovery (µg) | 16.6 ± 0.3 | 18.8 ± 0.8 | 17.7 ± 0.3 |
| Overall recovery (% of dose) | 88.5 ± 1.8 | 100.3 ± 4.3 | 94.4 ± 1.8 |
| Skin penetration (µg/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 6h | 0.06 ± 0.11 | 0 ± 0 | 0.03 ± 0.02 |
| T = 8h | 0.12 ± 0.14 | 0.09 ± 0.13 | 0.11 ± 0.04 |
| T = 12h | 0.48 ± 0.28 | 0.25 ± 0.26 | 0.37 ± 0.08 |
| T = 24h | 1.89 ± 0.73 | 1.32 ± 1.11 | 1.60 ± 0.25 |
| T = 30h | 2.74 ± 0.93 | 2.10 ± 1.39 | 2.42 ± 0.32 |
| T = 48h | 4.78 ± 1.12 | 4.23 ± 2.08 | 4.51 ± 0.44 |
Den totale methiocarb-deponering i huden efter 48 timer var 26 % af den påsatte mængde, hvilket fordelte sig med 2,4 % i epidermis og 23,5 % i dermis (Tabel 8). Omkring halvdelen af den påsatte mængde methiocarb absorberedes i løbet af de 48 timer og kunne genfindes i receptorkammeret, medens 17 % af den påsatte mængde methiocarb fortsat var at finde i donorkammeret ved forsøgets afslutning efter 48 timer (Tabel 8). Der var en genfinding på gennemsnitlig 94 %.
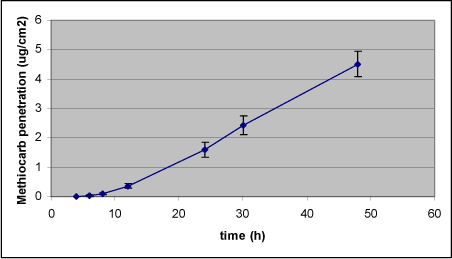
Figur 9. Dermal penetration for methiocarb.
2.1.8 Paclobutrazol
Paclobutrazol blev påsat i en mængde af 30,0 µg, svarende til en koncentration i donorkammeret på 49,9 µg/mL. De to uafhængige forsøg med paclobutrazol viser en signifikant kortere lag-time (13 timer) i forsøg 04-2.2 i forhold til forsøg 04.1 (24 timer) (Tabel 9) som udtryk for en længere passagetid og/eller større reservoir i huden fra de i forsøg 04-1 anvendte donorer. Dette er en analog observation med det ene forsøg med pirimicarb, hvor de samme humane donorer indgår. Den maksimale flux findes som hældningen på det lineære stykke af penetrationskurven for de samlede data for paclobutrazol (Figur 10), og beregnes til 0,15 µg/cm²*t (0,51 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 29,2 µm/t (Tabel 9).
Tabel 9. Penetration data for Paclobutrazol. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 04-1 | MST 04-2.2 | All | |
| N | 8 | 8 | 16 |
| Maximal flux (µg/cm2*h) | 0.15 ± 0.05 | 0.14 ± 0.04 | 0.15 ± 0.01 |
| Kp (um/h) | 30.4 | 27.9 | 29.2 |
| Lag-time (h) | 24.0 ± 0.0 | 12.9 ± 4.5 | 18.4 ± 1.6 |
| Epidermis deposition (% of dose) | 5.9 ± 1.2 | 1.5 ± 0.5 | 3.7 ± 0.6 |
| Dermis deposition (% of dose) | 19.1 ± 5.2 | 14.9 ± 4.4 | 17.0 ± 1.3 |
| Skin deposition (% of dose) | 24.9 ± 5.8 | 16.5 ± 4.8 | 20.7 ± 1.7 |
| Donor recovery (% of dose) | 42.6 ± 7.4 | 39.6 ± 10.9 | 41.1 ± 2.3 |
| Receptor recovery (% of dose) | 12.4 ± 3.4 | 33.1 ± 11.4 | 23.5 ± 3.4 |
| Overall recovery (µg) | 23.7 ± 1.7 | 26.7 ± 1.8 | 25.2 ± 0.6 |
| Overall recovery (% of dose) | 79.0 ± 5.7 | 89.2 ± 6.1 | 84.1 ± 2.0 |
| Skin penetration (µg/cm2) | |||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 6h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 8h | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 12h | 0 ± 0 | 0.18 ± 0.23 | 0.10 ± 0.05 |
| T = 24h | 0 ± 0 | 1.29 ± 0.85 | 0.68 ± 0.22 |
| T = 30h | 0.94 ± 0.30 | 2.37 ± 1.10 | 1.70 ± 0.27 |
| T = 48h | 1.76 ± 0.48 | 4.68 ± 1.62 | 3.31 ± 0.48 |
Den kortere lag-time i det ene forsøg betyder også en større totalpenetration over de 48 timer (16 versus 6 nmol/cm²), ligesom receptor recovery af samme grund var signifikant højere i forsøg 04-2.2 end i forsøg 04-1 (Tabel 9). Den totale mængde pirimicarb, der gennemsnitligt blev absorberet over membranen på 2,12 cm² i løbet af 48 timer, var 3,31 µg/cm² (Tabel 9). Den totale deponering i huden efter 48 timer var i gennemsnit 21 % af den påsatte mængde, hvilket fordelte sig med 4 % i epidermis og 17 % i dermis (Tabel 9). Gennemsnitlig en fjerdedel af den påsatte mængde paclobutrazol absorberedes i løbet af de 48 timer, medens omkring 40 % af den påsatte mængde paclobutrazol fortsat var at finde i donorkammeret ved forsøgets afslutning efter 48 timer (Tabel 9). Der var en genfinding på gennemsnitlig 84 %.
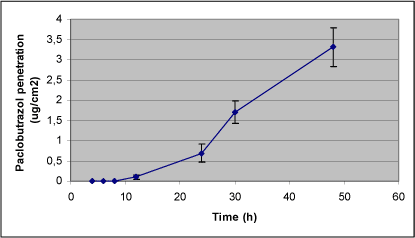
Figur 10. Dermal penetration for paclobutrazol.
2.1.9 Prochloraz
Prochloraz blev påsat i en mængde af 25,8 µg svarende til en koncentration i donorkammeret på 42,9 µg/mL. De to uafhængige forsøg med prochloraz viser en kortere lag-time (18 timer) i forsøg 05-2 i forhold til forsøg 05.1 (24 timer) (Tabel 10). En lav initial flux i forsøg 05-2 gør imidleretid, at denne forskel ikke influerer betydende på de øvrige penetrationsparametre. Den maksimale flux findes som hældningen på det lineære stykke af penetrationskurven for de samlede data for prochloraz (Figur 11), og beregnes til 0,08 µg/cm²*t (0,21 nmol/ cm²*t), hvilket resulterer i en Kp-værdi på 18,6 µm/t (Tabel 10).
Tabel 10. Penetration data for Prochloraz. Resultaterne er angivet som middelværdier + SD for de to uafhængige forsøg, og som middelværdi + SEM for det samlede resultat.
| MST 05-1 | MST 05-2 | All | |
| N | 8 | 7 | 15 |
| Maximal flux (µg/cm2*h) | 0.08 ± 0.10 | 0.07 ± 0.02 | 0.08 ± 0.02 |
| Kp (um/h) | 18.6 | 16.3 | 18.6 |
| Lag-time (h) | 24.0 ± 0.0 | 17.7 ± 4.0 | 21.1 ± 1.1 |
| Epidermis deposition (% of dose) | 4.0 ± 1.6 | 4.5 ± 1.6 | 4.2 ± 0.4 |
| Dermis deposition (% of dose) | 27.6 ± 10.6 | 27.3 ± 9.3 | 27.5 ± 2.5 |
| Skin deposition (% of dose) | 31.6 ± 11.8 | 31.8 ± 10.5 | 31.7 ± 2.8 |
| Donor recovery (% of dose) | 58.0 ± 15.1 | 58.6 ± 15.6 | 58.3 ± 3.8 |
| Receptor recovery (% of dose) | 14.5 ± 13.6 | 13.0 ± 7.6 | 13.7 ± 2.7 |
| Overall recovery (µg) | 26.0 ± 1.3 | 26.5 ± 0.3 | 26.2 ± 0.2 |
| Overall recovery (% of dose) | 100.7 ± 5.0 | 102.8 ± 1.0 | 101.7 ± 1.0 |
| Skin penetration (µg/cm2) | |||
| T = 0h | 0 ± 0 | 0.0 ± 0.0 | 0.0 ± 0.0 |
| T = 12h | 0.0 ± 0.0 | 0.0 ± 0.0 | 0.0 ± 0.0 |
| T = 15h | 0.0 ± 0.0 | 0.14 ± 0.17 | 0.07 ± 0.03 |
| T = 18h | 0.0 ± 0.0 | 0.24 ± 0.27 | 0.11 ± 0.06 |
| T = 24h | 0.0 ± 0.0 | 0.56 ± 0.51 | 0.26 ± 0.11 |
| T = 36h | 0.95 ± 1.19 | 1.37 ± 0.76 | 1.15 ± 0.29 |
| T = 42h | 1.77 ± 1.66 | 1.59 ± 0.92 | 1.67 ± 0.32 |
Den totale deponering af prochloraz i huden efter 42 timer var 32 % af den påsatte mængde, hvilket fordelte sig med 4 % i epidermis og 28 % i dermis (Tabel 10). Alene omkring 14 % af den påsatte mængde prochloraz absorberedes i løbet af de 42 timer og kunne genfindes i receptorkammeret, medens knap 60 % af den påsatte mængde prochloraz fortsat var at finde i donorkammeret ved forsøgets afslutning efter 48 timer (Tabel 10). Der var en genfinding på gennemsnitlig 102 %.
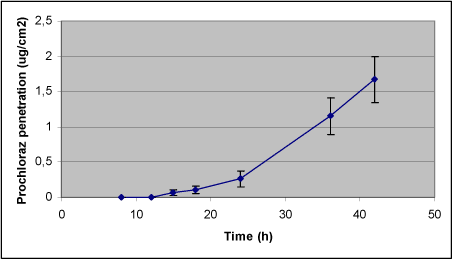
Figur 11. Dermal penetration for prochloraz.
2.1.10 Resultat-resumé
Nedenfor er opsummeret resultater for de ni modelstoffer anvendt i delstudie 1. Disse data vil danne baggrund for en diskussion af betydningen af opløselighedskarakteristika og molvægt for penetrationsegenskaber. Af overskuelighedsårsager er alene de fundne middelværdier angivet. De i de forudgående tabeller anførte spredninger er anvendt, når statistiske sammenligninger er anført.
Tabel 11. Opløseligheds- og penetrationskarakteristika for ni modelstoffer fra delstudie 1.
| Relative deposition | ||||||||||
| Solubility | logPow | MW | Kp | lag-time | receptor | epidermis | dermis | donor | recovery | |
| (g/L) | (g) | (um/h) | (h) | (%) | (%) | (%) | (%) | (%) | ||
| Glyphosat | 12 | -1,7 | 170 | 0,06 | 7,9 | 0,4 | 0,5 | 0,2 | 91,0 | 92,0 |
| Caffein | 21,7 | 0,16 | 194 | 3,8 | 6,9 | 18,7 | 3,4 | 3,6 | 72,8 | 99,6 |
| Dimethoate | 23,8 | 0,7 | 229 | 4,9 | 22,3 | 5,1 | 0,4 | 1,5 | 104,5 | 109,4 |
| Pirimicarb | 3 | 1,7 | 238 | 27,7 | 15,2 | 34,1 | 1,5 | 9,7 | 52,5 | 96,3 |
| Benzosyre | 3 | 1,83 | 122 | 50,6 | 1,5 | 93,4 | 0,4 | 1,1 | 4,2 | 99,0 |
| Malathion | 0,15 | 2,75 | 330 | 1,9 | 2,9 | 11,6 | 2,7 | 5,7 | 71,4 | 91,4 |
| Methiocarb | 0,027 | 3,34 | 225 | 38,6 | 11,7 | 50,9 | 2,4 | 23,5 | 17,1 | 94,4 |
| Paclobutrazol | 0,026 | 3,2 | 294 | 29,2 | 18,4 | 23,5 | 3,7 | 17,0 | 41,1 | 84,1 |
| Prochloraz | 0,034 | 4,4 | 377 | 17,8 | 21,1 | 13,7 | 4,2 | 27,5 | 58,3 | 101,7 |
2.2 Betydning af afvaskning og let hudbeskadigelse for penetration
Efter endt dermal eksponering vil en del stof være deponeret på huden, en del midlertidigt i den allerøverste del af huden (stratum corneum/epidermis) eller længere nede i selve dermis. Hidtidig regulering er baseret på, at alt fremmedstof fra og med stratum corneum og nedad henregnes som absorberet. Hvor meget, der er deponeret i de øverste lag, er belyst under delstudie 1. Her findes op til 4 % af den administrerede mængde i epidermis ved afslutning af eksperimenterne efter 48 timer, medens den relative deponering i dermis på tilsvarende tidspunkt var fra 0,2 % og op til over 25 % (Tabel 11). Variationen var betinget af stoffernes opløselighedskarakteristika, hvor de mest lipofile modelstoffer havde størst relativ deponering i såvel dermis som epidermis. Med så stor en andel af den administrerede mængde modelstof i huden efter 48 timer er det naturligvis relevant at forholde sig til, hvor stor den relative deponering er efter en mere erhvervsrelevant eksponeringsperiode (6 timer), samt i hvilket omfang denne fraktion kan fjernes ved afvaskning med en svag sæbeopløsning analog til anbefalede forholdsregler efter anvendelse af eller kontakt med for eksempel bekæmpelsesmidler. Problemstillingen omkring deponering (temporær) i huden er ikke tidligere studeret i forhold til flere modelstoffer dækkende et bredere spektrum af opløseligheder og molvægte. Formålet med dette delstudie er således at beskrive den betydning, den midlertidige ophobning i huden (reservoireffekten) har i forhold til en forsinket absorption efter eksponeringsophør, samt at vurdere hvorvidt man ved afvaskning efter endt eksponering kan fjerne en del af det på huden deponerede pesticid eller, om det fortsat skal henregnes som absorberet.
Endvidere inkluderes eksperimenter med lettere beskadiget hud, idet tidligere undersøgelser har indikeret, at beskadigelsen af stratum corneum kan ændre på deponeringsmønstret af fremmedstoffer (Nielsen 2004). Relevansen af denne problemstilling er åbenbar, idet hovedparten af arbejdsstyrken med potentiel pesticideksponering forventes i varierende grad at have lettere beskadiget hud betinget af eksem, smårifter etc.
Forsøgsrækken inkluderer seks modelstoffer. For hvert modelstof præsenteres den maksimale flux, penetrationskoefficienten Kp (Kp = maksimal flux/konc af teststof i donor), lag-time, huddeponering (epidermis samt dermis), total penetration samt genfinding, ligesom den resterende og ikke-absorberede mængde modelstof i donorkammeret er bestemt.
2.2.1 Glyphosat
Glyphosat blev påsat en mængde på 424 µg svarende til en koncentration i donorkammeret på 4 mg/mL. Glyphosat hører til de mest vandopløselige testsstoffer i dette studie med en opløselighed på 12g/L vand og en logPow på -1,7 (Tabel 1). To af grupperne fik efter seks timer vasket donorkammeret, hvor mere end 99 % af den påsatte mængde glyphosat på dette tidspunkt fortsat befandt sig (Tabel 12). Ganske begrænsede mængder glyphosat (0,1-0,3 % af påsat mængde) gennemtrængte huden i løbet af 48 timer i celler med ubeskadiget hud, hvilket også er i overensstemmelse med tidligere observationer fra delstudie 1 (Tabel 2, Tabel 12). I tilfælde af en lettere beskadiget hud er situationen dog anderledes, idet over 20 gange mere glyphosat gennemtrængte den lettere beskadigede hud i løbet af 48 timer i forhold til ubeskadiget hud, et resultat betinget af en signifikant større penetrationshastighed (flux) og dermed Kp (Tabel 12, Figur 12). Der var en tydelig effekt af afvaskning, idet afvaskning efter 6 timer reducerede den mængde glyphosat, der gennemtrængte den ubeskadigede hud i løbet af observationsperioden på 48 timer til en tredjedel. Denne effekt var endnu tydeligere i tilfælde af en lettere beskadiget hud, hvor afvaskning efter 6 timer reducerede den penetrerede mængde glyphosat med mere end 90 % (Tabel 12, Figur 12). Deponeringen i epidermis og dermis, hvilket er den potentielt absorberbare mængde pesticid, der findes som reservoir i huden, var for glyphosat kun 0,5 % af den påsatte mængde, en mængde der kunne reduceres med omkring 80 % ved afvaskning. Effekten af afvaskning på deponering af glyphosat i huden var endnu kraftigere i tilfælde af en lettere beskadiget hud (tabel 12). Her var udgangspunktet dog også anderledes, idet deponeringen i huden efter 48 timer var 5 gange højere for den lettere beskadigede hud i forhold til den ubeskadigede hud (Tabel 12). Trods en penetration over 48 timer, der er omkring 20 gange større for lettere beskadiget hud i forhold til intakt hud og en 5 gange højere deponering af glyphosat i huden, tyder de opnåede resultater på, at afvaskning kan nedsætte den absorberbare mængde glyphosat til et niveau tæt på det, der ses ved ikke-afvasket ubeskadiget hud (Tabel 12). Set under et er recovery for dette delstudie i orden, men blandt enkeltgrupperne ses en lav genfinding for de ikke-vaskede grupper, hvilket kan tænkes forårsaget af for lav donorrecovery (Tabel 12). Den samlede effekt af manglende afvaskning af en lettere beskadiget hud i forhold til afvasket intakt hud kan ses på den totale receptor recovery. Manglende afvaskning af en lettere beskadiget hud giver således anledning til over 65 gange så stor mængde absorberet glyphosat (Tabel 12).
Tabel 12. Penetration data for Glyphosat. Resultaterne er angivet som middelværdier + SEM.
| Intact Non-washed |
Damaged Non-washed |
Intact Washed |
Damaged Washed |
|
| N | 14 | 13 | 13 | 11 |
| Maximal flux (ug/cm2*h) | 0.016 ± 0.003 | 0.386 ± 0.080 AB | 0.015 ± 0.002 | 0.029 ± 0.010 |
| Kp (um/h) | 0.04 | 0.97 | 0.04 | 0.07 |
| Lag-time (h) | 3.3 ± 0.6 | 8.7 ± 1.3 AB | 4.2 ± 0.9 | 4.1 ± 0.5 |
| Donor wash at 6 h (µg) | 420.9 ± 4.2 | 417.7 ± 5.2 | ||
| Donor wash at 48 h (µg) | 334.9 ± 7.9 | 275.7 ± 5.5AB | 2.1 ± 0.3 A | 2.5 ± 0.3 |
| Donor recovery (µg) | 334.9 ± 7.9 | 275.7 ± 5.5 AB | 423.0 ± 4.3 A | 420.2 ± 5.2 |
| Epidermis deposition (µg) | 2.0 ± 0.4 | 9.5 ± 1.6 AB | 0.5 ± 0.0 AB | 1.4 ± 0.2 |
| Dermis deposition (µg) | 0.3 ± 0.1 | 1.6 ± 0.3 AB | 0.1 ± 0.0 | 0.1 ± 0.0 |
| Skin deposition (µg) | 2.3 ± 0.5 | 11.1 ± 1.7 AB | 0.6 ± 0.0 AB | 1.5 ± 0.2 |
| Skin deposition (% of dose) | 0.5 ± 0.1 | 2.6 ± 0.4 AB | 0.1 ± 0.0 AB | 0.4 ± 0.0 |
| Donor recovery (% of dose) | 79.0 ± 1.9 | 65.0 ± 1.3 AB | 99.8 ± 1.0 | 99.1 ± 1.2 |
| Receptor recovery (% of dose) | 0.3 ± 0.1 | 6.7 ± 1.6 AB | 0.1 ± 0.0 B | 0.5 ± 0.2 |
| Overall recovery (% of dose) | 79.8 ± 1.8 | 73.9 ± 1.1 AB | 100.0 ± 1.0 | 100.3 ± 1.3 |
| Skin penetration (µg/cm²) | ||||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 0.05 ± 0.01 | 0.12 ± 0.02 AB | 0.06 ± 0.01 | 0.05 ± 0.01 |
| T = 6h | 0.06 ± 0.01 | 0.28 ± 0.08 AB | 0.04 ± 0.01 | 0.09 ± 0.03 |
| T = 8h | 0.07 ± 0.01 | 0.58 ± 0.22 AB | 0.07 ± 0.01 | 0.09 ± 0.02 |
| T = 10h | 0.09 ± 0.02 | 1.05 ± 0.43 AB | 0.10 ± 0.02 | 0.14 ± 0.03 |
| T = 12h | 0.15 ± 0.02 | 1.73 ± 0.73 AB | 0.13 ± 0.03 | 0.22 ± 0.03 |
| T = 24h | 0.31 ± 0.06 | 5.12 ± 1.52 AB | 0.16 ± 0.03 AB | 0..38 ± 0.08 |
| T = 29h | 0.37 ± 0.07 | 6.83 ± 1.87 AB | 0.16 ± 0.02 AB | 0.42 ± 0.09 |
| T = 48h | 0.60 ± 0.12 | 13.35 ± 3.14 AB | 0.19 ± 0.03 AB | 0.59 ± 0.14 |
A – Significantly different from group with intact skin, non-washed (p<0.05, two-sided).
B – Significantly different from group with damaged skin, washed (p<0.05, two-sided).
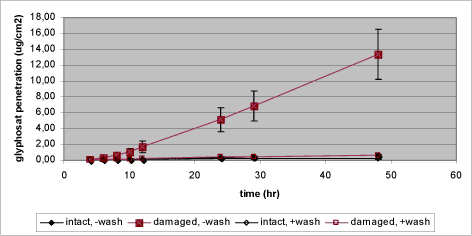
Figur 12. Effekt af afvaskning af huden på den dermale penetration af glyphosat gennem henholdsvis ubeskadiget og lettere beskadiget hud. Hvert datapunkt repræsenterer et gennemsnit af 12-14 enkeltmålinger +SEM. Efter 6 timer fjernes glyphosat fra alle donorkamre, hvorefter kamrene i to forsøgsserier vaskes i svag sæbeopløsning efterfulgt af skylning i vand (+wash).
2.2.2 Caffein
Caffein blev påsat i en mængde på 424 µg svarende til en koncentration i donorkammeret på 4 mg/mL. Caffein hører til de mest vandopløselige testsstoffer med en opløselighed på knap 22g/L vand og en logPow på 0,16 (Tabel 1). Resultaterne fra den ubeskadigede og ikke-vaskede hud viser god overensstemmelse med de parallelle resultater fra delstudie 1, både hvad angår totalpenetration, flux, lag-time, samt relativ deponering i hud (Tabel 3, Tabel 13). Lag-time påvirkedes ikke af, hvorvidt huden var lettere beskadiget eller intakt og var i alle tilfælde 5-6 timer (Tabel 13, Figur 13). I lighed med delstudie 1 observeres også i delstudie 2, at penetrationen af caffein sker med en hastighed, der betinger, at forudsætningen for anvendelsen af Ficks lov for beregning af penetrationskonstant alene er til stede de initiale godt 12 timer af forsøget (Figur 13). Som det fremgår af Figur 13 er der klare forskelle mellem de fire eksperimentelle grupper i forhold til såvel penetrationshastighed som totalpenetration. Den maksimale penetrationshastighed (flux) og dermed Kp er således forøget omkring 5 gange i tilfælde af en lettere beskadiget hud (Tabel 13). Endvidere ses, at afvaskning efter 6 timer reducerer den maksimale flux med 30-40 % samt totalpenetrationen over 48 timer med 50-60 % (Tabel 13). De observerede forskelle i totalpenetration kunne potentielt have været større såfremt en større mængde caffein var påsat donorkammeret, eller receptorvolumen havde været større, idet man i så fald havde opretholdt nær-ideale koncentrationsgradienter i længere tid. Ratioen mellem, hvad der er deponeret i dermis og epidermis, er højere i grupperne med lettere beskadiget hud (Tabel 13), hvilket indikerer at dette vandopløselige teststof lettere transporteres ind til dermis, når huden er lettere beskadiget. Dette betinger igen en større koncentrationsgradient mellem dermis og det underliggende receptorkammer, hvilket understøtter og forklarer den større totalpenetration. Ved afvaskning efter 6 timer fjernes størstedelen af den i epidermis deponerede caffein (Tabel 13), hvorved videre diffusion af caffein frem til dermis bremses. Denne opbremsning af tilførsel af caffein til dermis gør, at koncentrationsgradienten mellem dermis og receptorkammer ikke kan opretholdes, hvilket betinger en nedsat flux, der også tydeligt kan erkendes på Figur 13. Genfindingen var glimrende for alle fire grupper og således også for dette delstudie som helhed (Tabel 13). Den samlede effekt af manglende afvaskning af en lettere beskadiget hud i forhold til afvasket intakt hud kan ses på den totale receptor recovery, hvor manglende afvaskning af en lettere beskadiget hud giver anledning til over 8 gange så stor mængde absorberet caffein (Tabel 13).
Tabel 13. Penetration data for Caffein. Resultaterne er angivet som middelværdier + SEM.
| Intact Non-washed |
Damaged Non-washed |
Intact Washed |
Damaged Washed |
|
| N | 14 | 14 | 12 | 12 |
| Maximal flux (ug/cm2*h) | 1.80 ± 0.31 | 8.66 ± 1.22A | 1.01 ± 0.16 AB | 5.72 ± 0.65 |
| Kp (um/h) | 4.50 | 21.65 | 2.53 | 14.30 |
| Lag-time (h) | 6.5 ± 0.4 | 5.9 ± 0.4 | 5.0 ± 0.3 A | 4.8 ± 0.2 |
| Donor wash at 6 h (µg) | 380.3 ± 3.9 B | 259.0 ± 20.3 | ||
| Donor wash at 48 h (µg) | 285.6 ± 12.8 | 94.2 ± 18.1AB | 1.8 ± 0.2 A | 1.2 ± 0.2 |
| Donor recovery (µg) | 285.6 ± 12.8 | 94.2 ± 18.1 AB | 382.1 ± 4.0 AB | 260.2 ± 20.4 |
| Epidermis deposition (µg) | 7.1 ± 0.8 | 3.2 ± 0.8 AB | 0.5 ± 0.1 A | 0.5 ± 0.1 |
| Dermis deposition (µg) | 12.3 ± 1.3 | 17.0 ± 2.5 B | 1.8 ± 0.2 AB | 6.5 ± 1.3 |
| Skin deposition (µg) | 19.4 ± 1.4 | 20.3 ± 2.5 B | 2.3 ± 0.3 AB | 7.0 ± 1.4 |
| Skin deposition (% of dose) | 4.6 ± 0.3 | 4.8 ± 0.6 B | 0.5 ± 0.1 AB | 1.7 ± 0.3 |
| Donor recovery (% of dose) | 67.4 ± 3.0 | 22.2 ± 4.3 AB | 90.1 ± 0.9 AB | 61.4 ± 4.8 |
| Receptor recovery (% of dose) | 24.0 ± 2.9 | 65.1 ± 4.8 AB | 8.1 ± 0.9 AB | 34.9 ± 4.1 |
| Overall recovery (% of dose) | 95.9 ± 0.5 | 95.1 ± 0.9 | 98.7 ± 0.2 | 97.9 ± 0.5 |
| Skin penetration (µg/cm²) | ||||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 0.6 ± 0.2 | 3.8 ± 1.0 A | 0.6 ± 0.2 B | 2.5 ± 0.4 |
| T = 6h | 2.0 ± 0.5 | 11.7 ± 3.4 A | 1.7 ± 0.4 B | 8.7 ± 1.6 |
| T = 8h | 4.1 ± 1.1 | 24.6 ± 6.3 A | 3.2 ± 0.8 B | 19.3 ± 3.0 |
| T = 10h | 7.3 ± 1.7 | 40.0 ± 8.9 A | 5.3 ± 1.1 B | 31.8 ± 4.4 |
| T = 12h | 10.9 ± 2.4 | 56.2 ± 10.5 A | 7.3 ± 1.4 B | 41.7 ± 5.4 |
| T = 24h | 27.2 ± 4.3 | 111.9 ± 10.6 AB | 13.4 ± 1.6 AB | 64.6 ± 7.2 |
| T = 29h | 31.9 ± 4.8 | 117.4 ± 10.3 AB | 14.4 ± 1.7 AB | 66.3 ± 7.6 |
| T = 48h | 48.0 ± 5.9 | 136.2 ± 9.5 AB | 16.1 ± 1.7 AB | 69.8 ± 8.2 |
A – Significantly different from group with intact skin, non-washed (p<0.05, two-sided).
B – Significantly different from group with damaged skin, washed (p<0.05, two-sided).
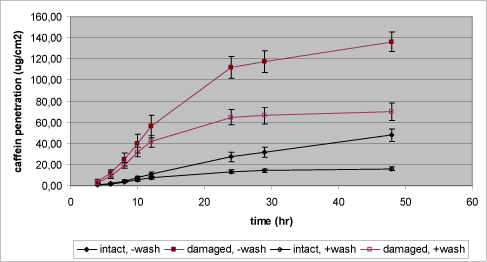
Figur 13. Effekt af afvaskning af huden på den dermale penetration af caffein gennem henholdsvis ubeskadiget og lettere beskadiget hud. Hvert datapunkt repræsenterer et gennemsnit af 12-14 enkeltmålinger +SEM. Efter 6 timer fjernes caffein fra alle donorkamre, hvorefter kamrene i to forsøgsserier vaskes i svag sæbeopløsning efterfulgt af skylning i vand (+wash).
2.2.3 Dimethoate
Dimethoat blev påsat i en mængde 137,5 µg svarende til en koncentration i donorkammeret på 1 mM (229 µg/mL). Dimethoat er blandt de mest vandopløselige modelstoffer i dette studie og er i delstudie 1 fundet at have en lag-time på over 20 timer, ligesom alene 5 % af den administrerede mængde dimethoat kunne genfindes i receptorkammeret efter 48 timers eksponering (Tabel 11). Netop for stoffer med lang lag-time er det interessant at vide, hvorvidt man ved en kortere eksponeringstid, som for eksempel ved normal erhvervseksponering, opnår en tilstrækkelig transport af stof ind i huden, til at dette stof efterfølgende kan trænge hele vejen gennem huden.
For dimethoate var resultatet entydigt klart. Således var der 42 timer efter de initiale seks timers eksponering intet dimethoate i epidermis, dermis, endsige i receptorkammeret, et resultat der sås ved eksperimenterne med beskadiget såvel som ubeskadiget hud. Heller ikke ved anvendelse af en salgsformulering af dimethoate (Perfekthion) sås nogen målbar huddeponering eller hudpenetration. Den samlede recovery nåede tilfredsstillende 89 %.
Tabel 14. Penetration data for Dimethoate samt salgsproduktet Perfekthion. Resultaterne er angivet som middelværdier + SEM.
| Dimethoate Intact, non-washed |
Dimethoate Intact, washed |
Perfekthion Intact, non-washed |
|
| Skin deposition (µg) | 0 | 0 | 0 |
| Receptor recovery (µg) | 0 | 0 | 0 |
| Donor recovery (µg) | 498.0 + 5.6 | 508.2 + 3.3 | 589.8 + 2.8 |
| Overall recovery (% of dose) | 83.0 + 0.9 | 84.7 + 0.5 | 98.3 + 0.5 |
Resultatet viser, at for et modelstof med en lang lag-time og en begrænset affinitet for den mere lipofile hudkompartment, kan man ikke forvente nogen målbar absorption gennem huden efter kortere tids eksponering (i dette tilfælde under en tredjedel af lag-time), ligesom en midlertidig ophobning i huden heller ikke ses. Årsagen er sandsynligvis, at der kræves en længerevarende kontinuerlig koncentrationsgradient favoriserende en penetration ind i huden, før man overvinder den modstand, der er betinget af den høje vandopløselighed. At andre faktorer end blot vandopløselighed er af betydning, illustreres tydeligt ved, at caffein med en sammenlignelig vandopløselighed og en kun lidt mindre molvægt fremviser klart anderledes penetrationskarakteristika (Tabel 13, Figur 13).
2.2.4 Benzosyre
Benzosyre blev påsat i en mængde af 424 µg i en koncentration af 4 mg/mL. Den maksimale flux i de første seks timer var generelt højere i grupperne med lettere beskadiget hud end i grupper med intakt hud, hvilket også afspejler sig i højere Kp værdier for grupperne med lettere beskadiget hud (Tabel 15). I forsøgene med benzosyre er lag-time ikke påvirket i betydelig grad af afvaskning af huden i svag sæbeopløsning (Tabel 15, Figur 19). Dette er sandsynligvis betinget af den i forvejen korte lag-time. Efter seks timer blev donorkammeret i halvdelen af grupperne således sæbevasket og skyllet med vand, hvilket alene resulterede i, at fluxen efterfølgende (flux fra 6-12 timer) faldt signifikant i forhold til grupper, hvor donorkamrene ikke blev vasket (Tabel 15). En sammenligning mellem de to grupper med afvaskning viser endvidere, at signifikant mindre benzosyre kunne fjernes ved donorvask efter 6 timer i gruppen med lettere beskadiget hud. Parallelt til denne observation ses også hos grupperne uden sæbeafvaskning efter 6 timer en signifikant større mængde benzosyre tilbage i donorkammeret ved forsøgets afslutning hos gruppen med ubeskadiget hud (Tabel 15). Donor recovery var således generelt signifikant højere i grupperne med intakt hud i forhold til grupperne med lettere beskadiget hud (Tabel 15).
Tabel 15. Penetration data for Benzosyre. Resultaterne er angivet som middelværdier + SEM.
| Intact Non-washed |
Damaged Non-washed |
Intact washed |
Damaged washed |
|
| N | 14 | 13 | 12 | 12 |
| Maximal flux (ug/cm2*h) | 20.4 ± 1.3 | 21.5 ± 1.6B | 15.8 ± 1.5 AB | 24.3 ± 1.7 |
| Kp (um/h) | 51.1 | 53.8 | 39.5 | 60.7 |
| Lag-time (h) | 1.8 ± 0.0 | 1.7 ± 0.1 | 1.7 ± 0.1 | 1.5 ± 0.1 |
| Flux (6h-12h) (ug/cm2*h) | 10.1 ± 0.4 | 10.7 ± 0.7B | 9.5 ± 0.4 AB | 8.0 ± 0.8 |
| Donor wash at 6 h (µg) | 41.8 ± 5.4 B | 24.4 ± 8.7 | ||
| Donor wash at 48 h (µg) | 13.2 ± 1.3 | 5.3 ± 1.0AB | 1.4 ± 0.3 A | 1.7 ± 0.3 |
| Donor recovery (µg) | 13.2 ± 1.3 | 5.3 ± 1.0 AB | 43.2 ± 5.3 AB | 26.1 ± 8.7 |
| Epidermis deposition (µg) | 1.0 ± 0.1 | 0.5 ± 0.1 AB | 0.3 ± 0.0 A | 0.2 ± 0.0 |
| Dermis deposition (µg) | 4.2 ± 0.1 | 3.6 ± 0.1 AB | 3.2 ± 0.2 A | 3.0 ± 0.1 |
| Skin deposition (µg) | 5.1 ± 0.2 | 5.3 ± 1.0 B | 3.5 ± 0.2 A | 3.3 ± 0.2 |
| Skin deposition (% of dose) | 1.2 ± 0.0 | 1.0 ± 0.0 AB | 0.8 ± 0.1 A | 0.8 ± 0.0 |
| Donor recovery (% of dose) | 3.1 ± 0.3 | 1.3 ± 0.2 AB | 10.2 ± 1.2 AB | 6.1 ± 2.0 |
| Receptor recovery (% of dose) | 89.8 ± 1.2 | 94.1 ± 1.3 AB | 77.2 ± 2.4 AB | 86.4 ± 2.3 |
| Overall recovery (% of dose) | 94.1 ± 1.1 | 96.3 ± 1.3 AB | 90.2 ± 0.4 AB | 93.3 ± 1.0 |
| Skin penetration (ug/cm²) | ||||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 2h | 10.7 ± 2.3 | 13.4 ± 2.9 | 10.9 ± 4.0 | 28.7 ± 5.7 |
| T = 4h | 93.1 ± 10.4 | 98.9 ± 12.6 | 75.0 ± 12.9 | 142.8 ± 16.6 |
| T = 6h | 184.1 ± 13.0 | 195.9 ± 15.6 | 144.8 ± 16.1 | 234.8 ± 18.4 |
| T = 8h | 244.2 ± 12.8 | 258.3 ± 14.8 | 201.6 ± 16.7 | 288.2 ± 16.5 |
| T = 10h | 281.3 ± 13.0 | 303.7 ± 14.1 | 240.6 ± 15.2 | 321.0 ± 13.4 |
| T = 12h | 313.1 ± 10.8 | 331.7 ± 11.8 | 266.0 ± 13.7 | 366.6 ±12.0 |
| T = 24h | 366.4 ± 5.2 | 387.6 ± 5.8 | 317.1 ± 10.2 | 362.7 ± 9.7 |
| T = 48h | 380.6 ± 4.9 | 399.0 ± 5.5 AB | 327.2 ± 10.1 AB | 366.3 ± 9.8 |
A – Significantly different from group with intact skin, non-washed (p<0.05, two-sided).
B – Significantly different from group with damaged skin, washed (p<0.05, two-sided).
Penetrationskurverne viser en general forøget initial penetrationshastighed såvel som totalpenetration over 48 timer hos grupperne med lettere beskadiget hud sammenlignet med grupperne med intakt hud (Figur 14). Endvidere ses en signifikant lavere totalpenetration efter 48 timer hos de grupper, der efter 6 timer fik afvasket donorkammeret (Tabel 15, Figur 14). Lag-time for benzosyre synes ikke påvirket af en lettere beskadigelse (Tabel 15).
Der var en signifikant mindre mængde benzosyre deponeret i huden ved forsøgsafslutning hos de grupper, hvor der var gennemført en afvaskning af huden (Tabel 15). Der var tale om en mindre deponering af benzosyre i såvel epidermis som dermis (Tabel 15).
Den relative deponering af benzosyre afspejler den større penetration gennem lettere beskadiget hud (større relativ receptor recovery) i forhold til grupper med intakt hud samt større donor recovery i grupper med afvaskning i forhold til de to andre grupper uden afvaskning (tabel 15). Den samlede genfinding var tilfredsstillende og varierede mellem 90 % og 96 % (Tabel 15).
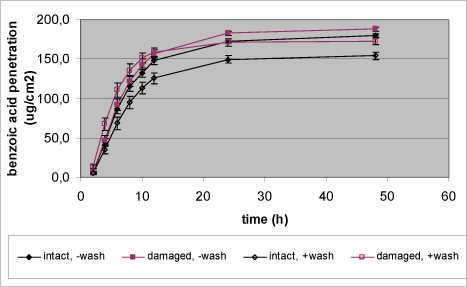
Figur 14. Effekt af afvaskning af huden på den dermale penetration af benzosyre gennem henholdsvis ubeskadiget og lettere beskadiet hud. Hvert datapunkt repræsenterer et gennemsnit af 12-14 enkeltmålinger +SEM. Efter 6 timer fjernes benzosyren fra alle donorkamre, hvorefter kamrene i to forsøgsserier vaskes i svag sæbeopløsning efterfulgt af skylning i vand (+wash).
2.2.5 Malathion
Malathion blev påsat i en mængde af 212 µg, svarende til en koncentration i donorkammeret på 2 mg/mL.
Den maksimale flux bestemmes ud fra den initiale lineære del af penetrationskurven (op til ca. 10 timer, Figur 20) og findes til 0,9 µg/cm²*h (2,7 nmol/cm²*h) for de celler, der var ubeskadigede og ikke blev afvaskede (Tabel 16). Den heraf afledte penetrationskoefficient (4,45 µm/h) er højere end den i delstudie 1 opnåede (1,85 µm/h), men stadig af samme størrelsesorden (Tabel 7, Tabel 16). Afvaskning efter 6 timers eksponering har ikke nogen reel betydning for penetrationskoefficienten for malathion, hvilket sandsynligvis er betinget af, at maksimal flux opnås allerede i løbet af de initiale 4-8 timer efter eksponeringens påbegyndelse. Generelt har afvaskningen ikke den store indflydelse på penetrationen af malathion, hvor markant og statistisk signifikant forskel alene ses ved eksperimenterne med lettere beskadiget hud og først efter 48 timer (Figur 20). Lettere beskadiget hud resulterer i en mere end fordobling af den maksimale penetrationshastighed og dermed også af Kp (Tabel 16). Der er overensstemmelse mellem lagtime i delstudie 1 og i delstudie 2 (Tabel 7, Tabel 16), ligesom lagtime kun marginalt, og ikke statistisk signifikant, nedsættes når huden er lettere beskadiget (Tabel 16).
Tabel 16. Penetration data for Malathion. Resultaterne er angivet som middelværdier + SEM.
| Intact Non-washed |
Damaged Non-washed |
Intact Washed |
Damaged washed |
|
| N | 14 | 13 | 12 | 13 |
| Maximal flux (ug/cm2*h) | 0.89 ± 0.11 | 1.67 ± 0.14 AB | 0.91 ± 0.11 B | 2.32 ± 0.16 |
| Kp (um/h) | 4.45 | 8.35 | 4.55 | 11.60 |
| Lag-time (h) | 2.6 ± 0.2 | 2.2 ± 0.1 | 3.0 ± 0.2 | 2.6 ± 0.3 |
| Donor wash at 6 h (µg) | 140.1 ± 6.5 B | 108.0 ± 4.3 | ||
| Donor wash at 48 h (µg) | 13.2 ± 2.0 | 9.2 ± 1.6 B | 3.3 ± 0.4 AB | 1.7 ± 0.2 |
| Donor recovery (µg) | 134.2 ± 5.1 | 38.0 ± 8.8 AB | 166.5 ± 4.0 AB | 114.1 ± 4.1 |
| Epidermis deposition (µg) | 7.1 ± 0.8 | 5.2 ± 0.7 B | 2.3 ± 0.3 AB | 1.0 ± 0.1 |
| Dermis deposition (µg) | 12.3 ± 1.3 | 45.6 ± 8.8 AB | 10.4 ± 2.0 | 8.6 ± 1.6 |
| Skin deposition (µg) | 19.4 ± 1.4 | 50.8 ± 8.7 AB | 12.7 ± 2.1 A | 9.6 ± 1.7 |
| Skin deposition (% of dose) | 9.2 ± 0.7 | 24.0 ± 4.1 AB | 6.0 ± 1.0 A | 4.5 ± 0.8 |
| Donor recovery (% of dose) | 63.3 ± 2.4 | 17.9 ± 4.2 AB | 78.5 ± 1.9 AB | 53.8 ± 1.9 |
| Receptor recovery (% of dose) | 20.7 ± 2.5 | 43.8 ± 3.1 AB | 18.3 ± 1.7 B | 34.0 ± 1.7 |
| Overall recovery (% of dose) | 95.0 ± 3.0 | 85.7 ± 3.1 A | 102.9 ± 2.0 AB | 92.3 ± 1.3 |
| Skin penetration (ug/cm²) | ||||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 |
| T = 4h | 1.4 ± 0.2 | 3.0 ± 0 .4 | 1.2 ± 0.2 | 3.8 ± 0.6 |
| T = 6h | 2.9 ± 0.4 | 6.2 ± 0.6 | 2.7 ± 0.4 | 7.9 ± 0.9 |
| T = 10h | 6.7 ± 0.9 | 13.0 ± 1.1 | 6.5 ± 0.9 | 17.2 ± 1.4 |
| T = 12h | 7.8 ± 1.0 | 16.0 ± 1.4 | 7.6 ± 1.0 | 20.1 ± 1.5 |
| T = 24h | 14.1 ± 1.8 | 29.4 ± 2.1 | 13.3 ± 1.4 | 31.8 ±1.7 |
| T = 29h | 15.2 ± 2.0 | 31.7 ± 2.3 | 14.5 ± 1.4 | 32.8 ± 1.7 |
| T = 48h | 20.7 ± 2.5 | 43.8 ± 3.1 AB | 18.3 ± 1.7 B | 34.0 ± 1.7 |
A – Significantly different from group with intact skin, non-washed (p<0.05, two-sided).
B – Significantly different from group with damaged skin, washed (p<0.05, two-sided).
Genfinding (recovery) af malathion i donorkammeret er højere for de to grupper med ubeskadiget hud i forhold til grupperne med lettere beskadiget hud, hvilket hænger fint sammen med den større penetrationshastighed gennem lettere beskadiget hud (Tabel 16) – efter 48 timer er en større del af den malathion, der ville kunne være til stede i huden diffunderet gennem den lettere beskadigede hud i forhold til den mere intakte hud. Den epidermale deponering efter 48 timer er 70 - 80 % lavere i de grupper, der fik foretaget en afvaskning af huden ved eksponeringsophør efter 6 timer (Tabel 16), hvilket indikerer, at man ikke alene har fået fjernet den mængde malathion, der resterede ovenpå huden, men også har kunnet fjerne en del af den malathion, der var deponeret i epidermis.
Det er sandsynligvis også den større penetrationshastighed gennem lettere beskadiget hud der gør, at dermis-deponeringen efter 48 timer er større i gruppen med lettere beskadiget hud (uden afvaskning) end i gruppen med ubeskadiget hud (Tabel 16). Det ses ikke i de to grupper med afvaskning efter 6 timer, hvilket skyldes, at man i gruppen med lettere beskadiget hud under afvaskningen fik fjernet en betydelig større mængde malathion end i gruppen med ubeskadiget hud (tabel 16). Der har i gruppen med lettere beskadiget hud efter afvaskning således ikke været mere malathion til rådighed for diffusion fra epidermis til den deponering i dermis man observerer efter 48 timer (Tabel 16). Samlet set findes en signifikant lavere huddeponering i de grupper der har fået foretaget afvaskning af huden efter 6 timer (Tabel 16). Samtidig ses en markant lavere relativ deponering i epidermis i grupperne med lettere beskadiget hud (10 %) i forhold til grupperne med intakt hud (20-35 %) (Tabel 16).
I grupperne med intakt hud havde afvaskning efter 6 timer ingen indflydelse på den samlede malathion penetration over 48 timer, mens afvaskning signifikant nedsatte den penetrerede mængde malathion gennem lettere beskadiget hud (Figur 15, Tabel 16). Endvidere fandtes en signifikant højere mængde penetreret malathion gennem lettere beskadiget hud end gennem intakt hud, en forskel der var tydelig allerede efter4-6 timer (Tabel 16, Figur 15).
Den samlede genfinding af malathion var udmærket i dette delstudie med malathion, idet genfindingen som gennemsnit for de fire grupper var 94 % (Tabel 16).
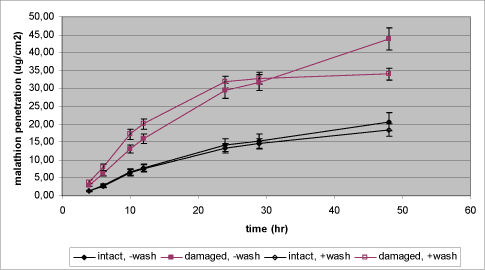
Figur 15. Effekt af afvaskning af huden på den dermale penetration af malathion gennem henholdsvis ubeskadiget og lettere beskadiget hud. Hvert datapunkt repræsenterer et gennemsnit af 12-14 enkeltmålinger +SEM. Efter 6 timer fjernes malathion fra alle donorkamre, hvorefter kamrene i to forsøgsserier vaskes i svag sæbeopløsning efterfulgt af skylning i vand (+wash).
2.2.6 Methiocarb
Methiocarb blev påsat i en mængde af 27,0 µg i et volumen på 600 µL svarende til en koncentration i donorkammeret på 45,0 µg/mL (200 µM). Methiocarb hører til de teststoffer med ringe vandopløselighed (0,03 g/L vand) og en logPow på 3,34 (Tabel 1). Resultaterne fra den ubeskadigede og ikke-vaskede hud viser god overensstemmelse med de parallelle resultater fra delstudie 1 både hvad angår totalpenetration, penetrationskoefficient (Kp), samt lag-time, hvorimod deponeringen i huden afviger. Således er specielt deponeringen i dermis betydelig større i delstudie 1 end her i delstudie 2, men som det fremgår af resultaterne, er netop dermisdeponeringen forbundet med ganske betydelig statistisk usikkerhed i delstudie 1 (variation mellem donorer) (Tabel 8, Tabel 17). En lettere beskadiget hud resulterede i en signifikant nedsat lag-time samt en tendens til øget penetrationshastighed og dermed penetrationskoefficient, hvilket betød en tendens til en større totalpenetration i løbet af de 48 timer (Tabel 17). Herudover betød den lettere beskadigede hud kun lidt for penetrationsforholdene for dette overvejende lipofile teststof (Figur 16, Tabel 17). I forhold til de mere hydrofile teststoffer er deponeringen i huden betydelig og med den relativt største deponering i dermis (Tabel 17). Undersøgelsen af salgsfomuleringen af methiocarb (Mesurol) viste ingen signifikante forskelle i forhold til aktivstoffet alene (Tabel 17, Figur 16). Efter 6 timer fjernedes methiocarb fra donorkammeret fra alle celler, men for to af gruppernes vedkommende blev huden efterfølgende afvasket med en tynd sæbeopløsning. I grupperne med sæbeafvaskning fandtes totalpenetrationen over 48 timer reduceret med omkring 40 % (Tabel 17, Figur 16). Deponeringen i huden fandtes reduceret tilsvarende, idet reduktionen var størst i epidermis (Tabel 17). Genfindingen af methiocarb var i dette delstudie ganske udmærket med et gennemsnit på godt 96 % (Tabel 17).
Tabel 17. Penetration data for Methiocarb. Resultaterne er angivet som middelværdier + SEM.
| Intact Non-washed Methiocarb |
Damaged Non-washed Methiocarb |
Intact Washed Methiocarb |
Damaged Washed Methiocarb |
Intact Non-washed, Mesurol |
Damaged Non-washed Mesurol |
|||
| N | 15 | 15 | 15 | 14 | 15 | 14 | ||
| Maximal flux (ug/cm2*h) | 0.18 ± 0.01 | 0.20 ± 0.02 | 0.13 ± 0.02 A | 0.16 ± 0.01 | 0.21 ± 0.02 | 0.16 ± 0.02 | ||
| Kp (um/h) | 39.5 | 45.5 | 30.0 | 35.0 | 47.0 | 35.5 | ||
| Lag-time (h) | 15.7 ± 1.0 | 11.7 ± 1.6 A | 14.3 ± 1.0 B | 8.5 ± 0.9 | 13.8 ± 1.0 C | 10.9 ± 0.9 | ||
| Removed from donor at 6 h (µg) | 9.6 ± 0.5 | 9.5 ± 0.5 B | 10.0 ± 0.6 | 9.2 ± 0.7 | 8.7 ± 0.4 | 8.7 ± 0.4 | ||
| Donor wash at 6 h (µg) | 8.1 ± 0.2 B | 6.0 ± 0.4 | ||||||
| Donor wash at 48 h (µg) | 2.1 ± 1.0 | 1.0 ± 0.2 B | 0.3 ± 0.0 A | 0.2 ± 0.0 | 1.1 ± 0.1 | 0.9 ± 0.1 | ||
| Donor recovery (µg) | 11.7 ± 1.0 | 10.5 ± 0.5 B | 18.4 ± 0.5 AB | 15.4 ± 0.6 | 9.8 ± 0.4 | 9.6 ± 0.4 | ||
| Epidermis deposition (µg) | 0.4 ± 0.1 | 0.4 ± 0.1 B | 0.2 ± 0.0 | 0.1 ± 0.0 | 0.3 ± 0.0 | 0.2 ± 0.1 | ||
| Dermis deposition (µg) | 3.6 ± 0.5 | 3.3 ± 0.4 B | 2.3 ± 0.4 A | 2.0 ± 0.2 | 4.0 ± 0.6 | 4.3 ± 0.7 | ||
| Skin deposition (µg) | 4.0 ± 0.5 | 3.7 ± 0.4 B | 2.5 ± 0.4 A | 2.1 ± 0.2 | 4.3 ± 0.6 | 4.5 ± 0.6 | ||
| Skin deposition (% of dose) | 14.8 ± 1.8 | 13.7 ± 1.5 B | 9.2 ± 1.5 A | 7.8 ± 0.7 | 15.9 ± 2.2 | 16.6 ± 2.2 | ||
| Donor recovery (% of dose) | 43.3 ± 3.7 | 38.8 ± 1.8 B | 68.0 ± 1.8 AB | 57.0 ± 2.2 | 36.2 ± 1.5 | 35.5 ± 1.5 | ||
| Receptor recovery (% of dose) | 40.0 ± 2.4 | 49.7 ± 4.4 B | 23.4 ± 1.7 AB | 34.0 ± 2.3 | 38.4 ± 1.9 | 42.4 ± 2.8 | ||
| Overall recovery (% of dose) | 98.2 ± 2.6 | 102.1 ± 4.8 C | 100.4 ± 2.1 | 98.6 ± 2.5 | 90.7 ± 3.0 | 87.6 ± 3.0 | ||
| Skin penetration (ug/cm²) | ||||||||
| T = 0h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | ||
| T = 4h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | ||
| T = 6h | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | 0 ± 0 | ||
| T = 8h | 0 ± 0 | 0.12 ± 0.09 | 0.06 ± 0.05 | 0 ± 0 | 0 ± 0 | 0 ± 0 | ||
| T = 10h | 0.07 ± 0.03 | 0.31 ± 0.13 BC | 0 ± 0 | 0 ± 0 | ||||
| T = 12h | 0.29 ± 0.06 | 0.89 ± 0.21 AC | 0.15 ± 0.03 AB | 0.59 ± 0.12 | 0.14 ± 0.02 AC | 0.40 ± 0.10 | ||
| T = 14h | 0.80 ± 0.15 | 0.29 ± 0.07 A | 0.30 ± 0.04 A | |||||
| T = 24h | 1.61 ± 0.23 | 2.68 ± 0.26 A | 0.92 ± 0.16 AB | 2.28 ± 0.22 | 1.49 ± 0.15 | 2.15 ± 0.30 | ||
| T = 30h | 2.70 ± 0.29 | 4.02 ± 0.41 A | 2.84 ± 0.36 B | 4.12 ± 0.29 | 3.00 ± 0.22 C | 4.32 ± 0.32 | ||
| T = 48h | 5.10 ± 0.30 | 6.34 ± 0.56 B | 2.98 ± 0.22 AB | 4.34 ± 0.29 | 4.90 ± 0.24 | 5.41 ± 0.36 | ||
A – Significantly different from group with intact skin, non-washed, methiocarb (p<0.05, two-sided).
B – Significantly different from group with damaged skin, washed, methiocarb (p<0.05, two-sided).
C - Significantly different from group with damaged skin, non-washed, Mesurol (p<0.05, two-sided).
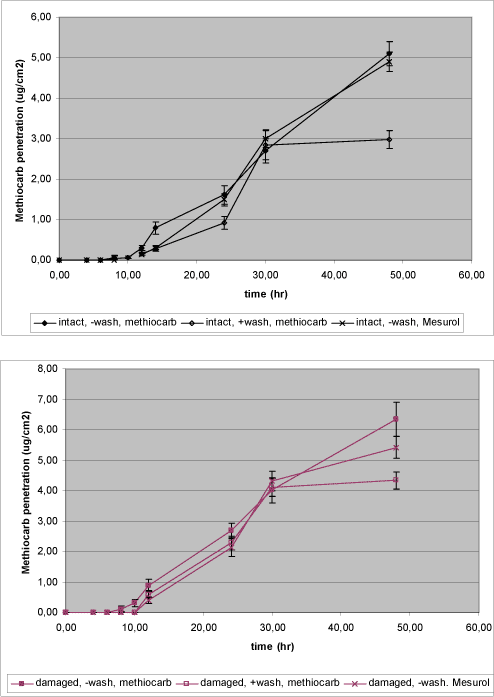
Figur 16. Effekt af afvaskning af huden på den dermale penetration af methiocarb samt Mesurol gennem henholdsvis ubeskadiget og lettere beskadiget hud. Hvert datapunkt repræsenterer et gennemsnit af 12-14 enkeltmålinger. Efter 6 timer fjernes methiocarb fra alle donorkamre, hvorefter kamrene enten skylles med vand (-wash) eller vaskes i svag sæbeopløsning efterfulgt af skylning i vand (+wash).
2.2.7 Resultat-resumé
Nedenfor er opsummeret hovedresultaterne for de seks modelstoffer med relevante penetrationsdata anvendt i delstudie 2. Disse data vil danne baggrund for en diskussion af betydningen af modelstoffernes opløselighedskarakteristika og molvægte, samt reservoireffekt, afvaskning samt lettere beskadigelse af huden for de overordnede penetrationsegenskaber. Af overskuelighedsgrunde er alene de fundne middelværdier angivet i nedenstående oversigtstabel.
Tabel 18. Penetrationskarakteristika for seks modelstoffer fra delstudie 2. Resultater er angivet som middelværdier af data fra 11-15 penetrationsceller.
| Intact Non-washed |
Damaged Non-washed |
Intact Washed |
Damaged Washed |
Sales product Intact Non-washed |
Sales product Damaged Non-washed |
|
| Kp (um/h) | ||||||
| Glyphosat | 0,04 | 0,97 | 0,04 | 0,07 | ||
| Caffein | 4,5 | 21,7 | 2,5 | 14,3 | ||
| Dimethoat | 0 | 0 | 0 | 0 | 0 | 0 |
| Benzosyre | 51,1 | 53,8 | 39,5 | 60,7 | ||
| Malathion | 4,5 | 8,4 | 4,6 | 11,6 | ||
| Methiocarb | 39,5 | 45,5 | 30,0 | 35,0 | 47,0 | 35,5 |
| Lag-time (h) | ||||||
| Glyphosat | 3,3 | 8,7 | 4,2 | 4,1 | ||
| Caffein | 6,5 | 5,9 | 5,0 | 4,8 | ||
| Dimethoat | - | - | - | - | - | - |
| Benzosyre | 1,8 | 1,7 | 1,7 | 1,5 | ||
| Malathion | 2,6 | 2,2 | 3,0 | 2,6 | ||
| Methiocarb | 15,7 | 11,7 | 14,3 | 8,5 | 13,8 | 10,9 |
| Donor-rec 6h. (%) | ||||||
| Glyphosat | 99,3 | 98,5 | ||||
| Caffein | 89,7 | 61,1 | ||||
| Dimethoat | 84,7 | |||||
| Benzosyre | 9,9 | 5,8 | ||||
| Malathion | 66,1 | 50,9 | ||||
| Methiocarb | 67.0 | 56,3 | ||||
| Total donor-rec (%) | ||||||
| Glyphosat | 79,0 | 65,0 | 99,8 | 99,1 | ||
| Caffein | 67,4 | 22,0 | 90,1 | 61,4 | ||
| Dimethoat | 83,0 | 84,7 | 98,3 | |||
| Benzosyre | 3,1 | 1,3 | 10,2 | 6,1 | ||
| Malathion | 63,3 | 17,9 | 78,5 | 53,8 | ||
| Methiocarb | 43,3 | 38,8 | 68,0 | 57,0 | 36,2 | 35,5 |
| Skin-dep (%) | ||||||
| Glyphosat | 0,5 | 2,6 | 0,1 | 0,4 | ||
| Caffein | 4,6 | 4,8 | 0,5 | 1,7 | ||
| Dimethoat | 0 | 0 | 0 | 0 | 0 | 0 |
| Benzosyre | 1,2 | 1,0 | 0,8 | 0,8 | ||
| Malathion | 9,2 | 24,0 | 6,0 | 4,5 | ||
| Methiocarb | 14,8 | 13,7 | 9,2 | 7,8 | 15,9 | 16,6 |
| Recep-rec (%) | ||||||
| Glyphosat | 0,3 | 6,7 | 0,1 | 0,5 | ||
| Caffein | 24,0 | 65,1 | 8,1 | 34,9 | ||
| Dimethoat | 0 | 0 | 0 | 0 | 0 | 0 |
| Benzosyre | 89,8 | 94,1 | 77,2 | 86,4 | ||
| Malathion | 20,7 | 43,8 | 18,3 | 34,0 | ||
| Methiocarb | 40,0 | 49,7 | 23,4 | 34,0 | 38,4 | 42,4 |
Donor-rec – relativ donor recovery; Skin-dep – relativ huddeponering; Recep-rec – relativ receptor recovery.
3 Diskussion
- 3.1 Hovedobservationer og diskussion
- 3.2 Betydning af stoffers opløselighed for absorptionsmængde og hastighed
- 3.3 Betydning af afvaskning og let hudbeskadigelse for penetration
3.1 Hovedobservationer og diskussion
Et kemisk stofs passage af huden er i princippet en passiv diffusion gennem forskellige lag med hver deres karakteristika i forhold til lipofilicitet. Et hydrofilt stof vil således nødigt flytte sig i retning af et mere lipofilt miljø, mens et lipofilt stof nødigt flytter sig i retning af et mere hydrofilt miljø. Over tid vil der dog indstille sig en ligevægt. Ved ligevægt vil der således eksistere en koncentration af modelstoffet i begge lag/fordelingsfaser. Givet at de to faser var henholdsvis oktanol og vand, ville man kunne udregne ratioen ved ligevægt som en oktanol-vand ratio. Det er det, der afspejles i logPow, som er den logaritmiserede værdi af ratioen mellem et stofs fordeling mellem oktanol og vand. En negativ LogPow er således et udtryk for, at et givet kemisk stof har en ratio under 1, og således ’foretrækker’ et vandigt miljø frem for et mere lipofilt miljø (oktanol). Der er klare paralleller mellem logPow og et stofs opløselighed i vand, men som det fremgår af oversigten over de anvendte modelstoffers logPow og opløselighed i vand (fx Tabel 11), er der stadig tale om to forskellige mål. Caffein er således omkring dobbelt så opløseligt i vand som glyphosat, mens caffeins præference for vand frem for oktanol er omkring 70 gange lavere end glyphosats. Det overordnede billede er dog, at en faldende opløselighed i vand modsvares af en stigende logPow-værdi.
Penetrationskoefficienten, Kp, fremkommer ved at dividere den maksimale penetrationshastighed med den påsatte koncentration af modelstof. Herved får man et koncentrationsuafhængigt mål for modelstoffets penetrationsegenskaber, der er gældende for så vidt, at betingelserne for Ficks lov er opfyldte i det eksperimentelle set-up. Idet diffusionen er afhængig af koncentrationsgradienten mellem de to fordelingsfaser, er en forudsætning for beregning af penetrationskoefficienter i det eksperimentelle set-up, at denne gradient er tilnærmelsesvis uendelig, hvilket svarer til, at koncentrationen på donorsiden er tilnærmelsesvis uendeligt større end på receptorsiden. Denne forudsætning er naturligvis opfyldt ved påbegyndelse af eksperimenter, hvor receptorkoncentrationen er nul, men vil udlignes over tid, afhængig af den til donoren påsatte mængde modelstof. Denne situation afspejles på penetrationskurverne, ved at de bøjer af og bliver fladere, penetrationshastigheden nedsættes, og ved tilnærmelsesvis ligevægt mellem koncentrationerne i donor og receptor vil penetrationskurven blive flad. Dette observeredes for eksempel ved benzosyre efter to døgn (Figur 7). I tilfældet benzosyre er betingelserne for beregning af en penetrationskoefficient således alene til stede de initiale omkring seks timer.
Et stofs lag-time er som tidligere omtalt et mål for, hvor lang tid der går fra stoffet er påsat i donorkammeret, til det observeres i receptoren, altså hvor lang tid det bruger på at flytte sig fra en fase til en anden. Der er ikke nogen entydig sammenhæng mellem lag-time og penetrationshastighed. Billedligt kan man forestille sig at skulle flytte vand fra et kar til et andet gennem en vandslange. Afgørende for den maksimale hastighed - hvor hurtigt man kan flytte vandet - er dels trykforskellen (analog med koncentrationsgradienten) og dels diameteren på slangen. Afgørende for hvor lang tid der går, fra man åbner for vandet i den ene ende, til man ser vandet komme ud i den anden ende (analog med lag-time) er imidlertid længden på slangen, som jo ikke afhænger af diameteren. Derfor er det ikke uventet, at man kan se et stof A med en højere penetrationskoefficient end stof B, men samtidig en længere lag-time. Disse overvejelser er relateret alene til passage mellem to faser.
I forhold til passage af huden er billedet mere kompliceret, idet der er tale om passage mellem flere faser med forskellige opløselighedskarakteristika. I den simple version fra en donorfase ind i epidermis, herfra videre til dermis, for endelig at slutte i receptorfasen. De forskellige opløselighedskarakteristika i specielt epidermis og dermis gør, at man kan opleve, at visse modelstoffer har egne opløselighedskarakteristika, der passer bedre med forholdene i enten epidermis eller dermis, hvilket kan resultere i en ophobning af stof i disse compartments.
3.2 Betydning af stoffers opløselighed for absorptionsmængde og hastighed
Målet for dette delprojekt var gennem anvendelse af en række modelstoffer at fastlægge et interval i forhold til lipofilicitet, hvor den mest effektive absorption kan forventes. Denne diskussion må nødvendigvis også forholde sig til modelstoffernes størrelse (molvægt, MW) samt deres steriske forhold (illustreret ved strukturformler, Figur 21). Den mest effektive absorption vil i det givne eksperimentelle set-up være en kombination af høj penetrationshastighed, illustreret ved en høj Kp, kort lag-time. Det giver samlet en høj penetration over den eksperimentelle periode, illustreret ved en høj receptorgenfinding. Det vil endvidere være af betydning, hvor meget stof der findes deponeret i huden, epidermis plus dermis, idet denne mængde i et vist omfang (belyses nærmere i det senere delstudie) er til stede for senere absorption. For samtlige modelstoffer observeres i dette delstudie en fuldt tilfredsstillende genfinding, således at forsøgene både enkeltvis og samlet klart lever op til krav om genfinding statueret i OECD’s guidelines for eksperimentelle penetrationsforsøg.
Den laveste penetrationskoefficient (Kp) ses ved det mest hydrofile modelstof (glyphosat). Kp stiger derefter med faldende hydrofilicitet, indtil et maksimum for Kp nås ved benzosyre, hvor Kp er knap 1000 gange større end for glyphosat. Forskellen i hydrofilicitet udtrykt som oktanol/vand ratioen (Pow) er godt 3000 svarende til en forskel i logPow på godt tre. Forskellen mellem glyphosat og benzosyre i vandopløselighed er dog ikke tilnærmelsesvis lige så stor. For de tre mest lipofile modelstoffer (methiocarb, paclobutrazol, prochloraz) falder Kp igen i forhold til benzosyre. Faldet i logPow i forhold til benzosyre er dog ikke så markant for de mest lipofile modelstoffer som for de mest hydrofile. Resultaterne indikerer generelt en omvendt U-formet sammenhæng mellem Kp og logPow, således at hurtigst penetration opnås ved en logPow værdi mellem 1½ og cirka 4 (Figur 17). Vore resultater er i overensstemmelse med tidligere studier med færre modelstoffer, som beskriver den optimale penetration over huden for stoffer med en logPow omkring 2 (Morgan et al. 2003), medens et studie med en række mindre alkoholer med forskellig vandopløselighed viste størst absorption gennem fuldhud ved logPow værdier mellem 1 og 3 (Cross et al. 2003). I sidstnævnte studie var der imidlertid en direkte sammenhæng mellem vandopløselighed og molvægt, hvorfor en adskillelse af indflydelsen af disse to forskellige fysisk-kemiske parametre ikke var mulig.
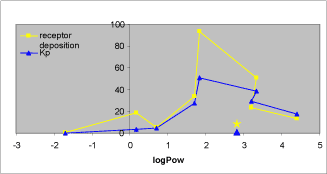
Figur 17. Sammenhæng mellem logPow og Kp samt relativ receptor deposition for ni modelstoffer. Kp og relativ receptor deposition for malathion er afsat separat med henholdsvis en blå trekant og en gul stjerne.
Der var ingen umiddelbar sammenhæng mellem molvægt og penetrationshastighed udtrykt som Kp. Dette var lidt overraskende, givet at et tidligere litteraturstudie baseret på en større database over studier involverende dermal penetration havde vist en umiddelbar sammenhæng mellem molvægt og maksimal penetrationshastighed (Magnusson et al. 2004). En nærmere analyse af de i dette arbejde inkluderede 87 modelstoffer viser dog, at sammenhængen har forholdsvis brede variationer, og at flere modelstoffer er taget ud af regressionsanalysen, idet de afveg for meget fra de andre stoffer. I nærværende undersøgelse har vi også enkeltstoffer, der falder udenfor det forventede (for eksempel malathion), og det kan ikke udelukkes, at vi med flere modelstoffer havde fundet samme sammenhæng som i det Australske litteraturstudie (Magnusson et al. 2004).
En afledt betydning af penetrationshastigheden er den mængde stof, der i løbet af den eksperimentelle periode når receptorfasen. Denne mængde er i Tabel 11 angivet ved den relative receptordeponering. Som ovenfor diskuteret er der et naturligt maksimum betinget af opnåelse af ligevægt mellem modellens compartments, men ikke desto mindre forventes en vis parallelitet mellem de to mål. Som det fremgår af Figur 17 er denne overensstemmelse mellem den fundne Kp og den observerede relative receptor deponering også tilstede.
Det var på baggrund af opløselighed og molvægt ventet, at malathions penetrationskarakteristika ville placere sig mellem methiocarbs og benzosyres. Som det imidlertid også fremgår af såvel Tabel 11 som Figur 17, var det ikke tilfældet. Der er søgt efter årsager omkring mulige eksperimentelle forhold (manglende opløselighed i donor/receptor, tab af stof under forsøg, analytiske problemer), men der er ikke fundet relevante forklaringer. Opløseligheden i donor/receptor væske er således undersøgt og fundet tilfredsstillende. I denne fase blev analyse gennemført med såvel HPLC som radioaktivitetsmåling for at sikre, at det målte stof ved radioaktivitetsmålingen stadig var helt (en ulempe ved mærkede stoffer er, at man i stedet for at følge et stof, følger et mærket atom - man vil derfor fortsat finde resultater, selvom udgangsstoffet for eksempel er omdannet til et andet stof med potentielt andre penetrationsegenskaber). Recovery var over 90 % og således på linie med de øvrige eksperimenter og OECD’s guidelines Malathion var et af de radioaktivt mærkede stoffer, hvorfor analytiske problemer var begrænsede. Tilbage står muligheden, at de oplyste værdier for logPow/opløselighed ikke er korrekte eller at kemiske/steriske forhold specifikke for malathion betinger de i forhold til de øvrige modelstoffer afvigende penetrationsegenskaber.
En anden væsentlig parameter for den absolutte mængde af et stof, der i løbet af en given periode kan absorberes over huden, er stoffets lag-time. Den tid, der går efter applikation af stoffet på donorsiden, indtil det kan måles på receptorsiden, kan tænkes at afhænge af såvel opløselighed som størrelse (molvægt) og steriske forhold. Sammenhængen med opløselighed er, at alt andet lige vil et stof med en hurtig penetrationshastighed også forventes at kunne observeres efter en kortere lag-time end et stof med en langsom penetrationshastighed. Derfor er den parallelitet, der ses mellem Figur 17 og Figur 18 ikke uventet, og viser at for de i dette studie anvendte modelstoffer gælder, at den korteste lag-time kan forventes af stoffer med en vandopløselighed mellem 3g/L og godt 20 g/L.
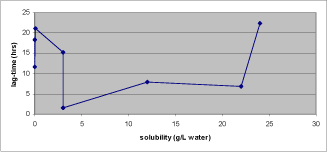
Figur 18. Sammenhæng mellem opløselighed i vand og lag-time for 9 modelstoffer.
Der er en tydelig sammenhæng mellem flertallet af modelstoffers molvægt og den observerede lag-time. Med stigende molvægt øgedes lag-time (Figur 19). Således var lag-time for det mindste modelstof med en molvægt på 122 gram nede på omkring 1½ time, medens lag-time ved molvægt over 350 gram oversteg 20 timer, hvilket er en ganske markant forskel, der også influerer på den mængde stof, der i løbet af en begrænset periode vil kunne absorberes dermalt.
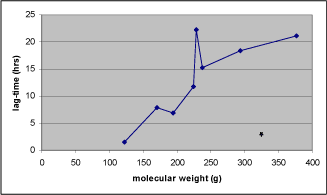
Figur 19. Sammenhæng mellem molvægt og lag-time for 9 modelstoffer. Lag-time for malathion er afsat separat med en stjerne på figuren.
Specielt i situationer med forholdsvis kort eksponeringstid vil en lang lag-time forventes at virke stærk begrænsende på den mængde stof, der kan absorberes, hvilket i forhold til de fleste erhvervsmæssige eksponeringer er relevant. En nærmere diskussion af denne problemstilling vil findes i relation til delstudie 2, hvor der netop er anvendt 6 timers eksponering for modelstoffer.
I lighed med sammenhængen mellem logPow og penetrationskoefficienten Kp ses malathion også ved denne sammenstilling af molvægt og lag-time at afvige markant fra de andre teststoffer. Således har malathion med en molvægt på 330 gram en lag-time på knap 3 timer svarende til et stof med en molvægt på under det halve.
Deponeringen i epidermis er relativt begrænset for alle modelstoffer, hvilket ikke er overraskende, givet at det alene drejer sig om de øverste hudlag (primært stratum corneum). Forskelle i epidermisdeponering mellem modelstofferne indikerer en relativt større deponering efter eksponering med de mest lipofile stoffer, idet caffein dog adskiller sig ved en relativ høj relativ epidermal deponering på godt 3 %.
For dermis ses en klart større relativ deponering af de lipofile stoffer (Figur 20), hvilket også var ventet, givet at dermis er et overvejende lipofilt matrix. Analoge resultater er vist i et studie inkluderende fem forskellige alkoholer med forskellige opløselighedskarakteristika (Cross et al. 2003).
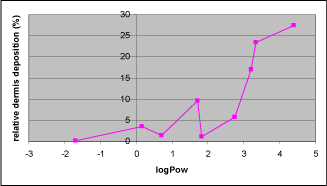
Figur 20. Sammenhæng mellem lipofilicitet udtrykt som logPow og den relative dermis deponering for ni modelstoffer.
Donordeponering ved forsøgsafslutning er udtryk for den fraktion af det påsatte modelstof, der ikke har forladt donorkammeret og diffunderet ind i huden. Det er klart blandt de mest hydrofile modelstoffer, at den største relative donordeponering observeres (Tabel 11), hvilket er fint i overensstemmelse med disse stoffers ringere affektion for de mere lipofile forhold i hudens compartments, som jo også ses i ovennævnte forhold omkring relativ deponering i dermis (Figur 20).
3.2.1 Delkonklusion
- Resultaterne indikerer generelt en omvendt U-formet sammenhæng mellem Kp og logPow, således at hurtigst penetration opnås ved en logPow værdi mellem 1½ og cirka 4. Et enkelt af de ni modelstoffer (malathion) falder udenfor denne generalisering.
- Der var ingen umiddelbar sammenhæng mellem molvægt og penetrationshastighed udtrykt som Kp.
- For de i dette studie anvendte modelstoffer gælder, at den korteste lag-time kan forventes af stoffer med en vandopløselighed mellem 3g/L og godt 20 g/L.
- Med stigende molvægt øgedes lag-time. Således var lag-time for det mindste modelstof med en molvægt på 122 gram nede på omkring 1½ time, medens lag-time ved molvægt over 350 gram oversteg 20 timer, hvilket er en ganske markant forskel, der også influerer på den mængde stof, der i løbet af en begrænset periode vil kunne absorberes dermalt. Igen adskiller malathion sig fra de øvrige modelstoffer.
- For dermis ses en klart større relativ deponering af de lipofile stoffer, hvilket også var ventet, da dermis er et overvejende lipofilt matrix.
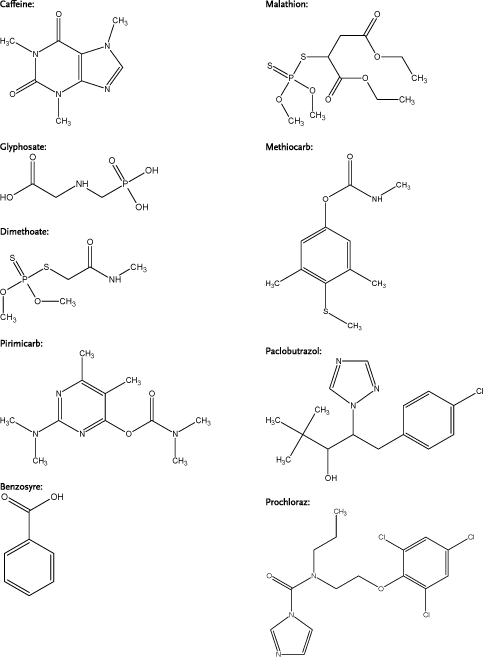
Figur 21. Strukturformler for modelstoffer anvendt i delstudie 1.
3.3 Betydning af afvaskning og let hudbeskadigelse for penetration
I delstudie 2 anvendtes seks timers eksponering efterfulgt af afvaskning i modsætning til delstudie 1, hvor huden kontinuert eksponeredes over 48 timer. For glyphosat, caffein, benzosyre, samt malathion er det eksperimentelle set-up for kontrolgrupperne i kolonne 1, tabel 18 (intakt, ikke-afvasket) identisk med det set-up der er brugt i delstudie 1. For to af stofferne med lang lag-time (dimethoat og methiocarb) er modelstoffet dog fjernet fra donorkammeret efter 6 timer i kontrolgruppen uden efterfølgende afvaskning med sæbeopløsning. Formålet var for disse to stoffers vedkommende at observere, hvorvidt alene en tidlig afbrydelse af eksponeringen i forhold til den kendte lag-time ville påvirke den efterfølgende penetration gennem huden, eller om penetrationen ville fortsætte uagtet den manglende koncentrationsgradient mellem donor og hudreservoir.
En direkte sammenligning for de fire modelstoffer, der indgik identisk i begge delstudier, viser, at der generelt er god overensstemmelse mellem de to sæt data fra delstudie 1 og delstudie 2, således at hverken penetrationskoefficient (Kp) eller lag-time er væsentlig forskellige (Tabel 11, Tabel 18). For methiocarb ses en øget donor-recovery i delstudie 2 i forhold til delstudie 1, hvilket ikke er uventet, givet at man efter 6 timer aktivt fjerner den mængde stof, der resterer i donorfasen, hvorimod man i delstudie 1 først fjerner reststof fra donorkammeret efter 48 timer. Differencen kan således tages som et forsigtigt bud på den mængde, der trænger ind i huden i de sidste 42 timer af eksponeringsperioden. Set i lyset af, at det er omkring 17 % af den administrerede dosis, som man genfinder efter 48 timer (Tabel 11) og 43 % efter 6 timer (Tabel 18), er der således en absorption til huden på omkring 25 % af den administrerede mængde i perioden mellem 6 og 48 timer. Analog med denne observation ses der da også en signifikant mindre deponering af methiocarb i huden og en mindre hudabsorption (udtrykt ved genfinding i receptorkammeret) for eksperimentet i delstudie 2 (Tabel 18) sammenlignet med delstudie 1 (Tabel 11). For det modelstof med den længste lag-time (dimethoat, lag-time = 22,3 timer) ses der slet ingen penetration i det tilfælde, hvor eksponeringen standses efter 6 timer. Resultatet viser, at for et modelstof med en lang lag-time og en begrænset affinitet for den mere lipofile hudkompartment kan man ikke forvente nogen målbar absorption gennem huden efter kortere tids eksponering (i dette tilfælde under en tredjedel af lag-time), ligesom en midlertidig ophobning i huden heller ikke ses. Årsagen er sandsynligvis, at der kræves en længerevarende kontinuerlig koncentrationsgradient favoriserende en penetration ind i huden, før man overvinder den modstand, der er betinget af den høje vandopløselighed. At andre faktorer end blot vandopløselighed er af betydning for hudpenetrationen illustreres tydeligt ved, at caffein med en sammenlignelig vandopløselighed og en kun lidt mindre molvægt fremviser klart anderledes penetrationskarakteristika (Tabel 13, Tabel 18).
3.3.1 Betydning af afvaskning for senere hudpenetration
Denne problemstilling er belyst gennem forsøg, hvor man efter 6 timers eksponering har foretaget en reel afvaskning af huden med en svag sæbeopløsning. Da pH potentielt har indflydelse på huden såvel som på stoffernes ioniseringsgrad, er der anvendt en pH-neutral sæbeopløsning. Det er tidligere vist, at vask med svag sæbeopløsning ikke influerer mere på hudens barriereegenskaber end afvaskning i vand (Bornkessel et al. 2005), hvorfor afvaskningen antages ikke at påvirke den efterfølgende penetration af modelstof tilstede i huden. Da afvaskningen først gennemføres efter 6 timers eksponering, er forsøgsbetingelserne indtil da identiske med forsøgene uden afvaskning. Da modelstofferne på nær dimethoat og methocarb grundet disse to modelstoffers lange lag-time er trængt ind i huden i løbet af de initiale 6 timer, er det derfor heller ikke overraskende, at lag-time for de anvendte modelstoffer ikke er påvirket af afvaskningen efter 6 timer. Centralt for diskussionen om betydningen af afvaskning er, hvorvidt det via en afvaskning med en svag sæbeopløsning er muligt at reducere den mængde modelstof, der er til rådighed i hudens reservoir for senere absorption. Det er i forsøgenes design givet, at en måling af deponeringen efter 6 timer ikke er mulig, hvorfor data alene haves for huddeponeringen ved forsøgsafslutning efter 48 timer. Resultaterne er derfor alene indikative for de forhold, der eksisterede 42 timer forud for den aktuelle måling. Tallene for huddeponering kan derfor sammenstilles med den mængde modelstof, der kunne opsamles ved afvaskningen efter de 6 timer. Resultaterne viser entydigt, at en afvaskning efter 6 timer fjerner den altovervejende del af den administrerede mængde modelstof, og nedsætter derved muligheden for senere huddeponering, således at man ved forsøgsafslutning ser en signifikant reduceret huddeponering i de grupper, hvor der er gennemført afvaskning efter 6 timer. For de mest vandopløselige modelstoffer (glyphosat og caffein) nedsættes huddeponeringen med 80-90 %, medens reduktionen for de mere lipofile stoffer såsom malathion og methiocarb er omkring 35 %. Den nedsatte mængde modelstof i huden betyder en mindre koncentrationsgradient mellem hud og receptorkammer, hvilket alt andet lige forventes at resultere i en nedsat flux af modelstof. Dette bekræftes af den nedsatte receptor recovery i de grupper, der fik sæbeafvaskning efter 6 timer. For de to mest vandopløselige stoffer reduceredes absorptionen (udtrykt gennem receptor recovery) til omtrent en tredjedel, medens absorptionen for benzosyre og methiocarb blev reduceret til 60-80 % af værdierne uden afvaskning. Penetrationskoefficienterne ændredes i overensstemmelse med ovennævnte ændringer i penetrationshastighed og mængde. Samlet kan det konkluderes, at en afvaskning efter endt eksponering signifikant nedsætter den samlede absorption af modelstofferne. For de mest vandopløselige stoffer er denne reduktion omkring 67 % og for de mere lipofile modelstoffer med lidt mindre. Det er således muligt ved almindelig let afvaskning at fjerne en del af den stofmængde, der er trængt ind i huden. Denne observation har klare forebyggelsesmæssige implikationer, og dokumenterer betydningen af afvask med sæbeopløsning efter endt arbejde med dermal kontakt til fremmedstoffer. Et tidligere studie, hvor man efter 90 minutters pesticideksponering (glyphosat, alachlor, methyl parathion, eller triflualin) af grisehud afvaskede med enten propanol eller en sæbeopløsning viste, at man kunne fjerne omkring halvdelen af den administrerede mængde pesticid (Campbell et al. 2000). Dette Amerikanske studie viste endvidere, at sæbevand var mere effektivt end for eksempel polyethylen glycol til fjernelse af pesticid fra huden (Campbell et al. 2000). Sidstnævnte observation kunne være en konsekvens af, at polyethylen glycol i andre sammenhænge har været anvendt som bærestof/detergent med det formål at gøre meget hydrofile stoffer mere blandbare med vandige opløsninger, og således også kunne tænkes at befordre en absorption af for eksempel det meget hydrofile pesticid glyphosat. Tidligere undersøgelser gennemført i Odense har netop dokumenteret betydningen af detergenter og bærestoffer for absorptionen af pesticider over human hud (Nielsen 2004).
Den nuværende regelsætning omkring vurdering af penetrationsforsøg følgende gældende OECD guidelines foreskriver, at man skal henregne alt stof, der ikke er genfundet i donordelen som absorberet og dermed potentielt tilgængeligt for systemisk toksicitet. Dette gælder således også den fraktion af den administrerede dosis, der er ophobet i huden. Nærværende undersøgelse viser, at absorption fra huden og ud i receptordelen fortsætter efter endt eksponering. For visse stoffer fortsætter absorptionen i over et døgn efter endt eksponering. Der er derfor ingen tvivl om, at en vis del af den i huden deponerede mængde modelstof senere vil absorberes. Det er imidlertid ikke afklaret, hvor stor en fraktion af den i huden midlertidigt deponerede mængde modelstof, der vil fjernes uden at nå systemisk cirkulation, det vil sige ovenud af huden. I den eksperimentelle situation svarer det til den fraktion, der vil returnere til donorkammeret efter endt eksponering. En indikation på størrelsen af denne fraktion er, at knap 8 % af den administrerede mængde methiocarb kunne opsamles i donorkammeret efter 48 timer i de grupper, hvor cellerne blev skyllet efter 6 timer (Tabel 17; 2,1 ug/27,0 ug). Da det ikke er mere end 15 % af den administrerede methiocarb-dosis, der genfindes i huden efter 48 timer (Tabel 17), udgør de 8 % således knap en tredjedel af den mængde, der ville have været deponeret i huden, såfremt der ikke havde været en tilbagediffusion til donordelen. Disse data indikerer således, at det er en betydende fraktion af det i huden midlertidigt deponerede modelstof, der faktisk returnerer til donorsiden af huden. For de lipofile stoffer indikerer de disse, om end begrænsede data, at den nuværende anvendelse af data ved regelsætning for dermal absorption baseret på guideline-forsøg i en vis grad overestimerer den reelle absorberbare mængde fremmedstof ved at indregne alt stof ikke genfundet i donor som absorberet. Overestimatet er dog ikke voldsomt stort, og for de lipofile stoffers vedkommende synes den hidtil anvendte procedure pragmatisk anvendelig. For de hydrofile stoffer kan nærværende data ikke give fyldestgørende svar på denne problemstilling.
3.3.2 Betydning af lettere hudbeskadigelse for senere hudpenetration
En stor del af mennesker eksponeret dermalt for fremmedstoffer kan ikke antages altid at have fuldt intakt hud med optimale barriereegenskaber. Derfor er det en relevant problemstilling, hvorvidt fremmedstoffers penetrationsforhold ændrer sig i tilfælde af en lettere beskadiget hud. Tidligere undersøgelser har indikeret, at beskadigelsen af stratum corneum kan ændre på deponeringsmønstret af fremmedstoffer (Morgan et al. 2003, Nielsen 2005). Disse tidligere studier er udført med ganske få modelstoffer. Det Britiske studie konkluderer således på basis af en undersøgelse af to meget hydrofile modelstoffer (penciclovir og aciclovir, logPow omkring -2) i et eksperimentelt set-up med mikrodialyse af frivillige forsøgspersoner, at der er en direkte sammenhæng mellem graden af hudbeskadigelse og absorptionen af fremmedstof (Morgan et al. 2003). Denne undersøgelse baserer sig som ovenfor nævnt alene på to modelstoffer med meget høj hydrofilicitet, men en nærmere analyse inkluderende modelstoffer med forskellig størrelse og opløselighedskarakteristik er ikke tidligere gennemført.
Resultaterne fra delstudie 1 viste, at den dermale penetration af de anvendte modelstoffer forekom omvendt proportional med molvægten, medens der fandtes et centralt opløselighedsinterval med størst penetrationshastighed. En effekt af en lettere beskadigelse af huden på modelstoffernes penetrations-egenskaber kan forventes at være størst for de modelstoffer, der havde sværest ved at gennemtrænge den intakte hud. En nylig in vivo undersøgelse over effekten af en lettere beskadiget hud på penetrationen af tre polyethylenglykoler viste da også, at den relative forøgelse af penetrationen efter beskadigelse var størst for den glykol med størst molvægt (Jakasa 2006). Benzosyre havde meget let ved at gennemtrænge den intakte hud og har en relativ lav molvægt, og en lettere beskadigelse vil således ikke forventes at øge penetrationen eller penetrations-hastigheden væsentligt, hvorimod såvel de mere hydrofile som de mere lipofile modelstoffers penetrationsegenskaber forventes at ændre sig mere markant.
Den i dette studie anvendte model opererer i princippet med tre overordnede compartments: donorkammeret, huden, samt receptorkammeret. En lettere beskadigelse af huden med den anvendte metode er tidligere vist at nedsætte hudens integritet, men under bevarelse af en specificeret del af hudens barriereegenskaber (Nielsen 2005). En beskadigelse af huden via forbehandling med den lave koncentration af SLS (0,3 %) i tre timer forventes primært at have betydning for transporten fra donorkammer og ind i huden. Det er en transport mod et mere lipofilt miljø, hvorfor det forventes, at en nedsættelse af hudens integritet i højere grad vil have betydning for de hydrofile stoffer end for de lipofile, der i forvejen, lettere end de hydrofile, kommer fra donor og ind i huden.
Man kunne have forstillet sig, at lag-time blev påvirket af den lettere beskadigelse, men som det fremgår af de opnåede resultater, indikerer disse ikke, at det er tilfældet. Der er således i de fleste tilfælde alene tale om en begrænset ikke-signifikant reduktion i lag-time. Den observerede stigning i lag-time for glyphosat efter anvendelse af beskadiget hud skal i højere grad tages som udtryk for en mere usikker bestemmelse af lag-time ved de meget lave penetrationshastigheder for dette modelstof gennem ubeskadiget hud. For dimethoat sås i lighed med resultater fra ikke-beskadiget hud heller ingen penetration gennem den lettere beskadigede hud. Årsagen er sandsynligvis den samme; Den lange lag-time tillader ikke en relevant penetration ind i huden i løbet af de 6 timers eksponering.
For samtlige modelstoffer fandtes en forøget maksimal penetrationshastighed medførende en øget penetrationskoefficient (kp). Forøgelsen af Kp for benzosyre var dog marginal og ikke-signifikant, hvilket også til dels var ventet jævnfør tidligere argumentation. For de to mere lipofile modelstoffer, malathion og methiocarb, var der tale om en forøgelse med henholdsvis næsten 90 % og godt 15 % (Tabel 18). At effekten er størst på malathion kan være en konsekvens af, at malathion med sin betydelige molvægt på 330 g/mol som udgangspunkt har en penetrationskoefficient af samme størrelse som det langt mere hydrofile stof caffein, og derfor får en større gevinst ved den lettere beskadigede hud end methiocarb. For de mere hydrofile modelstoffer var penetrationshastigheden imidlertid forøget ganske markant mere, idet caffein penetrerede med en hastighed, der var forøget med omkring 500 %, medens glyphosats maksimale penetrationshastighed blev omkring 25 gange større som følge af den lettere beskadigede hud. Resultaterne indikerer således, at en lettere beskadiget hud resulterer i en generel forøget penetrationshastighed for alle stoffer, at forøgelsen er marginal for de stoffer, der allerede ved den intakte hud har gode penetrationsegenskaber, at forøgelsen er signifikant for de mere lipofile stoffer, men at den klart største effekt observeres ved eksponering for hydrofile modelstoffer. Den kraftigt forøgede penetration af specielt de mere hydrofile modelstoffer gennem lettere beskadiget hud kan have den konsekvens, at man reguleringsmæssigt er nødt til at forholde sig til, at den reelle situation blandt en stor del af ansatte med dermal eksponering og ikke-intakt hud er, at de absorberer ganske meget mere dermalt end de traditionelle in vitro guideline-forsøg indikerer.
Den øgede penetrationshastighed har den umiddelbare konsekvens, at den samlede mængde modelstof, der kan genfindes i receptorkammeret, og således er absorberet, er forøget tilsvarende. Marginalt for benzosyre, plus 25 % for methiocarb, godt og vel fordoblet for malathion og caffein, samt 30 gange forøget for glyphosats vedkommende. Forklaringen er analog med ovenstående og relateret til hydrofilicitet for caffeins og glyphosats vedkommende og størrelse for malathions vedkommende. Begge forklaringer er i overensstemmelse med observationer fra Hollandske in vivo undersøgelser omkring dermal penetration af glykol-forbindelser gennem lettere beskadiget hud (5 % SLS i 4 timer) (Jakasa 2006).
Betydningen af den lettere beskadigelse af huden for den temporære deponering af modelstof i huden er primært relateret til de to modelstoffer, der enten af opløselighedsgrunde havde sværest ved at komme fra donorkammeret og ind i huden (glyphosat), eller af størrelsesmæssige årsager havde svært ved at komme ind i huden og af opløselighedsgrunde havde sværest ved at komme fra huden og videre til receptoren. Den temporære deponering i huden var således forøget tre-fem gange for malathions og glyphosats vedkommende, men som nævnt sandsynligvis af forskellige årsager.
Den større absorption og til dels deponering i huden resulterer umiddelbart i en mindre mængde modelstof i donorkammeret ved forsøgsafslutning.
Også for forsøgsrækken med lettere beskadiget hud gennemførtes en parallel række forsøg med afvaskning efter 6 timers eksponering. Resultaterne fra opsamling af modelstof efter seks timer og afvaskning viser, at man næsten får opsamlet alt modelstof tilstede i donorkammeret efter seks timer, og at der alene i meget begrænset omfang senere frigives modelstof til donorkammeret i disse forsøg med lettere beskadiget hud. Differencen mellem donordeponeringen efter 6 timer i forsøgene med afvaskning og donordeponeringen efter 48 timer i forsøgene uden afvaskning er således udtryk for den fraktion af den administrerede dosis modelstof, der trænger ind i huden og i et vist omfang videre gennem huden, i de afsluttende 42 timer af den eksperimentelle periode. Differencen mellem, hvad der opsamles efter 6 timer i forsøgene med afvaskning, og hvad der opsamles efter 48 timer i samme forsøg, er derimod udtryk for den fraktion af dosis, der diffunderer tilbage til donorkammeret efter initialt at være diffunderet ind i huden. Denne fraktion er meget begrænset i disse forsøg med lettere beskadiget hud.
Afvaskning af den lettere beskadigede hud efter 6 timer resulterede for alle modelstoffer i en nedsat deponering af modelstof i huden. Mest markant var effekten på de to modelstoffer, hvis huddeponering var påvirket stærkest af den forudgående hudbeskadigelse. For både glyphosats og malathions vedkommende observeredes således, at man ved afvaskning af huden var tæt på at kunne neutralisere den stærkt forøgede huddeponering forårsaget af den lettere beskadigelse af huden. Faktisk kunne man for de to mest lipofile modelstoffer opnå en lavere huddeponering i den lettere beskadigede hud end i den ikke-beskadigede hud, et resultat hvis eneste forklaring synes at være, at man i højere grad er i stand til at vaske modelstof deponeret i huden ud af den lettere beskadigede hud end ud af ikke-beskadiget hud. I hvilken grad man i levende hud ville se samme billede er uafklaret idet man til en vis grad vil forvente en reparationsproces initieret i den levende hud i løbet af den eksperimentelle periode på 48 timer. Visse typer beskadigelser af huden har på den anden side mere permanent karakter, hvor reetablering af fuld barrierefunktion ikke kan forventes på 48 timer. I forhold til den mængde af den administrerede dosis, der når frem til receptorkammeret, og altså kan betragtes som absorberet, er effekten af afvaskning, i lighed med observationerne fra den ikke-beskadigede hud, størst for de to mest hydrofile modelstoffer caffein og glyphosat.
Tolkningen af forsøgene med lettere beskadiget hud er, at man ved eksponering af en lettere beskadiget hud opnår en kraftig forøget huddeponering såvel som en kraftig forøget reel absorption, og at effekten er størst for de stoffer, der har de største begrænsninger for uhindret absorption gennem ikke-beskadiget hud. Det vil sige de mest lipofile og specielt de mest hydrofile stoffer. Imidlertid vil en afvaskning efter endt eksponering i meget høj grad kunne reducere den forøgede absorption såvel som huddeponering, en reduktion til et niveau der dog mængdemæssigt stadig er signifikant højere end efter afvaskning af intakt hud.
3.3.3 Delkonklusion
- For et modelstof med en lang lag-time og en begrænset affinitet for den mere lipofile hudkompartment kan man ikke forvente nogen målbar absorption gennem huden efter kortere tids eksponering (i dette tilfælde under en tredjedel af lag-time), ligesom en midlertidig ophobning i huden heller ikke ses.
- En afvaskning efter 6 timer fjerner den altovervejende del af den administrerede mængde modelstof og nedsætter derved muligheden for senere huddeponering. For de mest vandopløselige modelstoffer (glyphosat og caffein) nedsættes huddeponeringen med 80-90 %, medens reduktionen for de mere lipofile stoffer såsom malathion og methiocarb er omkring 35 %.
- Den nedsatte mængde modelstof i huden betyder en mindre koncentrationsgradient mellem hud og receptorkammer, hvilket resulterer i en nedsat flux af modelstof.
- Samlet kan det konkluderes, at en afvaskning efter endt eksponering signifikant nedsætter den samlede absorption. For de mest vandopløselige stoffer nedsættes absorptionen med omkring 67 % og for de mere lipofile modelstoffer med lidt mindre. Det er således muligt ved almindelig let afvaskning at fjerne en del af den stofmængde, der er trængt ind i huden. Denne observation har klare forebyggelsesmæssige implikationer, og dokumenterer betydningen af afvaskning med sæbeopløsning efter endt arbejde indebærende dermal kontakt til fremmedstoffer.
- Nærværende undersøgelse viser, at absorption fra huden og ud i receptordelen fortsætter efter endt eksponering. For visse stoffer i over et døgn efter endt eksponering. Der er derfor ingen tvivl om, at en vis del af den i huden deponerede mængde modelstof senere vil absorberes.
- For de lipofile stoffer indikerer disse, om end begrænsede data, at den nuværende anvendelse af data ved regelsætning for dermal absorption baseret på guideline-forsøg i en vis grad overestimerer den reelle absorberbare mængde fremmedstof ved at indregne alt stof ikke genfundet i donor som absorberet. Overestimatet er dog ikke voldsomt stort, og for de lipofile stoffers vedkommende synes den hidtil anvendte procedure pragmatisk anvendelig. For de hydrofile stoffer kan nærværende data ikke give fyldestgørende svar på denne problemstilling.
- Dette studie indikerer, at en lettere beskadiget hud resulterer i en generel forøget penetrationshastighed for alle stoffer, at forøgelsen er marginal for de stoffer, der allerede ved den intakte hud har gode penetrationsegenskaber, at forøgelsen er signifikant for de mere lipofile stoffer, men at den klart største effekt observeres ved eksponering for hydrofile modelstoffer.
- Imidlertid vil en afvaskning af den beskadigede hud efter endt eksponering i meget høj grad kunne reducere den forøgede absorption såvel som huddeponering til et niveau, der dog mængdemæssigt stadig er signifikant højere end efter afvaskning af intakt hud.
- Den kraftigt forøgede penetration af specielt de mere hydrofile modelstoffer gennem lettere beskadiget hud kan have den konsekvens, at man reguleringsmæssigt er nødt til at forholde sig til, at den reelle situation blandt en stor del af ansatte med dermal eksponering og ikke-intakt hud er, at de absorberer ganske meget mere dermalt end de traditionelle in vitro guideline-forsøg indikerer.
4 Perspektivering
4.1 Videnskabelige perspektiver
Som modelstoffer til undersøgelsen af dermal absorption samt temporær deponering i huden udvalgtes ni modelstoffer, hvoraf 8 var bekæmpelsesmidler med anvendelse i Danmark på undersøgelsestidspunktet. Modelstofferne udvalgtes med baggrund i ønsket om at dække et bredt opløseligheds- og molvægts-spektrum. De eksperimentelle resultater indikerer generelt en U-formet sammenhæng mellem Kp og logPow, således at hurtigst penetration opnås ved en logPow værdi mellem 1½ og cirka 4. Et enkelt af de ni modelstoffer (malathion) falder udenfor denne generalisering. Der var ingen umiddelbar sammenhæng mellem molvægt og penetrationshastighed udtrykt som Kp. For de i dette studie anvendte modelstoffer gælder, at den korteste lag-time kan forventes af stoffer med en vandopløselighed mellem 3g/L og godt 20 g/L. Med stigende molvægt øgedes lag-time. Således var lag-time for det mindste modelstof med en molvægt på 122 gram nede på omkring 1½ time, medens lag-time ved molvægt over 350 gram oversteg 20 timer, hvilket er en ganske markant forskel, der også influerer på den mængde stof, der i løbet af en begrænset periode vil kunne absorberes dermalt. Igen adskiller malathion sig fra de øvrige modelstoffer.
Disse data planlægges anvendt i videre modellering af den dermale absorption. Fysiske og kemiske parametre for modelstoffer planlægges anvendt som determinanter for dermal absorption. At malathion falder ved siden af de øvrige modelstoffer indikerer, at andre faktorer end opløselighed og molvægt kan have betydning. Rumlig struktur vil derfor blandt andre parametre indgå som mulige determinanter.
Resultater fra nærværende undersøgelse indikerer, at der er en vis fraktion af det i huden midlertidigt deponerede modelstof, der rent faktisk returnerer til donorsiden af huden. Fraktionen er dog ikke voldsom stor for de lipofile stoffers vedkommende, men for de mere vandopløselige stoffer er data endnu ikke tilstrækkelige for valide tolkninger. Da det i andre sammenhænge har vist sig at den væsentligste barriere for netop de mere vandopløselige stoffer er den initiale passage fra donor og ind i huden, er der et reelt behov for med analoge eksperimentelle modeller at belyse denne problemstilling nærmere også for de mere vandopløselige stoffer.
Undersøgelserne med lettere beskadiget hud viste, at en sådan tilstand betyder en stærkt forøget dermal absorption for alle undersøgte stoffer. Udover umiddelbare reguleringsmæssige implikationer (beskrevet nedenfor) rejser fundene, der også er reproduceret af andre forskergrupper, en række relevante forskningsspørgsmål, der vil kræve eksperimentelle såvel som humane undersøgelser. Der er behov for flere eksperimentelle studier, herunder studier, der kan visualisere og dermed beskrive/dokumentere en beskadigelses omfang, samt hvorvidt en lettere beskadigelse betyder, at stoffer penetrerer ad veje, der normalt ikke er tilgængelige under intakte barriereforhold, eller om det blot er eksisterende adgangsveje, hvor transporten faciliteres. Der eksisterer metoder til denne form for visualisering, men potentialet i forhold til arbejdsmiljørelaterede problemstillinger er slet ikke udnyttet. Der er endvidere brug for humane undersøgelser omkring sammenhængen mellem en lettere beskadiget hud, tilstedeværelsen af kemiske stoffer på huden, samt regenereringen af hudens barrierefunktion. Det vil være undersøgelser der belyser såvel tids- som mængdemæssige forhold omkring absorption og regenerering.
Mange personer med hudeksponering fra kemiske stoffer beskytter sig med beskyttelsescremer eller handsker. Tidligere eksperimentelle studier har belyst effekten af forskellige handsketyper med enkelte modelstoffer. Der er med baggrund i nærværende undersøgelses påvisning af den markante indflydelse af stoffernes fysisk-kemiske parametre for penetration behov for at gentage en del af tidligere handskeforsøg med flere modelstoffer. Ligeledes er en meget interessant problemstilling handskernes beskyttelsesgrad i forhold til en underliggende beskadiget hud.
4.2 Regulerings og forebyggelsesmæssige perspektiver
Den nuværende regelsætning omkring vurdering af penetrationsforsøg følger gældende OECD guidelines, der foreskriver, at man skal henregne alt stof, der ikke er genfundet i donordelen som absorberet og dermed potentielt tilgængeligt for systemisk toksicitet. Dette gælder således også den fraktion af den administrerede dosis, der er ophobet i huden. Nærværende undersøgelse viser, at absorption fra huden og ud i receptordelen fortsætter efter endt eksponering. For visse stoffer fortsætter absorptionen i over et døgn efter endt eksponering. Der er derfor ingen tvivl om, at en vis del af den i huden deponerede mængde modelstof senere vil absorberes. Det er imidlertid ikke afklaret, hvor stor en fraktion af den i huden midlertidigt deponerede mængde modelstof, der vil fjernes uden at nå systemisk cirkulation, det vil sige ovenud af huden. Data fra nærværende undersøgelse indikerer, at der er en vis fraktion af det i huden midlertidigt deponerede modelstof, der rent faktisk returnerer til donorsiden af huden. For de lipofile stoffer indikerer de nærværende data således, at den nuværende anvendelse af data ved regelsætning for dermal absorption baseret på guideline-forsøg i en vis grad overestimerer den reelle absorberbare mængde fremmedstof ved at indregne alt stof ikke genfundet i donor som absorberet. Overestimatet er dog ikke voldsomt stort for de lipofile stoffers vedkommende og her synes den hidtil anvendte procedure pragmatisk anvendelig. For de mere vandopløselige stoffer er data endnu ikke tilstrækkelige for valide tolkninger.
Det kan på basis af de opnåede resultater konkluderes, at en afvaskning af huden efter endt eksponering signifikant nedsætter den samlede dermale absorption. For de mest vandopløselige stoffer med omkring 67 % og for de mere lipofile modelstoffer med lidt mindre. Det er således muligt ved almindelig let afvaskning at fjerne en del af den stofmængde, der allerede er trængt ind i huden. Denne observation har klare forebyggelsesmæssige implikationer, og dokumenterer betydningen af afvaskning med sæbeopløsning eller lignende efter endt arbejde, hvor man har haft dermal kontakt til fremmedstoffer.
En lettere beskadiget hud resulterer i en generel forøget penetrationshastighed for alle stoffer. Den kraftigt forøgede penetration af specielt de mere hydrofile modelstoffer gennem lettere beskadiget hud bør have den konsekvens, at man reguleringsmæssigt forholder sig til, at den reelle situation blandt en stor del af ansatte med dermal eksponering og ikke-intakt hud er, at de absorberer ganske meget mere dermalt, end de traditionelle in vitro guideline-forsøg, der anvendes som reguleringsgrundlag, indikerer. Man må her være opmærksom på, at det ikke alene drejer sig om personer med rifter eller lignende på huden, men potentielt også har relevans for den store del af befolkningen med mere eller mindre kroniske hudproblemer.
5 Referencer
Archibald BA, Solomon KR, Stephenson GR. Estimating pirimicarb exposure to greenhouse workers using video imaging. Arch Environ Contam Toxicol. 1994; 27: 126-129.
Benford DJ, Cocker J, Sartorelli P, Schneider T, van Hemmen J, Firth JG. Dermal route in systemic exposure. Scand J Work Environ Health. 1999; 25: 511-520.
Bornkessel A, Flach M, Arens-Corell M, Elsner P, Fluhr JW. Functional assessment of a washing emulsion for sensitive skin: mild impairment of stratum corneum hydration, pH, barrier function, lipid content, integrity and cohesion in a controlled washing test. Skin Res Technol 2005; 11: 53-60.
Brand RM, Mueller C. Transdermal penetration of atrazine, alachlor, and trifluralin: effect of formulation. Toxicol Sciences. 2002; 68: 18-23.
Campbell JL, Smith MA, Eiteman MA, Williams PL, Boeniger MF. Comparison of solvents for removing pesticides from skin using an in vitro porchine model. Am Ind Hyg Assoc J 2000; 61: 82-88.
Cnubben NHP, Elliott GR, Hakkert BC, Meuling WJA, van de sandt JJM. Comparative in vitro-in vivo percutaneous penetration of the fungicide ortho-phenylphenol. Reg Toxicol Pharmacol 2002; 35: 198-208.
Cross SE, Magnusson BM, Winckle G, Anissimov Y, Roberts MS. Determination of the effect of lipophilicity on the in vitro permeability and tissue reservoir characteristics of topically applied solutes in human skin layers. J Invest Dermatol 2003; 120: 759-764.
Dick IP, Blain PG, Williams FM. The percutaneous absorption and skin distribution of lindane in man. I. In vivo studies. Hum Exp Toxicol 1997; 16: 645-651.
Elias PM. Epidermal lipids, barrier function, and desquamation. J Invest Dermatol 1983; 80: 44S-49S.
Forslind B, Engström S, Engblom J, Norlén. A novel approach to the understanding of human skin barrier function. J Dermatol Sc 1997; 14: 115-125.
Grandjean P. Skin penetration. Hazardous chemicals at work. Taylor & Francis, London, 1990: 1-187.
Jakasa I. Dermal absorption of chemicals through normal and compromised skin. PhD-thesis, Coronel Institute of Occupational Health, University of Amsterdam, the Netherlands 2006, 166 pp.
Magnusson BM, Anissimov YG, Cross SE, Roberts MS. Molecular size as the main determinant of solute maximum flux across the skin. J Invest Dermatol 2004; 122: 993-999.
Morgan CJ, Renwick AG, Friedmann PS. The role of stratum corneum and dermal microvascular perfusion in penetration and tissue levels of water-soluble drugs investigated by microdialysis,. Br J Dermatol 2003; 148: 434-443.
Nielsen JB. Hudpenetration af pesticider – en undersøgelse af effekten af hjælpestoffer, kombinationseffekter, handsker, samt lettere beskadiget hud. Bekæmpelsesmiddelforskning fra Miljøstyrelsen 2004, 90: 1-62.
Nielsen JB. Percutaneous penetration through slightly damaged skin. Arch Dermatol Res 2005; 296: 560-567.
Nielsen JB, Nielsen F. Dermal in vitro penetration of methiocarb, paclobutrazol and pirimicarb. Occup Envir Med 2000; 57: 734-737.
Nielsen JB, Nielsen F, Sørensen JA. In vitro percutaneous penetration of five pesticides - effects of molecular weight and solubility characteristics. Ann Occup Hygiene 2004; 48: 697-705.
Ramsey JD, Woollen BH, Auton TR, Scott RC. The predictive accuracy of in vitro measurements for the dermal absorption of a lipophilic penetrant (fluazifop-butyl) through rat and human skin. Fundam Appl Toxicol 1994; 23: 230-236.
van de Sandt JJM, van Burgsteden JA, Cage S, Carmichael PL, Dick I, Kenyon S, Korinth G, Larese F, Limasset JC, Maas WJM, Montomoli L, Nielsen JB, Payan J-P, Robinson E, Sartorelli P, Schaller KH, Wilkinson SC, Williams FM. In vitro predictions of skin absorption of caffeine, testosterone and benzoic acid: a multi:centre comparison study. Reg Toxicol Pharmacol 2004; 39: 271-281.
Zendzian RP. Pesticide residue on/in the washed skin and its potential contribution to dermal toxicity. J Appl Toxicol. 2003; 23: 121-136.
Version 1.0 Maj 2007 • © Miljøstyrelsen.