[Forside] [Indhold] [Forrige] [Næste]
Naturlig nedbrydning af olie og chlorerede opløsningsmidler i grundvandet på Drejøgade 3-5.
Bilag 8: Kvantificering af den naturlige omsætning af BTEX ud fra
kulstofmetoden
Formål
At kvantificere den naturligt forekommende omsætning af organisk stof i en aquifer
Metode
Kulstofmassebalancen, som udgøres af uorganisk kulstof (TUC), ikke-flygtigt organisk kulstof (NVOC) samt flygtigt organisk kulstof (VOC), betragtes.
Nedenstående er baseret på /Ref.16/
Definitioner
TUC (mol/l eller mg C/l)
Uorganisk kulstof
[CO2] + [HCO3-] + [H2CO3] + [CO32-]
= [CO2] + [HCO32-], ved pH < 8
NVOC (mol/l eller mg C/l)
Ikke flygtigt organisk kulstof [C6H12O6] mv.
VOC (mol/l eller mg C/l)
Flygtigt organisk kulstof
[PCE] + [VC] + [BTEX] + [CH4] mv.
ALK (mekv/l)
Alkalinitet
[HCO3-] + [CO32-] + [OH-] + [H+]
@ [HCO3-], da man for pH-værdier i
normale danske grundvandsmagasiner kan se bort fra
[OH-] og [H+], samt [CO32-] for pH < 8
Flowdiagram
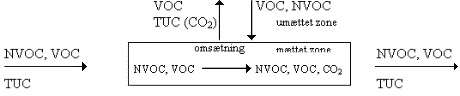
Massebalance
(NVOC + TUC + VOC)ind = (NVOC + TUC + VOC)ud Ű
D (NVOC + TUC + VOC) = 0
D TUC = D NVOC + D
VOC
(ligning 1)
Antagelse
En forøgelse af TUC (samt CH4) er forårsaget af omsætning af organisk stof.
Kommentarer
TUC-forøgelsen, og dermed den naturlige omsætning af organisk stof, vil undervurderes, hvis:
- der sker en afgasning af CO2 (og CH4) til den umættede zone
- der sker en opblanding på tværs af strømningsretningen med uforurenet grundvand
TUC-forøgelsen, og dermed den naturlige omsætning af organisk stof, vil overvurderes, hvis:
- der sker en opløsning af carbonatholdige forbindelser
- der sker alkalinitets-øgende processer (andre end oxidation af organisk stof, som f.eks. oxidation af jern)
Beregninger
TUC = ALK (1+10(pK1-pH)) (ligning 2)
pK1 er første dissociationskonstant for H2CO3 (=6,48 ved 9° og ionstyrke 0)
I denne beregning er der imidlertid ikke taget hensyn til, at CO2, dannet ved oxidation af NVOC og VOC, reagerer med jordens indhold af carbonatholdige mineraler som f.eks. kalk.
CO2 + CaCO3 + H2O = Ca2+ + 2*HCO3-
Herved sker der en forøgelse af TUC, som ikke skyldes oxidation af organisk stof, men som er en følge af en forskydning i carbonatsystemet. 1 mol C (CO2) fra oxidation af organisk stof, er nu blevet til 2 mol C (2*HCO3-), hvilket der bør korrigeres for, da det kun er C, som stammer fra redoxprocessen, hvor NVOC og VOC oxideres, der ønskes medregnet.
D TUCredox = D TUC - ˝*D ALK*1 mmol/mekv (ligning 3)
Beregning
Følgende er målt:
Enhed |
Opstrøms |
I kilden |
I fanen |
|
| Benyttede boringer | MB3 |
MB6 |
MB14 |
|
| pH | - |
7 |
6,63 |
6,7 |
| [HCO3-] | mg/l |
360 |
870 |
710 |
| CH4 | mg/l |
0,16 |
17 |
0,64 |
| NVOC | mgC/l |
3,4 |
16 |
2,7 |
| Total kulbrinter | mg/l |
3 |
12 |
0,5 |
Følgende er beregnet:
Enhed |
Opstrøms |
I kilde |
I fanen |
|
| ALK = [HCO3-]/(61 mg/mmol)*(1mekv/mmol) | mekv/l |
5,9 |
14,3 |
11,6 |
| D ALK | mekv/l |
8,4 |
5,6 |
|
| TUC = ALK (1+10(pK1-pH)) | mmol/l |
7,7 |
24,4 |
18,3 |
| D TUC | mmol/l |
16,7 |
10,6 |
|
| D TUCredox = D TUC - ˝*D ALK*1 mmol/mekv | mmol/l |
12,5 |
7,8 |
|
| D TUCredox = D TUCredox (mmol/l)* 12 mg/mmol | mgC/l |
150 |
94 |
| Enhed | Opstrøms | I kilde | I fanen | |
| D CH4 | mg/l |
17 |
0,64 |
|
| D CH4 = D CH4 (mg/l) * 12/(12+4*1) | mgC/l |
12,75 |
0,48 |
Molarmassen af HCO3- = 61 g/mol
Molarmassen af C = 12 g/mol
Molarmassen af H = 1 g/mol
|
|