Udvikling af måleteknik for optimering og beskrivelse af lugtbegrænsende teknologier til husdyrbrug
3 Målemetoder
3.1 Olfaktometri
De olfaktometriske målinger foretaget i dette projekt er foretaget efter den gældende standard og vil derfor ikke blive detaljeret gennemgået her.
Lugtmålingerne blev foretaget ved opsamling af en repræsentativ luftmængde. I ventilationsafkastet var isat en Teflon-slange, som var monteret til en 30 liter Teflon-pose. Opsamlingen blev foretaget efter CEN-norm (CEN/TC264/WG2/N222/e – analyseforskrift 66009-ANF-016-udgave 05). I CEN-normen stilles ingen krav om, hvor hurtigt luftprøverne skal opsamles, men det blev valgt at fylde poserne med 0,7 liter pr. minut, det vil sige i løbet af 40 minutter.
Poserne med luftprøver blev fragtet til Slagteriernes Forskningsinstituts Lugtlaboratorium, Roskilde. Lugtkoncentrationen blev bestemt ved Olfaktormetermetoden efter CEN-norm (CEN/TC264/WG2/N222/e – analyseforskrift 66009-ANF-012-udgave 05).
3.2 MIMS
3.2.1 Introduktion
MIMS er en forkortelse for membran-inlet massespektrometri. Denne målemetode er baseret på, at flygtige stoffer absorberes i en silikonemembran, der er placeret umiddelbart foran ionkilden på et massespektrometer. Som følge af det meget lave tryk, der findes i massespektrometret (< 10-5 mbar), vil disse stoffer diffundere gennem membranen og afgasse på indersiden. Forbindelserne ioniseres i gasfasen, og de dannede ioner detekteres ved hjælp af et quadropol massespektrometer (Balzer QMA 125).
Teknikken giver anledning til massespektroskopiske signaler udtrykt som en intensitet (et elektrisk signal, fx Ampere) som funktion af forholdet mellem masse og ladning m/z. Normalt opnår de dannede ioner kun en ladning på 1, således at den detekterede m/z-værdi svarer til massen af en molekylar- eller fragment-ion.
Ioniseringen af de kemiske forbindelser giver anledning til dannelse af molekylar-ioner eller fragment-ioner afhængig af stabiliteten af de dannede ioner. Som eksempel er i Tabel 1 vist de vigtigste massespektroskopiske fragmenter og det resulterende massespektrum (Figur 1) for butansyre (smørsyre).
Tabel 1 Udvalgte masse-spektroskopiske fragmenter for butansyre med tilhørende m/z-værdier.
| Struktur | M/z-værdi | Type |
| 88 | Molekylar-ion | |
| 73 | Fragment-ion | |
| 71 | Fragment-ion | |
| 60 | Fragment-ion | |
| 45 | Fragment-ion | |
| 43 | Fragment-ion |
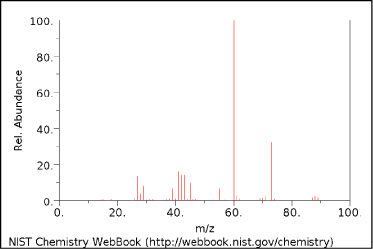
Figur 1 Standard masse-spektrum af butansyre.
Fragmenteringsmønstret for et givet stof er reproducerbart for den ioniseringstype, der anvendes, og kan således anvendes til at detektere og identificere stoffet.
Lugtkomponenterne kan enten måles ved selektiv ion-monitering (SIM), hvor et antal udvalgte molekylar- eller fragment-ioner moniteres over et passende tidsrum (typisk 5-20 sekunder ad gangen) eller ved at måle hele masse-spektre, hvor der fx scannes fra m/z 45 til m/z 200 i løbet af 1-2 minutter. SIM-teknikken giver den klart bedste følsomhed (lavere detektionsgrænse), eftersom der kan måles længere tid på hver enkelt ion, og er mere velegnet til kontinuerte målinger. Der kræves til gengæld et vist forhåndskendskab til sammensætningen af kemiske forbindelser.
3.2.2 Test af MIMS på en blanding af relevante lugtstoffer
For at afprøve MIMS-teknikkens muligheder mht. måling af lugtstoffer blev der gennemført en indledende laboratorieundersøgelse af instrumentets respons over for en udvalgt blanding af lugtstoffer, der typisk findes i gylle og afkast fra svinestalde.
Stofferne blev udvalgt på baggrund af et litteraturstudie (Hartung og Hilliger, 1111; Hartung og Phillips, 1994; Hobbs et al., 1997; Hobbs et al., 2005; Persaud et al., 2005; Schiffman et al., 2001; Zahn et al., 1997) samt tidligere GC/MS-analyser af svinestaldsluft udført af Teknologisk Institut.
De udvalgte stoffer er præsenteret i Tabel 2 sammen med koncentrationen i den kraftigste blanding og stoffets lugttærskelværdi fra Devos et al. (1990). Der er anvendt de af Devos et al. (1990) foreslåede standardiserede lugttærskelværdier opstillet på baggrund af en vægtning af de på det pågældende tidspunkt kendte målinger af lugttærskler for enkeltstoffer. Der findes desværre ikke nyere kompilerede opslagsværker for lugttærskler på trods af, at der er gennemført talrige bestemmelser af lugttærskelværdier siden udgivelsen af Devos et al. (1990). De anvendte lugttærskelværdier skal generelt omfattes med en vis forsigtighed, da der for mange stoffer er stor spredning på de målte tærskelværdier. Desuden er lugttærsklen for visse stoffer baseret på få målte værdier.
I Tabel 2 er endvidere medtaget stoffets relative bidrag til den samlede lugt, hvis det antages, at stoffernes effekt er additiv. De relative bidrag er beregnet ud fra stoffets ”kemiske lugtenhed” (COU; Chemical Odour Units), hvor COU er defineret som koncentration divideret med lugttærskel. Dette bidrag er omfattet af en betydelig usikkerhed som følge af den førnævnte usikkerhed, der er på bestemmelsen af de anvendte standardiserede lugttærskelværdier.
Specielt skal det bemærkes, at lugttærskelværdien for indol opgivet i Tabel 2 er usikker, idet den er baseret på en enkelt undersøgelse af ældre dato, og at lugttærsklen for skatol er påvirket af en enkelt afvigende undersøgelse af ældre dato. En enkelt undersøgelse, hvor lugttærsklerne for disse to stoffer blev bestemt under identiske betingelser, indikerer, at lugttærkslen for skatol er lavere end lugttærsklen for indol (van Gemert, 2003).
Det skal endvidere understreges, at effekten af enkeltstofferne formentlig ikke er additiv, idet det må antages, at der skal tages højde for såvel synergistiske som antagonistiske effekter.
Tabel 2 Udvalgte stoffer, højeste koncentration (µg/m³), lugttærskel (µg/m³) og relativt bidrag.
| Lugtstof | Koncentration | Lugttærskel | Relativt bidrag (COU %)¹ |
| Dimethylsulfid | 182,5 | 5,8 | 1,3 |
| Trimethylamin | 3473,4 | 5,9 | 24,6 |
| Eddikesyre | 5298,4 | 361,5 | 0,6 |
| Butansyre | 7771,1 | 14,3 | 22,7 |
| 3-Methylbutansyre | 4062,1 | 10,4 | 18,0 |
| Nonanal | 104,5 | 13,3 | 0,3 |
| 4-Methylphenol | 1589,5 | 8,4 | 7,9 |
| Indol | 86,1 | 0,2 | 23,3 |
| Skatol | 96,4 | 3,1 | 1,3 |
¹ Det relative bidrag er beregnet som stoffets COU-værdi (konc./lugttærskel) i % af den samlede COU-værdi.
Koncentrationen af lugtstoffer blev fastlagt ud fra et ønske om at opnå lugtkoncentrationer i størrelsesordenen 2400 OU/m³ og lavere. Dette interval af lugtkoncentrationer er repræsentativt for svinestalde, hvor 2400 OU/m³ må betegnes som en høj lugtkoncentration. For at opnå en omtrentlig forudsigelse af lugtkoncentrationen blev de beregnede lugtbidrag fra de forskellige stoffer adderet, og totalkoncentrationen i den kraftigste lugtblanding blev derefter justeret til en koncentration svarende til ca. 2400 COU.
Den relative sammensætning er vist i Figur 2 som både koncentration og som chemical odour units (COU). Som det fremgår, kan et stof have en lav koncentration og alligevel bidrage betragteligt til total-COU (fx indol), hvis det har en meget lav lugttærskel. Ligeledes kan et stof have en høj koncentration uden at bidrage væsentligt til total-COU (fx eddikesyre).
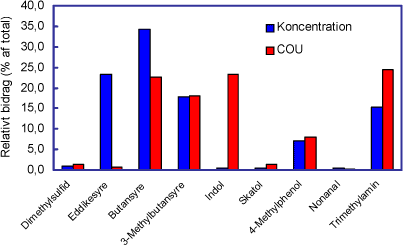
Figur 2 Sammensætning af syntetisk lugtblanding. Sammensætningen er vist som koncentration relativt til totalkoncentration og som COU relativt til total-COU.
Lugtstofblandingen vist i Tabel 2 blev fremstillet ud fra opløsninger af de rene stoffer i methanol eller vand, og en stamopløsning blev fremstillet ved fortynding med vand til en passende koncentration. For at opnå de ønskede luftkoncentrationer blev varierende mængder (2,5-10 µL) opløsning tilsat til 25-L Tedlar-poser indeholdende 20 L ren luft afmålt ved hjælp af en masse-flow-controller. For at opnå lave koncentrationer blev stamopløsningen fortyndet 1:10, og 5 eller 10 µL af denne fortynding blev tilsat posen.
Det er veldokumenteret, at Tedlar-poser afgiver phenol og N,N-dimethylacetamid, og at denne afgivelse stiger som funktion af tid. Det er derfor vigtigt, at alle poser behandles ens. Følgende fremgangsmåde blev anvendt:
- Umiddelbart efter påfyldning af luft blev en lugtblanding injiceret
- Efter præcis 15 minutter blev et flow på 100 ml/min. suget fra posen til MIMS-instrumentets membran-inlet
- Der måltes herefter kontinuert med MIMS, og et signal blev aflæst efter 10 minutter
De 15 minutters ventetid var nødvendigt for at sikre, at stofferne befandt sig på dampform.
Der blev fremstillet 2 poser for hver koncentration, således at alle prøver er dobbeltbestemt mht. påfyldning af luft og lugtstoffer såvel som selve analysen. Forsøget er fordelt over to dage. På hver af de to dage blev et sæt af poser med højest koncentration analyseret.
På baggrund af resultaterne blev signalerne for hvert stof plottet som funktion af koncentration.
For de tre carboxylsyrer (eddikesyre, butansyre og 3-methyl-butansyre) er anvendt et fælles signal ved m/z 60. I Figur 3 til Figur 5 er vist eksempler på plot af MIMS-signal som funktion af koncentration.
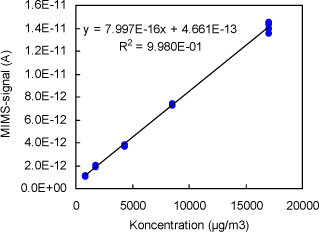
Figur 3 Plot af signal vs. koncentration for ?RCOOH (m/z = 60). Signalerne er ikke korrigeret for baggrundsbidrag fra Tedlar-poserne.
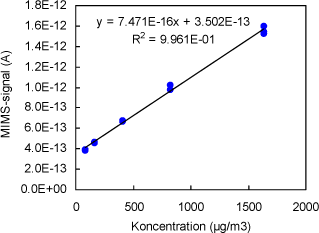
Figur 4 Plot af Signal vs. koncentration for 4-Methylphenol. Signalerne er ikke korrigeret for baggrundsbidrag fra Tedlar-poserne.
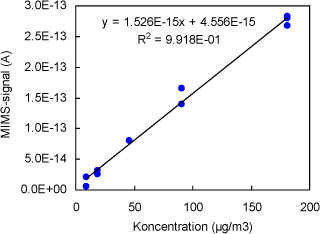
Figur 5 Plot af signal vs. koncentration for Dimethylsulfid (m/z = 47). Signalerne er ikke korrigeret for baggrundsbidrag fra Tedlar-poserne.
Data for alle komponenter er præsenteret i Tabel 3. RSD er den relative standardafvigelse i % beregnet ud fra analyser af de fire prøver med højest koncentration. Detektionsgrænsen er estimeret ud fra 3´standardafvigelse på måling af ren laboratorieluft og er således gældende for direkte målinger, hvilket er det mest relevante i forhold til de egentlige online målinger, der er foretaget i projektet, hvor luften ikke er opsamlet i poser. Hvis der anvendes poser, vil detektionsgrænserne blive højere som følge af et højere baggrundsbidrag pga. Tedlar-posernes tidligere nævnte afgivelse af stoffer.
Tabel 3 Analysekemiske parametre for komponenter i testblandingen.
| Komponent | M/z-værdi | RSD (%) | Det. grænse (µg/m³) |
R² |
| ΣRCOOH | 60 | 3,1 | 30,8a | 0,9980 |
| Dimethylsulfid | 47 | 2,6 | 1,3 | 0,9918 |
| Trimethylamin | 59 | 6,3 | 144,3 | 0,9616 |
| 4-Methylphenol | 108 | 2,4 | 18,2 | 0,9961 |
| Nonanal | 98 | 5,8 | 1,4 | 0,9943 |
| Indol | 117 | 4,7 | 5,7 | 0,9967 |
| Skatol | 130 | 3,9 | 2,8 | 0,9943 |
a Den estimerede detektionsgrænse gælder for den aktuelle blanding af carboxylsyrer (se tekst).
Som det fremgår af Tabel 3, giver MIMS-målingerne en tilfredsstillende lineær sammenhæng mellem koncentration og respons. Med undtagelse af trimethylamin er korrelationskoefficienterne R² > 0,99. For alle stoffer ses en tilfredsstillende reproducerbarhed. MIMS har generelt en ringere sensitivitet over for trimethylamin sammenlignet med de øvrige stoffer, hvilket giver sig udslag i en højere detektionsgrænse.
Ud fra kontrolmålinger af eddikesyre og butansyre hver for sig uden tilstedeværelse af andre komponenter viste det sig, at MIMS har en lavere sensitivitet over for eddikesyre end over for butansyre og 3-methylbutansyre. Det vurderes, at detektionsgrænsen for butansyre og 3-methylbutansyre er i størrelsesordenen 10-20 µg/m³, og at detektionsgrænsen for eddikesyre er ca. 50 µg/m³.
MIMS-instrumentets sensitivitet over for et stof afhænger af stoffets fysisk-kemiske karakteristika. Et stof opsamles i instrumentets membran-inlet og overføres til massespektrometret i tre trin: 1) absorption i membranen, 2) diffusion henover membranen og 3) fordampning på indersiden af membranen. Instrumentet er således følsomt over for forholdsvis små, flygtige og hydrofobe stoffer. Dimethylsulfid er et eksempel på et sådant stof. Små carboxylsyrer som eddikesyre og butansyre er ligeledes forholdsvis små og flygtige, men er til gengæld mere polære, hvorfor instrumentets følsomhed over for disse stoffer er lavere.
Den lineære sammenhæng mellem signal og koncentration er en generel observation i forbindelse med kalibrering af MIMS. Typisk ses en lineær sammenhæng over adskillige dekader. Dette har den implikation i forbindelse med undersøgelser af teknologier, der har til formål at reducere stoffer, der kan måles af MIMS, at det ikke er nødvendigt at omregne fra målesignal til koncentration for at opnå en reduktionsgrad.
Reduktionsgraden for en specifik komponent A, RA, kan udtrykkes som:
![]()
hvor CA er koncentrationen af et stof i et behandlet/renset system, og CA,0 er koncentrationer af et stof, der ønskes fjernet eller reduceret, i koncentrationen i ikke-behandlet luft, fx før et filter.
Koncentrationen af stoffet A, CA, er ligefrem proportional med målesignalet:
![]()
SA er det målte signal for stoffet A målt ved en relevant m/z-værdi, RFA er en responsfaktor svarende til hældningen på et plot af signal som funktion af koncentration, og SBG er et nulpunkts-signal (for ren luft) for den pågældende m/z værdi.
CA kan dermed udtrykkes som:
![]()
Hvoraf følger, at reduktionsgraden kan udtrykkes ved de målte nulpunktskorrigerede signaler:
![]()
3.3 TD-GC/MS-O
Flygtige organiske stoffer fra luftprøver er opsamlet ved dynamisk headspace på prøveopsamlingsrør (adsorptionsrør). Stofferne er frigivet fra røret ved termisk desorption (TD) og efterfølgende analyseret ved gaskromatografi (GC) med massespektrometrisk detektor (MS) samtidig med olfaktometriske detektorer (O (to næser)). En mere detaljeret gennemgang af metoden er givet i Adamsen og Schäfer (2006).
Ved kobling af olfaktometri sammen med en GC/MS-analyse fås en samtidig evaluering af stoffernes lugtbidrag. Begrænsningen er, at der ikke tages højde for eventuelle interaktioner, idet evalueringen sker på basis af de separerede stoffer enkeltvis og ikke i blanding. Lugt er ikke en simpel addering og subtraktion af lugte, men et komplekst sammenspil, hvor fænomener som hypo-additivitet (maskeringseffekt), additivitet og hyper-additivitet (synergistisk effekt) kan forekomme mellem flygtige stoffer. Kombinationen kan til gengæld være medvirkende til at afdække evt. stoffer til stede i så lave koncentrationer, at en GC/MS-analyse alene ikke ville detektere disse, men stofferne kan have en meget lav lugttærskelværdi og dermed have stor betydning for det samlede lugtbidrag.
3.3.1 Dynamisk headspace-opsamling og termisk desorption
Ved dynamisk headspace-opsamling suges et veldefineret volumen luft (kendt flow og opsamlingstid) gennem et prøveopsamlingsrør. Røret er pakket med et materiale, der adsorberer de flygtige organiske stoffer fra luften. Røret kan herefter transporteres til laboratoriet til videre analyse.
3.3.2 GC/MS
I en Automatisk Termisk Desorber (ATD) desorberes blandingen af de flygtige organiske stoffer fra røret til gaskromatografen. Blandingen af flygtige organiske stoffer separeres på den gaskromatografiske kolonne og eluerer ideelt set enkeltvis til den massespektrometriske detektor, hvorved stofferne kan identificeres og kvantificeres. Metoden benytter SCAN, hvor der skannes over et masseområde fra m/z 33 til 350. Massespektret, som fremkom, blev sammenlignet med massespektre fra NIST-database, som indeholder ca. 200.000 massespektre. Et udvalgt antal stoffer kvantificeres over for en standard af stoffet. I standarden indgår 38 stoffer. Prøven analyseres for indhold af disse 38 stoffer ud fra en kombination af retentionstid (Rt – den tid, hvor stoffet eluerer på den gaskromatografiske kolonne), og forholdet mellem target og qualifier-ioner (2-4 karakteristiske ioner fra massespektret af et stof). Øvrige identificerede stoffer er angivet i sniff-tabellen (Tabel 9) med en beregnet LRI-værdi (Lineær Retentionstids Indeks – en normering af retentionstiderne over for en standard med alkaner).
3.3.3 GC/Olfaktometri
GC/O, Gaskromatografi-Olfaktometri, også kaldet GC-sniff, er en vigtig analyseteknik i flavour-forskningen, fordi den karakteriserer lugtene af enkeltkomponenter eller komplekse blandinger af flygtige stoffer. Her agerer den menneskelige næsedetektor i bedømmelsen af en strøm af lugte fra GC’en. Næsen har en teoretisk lugtdetektionsgrænse på ca.
10-19 mol, hvilket er ensbetydende med, at GC/O er et meget værdifuldt og følsomt værktøj til detektering af lugtaktive flygtige stoffer (Pollien et al., 1997).
Undersøgelser har vist, at GC/O kan bruges i forbindelse med analyse af staldluft. Frekvensanalyse resulterede i detektion af 25 lugte, hvoraf propansyre, 2-methylpropansyre, butansyre, 4-methylphenol, oktansyre, indol og skatol blev identificeret (Kai og Schäfer, 2004). De øvrige 18 lugte blev ikke identificeret, men havde stadig betydning for det samlede lugtbidrag.
Begrænsningerne ved GC/O er, at lugtbidraget af et aromastof bedømmes separat, når det eluerer fra GC-kolonnen. Stoffet bedømmes ude af sammenhæng, og det gør evalueringen af dets bidrag til lugten besværlig. Andre begrænsninger ved GC/O er udmattelse, sensorisk mætning og tilvænning af den menneskelige næse, hvilket vil influere negativt på intensitetsmålinger og må forsøges undgået. Forholdene, under hvilke GC/O-analyse udføres, har signifikant indflydelse på validiteten af de opsamlede data. Larm, distraktion, lugte og ukomfortable forsøgsbetingelser kan introducere fejl i analysen. Disse begrænsninger tages der højde for i træningen af dommerne og i den daglige analyse.
De udførte analyser foregik ved, at flowet fra den gaskromatografiske kolonne bliver delt i tre strømme, hvor den ene går til den massespektrometriske detektor og de to øvrige til hver sin snif port. Ved snifporten sidder en dommer og bedømmer hver lugt, som eluerer. Dommeren markerer, hvornår lugten eluererer og indplacerer lugten i en af ti lugtbeskrivende kategorier. Hver prøve bliver bedømt af seks dommere, og resultatet af deres markeringer opsummeres i et aromagram. Hvis en lugt detekteres af alle seks dommere, har lugten stor betydning, og hvis en lugt kun detekteres af en eller to af dommerne, har lugten mindre betydning. Lugtene identificeres om muligt ved at sammenholde retentionstiderne for lugtmarkeringerne med den massespektrometriske analyse. For identificerede stoffer sammenholdes lugtbeskrivelserne fra litteraturen med de lugtbeskrivende kategorier som dommerne har indplaceret lugtene i. Resultatet er, at luftens indhold af flygtige organiske stoffer kan rangeres efter deres betydning for lugten.
Metoden er optimeret og beskrevet i sin helhed i ”Kemisk bestemmelse af lugtstoffer fra husdyr og udvikling af målemetoder” (Adamsen og Schäfer, 2005).
3.4 Indledende sammenligning af måleteknikker
De luftposer, der blev anvendt til test af MIMS med hensyn til detektion af lugtstoffer, blev målt olfaktometrisk den efterfølgende dag af SFs lugtlaboratorium. Der blev afsendt 2 sæt lugtposer, hvert bestående af 6 prøver. Det første sæt bestod af parvis ens prøver, der var tilsat hhv. 10, 5 og 2,5 µL af en kendt blanding af lugtstoffer.
Resultater af de olfaktometriske analyser af første sæt prøver er præsenteret i Tabel 4. Som det fremgår, var der ingen signifikant forskel mellem de tre sæt prøver på trods af, at koncentrationerne af lugtstoffer målt i laboratoriet den foregående dag var markant forskellige.
Tabel 4 Resultater af olfaktometriske analyser af første sæt kunstige lugtprøver.
| Vol. tilsat | Pose 1 | Pose 2 |
| 10 µL | 4700 | 4000 |
| 5 µL | 4100 | 4700 |
| 2,5 µL | 3800 | 4700 |
Det blev derfor besluttet, at næste sæt prøver skulle spænde over et større koncentrationsinterval.
Det andet sæt bestod derfor af parvis ens prøver, der var tilsat hhv. 10 µL af den oprindelige blanding, 10 µL af en 1:10 fortynding og 5 µL af en 1:10 fortynding. Resultaterne af olfaktometriske analyser af andet sæt er vist i Tabel 5.
Tabel 5 Resultater af olfaktometriske analyser af andet sæt kunstige lugtprøver.
| Vol. tilsat | Pose 1 | Pose 2 |
| 10 µL | 1900 | 2800 |
| 10 µL 1:10 | 2200 | 2200 |
| 5 µL 1:10 | 2000 | 2100 |
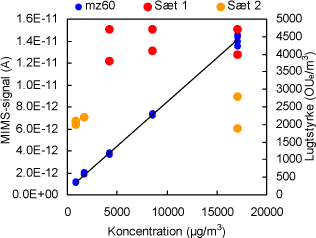
Figur 6 Plot af hhv. MIMS-signal for carboxylsyrer og lugtstyrke som funktion af koncentrationen af carboxylsyrer.
Det fremgår af Tabel 4, Tabel 5 og Figur 6, at der ikke er en klar sammenhæng mellem mængden af lugtstoffer, der er tilsat, og lugtstyrken, ligesom der heller ikke er nogen sammenhæng mellem MIMS-målingerne og lugtstyrken. Derimod er der en glimrende sammenhæng mellem mængden af lugtstoffer og MIMS-signalerne.
Det bemærkes endvidere, at de prøver, der er tilsat samme mængde lugtstof (10 µL blanding) med to dages mellemrum gav anledning til forskellige måleresultater for lugtstyrke på trods af, at MIMS-målingerne viste, at prøverne var sammenlignelige umiddelbart efter fremstilling.
Forklaringen herpå skal formentlig til dels findes i den usikkerhed, der er forbundet med olfaktometriske analyser. Endvidere kan eventuelle fysiske og/eller kemiske ændringer i tidsrummet (ca. 20-24 timer) mellem MIMS-analyse og olfaktometrisk analyse muligvis have påvirket resultaterne. Fx er det teoretisk muligt, at der kan have forekommet udfældning eller adsorption på luftposernes inderside. Hvorvidt dette er sandsynligt, og hvilken rolle det kan have spillet, kan ikke afgøres på baggrund af de udførte forsøg. Det er dog tidligere konstateret, at der ikke sker en afgørende ændring af lugtstyrke ved transport af lugtprøver opsamlet i poser. Det bør noteres, at der i de kunstige lugtprøver arbejdes med forholdsvis tør luft, hvorimod der i rigtige prøver er betingelser med høj fugtighed.
Version 1.0 August 2006, © Miljøstyrelsen.