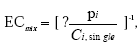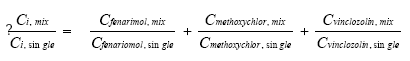|
Bekæmpelsesmiddelforskning fra Miljøstyrelsen nr. 88, 2004 Hormonforstyrrende effekter af kombinationer af pesticiderIndholdsfortegnelse
2 Mekanismer for kombinationseffekter af hormonforstyrrende stoffer
3 Hormonforstyrrende effekter af en kombination af almindeligt anvendte pesticider
4 Samlet diskussion og konklusion ForordNærværende projekt blev udført i perioden 1. april 2001 til 1. marts 2004. De deltagende institutter var Afdeling for Toksikologi og Risikovurdering, Danmarks Fødevare- og Veterinærforskning, Institut for Miljømedicin, Syddansk Universitet, Odense og Institut for Miljø- og Arbejdsmedicin, Århus Universitet. Projektet blev støttet af midler fra Pesticidforskningspuljen i Miljøstyrelsen. Forfatterne ønsker at takke Miljøstyrelsen for denne bevilling og vil specielt takke Jørn Kirkegaard for administrativ styring af projektet og Susanne Hougaard for faglig sparring. Denne rapport kunne ikke være blevet til uden en stor indsats fra videnskabelige medarbejdere, laboranter og dyrepassere. Vi ønsker at takke : Birgitte Møller Plesning, DFVF En styregruppe for projektet blev etableret under ledelse af Jørn Kirkegaard fra Miljøstyrelsen. Medlemmerne var Ulla Hass, Danmarks Fødevare- og Veterinærforskning, Torben Greve, Den Kongelige Veterinær- og Landbohøjskole, Anne Grethe Byskov, Rigshospitalet, og Phillipe Grandjean, Syddansk Universitet, Odense. Mørkhøj, Februar 2004 Sammenfatning og konklusionerBefolkningen er som oftest eksponeret for blandinger af kemikalier, hvoraf flere er mistænkt for at have hormonforstyrrende egenskaber. Mange af disse kemikalier har i sig selv en svag virkning i forhold til effekten af vores kønshormoner og det er vanskeligt at forklare mulige sundhedsrisici alene på basis af effekten af enkeltstofferne. Men det er sandsynligt, at disse hormonforstyrrende kemikalier spiller sammen på en måde, der forøger deres hormonale effekter og det er derfor vigtigt at få belyst de mekanismer for interaktioner, der måtte være mellem stofferne. Derfor er dette studie, der specielt sigter på at belyse kombinationseffekter af hormonforstyrrende pesticider, igangsat. Det overordnede formål er også at bidrage med et input til diskussionen om principper for risikovurdering af kemikalier, hvor der traditionelt ikke tages højde for, at vi er eksponeret for blandinger af kemikalier. Hovedparten af det arbejde, der er lavet omkring kombinationseffekter af hormonforstyrrende stoffer er baseret på in vitro undersøgelser af meget varierende kvalitet og meget få in vivo undersøgelser på blandinger af hormonforstyrrende stoffer er blevet udført hidtil. Undersøgelser af kombinationseffekter af antiandrogene kemikalier har ikke tidligere været udført. Det er vist, at kombinationseffekten kan variere i det samme eksperimentelle system afhængig af det valgte endpoint. Stoffer som eksempelvis virker synergistisk på det molekylære niveau (e.g. receptor binding) kan udvise additivitet, når der måles på mere komplekse funktionelle niveauer så som cellevækst. Af denne grund har vi anset det for vigtigt at udføre analyse af kombinationseffekter af hormonforstyrrende stoffer ved forskellige niveauer af molekylær kompleksitet inklusive in vivo studier. Mekanismen for samspilseffekter mellem pesticider med hhv. østrogen og antiandrogen aktivitet blev undersøgt dels i in vitro studier og dels in vivo i kort-tids dyreforsøg. Som modelstoffer for de østrogene pesticider blev o,p-DDT og methoxychlor valgt, og testsystemerne bestod dels af et brystcancercelle-proliferationsassay og en uterusvægttest i hunrotter, der har fået fjernet æggestokkene. I in vitro forsøgene sås god overensstemmelse mellem de målte effekter og de prædikterede værdier for additiv virkning beregnet ud fra isobolmetoden. I in vivo forsøgene blev undersøgt effekt på uterusvægt, effekt på serumniveauer af follikelstimulerende hormon (FSH), luteiniserende hormon (LH) og prolaktin, effekt på mRNA niveauer for østrogen receptorα og β (ER) og laktoferin i uterusvæv og på udvalgte neurotransmittere og acetylcholinesteraseaktivitet i hjernevæv. Kort fortalt sås med begge pesticider en stigning i uterusvægt og prolaktinniveau, mens LH-, FSH-niveau og ERα, ERβ og laktoferin mRNA niveauer faldt. Der sås ikke effekt på neurotransmitterniveauer og aktivitet af acetylcholinesterase. På baggrund af de opnåede resultater for organvægte, hormonniveauer og ER mRNA niveau kunne der ikke påvises afvigelse fra additivitet, d.v.s. der er ikke holdepunkter for at antage, at der er nogen synergistiske eller antagonistiske samspilseffekter mellem stofferne. Dette underbygges af, at in vitro forsøgene med de samme stoffer viser additivitet. Den østrogene aktivitet i serum fra rotteforsøgene blev undersøgt med en nyudviklet biomarkørmetode, hvor de naturligt dannede østrogener fjernes fra prøven og den resterende prøve testes in vitro for østrogen aktivitet. Derved fås et mål for den samlede østrogene aktivitet i serumprøven hidrørende fra xeno-østrogener – i dette tilfælde de anvendte pesticider og deres nedbrydningsprodukter. I de pesticideksponerede dyr sås en tydeligt dosis-relateret stigning i det østrogene respons, som indikerer at denne metode er velegnet til belysning af eksponering af forsøgsdyr for østrogene kemikalier. Som modelstoffer for pesticider med antiandrogen effekt blev vinclozolin og procymidon valgt og mekanismen for deres interaktion blev undersøgt, dels i et androgenreceptor reportergen assay, dels in vivo i en udbygget Hershberger test, der er udført med kastrerede hanrotter. I in vitro forsøgene blev observeret god overensstemmelse mellem de målte effekter og de prædikterede værdier for additiv virkning beregnet ud fra isobolmetoden. I in vivo forsøgene blev undersøgt effekt på vægt af reproduktionsorganer, effekt på serum FSH og LH niveauer, effekt på genekspression af TRPM-2 og 'prostate binding protein' (PBP) C3 mRNA i prostata og på udvalgte neurotransmitterniveauer og acetylcholinesteraseaktivitet i hjernevæv. Kort fortalt sås med stofferne et fald i vægte af alle reproduktionsorganer, en stigning i LH- og FSH-niveau og hhv. et fald og en stigning i mRNA niveauer af PBP C3 og TRPM-2. Følsomheden af de tre nævnte parametre for antiandrogener var i disse forsøg: reproduktionsorganvægte > serum LH niveau > genekspression i prostata. Hverken noradrenalin-, dopaminkoncentration, acetyl- eller butylcholinesterase-aktivitet i hjernevævet var påvirkede, hvilket indikerer, at de noradrenerge, dopaminerge, og cholinerge dele af centralnervesystemet ikke påvirkes markant af pesticiderne. Dog gav vinclozolin og procymidon enkeltvis og i kombination en signifikant forøgelse af totalhjernens serotoninkoncentration. Generelt vurderes at det anvendte eksperimentelle design giver en biologisk variation mellem dyrene på organvægtniveau, der er af en størrelsesorden, som tillader en relativ præcis og detaljeret undersøgelse af samspilseffekterne. De opnåede data giver således et klart billede af samspillet mellem vinclozolin og procymidon. På baggrund af de opnåede resultater for organvægte, hormonniveauer og mRNA niveauer kan der ikke påvises fravær af additivitet, d.v.s. der er ikke holdepunkter for at antage at der er nogle synergistiske eller antagonistiske samspilseffekter mellem stofferne. Dette underbygges af, at in vitro forsøgene med de samme stoffer viser additivitet. Som eksempler på almindeligt anvendte pesticider i Danmark blev valgt: karbamatinsekticidet methiocarb, der har vist svage østrogene og antiandrogene effekter in vitro, herbicidet tribenuron-methyl og pyrethroid insekticidet deltamethrin, der begge er svage østrogener in vitro, fungicidet prochloraz der har antiøstrogene og antiandrogene effekter in vitro og herbicidet simazin, der er en aromatase-inducer. De fem pesticider blev enkeltvis og i kombination testet for østrogent respons in vitro. Methiocarb og deltamethrin inducerede et østrogent respons målt ved øget MCF-7 celleproliferation, mens tribenuron-methyl, prochloraz og simazin ikke havde nogen effekt. Kombinationen af en 1:1:1:1:1 æquimolær blanding af de 5 pesticider gav ikke noget målbart østrogent respons og beregning af en isobolkoefficient på 7 for blandingen indikerer en antagonistisk effekt mellem stofferne i blandingen, sandsynligvis forårsaget af prochloraz som også reagerer antiøstrogent, når det testes sammen med 17β-estradiol. Desuden blev stofferne enkeltvis og i kombination testet for antiandrogene effekter in vitro og in vivo i Hershberger test. Hverken tribenuron-methyl eller simazin havde nogen antiandrogen effekt in vitro, mens både prochloraz, methiocarb og deltamethrin blokerede androgen receptoren. Kombinationen af en 1:1:1:1:1 æquimolær blanding af de 5 pesticider gav et antiandrogent respons, der lå på linie med det beregnede respons under antagelse af additivitet, så resultaterne indikerer, at stofferne i kombination virker additivt i dette assay. In vivo Hershberger forsøget blev kompliceret af, at det ikke var muligt at undersøge pesticiderne ved samme dosisniveau p.g.a. andre toksiske effekter af nogle af stofferne. Dosis af deltamethrin og methiocarb måtte derfor sænkes til 2,5 mg/kg/dag, mens prochloraz, simazin og tribenuron-methyl blev doseret med hver 25 mg/kg/dag. Kombinationsgruppen fik en dosis svarende til i alt 80 mg/kg (25+25+2.5+25+2.5 mg/kg). Mht. effekt på vægte af reproduktionsorganer sås ingen effekter af enkeltstofferne, hvorimod kombinationsgruppen viste signifikant reduceret vægt af musc. levator ani/bulbocavernosus. Der var også tendens til fald i prostatavægte og sædblærevægte, men der var ingen statistisk signifikans. Generelt sås ingen effekt på de valgte hormonniveauer. Derimod var der markant effekt af alle pesticider doseret enkeltvis og i kombination på ekspressionen af ornithin decarboxylase (ODC) mRNA og PBP C3 mRNA, med undtagelse af deltamethrin og tribenuronmethyl, der ikke gav effekt på PBP C3 mRNA. Konklusionen er, at de 5 pesticider udviser tydelig additivitet in vitro og at der ses en akkumulerende effekt på reproduktionsorganvægte in vivo. Det var overraskende, at enkeltstofferne inducerede så markante effekter på ekspression af PBP C3 og ODC mRNA. Enten er genekspressionen i disse forsøg en meget følsom parameter for antiandrogen effekt eller også reguleres generne af andre signalveje, der ikke er relaterede til androgen receptoren. Betydningen af disse ændringer er således uklar på nuværende tidspunkt, men kan tyde på en begyndende antiandrogen effekt, som ikke giver sig udslag i funktionelle ændringer. Undersøgelse af pesticidinducerede effekter i afkommet efter eksponering af mødrene under drægtigheden anses for at være den mest følsomme in vivo test for undersøgelse af hormonforstyrrende effekter. Kombinationen (20 mg/kg/dag: 15 mg/kg prochloraz og 1,25 mg/kg af de 4 andre pesticider) og prochloraz i sig selv (30 mg/kg/dag) havde en reversibel effekt på mødrenes vægt under drægtigheden, men der sås ingen markante føtotoksiske effekter ved de valgte doser. Den oprindeligt valgte dosis af kombinationen (40 mg/kg/dag: 30 mg/kg prochloraz og 2,5 mg/kg af de 4 andre pesticider) viste sig at være for høj, da der var synlige toksiske effekter på mødrene efter nogle få doser, og dosis blev derfor halveret. Denne toksicitet må skyldes enten deltamethrin, methiocarb, simazin eller tribenuron-methyl i blandingen, eller at et eller flere af stofferne gensidigt øger hinandens toksicitet. Både prochloraz og kombinationen forårsagede et markant reduceret testosteronniveau og et forhøjet progesteronniveau i hanfostre ved gestationsdag 21. Det reducerede testosteronniveau afspejler en antiandrogen effekt i lighed med den, der er observeret for flere phthalater. Effekten var forsvundet post natal dag 16. Men det er givetvis denne effekt, der giver sig udslag i, at begge behandlinger giver et øget antal brystvorter og dermed en feminisering af hannerne. Det øgede progesteronniveau i hanfostre hænger sandsynligvis sammen med den øgede længde af drægtigheden, som var signifikant forøget efter prochloraz behandling. Det er sandsynligt at det er prochloraz i kombinationen (15 mg/kg), der forårsagede de antiandrogene effekter på testosteronniveau og brystvorteantal, da stoffet indgivet alene i en dosis på 30 mg/kg gav de samme effekter Kombinationen gav ingen effekter på hverken adfærd eller sædkvalitet hos hannerne, hvorimod prochloraz i sig selv resulterede i en ændret adfærd hos hannerne i undersøgelser for aktivitetsniveau og sødestofpræference, og de fundne adfærdsændringer tyder på en feminisering af hannerne. Den overordnede konklusion på dette projekt er, at det ser ud som om at hormonforstyrrende stoffer, der virker via samme virkningsmekanisme, har additive effekter. Det er den klare konklusion på basis af in vitro forsøgene, og understøttes af de observationer, der er gjort i dyreforsøgene. Undersøgelsen af deltamethrin, methiocarb, prochloraz, simazin og tribenuron-methyl for antiandrogene effekter viste, at der er klare antiandrogene effekter både in vitro og in vivo af prochloraz, hvorimod der ikke kunne påvises funktionelle hormonforstyrrende effekter i dyreforsøgene af de 4 andre pesticider, der dog også blev testet ved lavere doser. Til gengæld sås der på genekspressionsniveau en række ændringer efter dosering med selv små doser af de 4 pesticider, men betydningen af disse ændringer er uklar. Dette projekt illustrerer den store force in vitro forsøg har til vurdering af kombinationseffekter pga. den store kapacitet af assayene, der gør, at der kan laves detaljerede dosis-respons kurver for mange blandingsratioer af stofferne. Projektet illustrerer også, at undersøgelse af kombinationseffekter i dyreforsøg kan lade sig gøre, men er ressourcekrævende og kan være en vanskelig opgave p.g.a. stoffernes ofte meget forskellige toksicitet, som gør, at man langt fra altid kan dosere dyrene med de blandingsforhold af stofferne, der fra et teoretisk synspunkt er optimale. Summary and conclusionsThe human population is in most situations exposed to mixtures of chemicals, some of which are suspected of having endocrine disrupting properties. The effect of many of these chemicals is weak compared to the effects of our natural sex hormones, and it is difficult to explain potential adverse effects on humans on the basis of effects observed for single compounds. However, it is conceivable that the endocrine disrupting chemicals interact in a way that enhances their hormonal effect, and, therefore, it is important to elucidate the mechanisms of interaction, that may come into play when compounds are combined. That is the reason why this investigation that specifically aims at elucidating mixture effects of endocrine disrupting chemicals has been initiated. The overall purpose is also to contribute with input to the discussion on principles of risk assessment of chemicals, that, traditionally, does not take account for the fact that humans are exposed to mixtures of chemicals. The major part of the work that has been done to study the mixture effects of endocrine disrupting chemicals is based on in vitro experiments of varying quality, and only very few experiments on mixtures of endocrine disrupting chemicals have been performed so far. Investigations of mixture effects of antiandrogenic chemicals have not previously been performed. It has been shown that mixture effects can vary in an experimental system depending on the selected end-point. Compounds that act synergistically at the molecular level (e.g. receptor binding) may show additivity when end-points at more complex functional molecular levels such as cell growth are measured. Because of this, it has been considered important to analyse mixture effects of endocrine disrupting pesticides at different levels of molecular complexity including in vivo studies. The mechanism of interaction of pesticides with estrogenic and antiandrogenic activity, respectively, was studied in in vitro studies and in vivo short-term animal experiments. As model compounds for the estrogenic pesticides o,p-DDT and methoxychlor were chosen and the test systems comprised a breast cancer cell proliferation assay and a uterus weight gain test in ovariectomized female rats. In the in vitro experiments good agreement between observed effects and predicted effects for additivity based on the concentration addition principle was found. In the in vivo experiments the following end-points were measured: uterus weight, serum levels of FSH, LH, and prolactin, mRNA levels of estrogen receptor (ER) and , and lactoferrin in uterus tissue, and selected neurotransmitters and acetylcholinesterase activity in brain tissues. Briefly, both pesticides gave rise to an increase of uterus weights and prolactin level, whereas LH, FSH level and ER, ER and lactoferin mRNA levels decreased. No effect on neurotransmitter levels and acetylcholinesterase activity was seen. On the basis of the results obtained for organ weights, hormone levels and ER mRNA levels, no deviations from additive effects could be detected, i.e there is no evidence for assuming that synergistic or antagonistic mixture effects take place between the compounds. This is further supported by the in vitro data showing a similar additivity. The estrogenic activity in serum from rats was analysed using a new biomarker method, in which the physiologically formed estrogens are removed from the sample and the remaining serum fraction is tested in vitro for estrogenic activity. Using this method, an integrated measure for the total estrogenic activity of the xeno-estrogens in the serum sample is obtained – in this case the total activity of the administered pesticides and their break-down products is measured. In the pesticide-exposed animals a clear dose-dependent increase of the estrogenic response was seen, indicating that this method is valuable for elucidating the extent of exposure of animals and humans to estrogenic chemicals. As model compounds for pesticides with antiandrogenic effects, vinclozolin and procymidon were chosen, and the mechanism of their interaction was studied in an androgen receptor reporter gene assay and in vivo in an extended Hershberger test, that involves the use of castrated male rats. In the in vitro experiments an excellent agreement between observed effects and the predicted values for additive action was found. In the in vivo experiments the following effects were analysed: weights of reproductive organs, serum FSH and LH levels, TRPM-2 and PBP C3 mRNA levels in prostates, and selected neurotransmitter levels and acetylcholinesterase activity in brain tissue. Briefly, both pesticides cause a decreased weight of all reproductive organs, an increase of LH and FSH serum levels and a decreased PBP C3 and an increased TRPM-2 mRNA level in prostates. The sensitivity of the three selected parameters was in these experiments found to be: reproductive organ weights > serum LH levels > gene expression in prostates. Neither norepinephrine, dopamine concentration, acetyl- or butylcholinesterase activity in brain tissue was affected, indicating that the involved parts of CNS were not affected by the pesticides. However, vinclozolin and procymidon separately and in combination gave rise to a significant increase of the serotonin concentration in the total brain. In general, it is estimated that the selected experimental design gives rise to a biological variation between the animals on organ weight level that has a magnitude which allows for a relatively precise and detailed investigation of mixture effects. The results obtained give a clear picture of mixture effects for vinclozolin and procymidon. On basis of the present results on organ weights, hormone levels and mRNA levels, no deviations from additivity can be detected that is there is no evidence that any synergistic or antagonistic mixture effects take place. This is further supported by data from the in vitro experiments in which the same additivity is found. As examples of commonly used pesticides in Denmark were chosen: the carbamate insecticide methiocarb, that has weak estrogenic and antiandrogenic effects in vitro, the herbicide tribenuron-methyl and the pyrethroid insecticide deltamethrin, that both are weak estrogens in vitro, the fungicide prochloraz that has antiestrogenic and antiandrogenic effects in vitro and the herbicide simazin, that is an aromatase inducer. These five pesticides were separately and in combination tested for estrogenic activity in vitro. Methiocarb and deltamethrin induced an estrogenic response measured as an increase of breast cancer cell proliferation, whereas tribenuron-methyl, prochloraz and simazin had no effect. The 1:1:1:1:1 equimolear mixture of the five pesticides did not give any measurable estrogenic response and the calculation of an isobole coefficient of 7 for the mixture indicates an antagonistic effect between the compounds, probably caused by prochloraz that reacts as an antiestrogen when tested together with 17β-estradiol. Furthermore, the pesticides were tested separately and in combination for antiandrogenic effects in vitro and in vivo in an extended Hershberger test. Neither tribenuron-methyl or simazin had any antiandrogenic effect in vitro, whereas both prochloraz, methiocarb and deltamethrin blocked the androgen receptor. A 1:1:1:1:1 equimolear mixture of the five pesticides gave an antiandrogenic response, that was similar to the predicted response under assumption of additivity, and thus the results indicate that the pesticides in combination act additively in this assay. The Hershberger experiment was complicated by the fact that it was not possible to administer the pesticides at the same dose level because of other toxic effects caused by some of the compounds. The dose of deltamethrin and methiocarb therefore had to be lowered to 2.5 mg/kg/day, whereas prochloraz, simazin and tribenuron-methyl each was administered with 25 mg/kg/day. The mixture group got a dose of a total of 80 mg/kg (25+25+2.5+25+2.5 mg/kg). Regarding effects on weights of reproductive organs, no effects of single compounds was seen, whereas the mixture group showed a significantly reduced weight of musc. levator ani/bulbocavernosus. A tendency towards decreased prostate and seminal vesicles weights was seen but no statistical significance was obtained. In general, no effect on hormone levels was found. In contrast, a marked effect of all pesticides dosed separately and in combination on the expression of ODC mRNA and PBP C3 mRNA was seen, with the exception of deltamethrin and tribenuronmethyl that did not affect PBP C3 mRNA. In conclusion, the five pesticides showed clear additive effects in vitro, and, further, an accumulating effect on weights of reproductive organs in vivo was found. It was surprising that the single pesticides induced marked effects on expression of PBP C3 and ODC mRNA. Gene expression in these experiments may either be a more sensitive parameter for antiandrogenic effects or the genes are regulated by a signal pathway not related to the androgen receptor. The meaning of these changes is not clear at present, but may indicate a very weak antiandrogenic action that does not manifest itself in functional changes. Investigation of pesticide-induced effects in the offspring after in utero exposure is considered the most sensitive in vivo test for determination of endocrine disrupting effects. The mixture (20 mg/kg/day: 15 mg/kg prochloraz and 1.25 mg/kg of the four other pesticides) and prochloraz in itself (30 mg/kg/day) had a reversible effect on maternal weight during gestation, but no clear foetotoxicity was seen. The originally planned dose of the mixture (40 mg/kg/day: 30 mg/kg prochloraz and 2.5 mg/kg of the four other pesticides) appeared to be too high, as clear visible maternal toxicity was seen after a few doses, and the dose was therefore halved. This toxicity must be caused either by deltamethrin, methiocarb, simazin or tribenuron-methyl in the mixture or by interaction of one or more compounds. Both prochloraz and the mixture caused a markedly reduced testosterone level and an increased progesterone level in male foetuses at gestational day 21. The reduced testosterone level reflects an antiandrogenic effect comparable to that observed for several phthalates. The effect had disappeared at postnatal day 16. It is conceivable that this effect is the cause of the increased number of nipples seen in males after dosing of prochloraz and the mixture, thereby feminising the males. The increased progesterone level in male foetuses is probably related to the increased lenght of gestation that was significantly increased after prochloraz exposure. It is conceivable that prochloraz in the mixture (15 mg/kg) is responsible for the antiandrogenic effects on testosterone level and number of nipples, as the compound given alone at a dose of 30 mg/kg gave the same effects. The mixture caused no effects on neither behaviour nor semen quality in the males, whereas prochloraz in itself affected behaviour in males, as the activity level and behaviour in the sweet preference test was changed, indicating a feminising effect on the males. The overall conclusion of this project is that endocrine disrupting pesticides that act via the same mechanism of action, have additive effects. This is the clear conclusion from the in vitro experiments and is supported by the observations that have been made in the animal experiments. The investigation of deltamethrin, methiocarb, prochloraz, simazin and tribenuron-methyl for antiandrogenic effects indicates that there are clear antiandrogenic effects both in vitro and in vivo of prochloraz, whereas no functional endocrine disrupting effects of the four other pesticides in the animal experiments was found. In contrast a number of changes were found at the gene expression level after exposure to even low doses of the four pesticides, but the meaning - if any - of these changes is unknown. This project illustrates the great advantage of in vitro experiments for evaluation of mixture effects, because of the great capacity of the assays, that allows detailed dose-response curves for many mixture ratios of the compounds. The project also illustrates that investigation of mixture effects in animal experiments is possible, but demands more resources and can turn out to be a difficult task because of differing general toxicity of compounds, meaning that the doses in a mixture that - from a theoretical point of view are optimal,- cannot always be chosen. 1 Introduktion og baggrund
1.1 BaggrundUnormal kønsdifferentiering i vildtlevende dyr, stigningen i forekomsten af testikelkræft, øget forekomst af misdannede kønsorganer og forringet sædkvalitet hos drenge/mænd og den fortsatte stigning i forekomsten af brystkræft hos kvinder er årsag til udbredt bekymring (Sharpe and Skakkebæk 1993; Toppari et al. 1996; Crisp et al. 1998). Der er mistanke om, at disse effekter er relateret til eksponering for miljøkemikalier, som er i stand til at efterligne eller blokere effekterne af de endogene hormoner. Listen over kemikalier, der har vist sig at have østrogen aktivitet, er vokset betydeligt indenfor de senere år og inkluderer nu stoffer så forskellige som o,p-DDT, methoxychlor, non-coplanare PCBer, bisphenol A og alkoxyphenoler (Crisp et al. 1998). Der er evidens for, at nogen af disse kemikalier forårsager skadelige effekter i vildtlevende dyr, men forsøg på at etablere et link mellem human sundhedsrisiko og eksponering for østrogene kemikalier kompliceres af den kendsgerning, at mange af de mistænkte kemikalier har meget lav østrogen potens sammenlignet med 17β-østradiol samt, at stofferne findes i ukendte blandinger i de eksponerede individer. I de senere år har flere stoffer i cellekulturforsøg og i dyreforsøg vist sig at have antiandrogen virkning (Gray et al., 1999). De fleste hormonforstyrrende kemikalier er svage agonister eller antagonister af kønshormon-receptorerne og er effektive ved koncentrationer i M-området in vitro og er således flere 1000-gange mindre potente end de naturlige kønshormoner. Det er derfor vanskeligt at forklare de mulige sundhedsrisici alene på basis af toxiciteten af enkeltstoffer. Situationen kompliceres dog af, at miljøkemikalier ikke inducerer og bindes til forskellige plasmaproteiner, som tilfældet er for de endogene hormoner. Denne proteinbinding har stor betydning for den biologiske aktivitet, hvorfor man ikke kan vurdere det hormonforstyrrende potentiale af miljøkemikalier ved direkte at sammenligne serumkoncentrationer af disse og endogene hormoner. Den humane population er eksponeret for blandinger af hormonforstyrrende stoffer med en række forskellige virkningsmekanismer og det er sandsynligt at disse kemikalier spiller sammen på en måde så de samlede hormonale effekter er større end for enkeltsofferne alene. Derfor er studier af kombinationseffekter af pesticider et af de højt prioriterede områder indenfor pesticidforskningsområdet, hvilket også blev konkluderet i Bichel-rapporten (1999) udgivet af Miljøstyrelsen. Mange pesticider har vist et potentiale for hormonforstyrrende effekt. Forskellige virkningsmåder er blevet foreslået:
Det vil sige, at adskillige virkningsmåder og mekanismer kan være involverede i hormonforstyrrelser forårsaget af pesticider. Da befolkningen bliver eksponeret for en blanding af pesticider, er det yderst relevant at teste samspilseffekter af pesticider med både samme og forskellig virkningsmekanisme i nogle af de tests der dels er foreslået som OECD guideline tests og dels kan tænkes at blive anbefalet til test for hormonforstyrrende effekter. Den systematiske analyse af kombinationseffekter af hormonforstyrrende stoffer er kun lige begyndt. M.h.t. effekterne af blandinger af hormonforstyrrende stoffer har det primære fokus hidtil været på den østrogene aktivitet af blandinger i cellekulturer (Soto et al. 1994; Sumpter and Jobling, 1995; Bergeron et al. 1994; Arnold et al. 1996; Ramamoorthy et al. 1997; Wade et al. 1997; Soto et al. 1997). Specielt én artikel, der rapporterede om dramatiske synergistiske effekter på østrogen receptor aktivering med kombinationer af pesticider (Arnold et al.1996) forårsagede stor videnskabelig, regulatorisk og offentlig bekymring rundt om i verden. Men da eksperimenterne viste sig ikke at kunne reproduceres (Ramamoorthy et al. 1997; Gaido et al. 1997), blev artiklen trukket tilbage (McLachlan, 1997). Ved undersøgelse af de kombinerede effekter af østrogene stoffer er der i mange tilfælde anvendt et eksperimentelt design, hvor de enkelte stoffer så vel som blandinger udelukkende blev testet ved ét dosisniveau (Soto et al. 1994; Sumpter and Jobling 1995; Arnold et al. 1997; Soto et al. 1997). Denne fremgangsmåde er intuitivt tillokkende men giver ikke det fulde billede af eventuelle samspilseffekter, fordi den kun tillader vurdering af kombinationseffekter, som er baserede på forventninger om effektsummation. Imidlertid er anvendelsen af metoden baseret på effektsummation begrænset til kombinationer af stoffer, som producerer lineære dosis-respons kurver der går igennem nulpunktet af dosis-effekt plottet og disse ses sjældent indenfor toksikologien (Kortenkamp and Altenburger, 1998). De kan forekomme i lav-dosis området af ellers ikke-lineære kurver som for carcinogener. I de fleste af de ovenfor nævnte studier er lineære dosis-respons forhold ikke blevet vist. Derfor blev hovedparten af studierne fundet at være inkonklusive (Kortenkamp and Altenburger 1999). De fleste studier konkluderer, at der synes at være additive effekter, d.v.s. ingen interaktion mellem stofferne, skønt en detaljeret mekanistisk analyse altså sjældent er foretaget. Der er dog eksempler på studier, som har overset synergistiske effekter, hvilket blev demonstreret ved en efterfølgende detaljeret vurdering af data (Kortenkamp and Altenburger, 1998). I de seneste år er der udført nogle detaljerede og grundige studier over samspilseffekter mellem østrogene kemikalier in vitro af Kortenkamp og medarbejdere i London, UK (Payne et al. 2000; Rajapakse et al. 2001; Payne et al. 2001; Silva et al. 2002; Rajapakse et al. 2002). Sammenfattende konkluderer disse studier, at stoffer, der virker via samme virkningsmekanisme, virker additivt in vitro når data bliver analyseret ved hjælp af koncentrations-additionsmodellen eller isobolmetoden. De nævnte studier viser desuden, at koncentrations-additionsmodellen er bedre til at prædiktere kombinationseffekter i denne type undersøgelser end andre modeller som anvendes til at analysere kombinationseffekter. Koncentrations-additionsmodellen kræver ikke liniære dosis-responskurver, men bygger på en antagelse om, at effekten af en blanding af stoffer ikke ændres hvis et af stofferne erstattes med en 'iso-effektiv' dosis af et andet stof med samme virkningsmekanisme. Hovedparten af det arbejde, der er lavet indenfor området er baseret på in vitro experimenter, der lider af de velkendte begrænsninger som mangel på vurdering af absorption, metabolisme og ekskretion. Meget få in vivo eksperimenter på blandinger af hormonforstyrrende stoffer er blevet udført. Det er vist at kombinationseffekten varierer i det samme eksperimentelle system afhængig af det valgte endpoint (Altenburger et al. 1993). Stoffer som virker synergistisk på det molekylære niveau (e.g. receptor binding) kan udvise additivitet, når der måles på endpoints på mere komplekse funktionelle niveauer såsom cellevækst eller celledød (Grimme et al. 1996). Af denne grund er det vigtigt at udføre analyse af kombinationseffekter af hormonforstyrrende stoffer ved forskellige niveauer af molekylær kompleksitet inklusive in vivo studier. 1.2 Projektets formålIdeen med nærværende projekt var for det første at udføre in vitro og in vivo undersøgelser, der fokuserede på detaljeret at belyse typen af interaktion mellem pesticider med kendt hormonforstyrrende effekt (Delprojekt 1). Pesticiderne blev valgt som modelstoffer og bliver ikke længere anvendt i Danmark. Formålet med det andet delprojekt var at udføre in vitro og in vivo undersøgelser med kombinationer af pesticider, som er i almindelig anvendelse i Danmark og for hvilke der er fundet svage in vitro hormonforstyrrende effekter (Delprojekt 2). 1.3 Hypotese og strategi for delprojekt 1Formålet med dette delprojekt var at undersøge interaktion af kendte potente pesticider, som fra in vivo og forskellige in vitro eksperimenter vides at have hormonforstyrrende effekter. Pesticider med formodet samme virkningsmekanisme blev kombineret og samspilseffekten belyst både in vitro samt in vivo i rotteforsøg. Desuden er kombinationseffekter for tre pesticider, som ikke har samme virkningsmekansime, undersøgt in vitro. Dosis-respons kurver for henholdsvis østrogene eller antiandrogene effekter af hvert enkelt stof og af blandingerne er undersøgt. Data er efterfølgende analyseret og fortolket ved hjælp af isobolmetoden, der bygger på koncentrations-additionsprincippet. Serum fra pesticideksponerede rotter er desuden undersøgt for østrogen aktivitet in vitro, efter fjernelse af de naturlige østrogener fra prøven. Ved at sammenligne resulaterne fra disse målinger med resultater fra in vitro undersøgelserne af de rene pesticider og med de øvrige resultater fra rotteforsøgene, er det muligt at vurdere værdien af denne nye biomarkørmetode. De valgte parametre i in vivo undersøgelserne inkluderer effekter på morfologi, hormonniveauer, genekspression og neurokemiske parametre.
1.4 Hypotese og strategi for delprojekt 2Strategien for dette delprojekt var at undersøge en blanding af nogle almindeligt anvendte pesticider i Danmark, for hvilke der er fundet svage hormonforstyrrende effekter in vitro. Disse pesticider er relevante fra både et miljømæssigt synspunkt (dvs. ansatte i gartnerier, hvor stofferne anvendes) og fra et forbrugersynspunkt. For disse individuelle stoffer er der ikke nogen viden om hormonforstyrrelser in vivo, men de er alle blevet testet for østrogene, (anti)androgene og aromatasehæmning in vitro (Andersen et al. 2002) og de udviser effekt i mindst et af assayene. Kun i in vitro forsøgene og ikke i in vivo studierne blev der lavet komplette dosis-respons kurver for de enkelte stoffer, hvilket betyder, at der ikke opnås et fuldt billede af interaktionen mellem stofferne in vivo. Blandingen er testet for antiandrogen aktivitet in vitro og in vivo. Derudover er blandingen testet i et in utero eksperiment, hvor adskillige parametre i det hanlige afkom er inkluderet. 2 Mekanismer for kombinationseffekter af hormonforstyrrende stoffer
2.1 Østrogene pesticider testet in vitroDen østrogene virkning af pesticiderne er undersøgt i et MCF-7 celle proliferationsassay. Dette assay er baseret på en human brystcancercellelinie, som differentierer og deler sig når der er østrogen til stede. Proliferation af denne cellelinie er således indikation for, at der er et stof til stede med østrogen aktivitet. Metoden anvendes rutinemæssigt til screening for miljøkemikalier med østrogene egenskaber flere steder, herunder på Afdeling for Miljømedicin på Syddansk Universitet i Odense (Andersen et al. 1999). Kort beskrevet blev MCF-7 celler udsået i mikrotiterplader og efter 24 timer blev en række koncentrationer (0,01– 50 μM) af pesticider tilsat, dels enkeltvis, dels i kombination. Pesticiderne blev testet både med og uden 10 pM 17-østradiol (som inducerer ca 50 % af det maximale proliferationsrespons i cellerne) for at undersøge både agonist og antagonist effekter overfor østradiol. Efter 6 dages inkubation blev cellerne fikseret og farvet. Farveintensiteten, som er et mål for antallet af levende celler, blev aflæst i en ELISA-reader. Hvert forsøg inkluderede en standardrække af 17β-østradiol (1 pM til til 10 nM), hvor maximalt respons sås ved 100 pM. Resultaterne er angivet som den Relative Proliferative Effekt (RPE), hvorved data er normaliseret til både ubehandlede kontrolceller og det maksimale respons induceret af 1 nM 17β-østradiol i det respektive forsøg: RPE = (PEteststof – 1)/(PEmax 17β-østradiol -1), hvor PE er responset normaliseret i forhold til kontrol. Den forventede effekt af blandingerne er beregnet ud fra koncentrations-additions modellen, hvor den følgende ligning gælder for alle effektniveauer:
hvor Ci, mix er koncentrationen af stof i i en blanding, som giver en given effekt og Ci, single er den koncentration, som skal til af det rene stof for at give den samme effekt. Ligningen kan omskrives til:
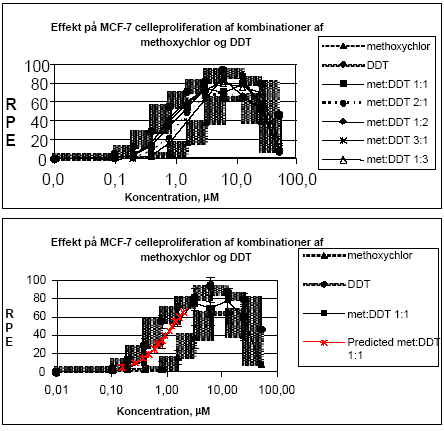
hvor pi er den relative andel af det i 'te stof ud af den totale koncentration af blandingen. Ud fra denne ligning kan den koncentration af blandingen som forventes at give en bestemt effekt beregnes, idet effekten af de enkelte stoffer som funktion af koncentrationen er bestemt ud fra fittede kurver. For pesticidblandinger testet direkte for østrogene effekter var det bedste kurvefit den sigmoide Chapman funktion (3 parametre) mens den sigmoide funktion (4 parametre) er anvendt for agonistiske effekter for blandinger testet sammen med 17β-østradiol. For antagonistiske effekter er funktionen for ekspotentielt henfald (5 parametre) anvendt som bedste kurvefit. Regressionskoefficenterne for de fittede kurver lå mellem 0,89 og 0,99 for de forskellige blandinger. 2.1.1 Effekt af methoxychlor og o,p-DDT på MCF7 celleproliferationMethoxychlor og o,p-DDT er to pesticider med kendte østrogene effekter. En mulig samspilseffekt mellem stofferne med hensyn til deres østrogene virkning er undersøgt i dette assay. Indledningsvist var der nogle metodologiske problemer, idet o,p-DDT afdampede under inkubationen og forurenede de omkringliggende dyrkningshuller på mikrotiterpladen. Hver koncentration af o,p-DDT er derfor blevet testet på separate mikrotiterplader. Pesticiderne blev blandet i molære ratioer på 1:1, 1:2, 2:1, 1:3 og 3:1. Der blev udført tre uafhængige forsøg og data blev analyseret ved isobolmetoden. Både methoxychlor og o,p-DDT stimulerede koncentrationsafhængigt proliferationen af MCF-7 cellerne som tegn på østrogen virkning. For begge pesticider var der et fald i celleproliferationen ved de to højeste koncentrationer (25 og 50 μM) på grund af cytotoksicitet, hvorfor disse koncentrationer ikke blev medtaget i de videre beregninger. Som det ses af Fig 2.1.1 er der god overenstemmelse mellem de målte effekter og de prædikterede værdier for additiv virkning beregnet ud fra isobolmetoden.
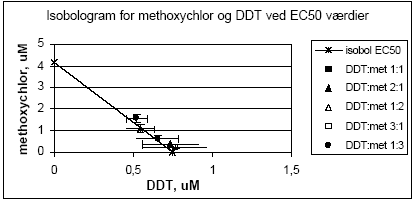
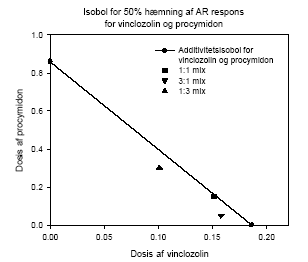
Figur 2.1.1. Effekten af methoxychlor og o,p-DDT samt kombinationer af de to stoffer på proliferationen af MCF-7 celler samt den predikterede effekt under antagelse af additivitet beregnet ved isobolmetoden. De observerede effekter er gennemsnit af mindst tre uafhængige forsøg udført i trippelbestemmelse. Isobolen for de koncentrationer af o,p-DDT og methoxychlor som inducerer 50% stigning i MCF-7 celleproliferationen i forhold til ubehandlede kontrolceller er afbilledet på Figur 2.1.2. Den koncentration af o,p-DDT som øger proliferationen med 50 % er angivet på x-aksen og den tilsvarende koncentration for methoxychlor er angivet på y-aksen. Ved additivitet vil værdierne for blandinger af de to stoffer ligge på den rette linie som forbinder disse to punkter (isobolen). Det ses at de målte værdier for blandingerne ligger tæt på isobolen, hvilket viser god overenstemmelse med additivitet for de to stoffers kombinationseffekt.
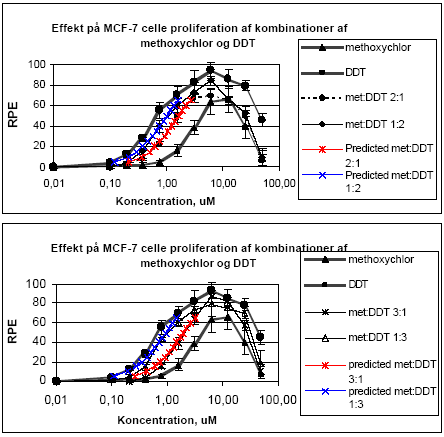
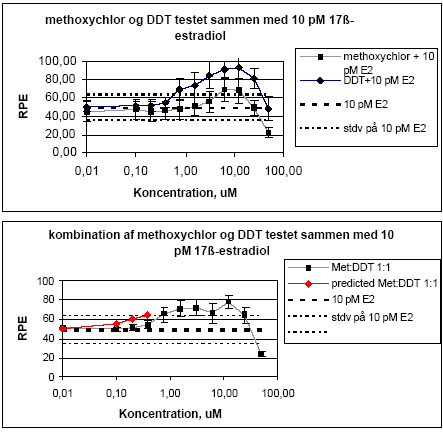
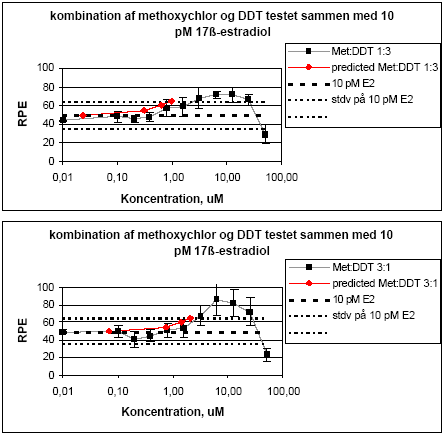
Figur 2.1.2. Isobologram for de koncentrationer af o,p-DDT og methoxychlor som inducerer 50% stigning i MCF-7 celle- proliferationen samt de observerede værdier for blandinger af de to pesticider. Når methoxychlor og o,p-DDT blev testet sammen med 10 pM af 17β-østradiol var der ingen tegn på antagonistisk effekt overfor 17-østradiol i dette assay. Derimod medførte begge stoffer en yderligere stigning i celleproliferationen (Figur 2.1.3). Denne effekt var mest markant for o,p-DDT, som også var mest potent, når stofferne blev testet uden 17β-østradiol. Tilsvarende sås heller ingen antagonistisk effekt overfor 17β-østradiol, når de forskellige blandinger af o,p-DDT og methoxychlor blev testet sammen med 10 pM 17β-østradiol, men et øget respons svarende til det additive respons for blandinger af o,p-DDT og methoxychlor.
Figur 2.1.3. Effekten af methoxychlor og o,p-DDT samt blandinger heraf testet sammen med 10 pM 17-østradiol på proliferationen af MCF-7 celler samt den prædikterede effekt under antagelse af additivitet beregnet ved isobolmetoden. De observerede effekter er gennemsnit af mindst tre uafhængige forsøg udført i tripelbestemmelse. 2.1.2 Effekt af kombinationer af vinclozolin, methoxychlor og fenarimolSom eksempel på tre pesticider med forskellige hormonforstyrrende virkningsmekanismer blev fenarimol, methoxychlor og vinclozolin valgt. Fenarimol og methoxychlor er begge østrogene. Fenarimol er desuden en aromatasehæmmer og alle tre pesticider har antiandrogene egenskaber. De tre pesticider samt blandinger heraf blev testet i MCF-7 celleproliferationsassayet i 3 uafhængige forsøg. Fenarimol og methoxychlor inducerede begge proliferation af MCF-7 cellerne. Begge pesticider optrådte som partielle agonister idet det maksimale respons kun var ca. 60% af det maksimale respons induceret af 17β-estradiol (Figur 2.1.4). Vinclozolin havde ingen effekt i assayet. Ved testning af 5 forskellige blandingsforhold af de tre pesticider var der god overenstemmelse mellem de registrerede effekter og de prædikterede effekter beregnet ud fra isobolmetoden.
Figur 2.1.4. Effekten af fenarimol, methoxychlor og vinclozolin samt kombinationer af de tre stoffer på proliferationen af MCF-7 celler samt den predikterede effekt under antagelse af additivitet beregnet ved isobolmetoden. De observerede effekter er gennemsnit af tre uafhængige forsøg udført i tripelbestemmelse. Isobolkoeficienter ved de blandingskoncentrationer der giver et respons på henholdsvis 5, 25 og 50 RPE er beregnet for de fem blandinger ud fra formlen:
idet bidraget fra vinclozolin er sat til nul (Tabel 2.1). Tabel 2.1 Isobolkoeficienter ved EC5 , EC25 og EC50 for blandinger af fenarimol, methoxychlor og vinclozolin
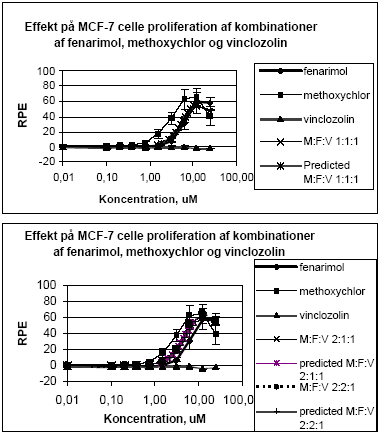
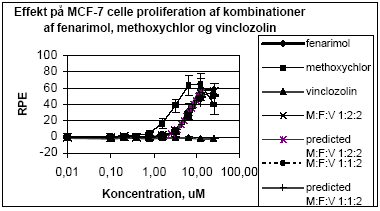
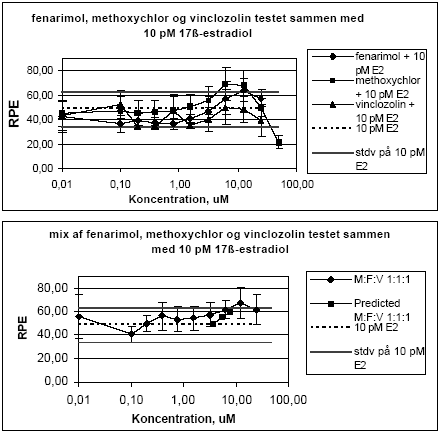
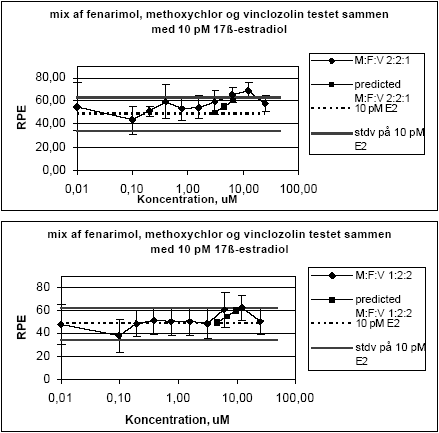
Når de tre pesticider enkeltvist blev testet sammen med 10 pM 17β-østradiol sås en tendens til en svag øgning af responset ved de højeste ikke-cytotoksiske koncentrationer (10-25 μM) i forhold til 17β-østradiol alene, undtagen for vinclozolin. Ved de lave koncentrationer af fenarimol og vinclozolin var der en tendens til en reduktion af 17β-østradiol responset, som dog ikke er signifikant da det ligger indenfor standardafvigelsen for 17β-østradiol (Figur 2.1.5). Også for kombinationer af fenarimol, methoxychlor og vinclozolin testet sammen med 10 pM 17β-østradiol sås en tendens til et øget respons som svarede rimeligt godt med det forventede respons under forudsætning af additivitet mellem fenarimol og methoxychlor (Figur 2.1.5).
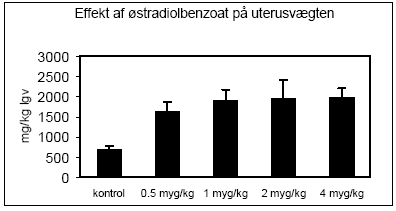
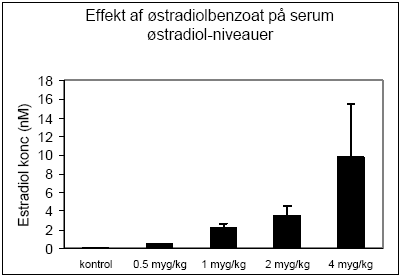
Figur 2.15. Effekten af fenarimol, methoxychlor og vinclozolin samt blandinger heraf testet sammen med 10 pM 17β-østradiol på proliferationen af MCF-7 celler samt den predikterede effekt under antagelse af additivitet beregnet ved isobolmetoden. De observerede effekter er gennemsnit af mindst tre uafhængige forsøg udført i tripelbestemmelse. 2.2 Østradiol-inducerede effekter in vivoDen klassiske uterustest blev anvendt til undersøgelse af samspillet mellem methoxychlor og o,p-DDT in vivo. For at få valideret og endelig indkørt de metoder, der skulle anvendes i forbindelse med uterustest af pesticiderne, blev der udført indledende forsøg med 4 doser østradiolbenzoat. Den anvendte model for uterustesten bygger i dette tilfælde på ovariektomerede voksne Wistar hunrotter der behandles med pesticiderne og et positivt kontrolstof peroralt i 4 dage. Efter aflivning af dyrene blev uterusvægten målt, serum fremstillet til hormonanalyser og biomarkøranalyser og mRNA blev isoleret fra uterus til genekspressionsanalyser. Metoden er blevet etableret ved Danmarks Fødevare- og Veterinærforskning (Hossaini et al. 2000) og har indgået i et interkalibreringsstudie i OECD regi. 2.2.1 Effekt på organvægteMed stigende doser af østradiolbenzoat (s.c.) sås en markant forøgelse af uterusvægten, mens lever- og nyrevægt var uændret. En statistisk signifikant forøgelse af uterusvægten sås allerede ved den laveste dosis på 0.5 g/kg (Fig 2.2.1).
Figur 2.2.1 2.2.2 Effekt på hormonniveauerNiveauer af østradiol i serum fra dyrene blev analyseret ved hjælp af Delfia tidsforsinket fluorescens efter forudgående fast-fase ekstraktion på C18-søjler. Med stigende doser af østradiolbenzoat sås en markant forøgelse af østradiolniveauet, hvilket afspejler de stigende doser af stoffet som dyrene blev doseret med og dermed tjener som en kvalitetskontrol for fremstilling af opløsninger, dosering af dyrene og hormonananalysen (Fig 2.2.2).
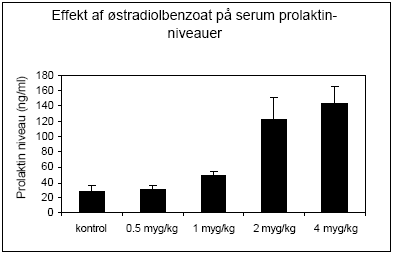
Figur 2.2.2 Hypofysehormonet prolaktin secerneres fra hypofysen efter østrogenbehandling af hunner og kan muligvis bruges som markør for eksponering for østrogene miljøkemikalier. Rotteprolaktin blev i dette tilfælde analyseret ved hjælp af et enzymimmunoassay (BiotrakTM) udviklet af Amersham og der sås stigende niveauer af hormoner ved doser på 1 μg/kg og derover (Fig 2.2.3).
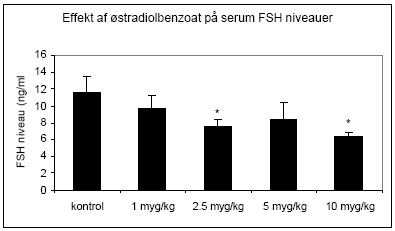
Figur 2.2.3. Follikelstimulerende hormon (FSH) er et andet hypofysehormon, der er under regulation af østradiol, som ved stigende doser bevirker en feedback hæmning af sekretionen af FSH fra hypofysen. Rotte FSH i serum blev analyseret ved hjælp af Delfia tidsforsinket fluorescens og der sås et fald i niveauet, der var statistisk signifikant ved doser på 2.5 μg/kg og derover (Fig 2.2.4).
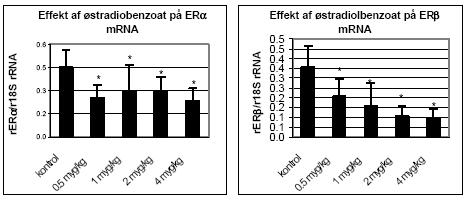
Figur 2.2.4 2.2.3 Effekt på østrogenregulerede generØstrogener, som er kvindelige kønshormoner, påvirker udvikling, differentiering og funktionen af det mandlige og kvindelige reproduktionssystem (Enmark & Gustafsson, 1999). Østrogener spiller også en vigtig rolle i funktionen af knogler, centralnervesystem, immunsystem, hud og det kardiovaskulære system (Ahmed 2000; Enmark & Gustafsson 1999; Gaido et al. 1999; Enmark et al. 1997; Couse et al. 1997). Østrogen receptor (ER) α og β medierer den biologiske effekt af østrogener og er ligand-aktiverede transkriptionsfaktorer, som regulerer ekspression af steroid-responderende gener (Levin 2002; Nielsson et al. 2001). ERα og ERβ har specifikke fordelinger i celler og væv (Enmark et al. 1997) og regulerer forskellige gener (Pettersson & Gustafsson 2001) og det er blevet foreslået, at ERβ modulerer effekter medieret af ERα ved f.eks. at hæmme celleproliferation (Cappelletti et al. 2003; Pettersson et al. 2000). Selv om der er foreslået mange funktioner af ERβ, er denne recptors rolle stadig kontroversiel. Østradiol er vist at nedregulere genekspression af ER i bl.a. MCF-7 celler (Vienonen et al. 2003; Clayton et al. 1997; Donaghue et al. 1999). Hypotesen er, at nedreguleringen af ER mRNA bl.a. involverer en negativ feedback autoregulering af ER på egen transkription, hvor promotor nedregulering tilsyneladende medieres via cellers specifikke transkriptionsfaktorer (Donaghoue et al. 1999). Metoden til at bestemme effekter af miljøkemikalier på genekspression af bl.a. ERα og ERβ og lactoferin er etableret ved Institut for Miljø og Arbejdsmedicin, Aarhus Universitet. Tidligere resultater fra laboratoriet har vist en nedregulering af ER og opregulering af ERα/β mRNA ved eksponering af MCF-7 celler til 17β-østradiol samt effekter på ERα/β mRNA niveau af en række pesticider (Hofmeister & Bonefeld-Jørgensen, 2003; Grünfeld & Bonefeld-Jorgensen, 2003). I dette studie er effekten af østradiol på østrogent-regulerede gener undersøgt i uterus fra eksponerede rotter ved hjælp af semikvantitativ real-time PCR. Lightcycler (Roche) bruges som et thermocycling on-line detektionssystem for at kvantificere RT-PCR produkter og anvendes rutinemæssigt ved Institut for Miljø og Arbejdsmedicin, Århus Universitet (Krüger et al. 2003). Total RNA fra uterus blev isoleret med RNeasy (Qiagen, Merck Eurolab) og omdannet til cDNA med Reverse Transcriptase (Superscript II, LifeTechnologies). Ekspressionen af de østradiol-regulerede gener ER, ER og lactoferrin og det interne kontrolgen ribosomal 18S (r18S) blev målt ved hjælp af genspecifikke primersæt og fluorescerende probersæt (DNA Technologies, Research Park, Aarhus). Da det viste sig, at β2-globulingenet responderede på østradioleksponering og derfor ikke kunne anvendes som intern kontrol anvendtes i stedet r18S genet som intern kontrol. Parallelt i hver PCR-kørsel blev analyseret en standardkurve med fortyndinger af plasmid DNA indeholdende det specifikke genfragment som testes. Desuden blev der parallelt i hver PCR-kørsel analyseret en kendt positiv kontrol. De genspecifikke værdier blev normaliseret til den kendte positive kontrol (for at udligne forskelle imellem kørsler fra dag til dag) og derefter til r18S niveauet (intern kontrol). Hver prøve blev analyseret i mindst 2 uafhængige målinger for hvert gen. Dosis-respons effekt af østradiolbenzoat på uterus ERα/β mRNA genekspression ses på Fig 2.2.5. Ved eksponering af rotter med stigende østradiolbenzoat (0,5 – 4 μg/kg/dag) blev der observeret et signifikant (t-test; p 0,05) fald i både ER og uterus mRNA i forhold til kontroldyr. Resultatet støtter hypotesen om en negativ feedback autoregulering af aktiveret ER.
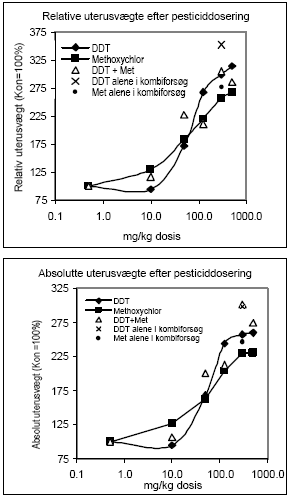
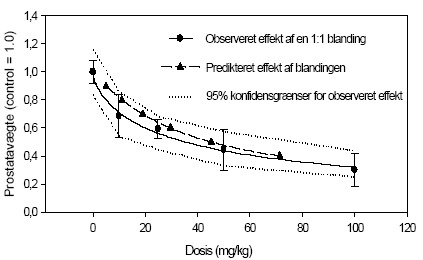
Figur 2.2.5. Dosis-respons af østradiolbenzoat på uterus ERα/β genekspression. Kontrolgruppen har fået jordnøddeoli.Resultatet er gennemsnit af n= 5 dyr, undtagen for det højest doserede hold hvor n=4. *: p 0,05. Det skal bemærkes, at ekspressionsniveauet af mRNA for ER er ca. 1000 gange lavere end for ER. Dette kan ikke ses på diagrammerne pga. normalisering til den kendte positive kontrol. 2.2.4 Effekt på neurotoksiske parametreHjernens signalstoffer (neurotransmittere) er af essentiel betydning for dennes organogenese, kønsdifferensiering og funktion under udvikling og i voksne individer. Vigtige CNS-neurotransmittere er acetylcholin (ACh), noradrenalin (NA), dopamin (DA) og 5-hydroxytryptamin (5HT). Forstyrrelse af funktionen af neurotransmittere kan give anledning til fejludvikling og funktion af hjernen. Indenfor forskningsområdet vedrørende de hormonforstyrrende stoffer ved man endnu meget lidt om stoffernes neurotoksiske effekter og effekter på adfærd, men det er et af de områder, som der højst sandsynligt vil blive fokuseret mere på fremover. Derfor har vi som noget nyt inkluderet disse parametre i dyreforsøgene for at få belyst om nogen af de kendte østrogene stoffer påvirker hjernens funktion. De neurokemiske parametre, der er blevet undersøgt for i udvalgte hjerneregioner, inkluderer neurotransmitterne noradrenalin, dopamin og 5-hydroxytryptamin (Lam et al., 1992), der anvendes som markører på effekt på hjernens noradrenerge, dopaminerge og serotonerge system. Cholinesteraseaktivitet i hjernevæv blev ligeledes målt (Ellman et al., 1961). Acetylcholinesterase (AChE) spalter og inaktiverer signalstoffet acetylcholin (ACh) når dette frigives ved impulsledning i det cholinerge nervesystem. Når dette enzym hæmmes, ophører effekten af ACh meget langsommere, hvilket er den tilgrundliggende mekanisme for flere pesticiders neurotoksiske effekt. Også andre cholinesteraser kan hæmmes af pesticider, f.eks. buturylcholinesterase (BuChE). I de gennemførte forsøg på hunrotter er der foretaget NA, DA, 5HT, AChE og BuChE analyser af alle prøverne af totalhjerner. Resultaterne indikerer, at østradiol ikke påvirker totalhjernens vægt, NA-, DA-, 5HT-koncentration eller AChE- eller BuChE-aktivitet i hunrotter, der har fået fjernet ovarierne. 2.2.5 Diskussion og konklusion på de østradiol-inducerede effekter in vivoOverordnet set gav østradiol-benzoat anledning til de forventede effekter, idet der sås en markant stigning i uterusvægten og hormonanalyserne viste et øget østradiolniveau med stigende dosis, et øget prolaktinniveau og et faldende FSH-niveau. Metoderne var dermed indkørt og kvalitetskontrollen viste, at procedurerne fungerer. Genekspressionsanalyserne viste at ovariektomi af dyrene bevirker en opregulering af både ERα og ERβ (se Fig 2.3.3), mens stigende doser østradiol forårsager en nedregulering af begge gener, hvilket er i overensstemmelse med teorien om, at østradiolniveauet i serum er afgørende for, hvor mange receptorer der dannes. Tidligere cellekulturstudier har vist, at østradiol nedregulerer ERα mRNA og proteinniveau (Vienonen et al. 2003; Clayton et al. 1997; Donaghue et al. 1999; Hofmeister & Bonefeld-Jørgensen, 2003). Hypotesen er, at der foregår en negativ autoregulerende feed-back involverende en hæmning af ER gentranskription, nedsat mRNA stabilitet og en induceret proteolyse af ER protein. Nylige tidsstudier i MCF-7 cellekultur har vist en nedregulering af ERα mRNA og en opregulering efterfulgt af nedregulering af ERβ mRNA ved eksponering for 17β-østradiol. Derudover er set effekter på ERα/β mRNA niveau af en række pesticider inklusive prochloraz (Hofmeister & Bonefeld-Jørgensen, 2003; Grünfeld & Bonefeld-Jørgensen, 2003). I dette studie blev der efter eksponering af ovariektomerede hunrotter for østradiolbenzoat, observeret en signifikant nedregulering af ERα og ERβ mRNA i uterusvæv allerede ved laveste koncentration (0,5 μg/kg/dag). Sammenholdt med, at der ligeledes blev observeret en statistisk signifikant stigning af uterusvægt i de samme østradiolbenzoateksponerede rotter ved samme lave koncentration, tyder disse resultater på at effekter på uterus (ER genekspression og vægt) er relativt følsomme parametre, som sandsynligvis kan respondere på endnu lavere doser østradiol. Uterusvægten og ER mRNA niveauer viste sig klart at være følsomme markører for den østrogene effekt end nogen af hormonanalyserne. Som noget nyt blev testet for neurotoksiske effekter af de østrogene stoffer, hvor det var et åbent spørgsmål om vi ville finde effekt eller ej. Data indikerer, at østradiol ikke påvirker niveauerne af de valgte transmitterstoffer. 2.3 Østrogene pesticider testet in vivo2.3.1 Effekt på organvægteTre dosis-responskurver for østrogene effekter in vivo for hhv. o,p-DDT, methoxychlor og stofferne i en 1:1 kombination blev udført. Den samme dyremodel som beskrevet under 2.2 blev anvendt. Hver gruppe indeholdt 6 dyr og pesticiderne blev doseret oralt i 4 dage i jordnøddeolie med et doseringsvolumen på 5 ml/kg kropsvægt. Pesticider blev doseret med 10, 50, 125, 300 og 500 mg/kg/dag hver for sig og i en 1:1 blanding. Ethinyløstradiol (doseret oralt) 100 μg/kg blev inkluderet i hvert forsøg og gav det forventede positive respons. Nyre-, hjerne- og hypofysevægte var uændrede, mens levervægten steg med både o,p-DDT og methoxychlor hver for sig og sammen. Kropsvægten var faldende for de højeste doser af begge stoffer og der sås toksisk effekt på dyrene doseret med hhv. o,p-DDT 500 mg/kg og o,p-DDT plus methoxychlor 500 mg/kg, mens dyr doseret med methoxychlor 500 mg/kg alene ikke havde iøjnefaldende påvirket almentilstand. Uterusvægten af kontroldyrene lå i de tre forsøg på hhv. 91, 79 og 107 mg. Data er normaliserede til disse værdier og både absolutte og relative uterusvægte er afbildet (Fig 2.3.1). Ved den laveste dosis på 10 mg/kg sås en effekt på uterusvægten af methoxychlor, men ikke af o,p-DDT. Derimod sås en mere markant effekt af o,p-DDT ved de højeste doser. Grunden til, at de relative uterusvægte stiger en anelse mere ved de højere doser end de absolutte vægte skyldes den faldende kropsvægt af dyrene.
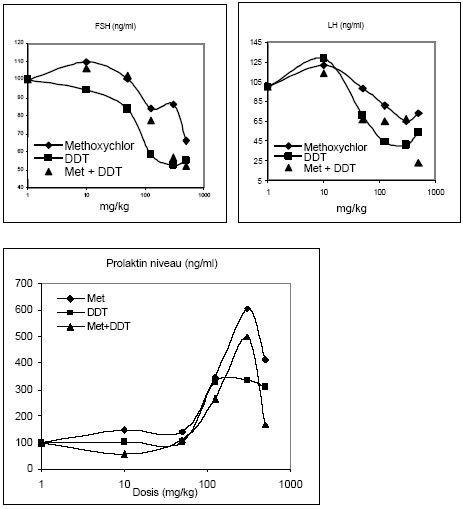
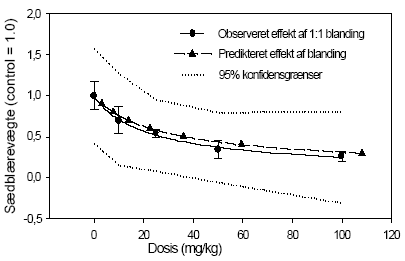
Figur 2.3.1 2.3.2 Effekt på hormonniveauerRotte luteiniserende hormon (LH) og follikelstimulerende hormon (FSH) blev analyseret ved hjælp af Delfia tidsforsinket fluorescens (Haavisto et al. 1993) (Fig 2.3.2). Niveauerne af begge hypofysehormoner faldt med stigende doser af o,p-DDT og methoxychlor. FSH niveauerne i kontroldyrene lå mellem 33-39 ng/ml, mens LH niveauerne i kontroldyrene lå mellem 12-20 ng/ml. For begge hormoner sås en tendens til at o,p-DDT havde den største hæmmende effekt. For de dyr, der var doseret med både o,p-DDT og methoxychlor, lå niveauerne af de to hormoner generelt imellem niveauerne for enkeltstofferne. Tages den biologiske variation og dermed spredningen på resultaterne i betragtning, der illustreres af, at CV% for FSH niveauerne i gennemsnit var 21%, mens den tilsvarende gennemsnitlige CV% for LH niveauerne var 47%, kan der ikke påvises nogen signifikant forskel mellem effekt af enkeltstofferne og af blandingen. For at teste om der var statistisk forskel på DDTs og methoxychlors effekt på LH niveauer blev det v.hj.a. en F-test testet om de to regressionslinier for dosis-responskurverne var signifikant forskellige fra hinanden. Der kunne ikke påvises nogen signifikant forskel på DDTs og methoxychlors effekt på serum LH niveau. Både o,p-DDT og methoxychlor gav anledning til stigende prolaktinniveauer i serum, men effekten var først markant ved en dosis på 125 mg/kg (fig 2.3.2). Generelt var der ikke nogen påviselig forskellig effekt af blandingen af pesticiderne sammenlignet med enkeltstofferne.
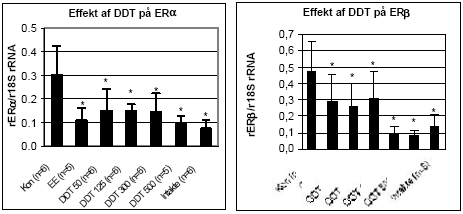
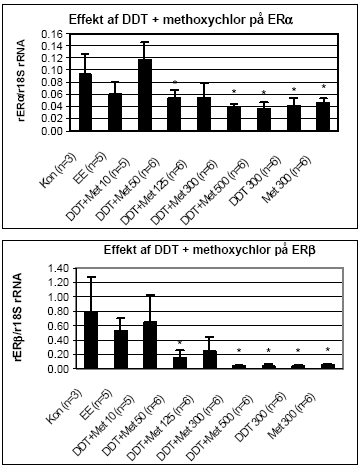
Figur 2.3.2 2.3.3 Effekt på østrogen-regulerede generEffekt af o,p-DDT og methoxychlor på ER mRNA i uterus blev analyseret v.hj.a. den metode der er beskrevet under 2.2.3. mRNA blev oprenset, cDNA syntetiseret og PCR analyser for ERα og ERβ blev udført. Effekten af o,p-DDT på uterus ER/ genekspression ses på Fig 2.3.3. En signifikant (t-test; p 0,05) nedregulering af ERα/β genekspression blev observeret for 100 μg/kg/dag oral eksponering af ethinylestradiol og for alle doser af o,p-DDT (50 mg/kg til 500 mg/kg) i forhold til kontroldyr, som fik indgivet jordnøddeolie. De intakte dyr er ikke-ovariektomerede dyr, som har fået jordnøddeolie. Resultatet viser dermed, at i normale intakte dyr er ERα og ERβ mRNA nedreguleret af østrogener produceret i ovarierne til et niveau svarende til indgivelse af 100μg/kg/dag af ethinylestradiol eller 50 mg/kg/dag o,p-DDT.
Figur 2.3.3. Effekt af o,p-DDT på uterus ERα og ERβ genekspression. Resultatet er gennemsnittet af det antal dyr, som er angivet i parentesen (n=) under de forskelligegrupper. Kontroldyr: olie; EE: 100 μg/kg/dag ethinyløstradiol; DDT 50: 50 mg/kg etc. for de andre grupper, hvor tallet angiver den totale orale dosis i mg/kg/dag. Alle eksponeringer var signifikant (p 0,05) forskellig fra kontrollen. Da o,p-DDT er vist at udøve en østrogen effekt ved såvel uterus vægtstigning som i MCF7-celleproliferationsanalysen, styrkes hypotesen, at østrogene stoffer der aktiverer ER medfører en negativ feedback autoregulering af ER transkription (mRNA niveau) som er gældende såvel in vitro som in vivo i uterusvæv. Resultatet for ERα og ERβ genekspression i uterus efter eksponering af rotter for methoxychlor ses i Fig 2.3.4. En signifikant nedregulering af begge ER receptorer blev observeret for alle testede koncentrationer.
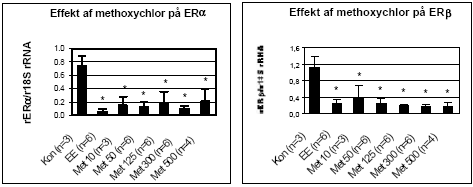
Figur 2.3.4. Effekt af methoxychlor på uterus ERα/β genekspression. Resultatet er gennemsnittet af det antal dyr, som er angivet i parentesen (n=) under de forskellige grupper. Kontrol: olie; EE: 100 μg/kg/dag ethinyløstradiol; Met 10: 10 mg/kg etc. for de andre grupper, hvor tallet angiver den totale orale dosis i mg/kg/dag. Alle eksponeringer var signifikant (p 0,05) forskellig fra kontrollen.
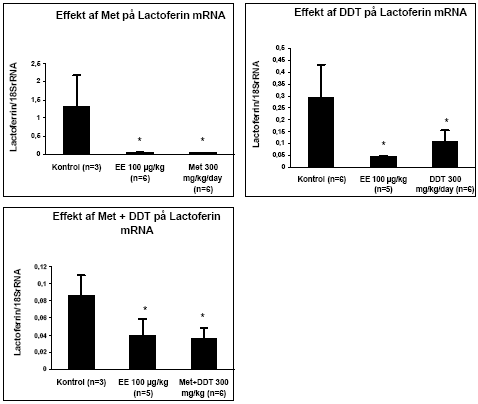
Figur 2.3.5. Effekt af en blanding af o,p-DDT og methoxychlor på uterus ERα/β genekspression. Resultatet er gennemsnittet af det antal dyr, som er angivet i parentesen (n=) under de forskellige grupper. Kon: jordnødde olie; EE: 100 μg/kg/dag ethinyløstradiol;DDT + Met 10: 5 mg/kg DDT plus 5 mg/kg methoxychlor givet oralt. Tilsvarende gælder for de andre grupper, hvor tallet angiver den totale dosis i mg/kg/dag. Alle eksponeringer på 50mg/kg og derover var signifikant (p 0.05) forskellig fra kontrollen. I kombinationsforsøget gav den positive kontrol ethinyløstradiol ikke noget signifikant respons på ERα/β i modsætning til de to tidligere forsøg. Det kan muligvis skyldes, at det kun var muligt at isolere RNA fra 3 kontroldyr i dette forsøg, hvilket resulterer i en høj standardafvigelse. Sammenlignes effekten på både ERα og ERβ af 300 mg/kg af enkeltstofferne (fig. 2.3.3 og fig. 2.3.4) med effekten af blandingen af samme koncentration (fig 2.3.5) ses, at effekten ikke er signifikant forskellig, hvilket indikerer additivitet af stofferne også på gen-niveau. Effekten af o,p-DDT og methoxychlor på lactoferin mRNA blev undersøgt for udvalgte grupper (Fig 2.3.6). Resultaterne viste, at begge pesticider ved en dosis på 300 mg/kg sænkede lactoferin mRNA til et niveau svarende til det, der blev opnået med den positive kontrol ethinyløstradiol. I kombinationsforsøget reducerede både ethinyløstradiol og o,p-DDT og methoxychlor 300 mg/kg hver for sig og sammen signifikant lactoferin mRNA niveau.
Figur 2.3.6. Effekt af henholdsvis methoxychlor (Met 300 mg/kg), o,p-DDT (300 mg/kg) og stofferne i kombination (150+150 mg/kg) på lactoferin mRNA i rotteuterus. 2.3.4 Effekt på neurotoksiske parametreNeurotransmitteranalyse blev foretaget for forsøgene med o,p-DDT, methoxychlor og kombinationer af stofferne på samme måde som beskrevet i 2.2.4. Data indikerer at hverken o,p-DDT, methoxychlor eller kombinationerne heraf påvirker totalhjernens vægt, proteinkoncentration, NA-, DA-, 5HT-koncentration eller AChE- eller BuChE-aktivitet. 2.3.5 Biomarkør for xenoøstrogent respons i serumPå afdeling for Miljømedicin ved Syddansk Universitet er en biomarkørmetode til måling af xenoøstrogent respons i humant serum indkørt (Rasmussen et al, 2003). Metodens princip er, at endogene østrogener fjernes fra serum ved fastfase ekstraktion og efterfølgende HPLC-fraktionering. Fraktioner uden endogene østrogener testes efterfølgende for østrogen aktivitet i MCF-7 celleproliferationsassayet. Serum fra rotter, der indgik i forsøgene for østrogene kombinationseffekter, er blevet testet ved hjælp af denne metode. Indledningvist blev metoden til rotteserum indkørt ved at teste serum fra rotter doseret med det positive kontrolstof østradiolbenzoat. Der var problemer med et østrogent stof der eluerede i den serumfraktion, hvor en del af pesticiderne eluerede og hvor der ikke i humant serum eluerer østrogener. Det viste sig, at skyldes østradiolbenzoat, som dyrene blev doseret med, og som ikke tilhører de fysiologiske østrogener. Metoden er herefter blevet modificeret, så den fraktion som indeholder østradiolbenzoat blev fjernet i de forsøg hvor rotterne er doseret med østradiolbenzoat som positiv kontrol, inden serumprøven blev testet i MCF-7 celleassayet (Fig 2.3.7). Serum fra hunrotter behandlet med o,p-DDT og methoxychlor alene og i kombination blev analyseret v.hj.a. denne metode. I pesticidforsøgene blev ethinyløstradiol anvendt som positivt kontrolstof, hvorfor den oprindelige fraktioneringsmetode for serumprøverne kunne anvendes. For at få en tilstrækkelig mængde serum til HPLC-fraktioneringen har det været nødvendigt at poole serum fra dyrerne i hver doseringsgruppe. Den poolede serumprøve er herefter blevet fraktioneret. De fraktioner som indeholdt de fysiologiske østrogener samt ethinyløstradiol blev kombinerede og kaldes Fraktion 2. De resterende fraktioner, hvor pesticiderne eluerede, blev kombineret og kaldes Fraktion 1. Begge fraktioner er blevet testet både med og uden 17β-østradiol i en fortyndingsrække, for at sikre at responset ligger indenfor 17β-østradiol standardkurven (som medtages i hvert set-up) og at prøven ikke har toksiske effekter i assayet. Hver fortynding blev testet i tripelbestemmelse. Den fortynding, som gav det højeste respons, er anvendt til de videre beregninger. For fraktion 1 fra negative kontroller (doseret med jordnøddeolie) og postive kontroller sås det maximale respons ved en 5 ganges fortynding. For grupperne doseret med methoxychlor og o,p-DDT (alene og i kombination) sås det maksimale respons ved en 10 ganges fortynding. Fraktion 2 er testet for at sikre at HPLC-fraktioneringen har virket korrekt, dvs at det forventede respons fra ethinyløstradiol ses i denne fraktion og at der ikke er forhøjet respons i de pesticideksponerede dyr. Dette var opfyldt for alle grupperne. Nedenfor vises resultaterne for fraktion 1. Resultaterne er udtrykt som den Relative Proliferative Effekt (RPE) per ml serum efter korrektion for fortynding samt den mængde af serum, der blev fraktioneret. RPE = (PEserumprøve-1)/( PE max 17β-østradiol – 1), hvor PE er responset normaliseret til kontrol.
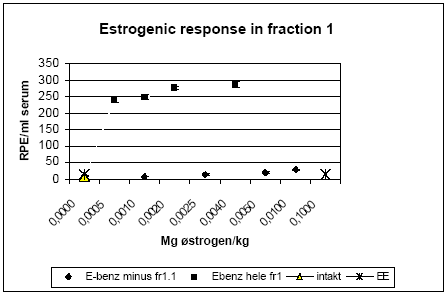
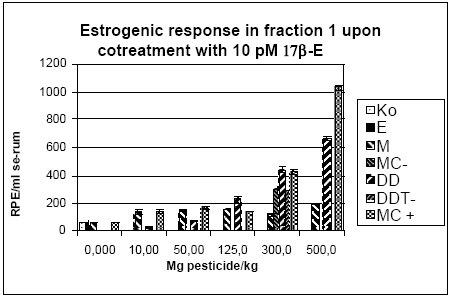
Figur 2.3.7. Respons i MCF-7 celleproliferationsassayet fra HPLC-fraktioneret rotteserum. Fraktion 1 repræsenterer serumprøven efter fjernelse af de endogent producerede østrogener. Intakt: er 'hele' ikke-ovariektomerede dyr. E-benz-fr1.1 er dyr doseret med østradiolbenzoat (s.c.) og hvor en subfraktion indeholdende østradiolbenzoat er fjernet.
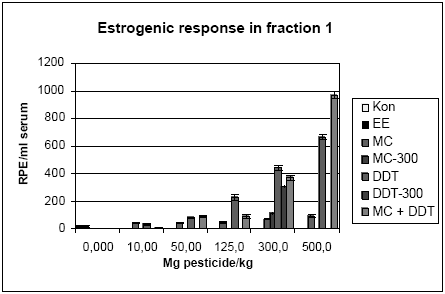
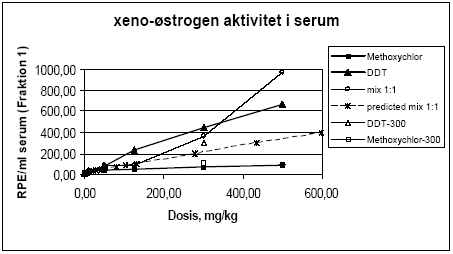
Figur 2.3.8. Respons i MCF-7 celleproliferation assayet fra HPLC-fraktioneret serum.Kon: olie; EE: 100 μg/kg/dag ethinylestradiol; MC: methoxychlor. MC-300 og o,p-DDT-300 er grupper der indgik i kombinationsforsøget men som blev doseret med methoxychlor eller o,p-DDT enkeltvis i en dosis på 300 mg/kg. For hver pesticid doseringsgruppe repræsenterer resultatet responset fra serum poolet fra de 6 dyr i gruppen. For Kon og EE repræsenterer resultatet gennemsnittet for 3 uafhæbgige grupper hidrørende fra de tre forskellige pesticidforsøg. Da der kun er testet en serumprøve per doseringsgruppe er der ikke udført statistiske analyser. Der ses dog et tydeligt dosis-relateret respons for begge pesticider samt for kombinationen af de to pesticider. I lighed med in vitro forsøgene i MCF-7 celle assayet (Fig 2.1.1) ses et kraftigere respons for o,p-DDT end for methoxychlor, når stofferne er doseret enkeltvis til dyrerne. Den kraftigste stigning i respons ses for gruppen doseret med kombinationer af methoxychlor og o,p-DDT. Stigningen i det målte respons er højere end man ville forvente hvis man analyserer resultaterne ved hjælp af isobolmetoden (Fig 2.3.9). Dette kunne tyde på en synergistisk effekt af de to pesticider på det xeno-østrogene respons. Der er imidlertid stor usikkerhed på målingerne, idet der kun er et datapunkt per dosis og fordi der ikke for alle dosisgrupper var 4,0 ml serum til rådighed for analyserne, som er den mængde serum assayet er valideret ved. Generelt var der mindre serum ved de højeste dosisgrupper og for den gruppe rotter som blev doseret med 500 mg/kg af 1:1 blandingen af o,p-DDT og methoxychlor var der kun 0,95 ml serum. Ved beregningen af resultaterne er der taget højde for disse forskelle i prøvemængde men der vil være større usikkerhed på målingerne ved de lave prøvemængder. Den observerede synergistiske effekt skal derfor tolkes med forsigtighed. En mulig biologisk forklaring kunne være at o,p-DDT og methoxychlor måske påvirker hinandens metabolisme så der enten sker en langsommere nedbrydning af o,p-DDT eller en øget dannelse af østrogene metabolitter af methoxychlor, idet methoxychlor vides at blive omdannet in vivo til en række metabolitter hvoraf mindst en er et mere potent østrogen end methoxychlor selv (Gaido et al., 1999).
Figur 2.3.9. Det observerede respons i fraktion 1 fra serum fra rotter doseret med methoxychlor og o,p-DDT enkeltsvist og i 1:1 kombinationer sammenlignet med det prædikterede respons for 1:1 kombinationerne under antagelse af additivitet beregnet ud fra isobolmetoden. For at undersøge eventuelle antiøstrogene eller additive effekter af pesticiderne overfor 17β-østradiol blev fraktion 1 også testet sammen med 10 pM 17β-østradiol på samme måde som i in vitro forsøgene (Fig 2.1.2).
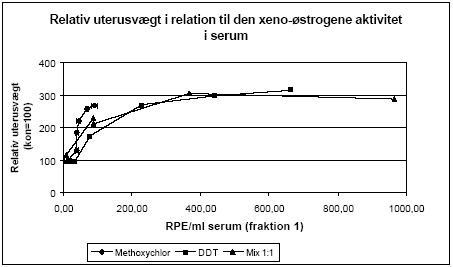
Figur 2.3.10. Respons i MCF-7 celle proliferations assayet fra HPLC-fraktioneret serum testet sammen med 10 pM 17β-østradiol.. Kon: olie; EE: 100 μg/kg/dag ethinylestradiol; MC: methoxychlor. MC-300 og o,p-DDT-300 er grupper, der indgik i kombinationsforsøget, men som blev doseret med methoxychlor eller o,p-DDT enkeltvis i en dosis på 300 mg/kg.For hver pesticiddoseringsgruppe repræsenterer resultatet responset fra serum pooled fra de 6 dyr i gruppen. For Kon og EE repræsenterer resultatet responset gennemsnittet fra 3 uafhængige grupper hidrørende fra de tre forskellige pesticidforsøg. Resultaterne stemmer godt overens med in vitro resultaterne, idet der ses en stigning i MCF-7 celleproliferationen, når serum fra de pesticidbehandlede dyr testes (fig 2.3.10). Dette tyder på at pesticiderne øger det samlede østrogene respons i dyrerne, mens der ikke er tegn på en antiøstrogen virkning. Sammenholdes den relative stigning i uterusvægten hos de doserede dyr med det xeno-østrogene respons i serum ses en stigning i uterusvægten ved RPE-værdier op til ca. 400. Herefter flader kurven ud, hvilket indikerer en mætning af vægtresponset i uterus. I en undersøgelse hvor effekten af lave doser af o,p-DDT og β-HCHs på epithelhøjde i uterus og vaginal epitheltykkelse i mus blev undersøgt som mål for østrogen virkning, sås ligeledes et plateau for epithelhøjden i uterus når blodkoncentrationen nåede et bestemt niveau af β-HCH (Ulrich et al., 2000) mens et tilsvarende plateau ikke sås for o,p-DDT ved de anvendte doseringer. Pesticiderne blev doseret ved subkutan implantation af kapsler hvorfra pesticiderne langsomt blev frigivet og blodkoncentrationerne af pesticiderne var væsentlig lavere end i vores undersøgelse, hvor den maksimale o,p-DDT koncentration kan estimeres til ca. 750 μg/ml serum (vurderet ud fra HPLC-målingerne) mod 622 ng/ml i den refererede undersøgelse.
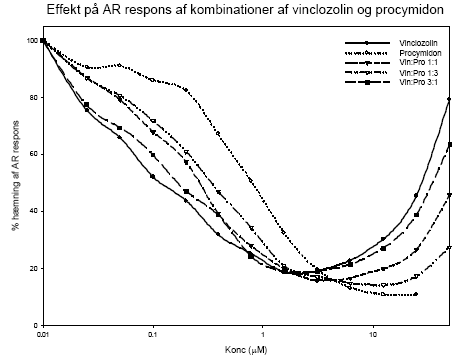
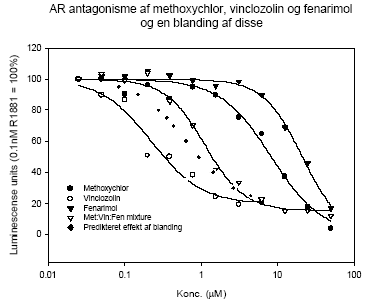
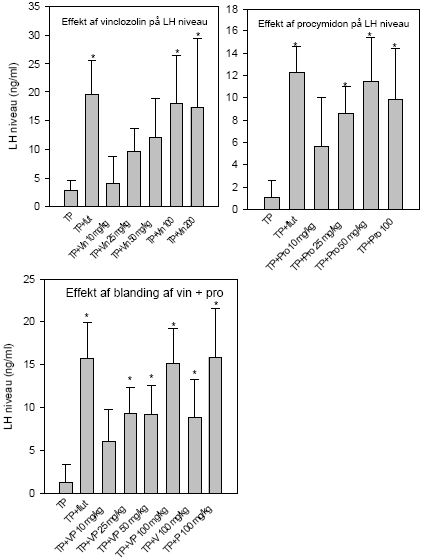
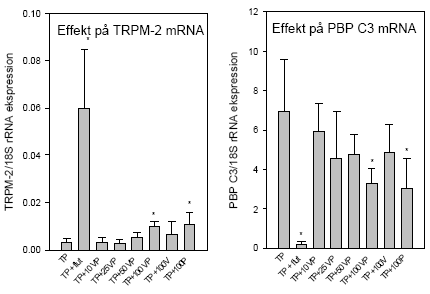
Figur 2.3.11.Stigning i relativ uterusvægt som funktion af respons i MCF-7 celle proliferation assayet fra HPLC-fraktioneret. De opnåede resultater viser, at biomarkørmetoden er anvendelig til at undersøge det samlede østrogene respons fra xeno-østrogener i en serumprøve. Responset ved de højeste pesticiddoser kan i denne undersøgelse være overestimeret, især for gruppen eksponeret for blandingen af de to pesticider, fordi der ikke var den optimale mængde serum til analysen. Under alle omstændigheder ses en klar dosis-relateret stigning i det xeno-østrogene respons i serum. Fordelen ved metoden er, at den tager højde for optagelse i organismen samt dannelse af eventuelle østrogene metabolitter samt nedbrydningen af pesticiderne til inaktive substanser. Den er således egnet til at vurdere den samlede interne eksponering for østrogene stoffer, herunder også af komplekse blandinger. 2.3.6 Diskussion og konklusion på de pesticid-inducerede østrogene effekterI in vitro forsøgene er der god overenstemmelse mellem de målte effekter og de predikterede effekter for additiv virkning beregnet ud fra isobolmetoden. For methoxychlor og o,p-DDT indikerer resultaterne, at der ikke er synergistisk eller antagonistisk interaktion mellem de to pesticider in vitro men en klar additiv virkning. Dette tyder på, at de to pesticiders østrogene virkning skyldes samme virkningsmekanisme, nemlig direkte interaktion af stofferne med ER. Ligeledes indikerer resultaterne for blandinger af methoxychlor, fenarimol og vinclozolin, at de to pesticider med østrogen virkning, fenarimol og methoxychlor, udviser additivitet, mens vinclozolin, som ikke er østrogent, ikke påvirker responset i blandingerne. Også andre in vitro undersøgelser af blandinger af østrogene stoffer har tydeligt vist additivt respons under anvendelse af koncentrations-additionsmodellen. Dette gælder således ved testning af o,p-DDT, p,p-DDT, p,p-DDE og β-HCH i MCF-7 celleassayet (Payne et al., 2001) og for 2-, 3- og 4- komponentblandinger af o,p-DDT, genistein, 4nonylphenol og 4-n-octylphenol i et ER reportergen assay (Payne et al., 2001). I in vivo forsøgene med o,p-DDT og methoxychlor er undersøgt effekt på uterusvægt, effekt på FSH-, LH- og prolaktinniveauer, effekt på ERα og ERβ mRNA i uterus og på udvalgte neurotransmittere og cholinesteraser i hjernevæv. Kort fortalt ses med stofferne en stigning i uterusvægt og prolaktinniveau, mens LH-, FSH-niveau og ERα og β mRNA falder. Effekten af både o,p-DDT og methoxychlor på uterusvægt og LH niveauer sås ved den næstlaveste dosis på 50 mg/kg. Derimod sås effekt allerede ved 10 mg/kg methoxychlor på genekspressionsniveau, hvilket indikerer at dette er den mest følsomme af de undersøgte parametre. Der ses ikke umiddelbart effekt på neurotransmitterniveauer og acetylcholinesteraseaktivitet. Generelt kan der ikke ses bort fra, at den uundgåelige biologiske variation mellem dyrene i disse forsøg bevirker, at en meget præcis og detaljeret undersøgelse af samspilseffekterne er vanskelig og understreger behovet for i in vivo forsøg at undersøge flere dosisniveauer for at få det fulde billede af stoffernes virkning hver for sig og i kombination. De hidtil opnåede data giver dog alligevel et relativt klart billede af samspillet mellem o,p-DDT og methoxychlor. På baggrund af de opnåede resultater for organvægte, hormonniveauer og ER mRNA niveau kan der ikke påvises fravær af additivitet, d.v.s. der er ikke holdepunkter for at antage, at der er nogen synergistiske eller antagonistiske samspilseffekter mellem stofferne. Dette underbygges af, at in vitro forsøgene med de samme stoffer viser samme additivitet. Baseret på in vitro og in vivo studier er en række pesticider herunder o,p-DDT og methoxychlor blevet klassificeret som potentielle miljøøstrogener (Scippo et al. 2003; Diel et al. 2002; Welsh et al. 1969; Gray et al. 1999; Brody and Rudel, 2003). I det aktuelle studie udviste både o,p-DDT og methoxychlor samt en kombination af de to pesticider en signifikant nedregulering af begge østrogenreceptorer ved de lavest testede koncentrationer henholdsvis 50 mg/kg/dag og 10 mg/kg/dag. Resultaterne indikerer, at uterus ER genekspressionsanalyser er meget følsomme og vil være i stand til at respondere til eksponering af disse pesticider ved lavere koncentrationer. Effekter på genekspression af et tredje østrogen-responsivt gen i uterusvæv, lactoferrin, blev ligeledes signifikant nedreguleret og viste den samme høje følsomhed ved eksponering til østradiol, o,p,-DDT og methoxychlor samt en kombination af de to pesticider. De observerede effekter af kombinationer af de to pesticider på ekspressionen af de tre gener indikerer, at der er tale om en additiv effekt. Sammenligning af test for østrogenicitet i tidligere in vitro studier af pesticidet prochloraz (Andersen et al., 2002) med in vitro effekter på ER α/β mRNA (Hofmeister & Bonefeld-Jørgensen, 2003; Grünfeld & Bonefeld-Jørgensen, 2003) og effekter på ERα og ERβ mRNA niveau i uterusvæv (nye upublicerede resultater, Bonefeld-Jørgensen) tyder på, at der er overensstemmelse imellem effekter observeret in vitro og in vivo. 2.4 Antiandrogene pesticider testet in vitroPesticidernes evne til at blokere androgenreceptoren blev undersøgt ved hjælp af et reportergenassay for antiandrogene effekter (Vinggaard et al. 1999). Chinese Hamster Ovary celler (CHO K1) blev udsået i mikrotiterplader og hver brønd blev transfekteret med 75 ng DNA bestående af ekspressionsvektoren pSVAR0 og et MMTV-LUC reporterplasmid i en ratio på 1:100 ved hjælp af 0.15 μl af transfektionsreagenset FuGene. Androgenreceptoragonisten R1881 (0.01 nM) plus/minus pesticider blev tilsat og efter en inkubationsperiode på 24 timer blev cellerne lyseret og aktiviteten af den dannede luciferase blev målt i et BioOrbit Galaxy luminometer. 2.4.1 Effekt af kombinationer af vinclozolin og procymidonDer er udført forsøg til belysning af kombinationseffekter af vinclozolin og procymidon for androgenreceptorinhibering in vitro. De enkelte stoffer og tre kombinationer bestående af 1:1, 1:3 og 3:1 blandinger af pesticiderne blev undersøgt i 12 koncentrationer i området 0.025 – 50 μM (Fig 2.4.1). For procymidon alene ses en antiandrogen effekt i hele koncentrationsområdet, mens der for vinclozolin ses en antiandrogen effekt op til en koncentration på ca. 3 μM, hvorefter hæmningen forsvinder. Da det er metabolitterne af vinclozolin, der er de aktive antiandrogene stoffer, kan dette tænkes at skyldes at vinclozolin-metabolitterne er partielle agonister ved høje koncentrationer, som det også er observeret for det kendte antiandrogene stof hydroxyflutamid. Overordnet set blev de forventede antiandrogene effekter for enkeltstofferne observeret og IC50 for vinclozolin og procymidon fandtes at være henholdsvis 0.1 og 0.6 μM. Data for enkeltstofferne blev normaliseret (da der ses interassay variation) og der blev lavet kurvefitning v.hj.a. non-lineær regression, hvor 'Four parameter logistic curve fit' blev anvendt (F= min + (max-min)/(1+(x/EC50)^Hill-slope)). På baggrund af de fremkomne kurve-fit for enkeltstofferne blev det forventede respons af blandingerne beregnet, under antagelse af at stofferne virker additivt. Herefter blev de forventede og rent faktisk opnåede effekter sammenlignet for 1:1, 1:3 og 3:1 blandingerne (Fig 2.4.2).
Figur 2.4.1. Androgenreceptor blokering induceret af stigende koncentrationer af vinclozolin eller procymidon eller de to stoffer i kombination bestemt i tilstedeværelse af 0.01 nM R1881. Data repræsenterer gennemsnittet af n=4-6 forsøg hver udført i firdobbelt bestemmelse. Figur 2.4.2 Sammenligning af observeret respons og prædikteret respons for androgen receptor blokering induceret af blandinger af vinclozolin og procymidon. Data repræsenterer mean ±SD for n= 4-6 forsøg.
Figur 2.4.3 Additivitetsisobol for 50% hæmning af androgen receptor aktivering for blandinger af vinclozolin og procymidon til sammenligning med de faktisk observerede effekter af blandingerne. Isobolen som afbilder de effekter der angiver 50% hæmning af det R1881-inducerede respons ses i fig 2.4.3. Den dosis af vinclozolin der giver 50% androgen receptor blokering er afbildet på x-aksen, mens den tilsvarende dosis af procymidon er angivet på y-aksen. Punkterne for blandingerne ses at ligge tæt op ad additivitets-isobolen, som er den rette linie mellem punkterne på x- og y-aksen. Resultaterne i fig 2.4.2 og 2.4.3 indikerer, at vinclozolin og procymidon virker additivt og at der ikke er nogen interaktion mellem stofferne. I dette tilfælde opnås således i in vitro forsøg det predikterede additive respons, hvilket indikerer at der ikke umiddelbart er nogen grund til at tro, at synergistiske eller antagonistiske samspilseffekter for disse antiandrogene stoffer finder sted ved blokering af androgenreceptoren in vitro. 2.4.2 Effekt af kombinationer af vinclozolin, methoxychlor og fenarimolFormålet med dette studie var at undersøge kombinationeffekt in vitro af 3 pesticider med forskellig virkningsmekanisme. Udover at de 3 pesticider alle virker antiandrogent in vitro og hæmmer aktivering af androgen receptoren, virker både methoxychlor og fenarimol også østrogent in vitro og fenarimol har deuden den egenskab at den hæmmer aromataseaktivitet. Resultaterne i fig 2.4.4 viser, at når den forventede effekt af blandingen sammenlignes med den rent faktisk observerede effekt af blandingen under forudsætning af additivitet, så ses en effekt der er mindre end en additiv effekt. Isobolkoefficienterne som er opgivet i tabellen er generelt større end 1 og samlet indikerer disse data at de 3 pesticider virker antagonistisk i dette assay. En forklaring på dette kan være at den metaboliske kapacitet i cellerne har nået sin grænse, idet det gælder for både vinclozolin og methoxychlor at det er metabolitterne, der er de mest aktive antiandrogene stoffer.
Figur 2.4.4 Koncentrations-responskurver for hhv. vinclozolin, methoxychlor og fenarimol og en blanding af stofferne i æquimolært forhold (1:1:1). Androgenreceptor inhibering er analyseret i reportergen assay i tilstedeværelse af 0.1 nM R1881. Data repræsenterer 3 uafhængige forsøg udført i 4-dobbelt bestemmelse.
2.5 Antiandrogene pesticider testet in vivoAntiandrogene effekter in vivo er undersøgt ved hjælp af den klassiske Hershberger test. Metoden er baseret på ikke-kønsmodne kastrerede Wistar hanrotter (28 dage gamle ved kastrationen) som doseres dagligt i 7 dage (fra dag 42-48) med testosteron med og uden teststof. Det kendte antiandrogen flutamid bruges som den positive kontrol. Blod opsamles til hormonanalyser og reproduktionsorganerne: ventral prostata, sædblærer, musc. levator ani/bulbocavernosus og bulbourethralkirtlen udtages og vejes. Ventral prostata gemmes til efterfølgende genekspressionsanalyse. I kombinationsforsøget blev hjerner udtaget til analyser for neurotransmittere. Denne dyreforsøgsmodel er etableret på DFVF (Hossaini et al., Abstract 2000; Vinggaard et al. 2002) og har indgået som en del af et interkalibreringsstudie i OECD regi. Der er i alt udført 3 dosis-respons forsøg, 1 med vinclozolin og 1 med procymidon alene (0, 10, 25 ,50, 100 og 300 mg/kg) og 1 kombinationsforsøg med en 1:1 blanding i samme doser som beskrevet for enkeltstofferne. I det sidste forsøg blev også inkluderet to grupper, der fik administreret pesticiderne alene i en dosis på 100 mg/kg. 2.5.1 Effekt på organvægteEffekterne af vinclozolin på vægten af ventral prostata, sædblærer, musc.lev.ani og bulbourethralis var signifikant forskellige ved doser på hhv. 10, 10 , 25 og 25 mg/kg (Fig 2.5.1). Effekterne af procymidon på de tilsvarende organer var signifikant allerede ved 10 mg/kg i alle tilfælde. Kombinationen (1:1 blanding) af de to stoffer havde effekt på ventral prostata og sædblærer ved 10 mg/kg, mens effekten på musc.lev. ani/bulbocavernosus og bulbourethralkirtlen først opstod ved en 25 mg/kg dosis. Analyse af kombinationseffekterne på prostatavægte og sædblærevægte v.hj.a. isobolmetoden og efterfølgende sammenligning af prædikteret og faktisk opnået respons (fig 2.5.3 og 2.5.4) viser, at der er grundlag for at antage at de antiandrogene stoffer også in vivo virker additivt. Der er en tendens til - ved de lavere doser - at effekten er en smule kraftigere end den predikterede, men SD'erne for det opnåede respons overlapper det predikterede, og endelig ligger det predikterede respons (under antagelse af additivitet) indenfor 95% konfidensgrænserne for det faktisk opnåede respons.
Figur 2.5.1. Effekter af stigende doser af en 1:1 blanding af vinclozolin og procymidon på vægte af hhv. ventral prostata, sædblærer, m. levator ani/bulbocavernosus og bulbourethralkirtlen. De sidste to søjler i hver figur viser effekten af hhv. vinclozolin 100 mg/kg og procymidon 100 mg/kg doseret enkeltvis til dyrene og skal sammenlignes med den 3. sidste søjle hvor de er givet i kombination (50+50 mg/kg). Hver søjle repræsenterer middel ±SD for n=6 dyr.
Figur 2.5.2. Dosis-responskurver for effekt på prostatavægte af hhv. vinclozolin og procymidon. Se i øvrigt figurteksten 2.5.1.
Figur 2.5.3. Sammenligning af observeret effekt og forventet effekt under antagelse af additivitet på prostatavægte for en 1:1 blanding af vinclozolin og procymidon.
Figur 2.5.4. Sammenligning af observeret effekt og forventet effekt under antagelse af additivitet på sædblærevægte for en 1:1 blanding af vinclozolin og procymidon. 2.5.2 Effekt på hormonniveauerLH og FSH i serum blev analyseret v.hj.a. Delfia metoden (af Pirji Pakarinen, Turku Universitet, Finland). Begge pesticider gav som ventet en signifikant stigning i LH niveau, der opstod ved hhv. 100 mg/kg og 25 mg/kg for vinclozolins og procymidons vedkommende (fig 2.5.5). Ved dosering med en blanding af pesticiderne sås signifikant effekt ved doser på 25 mg/kg og opefter. Mht. FSH analyserne sås generelt mindre markante effekter end de der blev opnået med LH, men der sås en signifikant stigning af FSH for både vinclozolins og procymidons vedkommende ved 25 mg/kg (data ikke vist). Der var dog ikke nogen klar dosis-respons sammenhæng. I kombinationsforsøget sås en statistisk signifikant effekt allerede ved en total dosis på 10 mg/kg. Generelt for disse FSH data gælder, at der ikke fås nogen pæn dosis-responskurve for nogen af stofferne, f.eks. ses effekt af 50 og 200 mg/kg vinclozolin, men ikke af 100 mg/kg. For procymidons vedkommende ses effekt ved 25 mg/kg, men ikke ved andre doser. I kombinationsforsøget er alle doser derimod signifikant forhøjede, og der er åbenbart opnået maksimal effekt allerede ved laveste dosis for der er ingen hældning på kurven. Pga. den manglende dosis-respons effekt på FSH niveau og pga. de mindre konsistente data, kan der ikke drages nogen endelig konklusion udfra disse data.
Figur 2.5.5 Effekt af pesticider på serum niveau af luteiniserende hormon (LH). Øverst til venstre:Dosis-respons af vinclozolin alene. Øverst til højre: Dosis-respons af procymidon alene. Nederst: Dosis-respons af 1:1 blandinger af vinclozolin og procymidon plus en enkelt gruppe der fik pesticiderne hver for sig (100 mg/kg).'TP': testosteronpropionat 'Flut': flutamid. 2.5.3 Effekt på genekspressionLightcycler-teknologien, der er beskrevet i afsnit 2.2.3 blev anvendt til at kvantificere den relative ekspression i prostata af de androgent-regulerede gener, testosterone-repressed prostatic message 2 (TRPM-2) og prostata binding protein polypeptide C3 (PBP C3) sammenlignet med ekspressionen af 18S-mRNA (Nellemann et al. 2000). TRPM-2 udtrykkes ikke normalt i rottens ventrale prostata men induceres ved kastration og er sandsynligvis involveret i apoptosis. PBP C3 udgør ca. 50% af secerneret protein fra den normale rotteprostata og er derfor det mest forekommende androgent-regulerede gen i dette væv. Data viser, at flutamid som ventet giver et øget TRPM-2 mRNA niveau, mens PBP C3 mRNA blev signifikant nedsat (fig 2.5.6). Vinclozolin alene gav ikke noget signifikant respons ved 100 mg/kg, mens procymidon (100 mg/kg) gav signifikant forøget TRPM-2 og nedsat PBP C3 mRNA i forhold til testosteron-kontrollen. Disse resultater indikerer, at effekten på genekspressionsniveau i dette tilfælde indtræder ved højere doser end de der skal til for give effekt på organniveau og på LH niveauer.
Figur 2.5.6 Dosis-respons effekt af blandingen af vinclozolin og procymidon på TRPM-2 mRNA og PBP C3 mRNA i prostata. 2.5.4 Effekt på neurotoksiske parametreHverken vinclozolin eller procymidon hver for sig eller sammen påvirkede totalhjernens vægt, proteinkoncentration, NA-, DA-koncentration eller AChE- eller BuChE-aktivitet i disse forsøg. Dette indikerer, at de noradrenerge, dopaminerge, og cholinerge dele af CNS ikke påvirkes markant af pesticiderne. Multipel statistisk analyse (Dunnett's Metode) viste, at holdene doseret med 10, 25 og 50 mg/kg vinclozolin og procymidon i kombination og med 100 mg/kg vinclozolin eller 100 mg/kg procymidon alene statistisk signifikant afviger fra kontrolholdet doseret med testosteron med hensyn til totalhjernens 5HT- koncentration (fig 2.5.7). Der er efterfølgende udtaget totalhjerner fra ikke-behandlede og testosteron-behandlede kastrerede dyr for at få en afklaring af, om testosteronbehandlingen i sig selv påvirker hjernens 5HT-koncentration i forhold til kontrolbehandling. Dette viste sig ikke at være tilfældet. 5-HT vides at regulere LHRH sekretion fra hypothalamus i hunrotter (Moguilevsky & Wuttke, 2001) og også sekretion af hypofysehormoner og en effekt på 5-HT niveauet, kan ikke udelukkes at være involveret i stoffernes effekter. Flutamid gav dog ikke nogen effekt på 5-HT niveauet, hvilket tyder på at der ikke er tale om en generel effekt af antiandrogener.
Figur 2.5.7. Effekt af blandingen af vinclozolin og procymidon på 5-hydroxytryptamin niveau (serotonin) i hjernehomogenater. 2.5.5 Diskussion og konklusion på de pesticid-inducerede antiandrogene effekterI in vitro forsøgene for kombinationer af vinclozolin og procymidon er der god overenstemmelse mellem de målte effekter og de prædikterede værdier for additiv virkning beregnet ud fra isobolmetoden. Dette indikerer, at der ikke er synergistisk eller antagonistisk interaktion mellem de to pesticider men en klar additiv virkning. Dette tyder også på, at de to pesticiders antiandrogene virkning skyldes samme virkningsmekanisme. I in vivo forsøgene med vinclozolin og procymidon er undersøgt effekt på vægt af reproduktionsorganer, effekt på FSH- og LH-niveauer, effekt på TRPM-2 og PBP C3 mRNA og på udvalgte neurotransmitterniveauer og acetylcholinesteraseaktivitet. Kort fortalt ses med stofferne et fald i vægte af alle reproduktionsorganer, en stigning i LH- og FSH-niveau og hhv. et fald og en stigning i mRNA niveauer af PBP C3 og TRPM-2. Følsomheden af de tre nævnte parametre for antiandrogener var i disse forsøg: reproduktionsorganvægte > serum LH niveau > genekspression i prostata. Hverken noradrenalin-, dopaminkoncentration, acetyl- eller butylcholinesterase-aktivitet var påvirkede efter vinclozolin og procymidon behandling, hvilket indikerer at de noradrenerge, dopaminerge, og cholinerge dele af CNS ikke påvirkes markant af pesticiderne. Dog gav vinclozolin og procymidon enkeltvis og i kombination en signifikant forøgelse af totalhjernens serotoninkoncentration. Da serotonin regulerer sekretionen af hypothalamus- og hypofysehormoner på en kompleks måde (Moguilevsky & Wuttke, 2001), kan det ikke udelukkes, at effekt på denne neurotransmitter indirekte kan bidrage til nogle af de hormonforstyrrende effekter af pesticiderne. Generelt vurderes, at der med det anvendte eksperimentelle design ses en biologisk variation mellem dyrene på organvægtniveau, der er af en størrelsesorden, som tillader en relativ præcis og detaljeret undersøgelse af samspilseffekterne. De opnåede data giver således et klart billede af samspillet mellem vinclozolin og procymidon. På baggrund af de opnåede resultater for organvægte, hormonniveauer og mRNA niveauer kan der ikke påvises fravær af additivitet, d.v.s. der er ikke holdepunkter for at antage at der er nogen synergistiske eller antagonistiske samspilseffekter mellem stofferne. Dette underbygges af, at in vitro forsøgene med de samme stoffer viser samme additivitet. Ovennævnte resultater er publiceret i Nellemann et al. 2003. In vitro forsøget, hvor blandinger af pesticider med forskellig virkningsmekanisme blev undersøgt (vinclozolin, menthoxychlor og fenarimol) viste dog ikke en klar additiv effekt, men der var tendens til antagonistiske effekter. Dette indikerer at pesticider i visse tilfælde kan spille sammen på en sådan måde at den totale effekt bliver mindre end man skulle forvente ud fra additivitetsprincippet. Dette understreger behovet for at undersøge kombinationer af pesticider med både samme og forskellig virkningsmekanisme. 3 Hormonforstyrrende effekter af en kombination af almindeligt anvendte pesticider
3.1 Østrogen effekt af kombinationer af 5 pesticider in vitroSom eksempler på almindeligt anvendte pesticider i Danmark blev valgt:
Den østrogene effekt in vitro af de 5 pesticider blev testet i MCF-7 celle proliferationsassayet som beskrevet i afsnit 2.1. Pesticiderne blev testet enkeltvis og i en ækvimolær (1:1:1:1:1) blanding i koncentrationer op til 25 μM. Pesticiderne blev testet både uden og med 10 pM 17β-østradiol for at undersøge såvel agonistisk som antagonistisk effekt (Figur 3.1.1 og 3.1.2). Ved testning af pesticiderne uden 17β-østradiol var det kun methiocarb og deltamethrin, som inducerede et østrogent respons. Tribenuron-methyl, som i en tidligere undersøgelse var svagt østrogent ved 25 og 50 μM (Andersen et al., 2002), gav ikke noget respons i denne undersøgelse. Som det ses af Figur 3.1.1 gav blandigen ikke noget synligt respons indenfor de undersøgte koncentrationer. Ud fra de fittede kurver er isobolkoefficient ved EC5 beregnet:
Da isobolkoeficcienten er > 1 tyder det på en antagonistisk effekt i blandingen. Den antagonistiske effekt skyldes sandsynligvis prochloraz, som udviser en tydelig hæmning af 17β-østradiol-induceret MCF-7 celleproliferation (Figur 3.1.2). Prochloraz udviser ingen østrogen aktivitet når det testes uden østradiol. Methiocarb, som udviste østrogen effect når det blev testet alene, havde også en svag antiøstrogen virkning overfor 17β-østradiol. Da blandingen ikke havde nogen effekt på det østradiol-inducerede respons, var det ikke muligt at udregne en isobolkoefficient for blandingen. På figuren ses det dog, at den forventede antagonistiske virkning er større end den observerede, hvilket indikerer, at den antiøstrogene virkning af prochloraz modvirkes af de østrogene pesticider. Figur 3.1.1. Koncentrations-responskurver for MCF-7 celle proliferation for de fem pesticider enkeltvis og i en 1:1:1:1:1 blanding. Data er angivet som middel ±SD for 3-5 uafhængige forsøg, undtagen for tribenuroin-methyl hvor n=1. Figur 3.1.2. Koncentrations-responskurver for MCF-7 celle proliferation for de fem pesticider enkeltvis og i en 1:1:1:1:1 blanding testet sammen med 10 pM 17β-østradiol. Data er angivet som middel ±SD for 3-5 uafhængige forsøg. 3.2 Antiandrogen effekt af kombinationer af 5 pesticider in vitroDe 5 pesticiders effekt på AR blokering in vitro blev testet i det beskrevne reportergen assay (afs. 2.4). Samtidig blev cytotoksiciteten af stofferne testet ved co-transfektion af cellerne med reportergen vektoren MMTV-LUC og AR13, der er en vektor der koder for en konstitutivt udtrykt AR, men som mangler det ligand-bindende domæne. En cytotoksisk effekt på transkriptionsprocessen vil give sig udslag i et fald i luciferaseaktiviteten. Prochloraz havde cytotoksisk effekt ved 50 μM og derover og deltamethrin var cytotoksisk ved koncentrationer på 12.5 μM og derover, mens de resterende pesticider ikke var cytotoksiske ved koncentrationer ≤50 μM. Hverken tribenuron-methyl eller simazin havde nogen antiandrogen effekt i dette assay, mens både prochloraz og methiocarb blokerede AR med IC50 værdier på hhv. 7 og 15 μM (Fig 3.2.1). Da deltamethrin var cytotoksisk ved koncentrationer højere end 12.5 μM, var det ikke muligt at bestemme en IC50 værdi. Kombinationen af en 1:1:1:1:1 blanding af de 5 pesticider gav et antiandrogent respons, der lå på linie med det prædikterede respons under antagelse af additivitet (Fig 3.2.2). Figur 3.2.1. Koncentrations-respons kurver for androgenreceptor inhibering in vitro for de fem pesticider hver for sig og for en 1:1:1:1:1 blanding af pesticiderne. Data er angivet som middel ±SD for 3 uafhængige forsøg
Figur 3.2.2 Sammenligning af pesticidblandingens (1:1:1:1:1) prædikterede og observerede hæmning af AR-aktivering in vitro.50 μM svarer til 10 μM af hvert pesticid i blandingen. Data er angivet som middel ±SD for 3 uafhængige forsøg. Databehandling v.hj.a. isobolmetoden blev udført ved forskellige valgte effektniveauer og som eksempel er vist udregningen af isobolkoefficienten ved effektniveau IC25, som resulterede i en koefficient på 0.94. Ved en koefficient på 1 er der additivitet, er den < 1 er der synergisme og > 1 antagonisme, så resultatet indikerer, at stofferne i kombination virker additivt i dette assay. Eksempel på beregning af isobolkoefficient ved effektniveau IC25: 3.3 Antiandrogen effekt af kombinationer af 5 pesticider in vivoDe samme 5 pesticider som blev testet for antiandrogen effekt in vitro, blev testet in vivo i et udbygget Hershberger assay, hvor effekter på både organvægte, hormonniveauer og genekspression blev analyseret. I første omgang var ideen udelukkende at screene en blanding af de 5 stoffer for at afsløre om der var effekt eller ej. Det blev senere besluttet at inkludere 5 grupper dyr, som fik indgivet enkeltstofferne alene. På basis af et sådant forsøg er det udelukkende muligt at få en indikation af om der er en kombinationseffekt. Da der ikke er udført dosis-respons forsøg, kan en eventuel mekanisme for interaktion ikke udledes. 54 Wistar hanrotter blev kastrerede ca. 4 uger gamle og ankom en uge før dosering, ca. 5 uger gamle. De blev randomiseret efter vægt, således at der ikke var statistisk signifikant forskel på middellegemsvægt mellem grupperne. Dyrene blev fodret med Syn 8.IT, en diæt fri for fytoøstrogener, og fik adgang til syrnet vand, begge dele ad libitum. Stalden havde en rumtemperatur på 22 ±1°C og en luftfugtighed på 55± 5 %. Der var luftskifte 10 gange i timen, mens der blev holdt en tolv-timers lys/mørke cyklus fra 9-21 og 21-9. Rotterne blev tilset for helbredseffekter og vejet to gange dagligt under doseringsperioden, som fandt sted i syv dage, en uge efter ankomst. Gruppe 1 blev doseret dagligt med jordnøddeolie, som var mediet teststofferne var opløst i. De resterende 8 grupper blev doseret med 0.5 mg/kg testosteronpropionat plus/minus teststof. Gruppe 2 fik kun testosteronpropionat og fungerede som kontrolgruppe. Flutamid, som er et kendt antiandrogen der anvendes klinisk, fungerede som positiv kontrol i gruppe 3 med en dosering på 20 mg/kg s.c. Gruppe 4-8 blev doseret enkeltvis med teststofferne: prochloraz, simazin, deltamethrin, tribenuron-methyl og methiocarb med en dosis på henholdsvis 25, 25, 2.5, 25 og 2.5 mg/kg. En kombination af teststofferne svarende til 80 mg/kg (25+25+2.5+25+2.5 mg/kg) blev administreret til gruppe 9. Testosteronpropionat og flutamid blev givet s.c. med et doseringsvolumen på 2 ml/kg, mens teststofferne blev givet oralt med sonde i et volumen på 5 ml/kg. Testosteron blev indgivet 2-10 min. efter teststofferne og den sidste dosering skete om morgenen den dag sektion af dyrene skulle foregå. Under bedøvelse med CO2/O2 blev blodet fra dyrene tappet ved hjertepunktur og serum fremstillet og nedfrosset ved –80°C til senere analyse for LH, testosteron, thyroxin og prolaktin. Lever, nyrer og binyrer blev udtaget, renset og vejet, det samme skete for thyroidea, bulbourethralkirtler, sædblærer, ventral prostata samt Musc.levator ani/bulbocavernosus. Efter vejning blev ventral prostata hurtigt placeret i 0.5 ml RNAlater (Ambion, Huntingdon, England), sat på –20°C frys indtil oprensning af RNA, cDNA-produktion og efterfølgende genekspressionsanalyser. Et forforsøg til testning af optimal dosis af deltamethrin (25 mg/kg) og methiocarb (2.5 mg/kg) blev foretaget på gamle ikke-kastrerede Wistar hanrotter med det formål at undersøge, hvorvidt rotterne kunne tåle dosis. Pga. tydelig toxicitet af 25 mg/kg deltamethrin blev yderligere et forforsøg med 5 mg/kg deltamethrin foretaget. Ud fra disse forsøg blev en dosis på 2.5 mg/kg valgt for begge dyregrupper. De endelige legems- og organvægte er angivet i Tabel 3.3.1. Generelt sås ingen effekt af enkeltstofferne på hverken lever-, nyre-, binyre- eller thyroideavægte, bortset fra at prochloraz gav forøget levervægt. Derudover var binyrevægten forøget efter dosering med blandingen. Tabel 3.3.1. Legems- og organvægte
N=6; *: p< 0,05. Med hensyn til effekt på vægte af reproduktionsorganer sås at den positive kontrol, flutamid, som ventet havde signifikant effekt på vægte af både ventral prostata, sædblære, m.levator ani/bulbocavernosus og bulbourethralkirtlen (Tabel 3.3.2). Der sås ingen effekt af enkeltstofferne, men kombinationsgruppen viste et signifikant fald i vægte af m.levator ani/bulbocavernosus og bulbourethralkirtlen. Der var også en tendens til en reduktion af prostata- og sædblærevægte, men disse slog ikke signifikant ud. Resultaterne indikerer en akkumulerende effekt af pesticiderne, som ikke kan påvises når de administreres enkeltvis til dyrene, men kun når de indgives i kombination. Tabel 3.3.2. Absolutte vægte af reproduktionsorganer
*Statistisk signifikant forskellig (p < 0,05) fra testosterongruppen. N=6. 'T' eller 'Testo': testosteronpropionat 0.5 mg/kg/dag s.c.; 'Flut': flutamid 20 mg/kg/dag s.c.; 'Pro': prochloraz 25 mg/kg/dag oralt; 'Sima': simazin 25 mg/kg/dag oralt; 'Delt': deltamethrin 2.5 mg/kg/dag oralt; 'Trib': tribenuron-methyl 25 mg/kg/dag oralt; 'Meth': methiocarb 2.5 mg/kg/dag oralt; 'Kombi': prochloraz (25 mg/kg/dag) + simazin (25 mg/kg/dag) + deltamethrin (2.5 mg/kg/dag) + tribenuronmethyl (25 mg/kg/dag) + methiocarb (2.5 mg/kg/dag). Resultaterne af hormonanalyserne fremgår af nedenstående tabel og viser, at flutamid giver et signifikant forhøjet LH niveau, mens de andre hormonniveauer er upåvirkede. Ingen af pesticiderne doseret enten enkeltvis eller i kombination påvirkede de fire hormoner. Dog gav tribenuron-methyl et signifikant fald i prolaktinniveauet. Tabel 3.3.3. Hormonniveauer målt i serum fra kastrerede Wistar rotter behandlet med testosteronpropionat alene eller sammen med teststof
*Statistisk signifikant forskellig (p < 0,05) fra testosterongruppen n.d.: not detectable. Se i øvrigt tabeltekst til tabel 3.3.2. Effekten af flutamid og pesticiderne på genekspressionsniveau i prostata blev undersøgt. Som ventet gav flutamid et signifikant fald i PBP C3 og ODC mRNA niveau, mens niveauet af TRPM-2 mRNA var signifikant forhøjet (Fig 3.3.1). Disse resultater er i overenstemmelse med tidligere fund (Nellemann et al. 2003). Prochloraz gav en signifikant reduktion af PBP C3 og ODC mRNA niveauet, men havde ingen effekt på TRPM-2 mRNA. Denne effekt har vi tidligere rapporteret for stoffet givet i en dosis på 50 mg/kg (Vinggaard et al. 2002) og nu kan vi konkludere, at effekten også ses efter en dosis på 25 mg/kg. Samtlige pesticider enkeltvis og i kombination gav et signifikant fald i ODC mRNA niveauet og ligeledes sås der et fald i PBP C3 mRNA for alle pesticider undtagen deltamethrin, tribenuron-methyl og kombinationsgruppen. Det er et enkelt dyr som er årsag til at kombinationsgruppen ikke slår ud. Da der er vist antiandrogene effekter in vitro for både prochloraz og methiocarb kan dette forklare faldet i det androgen-regulerede gen PBP C3. Det er overraskende at pesticidet simazin også påvirker PBP C3 mRNA, da det ikke binder direkte til androgen receptoren. Effekten kan muligvis forklares udfra den aromatase-inducerende effekt af simazin, der er påvist in vitro. En øget aromataseaktivitet vil resultere i en øget omsætning af testosteron til østradiol, hvilket kunne tænkes at sænke testosteronniveauet i dyrene og dermed indirekte forårsage den antiandrogene effekt. Men da der ikke kan påvises reduceret testosteronniveau i serum (Tabel 3.3.3) virker denne forklaring ikke umiddelbart plausibel. Vi må konstatere, at der på genniveau sker en række ændringer, som ikke er direkte relaterede til ændringer i organvægte eller hormonniveauer, og som vi ikke umiddelbart kan forklare. Figur 3.3.1. Effekt af de fem pesticider hver for sig og i en blanding på PBP C3, ODC og TRPM-2 mRNA i ventral prostata. Data er angivet som middel ±SD for n=6. Dyr i alle grupper har fået testosteronpropionat med undtagelse af kontrolgruppen. 'Testo': testosteronpropionat 0.5 mg/kg/dag s.c.; 'Flut': flutamid 20 mg/kg/dag s.c.; 'Delt': deltamethrin 2.5 mg/kg/dag oralt; 'Meth': methiocarb 2.5 mg/kg/dag oralt;'Pro': prochloraz 25 mg/kg/dag oralt; 'Sima': simazin 25 mg/kg/dag oralt;'Trib': tribenuronmethyl 25 mg/kg/dag oralt;'Kombi': prochloraz (25 mg/kg/dag) + simazin (25 mg/kg/dag) + deltamethrin (2.5 mg/kg/dag) + tribenuronmethyl (25 mg/kg/dag) + methiocarb (2.5 mg/kg/dag). 3.4 Effekt af kombinationer af 5 pesticider efter in utero eksponering af hanrotter3.4.1 Formål med studietFormålet med dette eksperiment var at undersøge, om en blanding af de 5 pesticider ville forårsage nogen føtotoksiske eller hormonforstyrrende effekter på rotteunger, der var blevet doseret in utero. Dosering af dyr under fostertilværelsen forventes, at ville forårsage de mest markante effekter pga. forøget følsomhed af dyrene i denne periode. 3.4.2 Design af studietUnge voksne hunrotter med en legemsvægt på ca. 200 g (Mol:WIST,SPF Møllegaard Breeding Center Ltd., Ejby, Danmark) blev parret indenfor 1 døgn og leveret på dag 3 af drægtigheden (GD3). Hunnerne blev tilfældigt fordelt parvis og blev opstaldet under standard betingelser og med kontrollerede miljøbetingelser. På ankomstdagen blev hunnerne vejet og fordelt i grupper med ligelig vægtfordeling. Indtil GD20 blev hunnerne opstaldet parvis og individuelt derefter. De blev observeret 2 gange dagligt for tegn på toxicitet. Legemsvægt blev registreret dagligt fra GD7 til postnatal dag (PND) 16. Fra GD21 blev dyrene inspiceret to gange dagligt og fødselstidspunkt registreret. Efter fødslen blev legemsvægt af mødre og unger registreret. Ungerne blev talt, kønsfordelt og checket for anomalier. Dagen for fødslen blev kaldt PND 0. I første del af forsøget blev 3 grupper af 8 mødre doseret oralt med jornøddeolie, 30 mg/kg/dag prochloraz eller en blanding af de 5 pesticider i alt 20 mg/kg/dag fra GD 7 til GD21 i et doseringsvolumen på 2 ml/kg legemsvægt. De 20 mg/kg/dag bestod af 15 mg/kg/dag prochloraz og hver 1.25 mg/kg af de følgende pesticider deltamethrin, methiocarb, simazin og tribenuron-methyl. På GD21 blev fostrene udtaget ved kejsersnit. Oprindelig var det planlagt at give dyrene 40 mg/kg/dag af blandingen, men efter 4 doseringer af halvdelen af mødrene viste der sig synlige toksiske effekter på mødrene og derefter blev dosis halveret til 20 mg/kg/dag. Under den efterfølgende databehandling blev der for alle parametre undersøgt om der var forskel på effekterne for 1. sæt der var startet på høj dosis og 2. sæt der havde fået den endelige dosis hele vejen igennem og der sås ingen forskelle, hvorefter alle data blev puljet og behandlet under et. I den anden del af studiet blev 3 grupper af 18 mødre doseret fra GD7 til PND 16 med de samme doser som i første del af studiet. På PND16 blev 1 han og 1 hun taget fra moderen og aflivet. Væv blev udtaget til hormonanalyser, genekspressionsanlyser og patologi. Èn han og én hun per kuld fortsatte i forsøget og der blev foretaget undersøgelse for kønsmodning, adfærd, hormonniveauer og sædkvalitet i de voksne hanner (PND220). 3.4.3 Undersøgelse af mødre og afkom for føtotoksiske og hormon-afhængige effekterSom det fremgår af tabel 3.4.1 sås der med kombinationen af pesticider en statistisk signifikant reduktion af mødrenes vægt efter fødslen og deres tilvækst i doseringsperioden. Vægtreduktionen sås også hos både det hanlige og hunlige afkom og varede ved til ungerne blev voksne (Tabel 3.4.2). Derudover sås ingen føtotoksiske effekter af kombinationen og der var ingen effekt på hverken anogenital afstand eller alder for kønsmodning. Mht. effekten på brystvorter i hanner var der ingen signifikant effekt på det gennemsnitlige antal brystvorter i kuldene efter pesticid-dosering, men derimod var procentdelen af kuld med 0 brystvorter markant reduceret (fra 32% til 4 %). I mødrene, der udelukkende var doseret med prochloraz, sås også en vægtreduktion fra GD7 til efter fødslen, mens vægten af mødrene efter fødslen og afkommet var upåvirket. Det viste sig, at prochloraz inducerede en forlængelse af drægtighedsperioden og gav markant flere brystvorter i hanner, mens anogenital afstand og alder for kønsmodning var upåvirkede. Table 3.4.1 Drægtigheds- og kulddata
# (no. implantations-live pups at day 6)/no. implantations * p < 5%; ** p < 1% compared to control group; Table 3.4.2. Legemsvægt efter fravænning og kønsmodning
* p < 5%; 3.4.4 Effekt på hormonniveauerVi observerede det interessante, at både kombinationen og prochloraz forårsagede et statistisk signifikant fald i både testikulær og plasma testosteron i GD21 hanner. Samtidig hermed var den testikulære progesteronkoncentration signifikant højere for begge grupper. Der var ingen signifikant effekt på plasma LH, men der sås en tendens til stigning. Generelt er det vanskeligt at opnå signifikans på hormonniveauer i plasma fra kejsersnitdyr, da det er nødvendigt at pujle blod fra alle dyr i kuldet og også nogle gange flere kuld for at få nok plasma til analyserne. Den markante effekt på testosteron- og progesteronniveauet var forsvundet i PND16 dyr. Tabel 3.4.3. Hormonniveauer i hanligt afkom GD21, PND 16 og PND 220
a) To pools per hold b) N= 16, 20 og 14 for de 3 hold c) N= 5, 4 og 4 (pools for 3-4 dyr) for de 3 hold d) N=16 for hvert af de 3 hold e) N= 9, 10, 9 for de 3 hold f) N= 18, 20, 14 for de 3 hold *) p< 0,05 3.4.5 Effekt på organerFor at vurdere om pesticiderne havde effekt på organer blev organerne vejet samt vurderet makroskopisk og mikroskopisk. Organvægte blev målt ved aflivning af PND16 han- og hunner samt på PND 220 hanner. På PND16 var legemsvægten signifikant reduceret i kombinationsholdet for både hanner og hunner (se tabel 3.4.4 og 3.4.5). Tillige var vægten af bulbourethralkirtlen signifikant reduceret hos både prochloraz- og kombinationsholdet (se tabel 3.4.4). Ændringen af vægten af bulbourethralkirtlen skyldes formentlig primært den antiandrogene effekt af prochloraz, da effekten ikke var større i kombinationsholdet. Hos voksne hanner (PND220) var der ikke længere nogen forskel mellem holdene (se tabel 3.4.6). Tabel 3.4.4 Legems-og organvægte for PND16 hanner
Data repræsenterer middel ± SD aKombinationsholdet blev doseret med en blanding af procloraz (15 mg/kg), simazin (1.25 mg/kg), deltamethrin (1.25 mg/kg), Tribenuronmethyl (1.25 mg/kg) and methiocarb (1.25 mg/kg) *Statistisk signifikant forskellig fra kontrolholdet (p<0.05) & Statistisk signifikant forskellig fra prochlorazholdet (p<0.05) §non-parametrisk test, data er ikke normalfordelt $Signifikant effekt af legemsvægt Tabel 3.4.5. Legems-, lever- og uterusvægt for PND16 hunner
aKombinationsholdet blev doseret med en blanding af procloraz (15 mg/kg), simazin (1.25 mg/kg), deltamethrin (1.25 mg/kg), tribenuronmethyl (1.25 mg/kg) and methiocarb (1.25 mg/kg) *Statistisk signifikant forskellig fra kontrolholdet (p<0.05) & Statistisk signifikant forskellig fra prochlorazholdet (p<0.05) Tabel 3.4.6. Legems- og organvægte for voksne hanner (PND 220)
Data repræsenterer middel ± SD fra 16 dyr per hold aKombinationsholdet blev doseret med en blanding af procloraz (15 mg/kg), simazin (1.25 mg/kg), deltamethrin (1.25 mg/kg), tribenuronmethyl (1.25 mg/kg) and methiocarb (1.25 mg/kg) ¤Store nyrer hos et dyr i kontrolholdet #En lille testikel med histologiske forandringer $Signifikant effekt af legemsvægt Makroskopisk og mikroskopisk vurdering af dyrene. Testiklerne blev undersøgt makroskopisk og mikroskopisk på GD21, PND16 og PND220 for alle tre hold. På GD 21 sås ingen makroskopiske forandringer i nogen af de 3 hold. Hverken PND16 eller PND 220 sås nogle generelle makroskopiske forandringer. En testikel (venstre eller højre) fra 1-4 hanner per kuld i 5-6 kuld per hold blev fixeret i Bouins fixativ. Et snit per testikel blev farvet med hæmatoxylin og eosin (HE) og undersøgt mikroskopisk. Hverken på GD21, PND 16 eller PND 220 var der nogen generelle dosis-relaterede forskelle mellem holdene. 3.4.6 Effekt på adfærd og sædkvalitetFor at undersøge om pesticiderne havde nogen vedvarende neurotoksisk effekt blev de voksne dyrs adfærd undersøgt. Der blev undersøgt for aktivitetsniveau, legeadfærd, hukommelse og indlæring i Morris Maze test og labyrinttest og endelig blev der lavet en 'Sweet preference test'. Alle disse tests er kendetegnede ved, at der er en signifikant forskel i adfærden hos de to køn. Både hunner og hanner blev undersøgt og der sås som ventet en statistisk signifikant kønsforskel i både labyrinttest, aktivitetstest og legeadfærdstesten. Det viste sig at prochloraz inducerede et signifikant forøget aktivitetsniveau og forøget indtag af sødestof i hanner, dvs. der sås tegn på feminisering af hannerne i to adfærdstests. Derudover sås ingen effekter på adfærden af de pesticid-eksponerede dyr. Det blev undersøgt hvorvidt in utero eksponering med prochloraz og kombinationen af de 5 pesticider havde effekt på sædkvaliteten i voksne hanner (PND 220). Der sås en tendens til fald i antallet af sædceller i både prochloraz og kombinationsgruppen sammenlignet med kontrolgruppen, men effekten var ikke statistisk signifikant (Fig 3.4.1). Der sås ingen effekt af stofferne på andelen af motile sædceller, sædcelle progressivitet samt hastighedsparametre mellem de tre grupper (Fig 3.4.2).
Figur 3.4.1. Effekt af in utero eksponering for prochloraz og kombinationen af de fem pesticider på sædkoncentrationen i voksne hanner (PND 220). Data er angivet som middel ± SEM for n=16.
Figur 3.4.2. Effekt af in utero eksponering for prochloraz og kombinationen af de fem pesticider på sædmotilitet i voksne hanner (PND 220). Data er angivet som middel ±SEM for n=16. 3.5 Konklusion på hormonforstyrrende effekter af 5 pesticiderMethiocarb og deltamethrin inducerede et østrogent respons målt ved øget MCF-7 celleproliferation mens tribenuron-methyl, prochloraz og simazin ikke havde nogen effekt. Kombinationen af en 1:1:1:1:1 ækvimolær blanding af de 5 pesticider gav ikke noget målbart østrogent respons og beregning af en isobolkoeficient på 7 for blandingen indikerer en antagonistisk effekt af stofferne i blandingen, sandsynligvis forårsaget af prochloraz, som også reagerer antiøstrogent, når det blev testet sammen med 17β-østradiol. Prochloraz, methiocarb og deltamethrin blokerede AR in vitro, men hverken tribenuron-methyl eller simazin havde nogen antiandrogen effekt. Kombinationen af en 1:1:1:1:1 ækvimolær blanding af de 5 pesticider gav et antiandrogent respons, der lå på linie med det predikterede respons under antagelse af additivitet. Resultaterne indikerer, at stofferne i kombination virker additivt i dette assay. In vivo Hershberger forsøget blev kompliceret af, at det ikke var muligt at undersøge pesticiderne ved samme dosis-niveau. Både deltamethrin og methiocarb inducerede neurotoksiske effekter (deltamethrindyrene fik krampe og måtte hurtigt aflives) og derfor måtte dosis af de to stoffer sænkes til 2.5 mg/kg/dag, mens prochloraz, simazin og tribenuron-methyl blev doseret med hver 25 mg/kg/dag. Kombinationsgruppen fik en dosis svarende til i alt 80 mg/kg (25+25+2.5+25+2.5 mg/kg). Mht. effekt på vægte af reproduktionsorganer sås ingen effekter af enkeltstofferne, hvorimod kombinationsgruppen viste signifikant reducerede vægte af m. levator ani/bulbocavernosus. Der var også tendens til fald i prostatavægte og sædblærevægte, men der var ingen statistisk signifikans. Generelt sås ingen effekt på de valgte hormonniveauer. Derimod var der markant effekt af alle pesticider doseret enkeltvis og i kombination på ekspressionen af ODC mRNA og PBP C3 mRNA, med undtagelse af deltamethrin, tribenuronmethyl og kombinationen, der ikke gav effekt på PBP C3 mRNA. Konklusionen er, at de 5 pesticider udviser tydelig additivitet in vitro ved binding til AR og at der generelt ikke ses de store effekter på reproduktionsorganvægte og hormonniveauer in vivo efter korttids-eksponering til de valgte dosisniveauer. Dog sås en akkumulerende effekt af kombinationen på vægte af m. levator ani/bulbocavernosus. Det var ikke overraskende, at deltamethrin og methiocarb, der viste antiandrogen effekt in vitro ikke gav nogen antiandrogen effekt på reproduktionsorganer, da de kun kunne testes ved en lav dosis på 2.5 mg/kg pga. anden toksicitet. Prochloraz har tidligere vist antiandrogen effekt in vivo ved 50 mg/kg, men vi kunne konstatere at det ikke havde denne effekt ved 25 mg/kg. Det var overraskende at mange af enkeltstofferne inducerede så markante effekter på ekspression af PBP C3 og ODC mRNA. Tilsyneladende er genekspressionen i disse forsøg en mere følsom parameter end organvægte og hormonniveauer. Betydningen af disse ændringer er uklar på nuværende tidspunkt, men kan indikere en begyndende antiandrogen effekt, som ikke giver sig udslag på organ- og hormonniveau. Undersøgelse af hormoninducerede effekter i afkommet efter in utero eksponering anses for at være den ultimative test for undersøgelse af hormonforstyrrende effekter. Kombinationen (20 mg/kg/dag bestående af 15 mg/kg prochloraz og 1.25 mg/kg af de 4 andre pesticider) og prochloraz i sig selv (30 mg/kg/dag) havde en reversibel effekt på mødrenes vægt under drægtigheden, men der sås ingen markante føtotoksiske effekter ved de valgte doser. Den oprindeligt valgte dosis af kombinationen (40 mg/kg/dag bestående af 30 mg/kg prochloraz og 2.5 mg/kg af de 4 andre pesticider) viste sig at være for høj, da der var synlige toksiske effekter på mødrene efter nogle få doser. Denne toksicitet må skyldes enten deltamethrin, methiocarb, simazin eller tribenuron-methyl i blandingen. Både prochloraz og kombinationen forårsagede et markant reduceret testosteronniveau og et forhøjet progesteronniveau i hanfostre ved GD21. Det reducerede testosteronniveau afspejler en antiandrogen effekt i lighed med den, der er observeret for flere phthalater. Effekten var forsvundet ved PND16. Men det er givetvis denne effekt, der giver sig udslag i, at begge behandlinger giver et øget antal brystvorter og dermed en feminisering af hannerne. Det øgede progesteronniveau i hanfostre hænger sandsynligvis sammen med den øgede længde af drægtigheden, som var signifikant forøget efter prochloraz behandling. Det er sandsynligt, at det er prochloraz i kombinationen (15 mg/kg) der forårsagede de antiandrogene effekter på testosteronniveau og brystvorteantal, da stoffet indgivet alene i en dosis på 30 mg/kg gav de samme effekter. Det kan dog ikke udelukkes, at et eller flere af de andre stoffer kan have bidraget til disse effekter. Prochloraz og kombinationen forårsagede en ændringen i vægten af bulbourethral kirtlen på PND 16. Dette skyldes formentlig primært den antiandrogene effekt af prochloraz, da effekten ikke var større i kombinationsholdet. Effekten var ikke længere tilstede hos de voksne dyr. Kombinationen eller prochloraz alene forårsagede ikke yderligere dosis-relaterede organ forandringer. Kombinationen gav ingen effekter på hverken adfærd eller sædkvalitet hos hannerne, hvorimod prochloraz i sig selv resulterede i en ændret adfærd hos hannerne i tests for aktivitetsniveau og sødestofpræference, og de fundne adfærdsændringer tyder på en feminisering af hannerne. Der sås ingen statistisk signifikant effekt af hverken prochloraz eller kombinationen på sædkvaliteten, men der var en tendens til forringet sædkvalitet i begge pesticid-grupper. Der var tydelige antiandrogene og dermed hormonforstyrrende effekter af prochloraz og i flere tilfælde sås de samme effekter i kombinationsgruppen. Dette tyder på, at det er prochloraz som er ansvarlig for de effekter, der er set for blandingen. Alt i alt viser resultaterne, at in utero forsøget som ventet var det mest sensitive system, hvor der sås både morfologiske, hormonelle og funktionelle ændringer efter pesticideksponering. 4 Samlet diskussion og konklusionSammenfattende tyder resultaterne fra denne rapport på, at hormonforstyrrende stoffer, der virker via samme virkningsmekanisme, virker additivt både i cellekulturforsøg og i dyreforsøg. Dette understøttes af den viden, man har fra litteraturen fra forsøg med andre cellekultursystemer. Det er bl.a. vist, at når man kombinerer en række enkeltstoffer ved koncentrationer, der ikke i sig selv har nogen effekt, så vil blandingen af stofferne give en effekt (Rajapakse et al. 2002). Dette er i overensstemmelse med hvad teorien omkring koncentrations-additionsprincippet prædikterer, som anvendelsen af isobolmetoden bygger på. Dette er første gang at kombinationseffekter for antiandrogene pesticider er undersøgt både in vitro og in vivo. Fungicidet prochloraz er påvist at være antiandrogent in vitro samt in vivo i voksne hanrotter (Vinggaard et al., 2001) og som nu påvist i denne undersøgelse også efter eksponering under drægtigheden (in utero eksponering). På Environmental Protection Agency i USA har man også testet in utero effekter af prochloraz og har fundet den samme effekt på føtale testosteron- og progesteronniveauer (Wilson et al. 2003). Prochloraz må derfor betragtes som muligt reproduktionstoksisk for mennesker. At de godkendte guide-line tests, der anvendes ved godkendelse af pesticider, ikke er tilstrækkelige til at afsløre hormonforstyrrende effekter ses f.eks. af at prochloraz ved sidste godkendelse i 1998 ikke blev fundet reproduktionstoksisk, ligesom der ikke nævnes noget om eventuelle hormonforstyrrende egenskaber. Der er således behov for, at de nuværende guidelines for testning af pesticider udbygges til også at omfatte undersøgelser af stoffernes hormonforstyrrende potentiale. In vivo undersøgelsen af de 5 pesticider, der bruges indenfor dansk gartneri og landbrug viste, at kombinationen af pesticiderne havde en markant effekt på kønshormonproduktion i hanfostre. Dette skyldes sandsynligvis tilstedeværelse af prochloraz i blandingen, da dette stof alene gav de samme effekter. En sådan antiandrogen effekt, der giver sig udslag i reduceret testosteronniveau i rottefostre, er også observeret for phthalaterne og menes at være den vigtigste mekanisme, der er involveret i de reproduktionsskadelige effekter af phthalaterne. Derfor er der grund til at undersøge eventuelle reproduktionsskadende effekter af dette fungicid mere indgående. Både methiocarb og deltamethrin har hormonforstyrrende effekter in vitro, men vi kan konstatere, at når det gælder toksicitet i rotter, er det andre toksiske effekter af disse pesticider, der dominerer over de hormonforstyrrende effekter. Bortset fra det vil man forvente, at pesticiderne vil kunne bidrage til den samlede humane eksponering for hormonforstyrrende stoffer via additive effekter, selv om man ikke for enkeltstofferne kan påvise effekter på hormonsystemet in vivo. Resultaterne i denne rapport og de få tidligere undersøgelser af kombinationseffekter in vitro af østrogene kemikalier tyder på, at hormonforstyrrende stoffer med samme virkningsmekanisme (f.eks. blokering af AR, aktivering af ER) virker additivt. Resultaterne fra rotteforsøgene i denne undersøgelse tyder på, at det samme gør sig gældende in vivo. Når man skal vurdere den humane risiko ved udsættelse for hormonforstyrrende stoffer er det således ikke tilstrækkeligt at se på udsættelsen for et enkelt hormonforstyrrende stof ad gangen. Endvidere vil selv meget lave eksponeringer for hormonforstyrrende stoffer kunne bidrage til det samlede respons, selvom effekten af det enkelte stof ligger under detektionsgrænsen. Dette er indtil videre dokumenteret in vitro for østrogene stoffer (Rajapakse et al., 2002, Silva et al., 2002). I stedet for vil det være langt mere relevant at se på den samlede belastning for stoffer med samme virkningsmekansme. Det vil imidlertid være meget vanskeligt at vurdere befolkningens og det enkelte individs samlede eksponering ud fra oplysninger om kost, levevaner, arbejdsforhold osv. Dertil kommer at alle hormonforstyrrende stoffer næppe er identificeret endnu. En langt bedre fremgangsmåde vil være at etablere pålidelige målemetoder til at vurdere eksponeringen. En lovende fremgangsmåde til at måle den samlede eksponering for østrogene kemikalier blev publiceret af Sonnenschein, Soto og deres medarbejdere i 1995 (Sonnenschein et al 1995). Metoden er siden blevet videreudviklet (Soto et al., 1997, Rivas et al., 2001, Nielsen et al., 1998). Princippet i metoden er, som beskrevet tidligere i rapporten, at naturligt producerede og farmaceutiske østrogener fjernes fra en opkoncentreret blodprøve som herefter testes i MCF-7 celleproliferationsassayet. For nylig er biomarkørmetoden blevet anvendt til at vurdere og sammenligne belastningen for østrogene stoffer i en gruppe af danske og færøske kvinder (Rasmussen et al., 2003). Et forhøjet østrogent respons var langt hyppigere blandt de færøske kvinder end blandt de danske kvinder, hvilket antages at hænge sammen med et højt indhold af østrogene stoffer ophobet i hvaler og fisk, som udgør en stor del af den færøske kost. Det var ikke muligt at identificere nogle specifikke kemiske stoffer i blodprøverne, som korrelerede direkte med det østrogene respons, hvilket sandsynlivis skyldes, at der måles på det samlede respons med bidrag fra både østrogene stoffer, østrogene metabolitter samt antiøstrogene stoffer. Ved at undersøge blodprøver fra rotter doseret direkte med østrogene stoffer i denne undersøgelse, ønskede vi at validere biomarkørmetoden ved at påvise en dosis-respons sammenhæng mellem pesticiddosis og det østrogene serumrespons. Dette blev klart demonstreret, selv om responset ved de højeste pesticiddoser er usikkert, fordi der ikke var så meget blod som ønskeligt til rådighed. I forbindelse med et projekt finansieret af Statens Sundhedsvidenskabelige Forskningsråd valideres metoden yderligere i rotteforsøg, hvor rotterne er eksponeret for andre østrogene eller antiøstrogene pesticider. Desuden er blodprøver fra ca. 400 kvinder som på blodprøvetagningstidspunktet arbejdede i fynske blomstergartnerier ved at blive analyseret på SDU, Odense. Resultaterne vil blive sammenholdt med en række andre målinger samt detaljerede oplysninger om kvindernes pesticideksponering i tiden op til prøvetagningen. De in vitro metoder der anvendes til testning for østrogene/antiøstrogene samt androgene/antiandrogene stoffer er typisk MCF-7 celleproliferationsassayet, ER og AR reportergen assays samt ER og AR bindingsassays. Mens bindingsassays kun detekterer stoffernes affinitet overfor receptorene og ikke kan skelne mellem agonister og antagonister, er de andre assays i højere grad i stand til at forudsige det funktionelle biologiske respons. En detaljeret diskussion af fordele og ulemper ved de forskellige in vitro assays ligger udenfor denne rapports formål (se eventuelt Andersen et al., 1999). Vi finder, at MCF-7 celle proliferatinsassayet samt reportergen assays baseret på mammale celler er de bedst egnede, og disse metoder har både i denne undersøgelse og i tidligere undersøgelser vist sig at være rimelig gode til at forudsige effekter in vivo (Vinggaard et al., 2002, Yamasaki et al., 2002) selv om metoderne naturligvis ikke kan tage højde for betydningen af absorption, fordeling, ekskretion og metabolisme i en hel organisme. Dette kan f.eks. resultere i at stoffer, som er meget potente in vitro, er mindre potente in vivo og omvendt afhængig af nedbrydningstid og om det overvejende er stoffet selv eller metabolitter, der er biologisk aktive. Et stof, som giver et signifikant respons in vitro, bør dog betragtes som muligt hormonforstyrrende indtil en eventuel in vivo effekt er afkræftet i pålidelige undersøgelser. Selv da kan det dog tænkes at spille en rolle og bidrage til en samlet sundhedsskadelig belastning. Hvad angår testning af blandinger af kemsike stoffer er der dog ingen tvivl om, at in vitro metoder må spille en afgørende rolle, da der kun i begrænset omfang vil være muligt at undersøge dette in vivo. Et af de spørgsmål, der ofte stilles i forbindelse med risikovurdering af stoffer er, hvorvidt genekspressionsanalyser kan anvendes i den sammenhæng eller ej. Som udgangspunkt mener vi, at genekspressionsændringer skal ses i sammenhæng med andre morfologiske, funktionelle eller biokemiske ændringer i organismen. I de tilfælde kan de være et værdifuldt supplement og sige noget om stoffets virkningsmekanisme. I andre tilfælde, hvor der udelukkende observeres genekspressionsændringer, kræves der et nøje kendskab til genets regulering, vævslokalisering og gerne dets funktion, men ofte mangler der pt. viden på det område. For at udbygge denne viden er det derfor fortsat vigtigt at inddrage genekspressionsanalyser i toksikologiske undersøgelser. Forskellige gener aktiveres og deaktiveres hele tiden afhængig af celle- eller vævstype, det cellulære stimulus og signalvej. For at etablere en specifik genekspression som en biomarkør for eksponering af væv eller celler, er det nødvendigt, at dosis-respons- og tidsstudier bliver udført, før det kan bruges i forbindelse med risikoidentifikation. For eksempel er østradiol, som er anvendt i vores dyrestudier, undersøgt for tids-afhængig effekt på ER og ER mRNA ekspression i et cellekulturstudie. Det viste sig, at østradiol bevirkede en nedregulering af ER og ER mRNA efter 48 timer, hvorimod der sås en stigning af ER efter 24 timer (Hofmeister & Bonefeld-Jørgensen, Toxicology In vitro 2004(in press). I vores forsøg tyder meget på, at analyser af ekspression af PBP C3 og TRPM-2 mRNA er anvendelige som markører for antiandrogen virkning i forsøgsdyr. Dog har vi observeret, at i nogle forsøg med visse stoffer synes de at være en tidlig og følsom markør, hvorimod i andre forsøg med andre stoffer har det vist sig at være en mindre følsom markør end f.eks. reproduktionsorganvægte. I de forsøg kigger vi udelukkende på genekspressionen på et enkelt tidspunkt i dyrets liv, og der kan være variationer i den tid der går fra sidste dosering til dyret aflives, selv om den parameter forsøges standardiseret. Hvorvidt disse forhold har afgørende betydning er pt. uklart og det er derfor nødvendigt med mere forskning på området for at kunne drage nogle endelige konklusioner. 5 PerspektiveringDen additive virkning af hormonforstyrrende pesticider med samme virkning demonstreret her og i andre undersøgelser understreger begrænsningerne i den traditionelle risikovurdering af kemikalier, hvor hvert enkelt kemikalie vurderes for sig og hvor der ikke tages højde for kombinationseffekter. En risikovurdering som ikke tager højde for mulige kombinationseffekter, vil kunne tænkes at underestimere den sundhedsmæssige risiko for mennesker. Indenfor dioxin- og PCB-området tager man i dag ved risikovurdering højde for, at vi typisk er eksponerede samtidigt for flere stoffer med dioxinlignende effekt. For hvert enkelt dioxinlignende stof, der er til stede i fødevaren eller f.eks. i modermælken, beregnes en toksisk equivalentfaktor (TEQ), hvor stoffets potens er beregnet relativt til den mest potente dioxin 2,3,7,8-TCDD, og det er den samlede TEQ for alle stoffer i fødevaren, der ligger til grund for den efterfølgende risikovurdering. Dette princip virker fornuftigt set i lyset af resultater, der indikerer at de dioxinlignende stoffer også virker additivt ved test i in vitro systemer. Det vil være vanskeligt at beregne TEQ'er for hormonforstyrrende stoffer, da man ikke indenfor dette område har nogle oplagte høj-potente referencekemikalier, som de andre stoffers potens kan beregnes relativt til. Der skal også tages højde for, at mennesker sandsynligvis også er eksponerede for kemikalier, der modvirker effekten af de hormonforstyrrende stoffer. F.eks. findes i kosten flere indholdsstoffer med antiøstrogen virkning, der kan tænkes at modvirke effekten af de østrogene stoffer. Derimod er der, så vidt vi ved, ingen væsentlig dokumentation for, at vi er eksponerede til kemikalier, der direkte modvirker de antiandrogene kemikaliers effekt. Det kan derfor være problematisk at finde en farbar vej til at finde principper for vurdering af potentielle kombinationseffekter af hormonforstyrrende stoffer, men behovet er der. Resultaterne fra denne rapport viser, at de in vitro testsystemer, der allerede findes, er meget anvendelige til undersøgelse af kombinationseffekter af hormonforstyrrende stoffer. Det er også muligt at anvende dyreforsøg til formålet, når blot man har nogle end-points, der kan måles med en rimelig grad af nøjagtighed, og for hvilke den biologiske variation ikke er for høj. Dette gælder specielt for reproduktionsorganvægte i de kortere varende dyreforsøg, men i noget mindre grad for hormonniveauer. Mht. genekspressionsanalyserne sås i Hershbergertesten en fin dosis-reponsafhængighed, mens der i uterustesten ikke sås denne dosis-afhængighed. Dette skyldes sandsynligvis, at effekterne på de undersøgte gener i uterus-testen var så markante, at maksimal effekt blev opnået allerede ved de laveste doser, hvilket indikerer at denne analyse er følsom og sandsynligvis vil give et pænt dosis-respons forløb ved lavere pesticiddoser end dem, der er testet i dette studie. Derfor kan det i visse undersøgelser, men ikke i andre, være nødvendigt at undersøge kombinationseffekter på organniveau ved visse dosisniveauer og kombinationseffekter på genniveau ved andre dosisniveauer. Generelt kan dog siges, at undersøgelsen af kombinationseffekter på forskellige niveauer af molekylær kompleksitet umiddelbart tydede på, at der ikke var hverken antagonistiske eller synergistiske effekter mellem pesticiderne. Det skal dog også siges, at der for mange gener pt. mangler viden om deres regulering og funktion, og at det på nuværende tidspunkt er vanskeligt at anvende genekspressionsparametre i risikovurderingen. Den nuværende godkendelsesprocedure for pesticider indeholder ikke specifikke tests for hormonforstyrrende egenskaber. Der er krav om testning for reproduktionstoksiske egenskaber af aktivstoffet i form af en teratogenicitetsundersøgelse i to arter (rotter og kaniner) samt en flergenerationstest over mindst to generationer i rotter. At disse test ikke er tilstrækkelige til at afsløre hormonforstyrrende effekter ses f.eks. af, at prochloraz ved sidste godkendelse i 1998 ikke blev fundet reproduktionstoksisk, ligesom der ikke nævnes noget om eventuelle hormonforstyrrende egenskaber. Der er således behov for, at de nuværende guidelines for testning af pesticider udbygges til også at omfatte undersøgelser af stoffernes hormonforstyrrende potentiale. Ved at inkludere relevante følsomme endpoints i flergenerationstesten kunne der opnås oplysninger om hormonforstyrrende egenskaber efter in utero eksponering. Desuden bør pesticiderne testes for hormonforstyrrende egneskaber in vitro og evt. andre kortidstest. Guidelines for korttidstest og langtidstest for hormonforstyrrende effekter er under udvikling internationalt (se f.eks. O'Conor et al., 2002 og Owens et al., 2002). Det er for nylig vist at en større andel af de pesticider, som anvendes i dag, har hormonforstyrrende egenskaber in vitro, idet 16 ud af 23 pesticder, udvalgt på baggrund af anvendelseshyppighed, virkede østrogene, antiøstrogene, antiandrogene eller som aromatasehæmmere. Seks af pesticiderne var enddog virksomme via mere end én mekanisme (Andersen et al., 2002). Selvom potensen af disse pesticider var lav sammenlignet med de naturlige hormoner og mere potente miljøkemikalier, vil udsættelsen for mange pesticider samt andre kemikalier med samme virkningsmekansime samtidtigt øge den humane sundhedsrisiko, når den additive effekt tages i betragtning. Andre undersøgelser tyder på, at gartneriansatte har en større risiko for at føde sønner med kryptorkisme (Weidner et al., 1998), og det er for nylig publiceret, at der muligvis kan være en sammenhæng mellem pesticideksponering og forringet sædkvalitet (Swan et al. 2003). Med hensyn til sammenhæng mellem pesticideksponering af gartnere og fekunditet, som er den tid der går fra et par planlægger en graviditet til den rent faktisk opnåes, er der divergerende resultater, idet man i ét studie har fundet en sammenhæng (Abell et al. 2000), men i et andet ikke fundet nogen sammenhæng (Thonneau et al. 1999). Det vil sige, at der er enkelte, spredte indikationer på, at der kan observeres sundhedsskadelige effekter af pesticider. Mange unge kvinder i den fertile alder arbejder indenfor gartneribranchen både i Danmark og i andre lande. Desuden udsættes befolkningen, inklusive sårbare grupper som gravide kvinder og børn, for flere pesticider igennem kosten. Selvom eksponeringen for de enkelte pesticider er lav, kan det ikke udelukkes, at den samlede eksponering kan nå et kritisk niveau, når den additive virkning tages i betragtning. Det er derfor vigtigt, at pesticider med hormonforstyrrende egenskaber identificeres i forbindelse med godkendelsesproceduren og ikke som nu i forbindelse med tilfældige forskningsprojekter. Alt i alt er der behov for fremover at undersøge kombinationseffekter af hormonforstyrrende stoffer specielt hvad angår effekter af stoffer med forskellig virkningsmekanisme. Derudover er der behov for mere detaljerede undersøgelser af kombinationseffekter i det hele taget efter in utero eksponering af forsøgsdyr og belysning af om de samme mekanismer for interaktion mellem stoffer gør sig gældende i sådanne forsøgsdyrmodeller. 6 ReferencerAbell A., Juul S., Bonde J.P. (2000). Time to pregnancy among female greenhouse workers. Scan. J.Work Environ. Health 26(2), 131-6. Ahmed, S.A. (2000). The immune system as a potential target for environmental estrogens (endocrine disrupters): a new emerging field. Toxicology, 150(1-3): 191-206. Andersen H.R., Andersson A.-M., Arnold S.F., Autrup H., Barfoed M.,
Beresford N.-A., Bjerregaard P., Christiansen L.B., Gissel B., Hummel R.,
Jorgensen E.B., Korsgaard B., Le Guevel R., Leffers H., McLachlan J.,
Moller A., Nielsen J.B., Olea N., Oles Karasko A., Pakdel F., Pedersen K.L,.
Perez P., Skakkebaek N.E., Sonnenschein C., Soto A.M., Sumpter J.P.,
Thorpe S.M., and Grandjean P. (1999) Comparison of short-term estrogenicity tests for identification of hormone-disrupting chemicals. Health Perspect.
Suppl., 107:1, 89-108. Andersen H.R., Vinggaard A.M., Rasmussen T.H., Gjermandsen I.M., and Bonefeld-Jørgensen E.C. (2002). Effects of currently used pesticides in assays for estrogenicity, androgenicity and aromatase activity in vitro. Toxicol. Appl. Pharmacol 179, 1-12. Altenburger R., Bödeker W., Faust M., and Grimme L.H. In: Corn,M. Editor. Handbook of hazardous materials. Academic Press, 1993,15-27. Arnold S.F. and McLachlan J.A. (1996) Synergistic signals in the environment. Environ.Health Perspect. 104 (10) 1020-1023. Arnold S.F., Klotz D.M., Collins B.M., Vonier P.M., Guilette L.J.Jr. and McLachlan J.A. (1996) Synergistic activation of estrogen receptor with combinations of environmental chemicals. Science 272 (5267),1489-1492. Arnold S.F., Vonier P.M., Colllins B.M., Klotz D.M., Guillette L.J.Jr., and McLachlan J.A. (1997) In vitro synergistic interaction of alligator and human estrogen receptors with combinations of environmental chemicals. Environ.Health Perspect. 105 Suppl.3, 615-618. Bergeron J.M., Crews D., McLachlan J.A. (1994) PCBs as environmental estrogens: turtle sex determination as a biomarker of environmental contamination. Environ. Health Perspect. 102, 780-781. Bichel report, 1999. Rapport fra Underudvalget for Miljø og Sundhed. Brody, J.G. and Rudel, R.A. (2003). Environmental pollutants and breast cancer. Environ Health Perspect, 111(8): 1007-19. Cappelletti, V., Saturno, G., Miodini, P., Korner, W. and Daidone, M.G. (2003). Selective modulation of ER-beta by estradiol and xenoestrogens in human breast cancer cell lines. Cell Mol Life Sci, 60(3): 567-76. Clayton S.J., May F.E., and Westley B.R. (1997). Insulin-like growth factors control the regulation of oestrogen and progesterone receptor expression by oestrogens. Mol. Cell. Endocrinol. 128, 57-68. Couse, J.F., Lindzey, J., Grandien, K., Gustafsson, J.A., and Korach, K.S. (1997). Tissue distribution and quantitative analysis of estrogen receptor-alpha (ERalpha) and estrogen receptor-beta (ERbeta) messenger ribonucleic acid in the wild-type and ERalpha-knockout mouse. Endocrinology, 138(11): 4613-21. Crisp T.M., Clegg E.D., Cooper R.L., Wood W.P., Anderson D.G., Baetcke K.P., Hoffmann J.L., Morrow M.S., Rodier D.J., Schaeffer J.E., Touart L.W., Zeeman M.G., and Patel Y.M. (1998). Environmental endocrine disruption: an effects assessment and analysis. . 106 Suppl 1, 11-56. Cummings A.M. (1997). Methoxychlor as a model for environmental estrogens. Crit.Rev.Toxicol. 27(4), 367-379. Diel, P., Olff, S., Schmidt, S. and Michna, H. (2002). Effects of the environmental estrogens bisphenol A, o,p'-DDT, p-tert-octylphenol and coumestrol on apoptosis induction, cell proliferation and the expression of estrogen sensitive molecular parameters in the human breast cancer cell line MCF-7. J.Steroid Biochem.Mol. Biol. 80(1): 61-70. Donaghoue C., Westley B.R. and May F.E.B.(1999). Selective promotor usage of the human estrogen receptor- gene and its regulation by estrogen. Mol.Endocrinol.13 (11), 1934-1950. Ellman G.L., Courtney K.D., Andres V., and Featherstone R.M. (1961). A new and rapid colorimetric determination of acetylcholinesterase activity. Biochem.Pharmacol. 7, 88-95. Enmark, E. and Gustafsson, J.A. (1999). Oestrogen receptors - an overview. J. Intern.Med. 246(2), 133-8. Enmark, E., Pelto-Huikko, M., Grandien, K., Lagercrantz, S., Lagercrantz, J., Fried, G., Nordenskjold, M. and Gustafsson, J.A. (1997). Human estrogen receptor beta-gene structure, chromosomal localization, and expression pattern. J.Clin. Endocrinol.Metab. 82(12), 4258-65. Fødevarerapport (2003). Combined actions and interactions of chemicals in mixtures. The toxicological effects of exposure to mixtures of industrial and environmental chemicals. Danish Food and Veterinary Administration, ID:200312. Gaido, K. W., Leonard, L. S., Maness, S. C., Hall, J. M., McDonnell, D. P., Saville, B., and Safe, S. (1999). Differential interaction of the methoxychlor metabolite 2,2-bis- (p-hydroxyphenyl)-1,1,1-trichloroethane with estrogen receptors alpha and beta. Endocrinology 140, 5746-5753. Gaido, K.W., Maness, S.C. and Waters, K.M. (1999). Exploring the Biology and Toxicology of Estrogen Receptor beta. CIIT Activities, 19(11): 1-5. Gaido K.W., McDonnel D.P., Korach K.S. and Safe S. (1997). Estrogenic activity of chemical mixtures: Is there synergism? CIIT Activities 17, 1-7. Gray, L.E., Jr., Ostby, J., Cooper, R.L. and Kelce, W.R. (1999). The estrogenic and antiandrogenic pesticide methoxychlor alters the reproductive tract and behavior without affecting pituitary size or LH and prolactin secretion in male rats. Toxicol Ind Health, 15(1-2): 37-47. Gray L.E. Jr., Wolf C., Lambright C., Mann P., Price M., Cooper R.L., Ostby J. (1999). Administration of potentially antiandrogenic pesticides (procymidone, linuron, iprodione, chlozolinate, p,p'-DDE, and ketokonazole) and toxic substances (dibutyl- and diethylhexyl phthalate, PCB 169, and ethane dimethane sulphonate) during sexual differentiation produces diverse profiles of reproductive malformations in the male rat. Toxicol.Ind.Health 15(1-2), 94-118. Grimme L.H., Faust M., Boedeker W., and Altenburger R. (1996). Aquatic toxicity of chemical substances in combination: still a matter of controversy. Human Ecol.Risk Assess. 2, 426-433. Grünfeld H.T. and Bonefeld-Jorgensen E.C. (2003). Effect of in vitro estrogenic pesticides on human estrogen receptor and mRNA levels. Submitted. Haavisto A.-M., Pettersson K., Bergendahl M., Perheentupa A., Roser J.F. and Huhtaniemi I. (1993). A supersensitive immunofluorometric assay for rat luteinizing hormone. Endocrinology 132, 1687-1691. Hofmeister M.V. and Bonefeld-Jørgensen E.C. (2003). Effects of the pesticides prochloraz and methiocarb on human estrogen receptor and β mRNA levels analyzed by on-line RT-PCR analyses. In vitro Toxicology (in press). Hossaini A., Dalgaard M., Nelleman C., Vinggaard A.M. and Larsen J.-J. Assesment of Androgenic and Anti-Androgenic Activity in Mature Castrated rats. Abstract at: Hormones and Endocrine Disrupters in Food and Water: Possible impact on human health. Rigshospitalet, 27-30 May 2000. Hossaini A., Larsen J.-J., and Larsen J.C. (2000). Lack of oestrogenic effects of food preservatives (parabens) in uterotrophic assays. Food Chem.Toxicol. 38, 319-323. Jørgensen E.C.B., Autrup H., and Hansen J.C. (1997). Effect of toxaphene on estrogen receptor function in human breast cancer cells. Carcinogenesis 18, 1651-1654. Kelce W. R., Lambright C. R., Gray L. E. Jr., and Roberts K. P. (1997). Vinclozolin and p,p'-DDE alter androgen-dependent gene expression: in vivo confirmation of an androgen receptor-mediated mechanism. Toxicol.Appl. Pharmacol. 142, 192-200. Kelce W.R. and Wilson E.M. (1997). Environmental antiandrogens: developmental effects, molecular mechanisms, and clinical implications. J.Mol.Med. 75 (3), 198-207. Kortenkamp A. and Altenburger R. (1998). Synergisms with mixtures of xenoestrogens: A reevalution using the method of isoboles. Sci.Total Environ. 221, 59-73. Kortenkamp A. and Altenburger R. (1999). Approaches to assessing combination effects of oestrogenic environmental pollutants. Sci.Total Environ. 233, 131-140. Krüger T., Sigsgaard T., and Bonefeld-Jørgensen E.C. (2003). Cytokine release and mRNA activation after incubation in the whole blood assay with moulds from water damaged schools in a panel of 10 atopics and 10 non-atopics. Cytokine 25(2), 77-84. Lam H.R., Löf A. and Ladefoged O. (1992). Brain concentration of white spirit components and neurotransmitters following three week of inhalation exposure of rats. Pharma.col.Toxicol. 70, 394-396. LeBlanc G.A., Bain L.J., and Wilson V.S. (1997). Pesticides: multiple mechanisms of demasculinization. Mol.Cell.Endocrinol. 126, 1-5. Levin, E.R. (2002). Cellular functions of plasma membrane estrogen receptors. Steroids, 67(6): 471-5. McLachlan J.A. (1997). Synergistic effect of environmental estrogens: report withdrawn. 277(5325), 462-3. Moguilevsky J.A. and Wuttke W. (2001). Changes in the control of gonadotrophin secretion by neurotransmitters during sexual development in rats. Exp.Clin.Endocrinol. Diabetes 109(4), 188-95. Nellemann C., Vinggaard A.M., Dalgaard M., Hossaini A. and Larsen J.-J. (2000). Quantification of anti-androgen action by Lightcycler technology. Toxicology 163, 29-38. Nellemann C., Dalgaard M., Lam H.R. and Vinggaard A.M. (2003). The combined effects of vinclozolin and procymidone do not deviate from expected additivity in vitro and in vivo. Toxicol.Sci. 71, 251-262. Nielsen, J. B., Nielsen, F., Andersen, H. R., and Grandjean, P. (1998). A possible biomarker of exposure to xeno estrogens. Epidemiology 9 (4 (suppl)), 54. (Abstract) Nilsson, S., Makela, S., Treuter, E., Tujague, M., Thomsen, J., Andersson, G., Enmark, E., Pettersson, K., Warner, M. and Gustafsson, J.A. (2001). Mechanisms of estrogen action. Physiol Rev, 81(4), 1535-65. O'Connor, J. C., Cook, J. C., Marty, M. S., Davis, L. G., Kaplan, A. M., and Carney, E. W. (2002). Evaluation of Tier I screening approaches for detecting endocrine-active compounds (EACs). Crit Rev.Toxicol. 32, 521-549. Ottoboni A., Bissell G.D., and Hexter A. (1977). Effects on DDT on reproduction in multiple generations of beagle dogs. Arch.Environ.Contam.Toxicol. 6, 83. Owens, J. W. and Ashby, J. (2002). Critical review and evaluation of the uterotrophic bioassay for the identification of possible estrogen agonists and antagonists: in support of the validation of the OECD uterotrophic protocols for the laboratory rodent. Organisation for Economic Co-operation and Development. Crit Rev.Toxicol. 32, 445-520. Payne J., Rajapakse N., Wilkins M., and Kortenkamp A. (2000). Prediction and assessment of the effects of mixtures of four xenoestrogens. Environ. Health Perspect. 108, 983-987. Payne J., Scholze M., and Kortenkamp A. (2001). Mixtures of four organochlorines enhance human breast cancer cell proliferation. Environ. Health Perspect. 109, 391-397. Pettersson, K., Delaunay, F. and Gustafsson, J.A. (2000). Estrogen receptor beta acts as a dominant regulator of estrogen signaling. Oncogene, 19(43), 4970-8. Pettersson, K. and Gustafsson, J.A. (2001). Role of estrogen receptor beta in estrogen action. Annu Rev Physiol, 63, 165-92. Rajapakse N., Ong D., and Kortenkamp A. (2001). Defining the impact of weakly estrogenic chemicals on the action of steroidal estrogens. Toxicol.Sci. 60, 296-304. Rajapakse N., Silva E., and Kortenkamp A. (2002). Combining xenoestrogens at levels below individual no-observed-effect concentrations dramatically enhances steroid hormone action. Environ.Health Perspect. 110, 917-921. Ramamoorthy K., Wang F., Chen I.C., Norris J.D., McDonnell D.P., Leonard L.S., Gaido K.W., Bocchinfuso W.P., Korach K.S., and Safe S.(1997). Estrogenic activity of a dieldrin/toxaphene mixture in the mouse uterus, MCF7 human breast cancer cells, and yeast-based estrogen receptor assays: no apparent synergism. Endocrinology 138(4),1520-1527 and Comment in Science (1997) 275,405. Rasmussen, T. H., Nielsen, F., Andersen, H. R., Nielsen, J. B., Weihe, P., and Grandjean, P. (2003). Assessment of xenoestrogenic exposure by a biomarker approach: application of the E-Screen bioassay to determine estrogenic response of serum extracts. Environ.Health 2, 12. Rivas, A., Fernandez, M. F., Cerrillo, I., Ibarluzea, J., Olea-Serrano, M. F., Pedraza, V., and Olea, N. (2001). Human exposure to endocrine disrupters: standardisation of a marker of estrogenic exposure in adipose tissue. APMIS 109, 185-197. Sanderson J.T., Heneweer M., Seinen W., Giesy J.P., Van den Berg M. (1999). Chloro-s-triazine herbicides and certain metabolites induce aromatase (CYP19) activity in H295R human adrenocortical carcinoma cells: a novel mechanism for estrogenicity? Toxicol Sci 54, 121-127. Scippo, M.L., Argiris, C., Van De Weerdt, C., Muller, M., Willemsen, P., Martial, J. and Maghuin-Rogister, G. (2003). Recombinant human estrogen, androgen and progesterone receptors for detection of potential endocrine disruptors. Anal Bioanal Chem, 25: 25. Sharpe, R.M. and Skakkebaek, N.F. (1993). Are oestrogens involved in falling sperm counts and disorders of the male reproductive tract. Lancet 341,1392-1395. Silva E., Rajapakse N., and Kortenkamp A. (2002). Something from "nothing"--eight weak estrogenic chemicals combined at concentrations below NOECs produce significant mixture effects. Environ.Sci.Technol. 36, 1751-1756. Sonnenschein, C., Soto, A. M., Fernandez, M. F., Olea, N., Olea Serrano, M. F., and Ruiz Lopez, M. D. (1995). Development of a marker of estrogenic exposure in human serum. Clin.Chem. 41, 1888-1895. Soto A.M., Chung K.L. and Sonnenschein C. (1994). The pesticides endosulfan, toxaphene, and dieldrin have estrogenic effects on human estrogen-sensitive cells. Environ.Health Perspect. 102, 380-383. Soto A.M., Sonnenschein C., Chung K.L., Fernandez M.F., Olea N., and Serrano F.O. (1995). The E-Screen assay as a tool to identify estrogens: An update on estrogenic environmental pollutants. Environ.Health Perspect. 103(7), 113-122. Soto A.M., Fernandez M.F., Luizzi M.F., Karasko A.S.O., and Sonnenschein C. (1997). Developing a marker of exposure to xenoestrogen mixtures in human serum. Environ. Health Perspect. 105 Suppl.3, 647-654. Sumpter J.P. and Jobling S. (1995). Vitellogenesis as a biomarker for estrogenic contamination of the aquatic environment. Environ.Health Perspect. 103 Suppl.7,173-178. Swan S. H., Brazil C., Kruse R. L., Liu F., Barr D.B., Drobnis E. Z., Redmon J. B., Wang C., Brazil C., Overstreet J. W., and The Study For Future Families Research Group (2003). Semen quality in relation to biomarkers of pesticide exposure. Environ. Health Perspect. 111(12), 1478-1484. Thonneau P., Abell A., Larsen S.B., Bonde J.P., Joffe M., Clavert A., Ducot B., Multigner L. and Danscher G.(1999). Effects of pesticide exposure on time to pregnancy: results of a multicenter study in France and Denmark. ASCLEPIOS Study Group. Am.J. Epidemiol. 150(2), 157-63. Toppari J., Larsen J.C., Christiansen P., Giwercman A., Grandjean P., Guillette L. J. Jr., Jegou B., Jensen T. K., Jouannet P., Keiding N., Leffers H., McLachlan J.A., Meyer O., Muller J., Rajpert De Meyts E., Scheike T., Sharpe R., Sumpter J., Skakkebaek N. (1996). Male Reproductive Health and Environmental Xenoestrogens. Environ.Health Perspect. 104 (Suppl 4) 741-803. Ulrich, E. M., Caperell-Grant, A., Jung, S. H., Hites, R. A., and Bigsby, R. M. (2000). Environmentally relevant xenoestrogen tissue concentrations correlated to biological responses in mice. Environ.Health Perspect. 108, 973-977. Vienonen A., Miettinen S., Manninen T., Altucci L.,Wilhelm E., and Ylikomi T. (2003). Regulation of nuclear receptor and cofactor expression in breast cancer cell lines. Eur.J.Endocrinol. 148, 469-79. Vinggaard A.M., Breinholt V. and Larsen J.C. (1999). Screening of selected pesticides for estrogen receptor activation in vitro. Food Add. Contam. 16 (12), 533-542. Vinggaard A.M., Hnida C., Breinholt V. and Larsen J.C. (2000). Screening of selected pesticides for inhibition of CYP19 aromatase activity in vitro. Toxicology in vitro 14(3), 227-234. Vinggaard A.M., Joergensen E.C.B. and Larsen J.C. (1999). Rapid and sensitive reporter gene assays for the detection of antiandrogenic and estrogenic effects of environmental chemicals. Toxicol.Appl.Pharmacol. 155, 150-160. Vinggaard A.M., Nellemann C., Dalgaard M., Joergensen E.C.B., Andersen H.R. (2002). Antiandrogenic effects in vitro and in vivo of the fungicide prochloraz. Toxicol.Sci. 69, 344-353. Wade M.G., Desaulniers D., Leingartner K., and Foster W.G.(1997). Interactions between endosulfan and dieldrin on estrogen-mediated processes in vitro and in vivo.Reprod.Toxicol. 11(6), 791-798. Weidner I.S., Møller H., Jensen T.K., and Skakkebæk N.E. (1998). Cryptochidism and hypospadias in sons of gardeners and farmers. Environ.Health.Perspect. 106 (12), 793-796. Welch, R.M., Levin, W. and Conney, A.H. (1969). Estrogenic action of DDT and its analogs. Toxicol.Appl.Pharmacol. 14(2): 358-67. Wilson V.S., Lambright C., Furr J., Ostby J., Wood C., Held G., Gray L.E. (2004). Phthalate ester-induced gubernacular lesions are associated with reduced insl3 gene expression in the fetal rat testis. 146(3), 207-15. Yamasaki, K., Takeyoshi, M., Yakabe, Y., Sawaki, M., Imatanaka, N., and Takatsuki, M. (2002). Comparison of reporter gene assay and immature rat uterotrophic assay of twenty-three chemicals. Toxicology 170, 21-30. You L., Sar M., Bartolucci E., Ploch S., and Whitt M. (2001). Induction of hepatic aromatase by p,p'-DDE in adult male rats. Mol. Cell. Endocrinol. 178, 207-214.
|