|
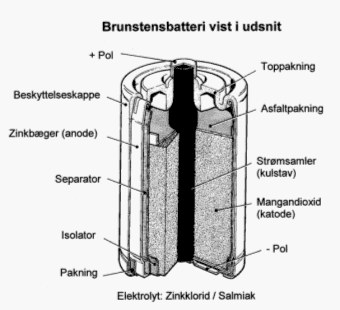
Behandlingsteknologier for batterier - Fase 1 2 De forskellige batterityperFælles for alle batterityper er, at de er opbygget af én eller flere elektrokemiske celler, der indeholder aktive materialer, hvis kemiske energi omdannes til elektrisk energi ved hjælp af en redoxreaktion. Ved afladning bevæger positive ioner sig fra én elektrode til en anden inden i batteriet, og for at udligne spændingsforskellen løber elektroner samtidigt fra den ene elektrode til den anden i en ekstern strømkreds. De to elektroder er henholdsvis anoden (-), der bliver oxideret, og katoden (+), der bliver reduceret. Mediet der leder ionerne inden i batteriet kaldes elektrolytten. Batterier opdeles som regel i to overordnede typer: Primærbatterier (engangsbatterier) og sekundærbatterier (genopladelige batterier). 2.1 Primære batterierI primærbatterier - eller engangsbatterier - er den kemiske energi indbygget i cellen én gang for alle, og cellereaktionen kan kun forløbe i én retning. De mest almindelige primære batterier er alkaliske og brunstensbatterier eller husholdningsbatterier, som disse typer også kaldes. Derudover er de mest anvendte lithiumbatterier og knapcellebatterier. 2.1.1 BrunstensbatterierHylstret, der også fungerer som anode, består af zink (se figur 2.1). Katoden består af en blanding af MnO2 (brunsten), carbon samt en binder, der holder sammen på blandingen. Elektrolytten er en vandig opløsning af enten ZnCl2 eller NH4Cl. Centralt er placeret en kulstav, der fungerer som strømsamler. Derudover vil der være et lille indhold af andre metaller, plastik, pap og urenheder. Tidligere indeholdt brunstensbatterier op til 100 ppm kviksølv, men i dag er det højst tilladte indhold 5 ppm (se afsnit 3.1.3). Figur 2.2 viser fordelingen af indholdsstoffer. Indholdet kan dog variere noget for forskellige mærker, og efter hvornår batterierne er produceret. Den angivne fordeling skal derfor tages som udtryk for et omtrentligt gennemsnit. Det ses at de væsentligste indholdsstoffer er mangandioxid, zink og jern. Brunstensbatterier anvendes i lomme- og cykellygter, radioer, legetøj m.v.
Figur 2.1. Skematisk opbygning af brunstensbatteri /1/
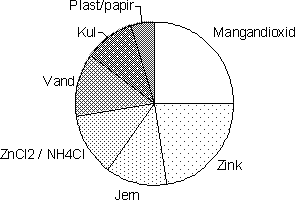
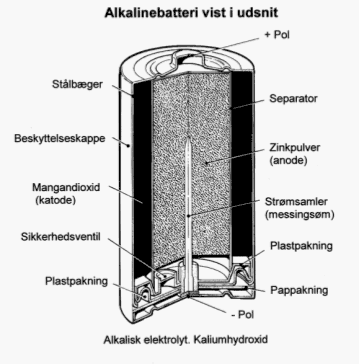
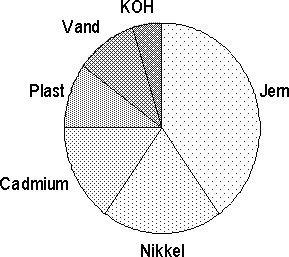
Figur 2.2. Brunstensbatteri. Gennemsnitlig fordeling af væsentlige indholdsstoffer /2/, /3/, /4/, /5/. 2.1.2 Alkaliske batterierHylstret består af stål og fungerer ikke som anode, og alkaliske batterier er i forhold til brunstensbatterier opbygget omvendt (se figur 2.3). Katoden består af et rør af sammenpresset MnO2, mens anoden er placeret i midten, og er en blanding af zinkpulver og elektrolyt, der oftest er vandig KOH. Katoden består af zinkpulver og en messingstav (kobber-zink legering), der fungerer som strømsamler. Derudover er der som ved brunstensbatterier også indhold af andre metaller, plastik, pap og urenheder. Alkaliske batterier var tidligere tilsat op til 10.000 ppm kviksølv, men må i dag ligesom brunstensbatterierne ikke indeholde over 5 ppm. Alkaliske batterier er kendetegnet ved en høj energitæthed og giver en lang driftstid ved kontinuerlig anvendelse i strømkrævende udstyr. Sammenlignet med brunstensbatterier har det også bedre lavtemperaturegenskaber. Figur 2.4 viser fordelingen af indholdsstoffer i alkaliske batterier. Indholdet kan dog variere noget for forskellige mærker og efter hvornår batterierne er produceret. Den angivne fordeling skal derfor tages som udtryk for et omtrentligt gennemsnit. Det ses, som ved brunstensbatterier, at de væsentligste indholdsstoffer er mangandioxid, zink og jern. De alkaliske batterier anvendes samme steder som brunstensbatterierne, men især i strømkrævende udstyr som f.eks. bærbare båndoptagere og cd-afspillere, kameraer m.v.
Figur 2.3. Alkalisk batteri /1/
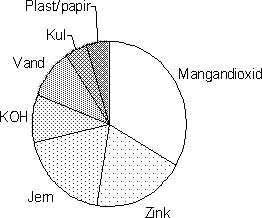
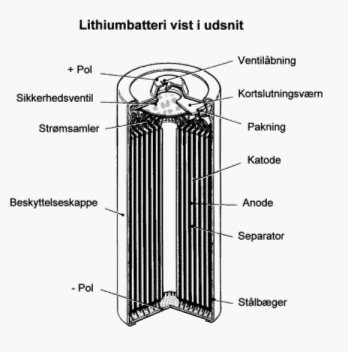
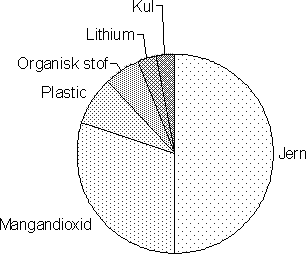
Figur 2.4. Alkalisk batteri. Gennemsnitlig fordeling af væsentligste indholdsstoffer /2/, /3/, /4/, /5/, /6/, /7/ 2.1.3 LithiumbatterierI primære lithiumbatterier består anoden af lithium mens katoden kan bestå af uopløselige, faste forbindelser (f.eks. MnO2, FeS2 eller polycarbonfluorider), opløselige forbindelser (SO2) eller flydende forbindelser (f.eks. SOCl2). Elektrolytten er som regel lithiumsalte opløst i organiske opløsningsmidler. Batterierne fremstilles både som knapceller og som cylindriske celler (se figur 2.5). I figur 2.6 er angivet et eksempel på indholdet af stoffer i et lithiumbatteri med MnO2 som katode. Bemærk at de væsentligste indholdsstoffer er jern og MnO2, mens lithium kun udgør en mindre del. Lithiumbatterierne er kendetegnet ved en høj energitæthed, og anvendes fortrinsvis i fotoudstyr, lommeregnere og lignende produkter med forholdsvis stort strømforbrug.
Figur 2.5. Cylindrisk lithiumbatteri /1/.
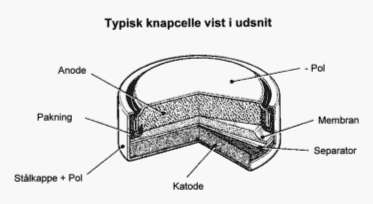
Figur 2.6. Lithiumbatteri. Eksempel på fordeling af indholdsstoffer i lithium-MnO2 type /2/ 2.1.4 KnapcellerPå grund af den store udvikling på markedet for miniature-elektronik, har knapcellebatterier fået en øget anvendelse. Knapcellerne er kendetegnet ved at være små, flade batterier på størrelse med knapper. Knapcellerne findes i følgende kemiske systemer: - kviksølvoxid. Den negative elektrode består af sintret zinkpulver og den positive elektrode af presset kviksølvoxid. Elektrolytten er kaliumhydroxid. Spændingen er meget konstant under afladningen. Anvendes i fotografiapparater, pacemakere, høreapparater m.v. - sølvoxid. Ligner kviksølvoxid cellen, men kviksølvoxid er erstattet af sølvoxiderne AgO eller AgO2. Indeholder desuden op til 2% kviksølv. Er på grund af sølvindholdet forholdsvis dyre at fremstille. Anvendes i armbåndsure, høreapparater m.v. - zink-luft. Den negative elektrode består af sintret zinkpulver. Elektrolytten er kaliumhydroxid, mens den positive elektrode består af aktivt kul, der optager og udnytter luftens ilt til oxidationsprocessen. Anvendes meget i høreapparater. Derudover findes der også alkaliske og lithium baserede knapceller.
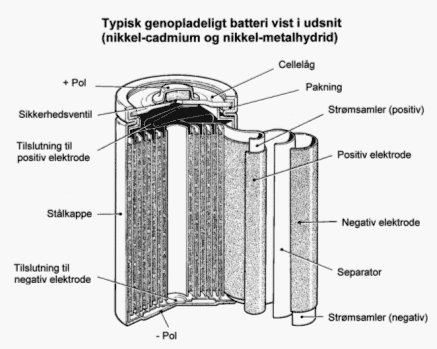
Figur 2.7. Opbygning af typisk knapcelle /1/ 2.2 Sekundære batterierI sekundære eller genopladelige batterier kan celleraktionen forløbe i begge retninger, hvorfor disse batterier kan tilføres energi fra en ekstern strømkilde således at de genoplades. De mest anvendte systemer er blybatterier, nikkel-cadmium batterier, nikkel-metalhydrid batterier og lithiumbatterier. 2.2.1 Blybatterier/blyakkumulatorerBlybatteriet eller blyakkumulatorer findes i mange versioner lige fra de velkendte startbatterier i biler, over traktionsbatterier i elektriske køretøjer til meget store stationære batterier i nødstrømsanlæg på adskillige tusinde amperetimer. I det opladede blybatteri udgør rent bly den negative elektrode og blyoverilte den positive. Under afladning omdannes begge elektroder til blysulfat. Elektrolytten, der er svovlsyre, indgår i den kemiske proces, således at syrekoncentrationen falder under afladning. Blybatterier er kendetegnet ved lav energitæthed. Langt den største anvendelse er som startbatteri i biler og motorcykler, men herudover anvendes de også til fritidsbrug i både, campingvogne m.v. Traktionsbatterier anvendes primært i elektriske gaffeltrucks, mens de stationære batterier oftest benyttes som nødstrømsanlæg i forbindelse med f.eks. fyrtårne, telefoncentraler, sygehuse m.v. 2.2.2 Nikkel-cadmium batterierI et opladet nikkel-cadmium batteri (NiCd-batteri) består den negative elektrode af rent cadmium og den positive elektrode af nikkeloxid. Elektrolytten består af en vandig opløsning af kaliumhydroxid, der ikke indgår i den elektrokemiske reaktion. Man skelner mellem åbne og lukkede NiCd-batterier. De åbne er store batterier, hvor det er muligt at aftappe elektrolytten, mens de lukkede er mindre hermetisk forseglede batterier. Lukkede NiCd-batterier var de første genopladelige batterier, der kunne anvendes i transportable apparater (se figur 2.8). NiCd-batterier i samme størrelser som brunstens- og alkalibatterier erstattede derfor i mange tilfælde disse, ligesom NiCd-batterierne blev anvendt i mobiltelefoner, bærbare computere, videokameraer, husholdningsapparater og håndholdt værktøj. Andre genopladelige batterityper har dog efterhånden erstattet NiCd-batterierne. En undtagelse er dog i håndværktøj og lignende, og dette skyldes at NiCd-batterier har gode højbelastningsegenskaber og er relativt kuldestabile. Åbne NiCd-batterier anvendes typisk hvor blyakkumulatorer er blevet vurderet til at aflade for hurtigt og til ikke at have tilstrækkelig kapacitet. Dette er specielt som nødstrømsanlæg på sygehuse, store trafikanlæg m.v. samt i startmotorer i tog og fly. Endvidere anvendes de åbne NiCd-batterier i el-biler. I figur 2.9 er vist et eksempel på det typiske indhold af stoffer i et Nikkel-cadmium batteri. Som det fremgår, er de væsentligste indholdsstoffer jern, nikkel og cadmium.
Figur 2.8. Genopladeligt batteri af cylindrisk type /1/
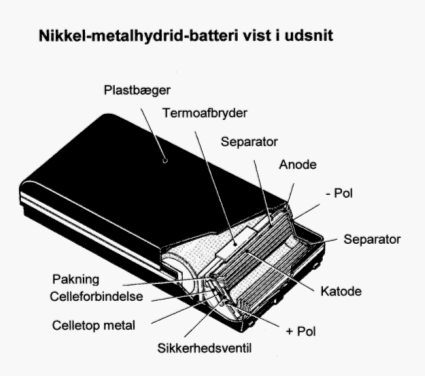
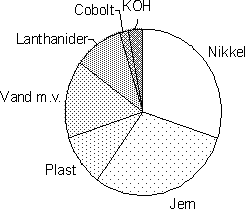
Figur 2.9. Eksempel på fordelingen af indholdsstoffer i Nikkel-cadmium batteri /2/, /3/, /8/ 2.2.3 Nikkel-metalhydrid batterierI nikkel-metalhydrid batteriet (NiMH-batteriet) består den positive elektrode, som i NiCd-batteriet, af nikkeloxid og elektrolytten af kaliumhydroxid. Derimod er cadmium erstattet af en stang af en metallegering, der kan optage lagre og afgive brint af elektrokemisk vej. Opbygningen af den cylindriske type er vist i figur 2.8 mens opbygningen af et flercellebatteri er vist i figur 2.10. I figur 2.11 er vist et eksempel på fordelingen af indholdsstoffer, og det ses at de væsentligste er nikkel og jern. NiMH-batterier har en høj energitæthed, og giver op til 50% længere driftstid end tilsvarende NiCd-typer. Endvidere har de ikke samme "memory-effekt" som NiCd-batterier, hvilket betyder at de nemmere kan oplades uden at tage skade. Endelig indeholder NiMH-batteriet ikke det miljøskadelige cadmium, og det er derfor blevet et naturligt miljømæssigt alternativ til erstatning af NiCd-batterier i mobiltelefoner, bærbare computere, videokameraer m.v.
Figur 2.10. Opbygningen af flercelle Nikkel-metalhydrid batteri /1/
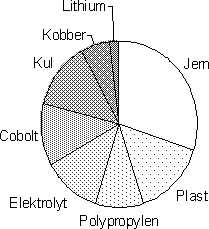
Figur 2.11. Eksempel på indholdet af stoffer i nikkelmetalhydrid batteri /8/ 2.2.4 Lithium-ion batterierDen nyeste anvendte teknologi inden for genopladelige batterier er lithium-ion batterier. Den negative elektrode består af kulstof og en strømsamler af kobber, mens den positive elektrode består af lagdelt lithium-metaloxid og en strømsamler af aluminium. Metallet kan f.eks. være kobolt, nikkel eller mangan. Elektrolytten er en opløsning af lithiumsalt i blandinger af organiske opløsningsmidler.
Figur 2.12. Eksempel på indholdet af stoffer i et lithiumbatteri med stålhylster /8/ Lithium-ion polymer batterier. Den seneste udvikling inden for lithium-batterier er lithium-ion polymer batterierne. Her er den flydende elektrolyt erstattet af en ion-ledende fast membran. Dette har bl.a. den fordel, at man kan lave batterierne meget tynde og fleksible. Lithium-ion batterier er det genopladelige batteri, der har den største energitæthed, og er derfor særlig velegnet til at strømforsyne bærbart udstyr, hvor laveste vægt/volumen og længst mulige driftstid ønskes, f.eks. i mobiltelefoner, bærbare computere etc. 2.3 Kviksølv i brunstens- og alkalibatterierPå grund af den elektrokemiske proces sker der en udvikling af gas (brint) under udladningen af et zinkbaseret batteri. Hvis gasudviklingen sker ukontrolleret kan det være årsag til, at batteriet selvudlades eller lækker. Tidligere tilsatte man kviksølv for at reducere og kontrollere denne gasudvikling, men overgangen til en ny batterikonstruktion med f.eks. en såkaldt "expanded can" muliggjorde fremstilling af alkaliske batterier uden tilsætning af kviksølv og uden at give afkald på driftssikkerheden. Før 1985 indeholdt alkaliske batterier således op til 10.000 ppm kviksølv, mens brunstensbatterier indeholdt op til 100 ppm kviksølv. På det tidspunkt igangsatte den europæiske batteri forening (EPBA) et program for at nedsætte indholdet af kviksølv i batterier, og siden 1994 har EPBA's medlemmer udelukkende solgt såkaldte kviksølvfrie brunstens- og alkalibatterier i Europa /9/. Det vil i praksis sige, at batterierne maksimalt indeholder 5 ppm kviksølv, da kviksølv kan optræde som urenhed i råvarerne. EPBA organiserer alle de væsentligste producenter af brunstens- og alkalibatterier i Europa, men da det indtil 1. januar 2000, med visse undtagelser, var tilladt at importere og sælge alkalibatterier med op til 250 ppm kviksølv til EU-landene, kan en del importerede batterier fra før denne dato stadig indeholde op til 250 ppm kviksølv. 1. januar 2000 blev det, som følge af et EU-direktiv, forbudt at importere og sælge alkaliske batterier med over 5 ppm kviksølv.
|