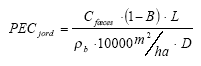|
Risikovurdering af anvendelse af lokalt opsamlet fæces i private havebrug 3 Risikovurdering af kemiske stoffer
Mennesker eksponeres for lægemidler primært gennem behandling, mens miljøfremmede stoffer og tungmetaller kommer fra et stort antal kilder, hvoraf fast føde og drikkevarer i de fleste tilfælde er de mest betydningsfulde. Der kan dog også optages stoffer ved indånding eller gennem huden, f.eks. i arbejdsmiljøet, ved brug af kosmetiske produkter eller i forbindelse med rengøring eller andre aktiviteter i hjemmet. Både lægemidler, miljøfremmede stoffer og tungmetaller udskilles gennem urin, fæces og i begrænset omfang udåndingsluft. Human fæces vil derfor indeholde lægemidler, men også et betydeligt antal miljøfremmede organiske stoffer og tungmetaller, der ikke eller kun delvis er metaboliseret i kroppen og med tiden udskilles med den faste afføring. Dette er imidlertid et emne, der kun er yderst sparsomt undersøgt og beskrevet i litteraturen i modsætning til f.eks. indhold af den slags stoffer i modermælk hos ammende kvinder, herunder ikke mindst dioxiner og polyklorerede biphenyler (PCB). Det vurderes, at langt de fleste stoffer vil blive transformeret og nedbrudt i den menneskelige organisme, og at interessen derfor må samle sig om de meget persistente miljøgifte, som f.eks. dioxiner, og om egentlige konservative stoffer, dvs. grundstoffer, primært tungmetaller som f.eks. bly og cadmium. Derudover vil fæces, der opsamles og komposteres, i mindre omfang, men med jævne mellemrum kunne blive "kontamineret" med kemiske stoffer i rengøringsmidler, der anvendes til toiletrengøring. Der er her primært tale om anioniske og nonioniske detergenter, overvejende alkoholethoxylater (AEO) og lineære alkylbenzensulfonater (LAS). Begge disse stoftyper er relativt ugiftige og biologisk letnedbrydelige under aerobe forhold, og de vurderes derfor ikke at udgøre et risikomoment af betydning (den primære eksponering af mennesker vurderes i øvrigt at finde sted ved den tilsigtede anvendelse af stofferne). Der er ikke fundet specifikke oplysninger i litteraturen om disse stoftyper i fæces. Rester af medicin som spredes i miljøet må betragtes som en forurening med en potentiel effekt ligesom andre af det industrialiserede samfunds kemikalierester. I forhold til de almindelige industrikemikalier, dog med den forskel at medicin ligesom pesticider og biocider i udgangspunktet anvendes netop fordi de har en iboende biologisk effekt. Viden om lægemidlers skæbne og effekt i miljøet er stadig relativ sparsom. Derfor er det nødvendigt at belyse lægemidlernes skæbne og effekter på den gødede jord. En gennemgang af litteraturen viser, at man efterhånden har fundet medicinrester af mere end 100 lægemiddelstoffer i miljøet (Ingerslev, 2000). Det er derfor en sandsynlighed for at nogle af disse også i miljøet kan udvise en effekt, om end effekter på nuværende tidspunkt sjældent kan påvises. Da lægemidler i sagens natur kan have meget specifikke effekter, kan de manglende effekter blandt andet skyldes, at der ikke er udviklet testprogrammer som kan måle de subtile måder effekter kan manifestere sig på. De mange fund af medicinrester i miljøet viser at stofferne må formodes at have en vis kemisk stabilitet i miljømatricen. For en detaljeret forståelse af lægemidlers eksponeringsvej, tilstedeværelse, skæbne og effekter på miljøet og indirekte effekter på mennesket henvises til f.eks. Stuer-Lauridsen et al. (2002), Halling-Sørensen et al. (2002) samt Halling-Sørensen et al. (1998). 3.1 Forekomst og vurdering af miljøfremmede stoffer og metaller i fæces i DanmarkI Tabel 3.1 sammenfattes oplysninger for et antal tungmetaller og dioxin om grænseværdier i affaldsprodukter til jordbrugsformål, jordkvalitetskriterier, værdier for tolerabel daglig eller ugentlig indtagelse (TDI/TWI) samt koncen-trationsniveauer i human fæces. Tabel 3.1 Grænseværdier for tungmetaller og dioxiner i miljømatricer og ved indtagelse, samt estimerede niveauer i human fæces på hhv. tørstof- og P-basis. Indhold i fæces på P-basis er baseret på Eilersen et al (1998) og ICON (2001) samt forholdet mellem tørstof of fosfor angivet i afsnit 2.3.
ts = tørstof; lgv = legemsvægt; P = fosfor (total fosfor) * TDI = tolerabel daglig indtagelse (over et helt livsforløb) ** Toksicitetsækvivalenter i forhold til "Seveso-dioxin", 2,3,7,8.T4CDD. 1 Miljøministeriet (2003). 2 Miljøstyrelsen (1995). Tysk grænseværdi for spildevandsslam. 3 ANZFA (2001). 4 Friedman (1994). 5 NHMRC (2002), TDI-værdi fra WHO 1998 . 6 NHMRC (2002). Opgivet som TWI-værdi på 14 E-09, altså tolerabel ugentlig indtagelse, fra EC (2001). 7 Eilersen et al. (1998). Beregnet ud fra totale mængder af slam og tungmetaller. 8 ICON (2001). 9 EIP (1997). Beregnet ud fra en mængde dioxin på 60 pg/prs./dag og en gennemsnitlig mængde fæces på 35 g TS/dag/prs. (beregnet ud fra Eilersen (1998)). Der gøres opmærksom på, at der generelt ikke er fundet oplysninger om omfanget af data, der ligger til grund for de angivne koncentrationsniveauer, som sikkert kan udvise betydelig variation. For eksempel vides det, at rygning har signifikant indflydelse på kroppens belastning med tungmetallet cadmium, som tillige er et ret mobilt metal, hvorfor rygevaner utvivlsomt også vil afspejle sig i koncentrationen af cadmium i fæces. Specielt hvad dioxiner angår, skal der gøres opmærksom på, at den angivne koncentration er beregnet ud fra oplysninger om en per capita ekskretion af dioxiner på 60 pg-TEQ/dag (EIP 1997) og en fæcesmængde på ca. 35 g tørstof/dag beregnet efter oplysninger i Eilersen et al. (1998). TEQ er mængden af dioxiner (som er en gruppebetegnelse for mere end 200 enkeltstoffer) omregnet til toksicitetsækvivalenter i forhold til den mest kendte og en af de mest giftige dioxiner; 2,3,7,8-T4CDD ("Seveso-dioxin"). Det skal yderligere bemærkes, at originaldata vedr. dioxinindholdet i fæces stammer fra en artikel publiceret i 1990 og bygger altså på målinger, der er foretaget sidst i 1980'erne. Eksponeringen for dioxin vides at være faldet betydeligt siden dengang, og der er således grund til at antage, at den angivne værdi er væsentligt overestimeret. Det ses af tabellen, at indholdet af tungmetaller i fæces for de fleste metallers vedkommende er betydeligt lavere end den tørstofbaserede grænseværdi, der jf. slambekendtgørelsen (Miljøministeriet 2003) gælder for spildevandsslam mv., der udbringes på dyrkningsjord, og det er også lavere eller på linie med de kriterier for jordkvalitet, der er fastsat i samme bekendtgørelse. Undtagelserne er cadmium, der ligger på linie med grænseværdien og kviksølv, der ser ud til at ligge lidt højere (men formodentlig inden for usikkerheden på estimatet). I forhold til de P-baserede grænseværdier, der alternativt må benyttes som beregningsgrundlag for bly, cadmium, kviksølv og nikkel, er det kun cadmiumindholdet, der ligger på kanten. De typiske værdier for P i slam medfører, at der må udspredes omtrent 0,1 kg slam tørstof/m2. Som beskrevet i afsnit 2.4 antages det i nærværende undersøgelse, at der udspredes op til 0,5 kg fæces tørstof/m2. De få og sparsomme oplysninger om indhold af tungmetaller i fæces antyder dermed, at for cadmium og kviksølv vil belastningen per arealenhed kunne være op til 10 gange højere end slambekendtgørelsens tørstofbaserede grænseværdier, såfremt komposteret fæces, der udbringes lokalt i private haver, var omfattet af bekendtgørelsens krav for disse stoffer. De 0,5 kg fæces ts/m2 svarer til 7 g tot-P/m2 eller 2,3 gange det tilladte ift. slambekendtgørelsen. Der vil dermed reelt kunne forekomme en (beskeden) overskridelse også af de P-baserede grænseværdier for cadmium og kviksølv ved udbringning af denne mængde fæces per arealenhed. Dioxiner udskilles på grund af deres lipofile (fedtelskende) karakter meget langsomt fra kroppen og først efter adskillige år (40-50 år) opnås steady-state mellem optagelse og udskillelse (NHMRC, 2002). For børn og yngre mennesker må udskillelsen og dermed indholdet i fæces derfor forventes at være lavere end den angivne værdi (der som tidligere nævnt i øvrigt formodentlig er lavere i dag end for 12 år siden da den blev beregnet). Geyer et al. (2002) angiver i en reviewartikel halveringstiden for udskillelse af 2,3,7,8-TCDD på 5,8-9,7 år og stigende med stigende chloreringsgrad (5-8 chloratomer/molekyle) op til 50-132 år for OCDD, der har 8 chloratomer. Man bemærker, at det i Tabel 3.1 angivne estimat på dioxinindholdet i fæces er mere end en faktor 50 lavere end den gældende tyske kravværdi for dioxin i slam, der ønskes udbragt på landbrugsjord. 3.2 Forekomst af medicinrester i fæces i Danmark3.2.1 Udvælgelse af stofferI år 2000 var der i alt 4100 lægemidler på det danske marked, der indeholdt ca. 1000 forskellige aktivstoffer (Lægemiddelstyrelsen, 2002). Da der i litteraturen ikke findes data der belyser økotoksikologiske såvel som indirekte effekter af ret mange lægemidler er det valgt at tage udgangspunkt i forbrugsdata og i viden om stoffernes potens hos mennesket. Følgende data er derfor indsamlet:
Data for denne bruttoliste er angivet i Tabel 3.2. På grund af datamangel er der i nærværende arbejde anvendt den relativ simpel vurderingsprocedure der anvendes til industrikemikalier, og ikke de foreslåede retningslinier for nye lægemidler (EMEA, 2001). Det er også undladt, at anvende den mere omfattende model for industrikemikalier, EUSES, som er beskrevet i (ECB, 1997). Modellens fundamentale antagelse om, at kemikaliers fordeling i miljøet kan beskrives ved hjælp af oktanol-vand fordelingskoefficienter kan ikke verificeres for lægemidler, der ofte også udviser andre bindingstyper grundet mange funktionelle grupper på molekylet (Loke et al. 2002; Tolls 2001). Humanlægemidler er udviklet til at virke på mennesket, dvs. hvirveldyr med organer, kredsløb, biokemiske receptormekanismer, der kan virke forskellige fra selv nærbeslægtede arter. Det kan derfor ikke nødvendigvis forventes at lægemidler, der er virksomme i lave doser på mennesket, også er meget potente med hensyn til effekter i miljøet. Lægemidler med en lav potens i mennesker har også omvendt vist sig at være meget potente i miljøtest. Eksempelvis er visse antibiotika ret potente i bakterieassays, men er kun virksomme i høje doser på mennesket. Det skal dog nævnes, at det er meget muligt at de standard økotoksikologiske test som anvendes, og som der ret beset kun er temmelig begrænsede resultater fra for lægemidler, ikke nødvendigvis identificerer de rette måleparametre for stoffer med specifikke virkninger. Eksempler på stoffer, hvis subtile effekter ikke fanges i standardtest er hormonforstyrrende stoffer. 3.2.2 Kort beskrivelse af de udvalgte stofferNedenfor gives en kort beskrivelse for den terapeutiske anvendelse af de lægemiddelstoffer der er udvalgt til nærmere undersøgelse i projektet med deres tilhørende ATC kode (lægemiddel nr.). Furosemid (ATC C03CA01). Vanddrivende middel af typen "Loop diuretika" der nedsætter nyrernes koncentrationsevne og øger generelt døgndiuresen og vandindtagelsen. Anvendes ofte til langtidsbehandling hvorfor det regnet i antal doser er det mest anvendte lægemiddel i Danmark (data fra år 2001). Østrogen (ATC G03CA). Naturligt forkommende kvindeligt hormon som er tilstede i p-piller og eksempelvis klimateriepræparater. Styrer udviklingen af kvinders sekundære kønskarakterer. Tabel 3.2 De screenede lægemiddelstoffer i den primære sundhedssektor i år 2000, opgjort i mængde som Definerede Døgn Doser (DDD), og som vægt (kg aktivt stof). Derudover er angivet den fraktion af det indtagne lægemiddel der udskilles med fæces og log Kow som mål for stoffernes lipofilicitet.
* Lægemiddel nr. ** Lægemiddelkataloget Online WWW.lk-online.dk *** ACD log P. De opgivne intervaller er 95% konfidensintervaller (Stuer-Lauridsen et al. 2002). Gestoden (ATC G03D). Hormonalt indholdsstof i p-piller der er artificiel pro-gesteron og som kan indtages oralt da det ikke inaktiveres i leveren. Desogestrel (ATC G03D). Hormonalt indholdsstof i p-piller der er artificiel progesteron og som kan tages oralt da det ikke inaktiveres i leveren. Er i sig selv inaktiv men omdannes i leveren til det aktive 3-keto-desogetrel. Amlodipin (ATC C08CA01). Middel mod hjertekramper (Angina pectoris). Virker som kalciumantagonist med overvejende kardilaterende virkning. Indtages som tabletter. Ibuprofen (ATC M01AE01). Smertestillende gigtmiddel af typen nonsteroidt antiinflammatorisk middel. Indtages som tabletter. Budesonid (ATC R03BA02) Astmamiddel. Indtages som inhalationsmiddel el. kapsler. Citalopram (ATC N06AB04) Antidepressivt middel. Indtages som tabletter. Terbutalin (ATC R03AC03) Astmamiddel. Indtages som tabletter el. inhalationspulver. Zopiclone (ATC N05CF01). Sovemiddel. Indtages som tabletter. Ketoconazol (ATC D01AC08) Mod svamp til udvortes brug. Salve. Omeprazol (ATC A02BC01) Mod for meget mavesyre. Indtages som tabletter eller ved injektion. Digoxin (ATC C01AA05) Hjerteglykosid mod hjertekramper. Indtages som tabletter eller ved injektion. Insulin (ATC A10AB01 ) Polypeptid der er nødvendig for opbygning af glykogendepoter, fedtdepoter og protein. Findes som langsom eller hurtigtvirkende. Gives ved injektion. Erythromycin (ATC J01FA01) Makrolid antibiotika som delvis udskilles med afføringen via galden. Indtages som tabletter og ved injektion. Ciclosporin (ATC L04AA01). Hyppigt anvendt Cytostatika som primært via galden udskilles med afføringen. Tages som tabletter eller infusionskoncentrat. 3.2.3 Skæbnen af lægemidlerMange lægemidler metaboliseres helt eller delvist i leveren før ekskretion. Herved forstås at stoffet undergår en kemisk omdannelse, der overordnet set har til hensigt at gøre stoffet mere vandopløseligt og mindre toksisk. Lægemiddelstoffer indeholder ofte mange funktionelle grupper så det kan være svært at forudsige præcist hvordan et stof vil blive metaboliseret. Flere faktorer såsom kroppens pH og evne til at metabolisere (tilstedeværelse af metaboliseringsenzymer), stoffets grad af lipofilicitet, og konkurrence med andre tilstedeværende stoffer har betydning for hvordan stoffet udskilles. Metabolitter udskilles oftest enten via det biliære system med fækalier eller transporteres med plasma til nyrerne for herefter at udskilles med urinen. For nærværende projekt er det derfor primært stoffer der udskilles via det biliære system (også kaldet galden) der har interesse. Det er oftes stoffer med lipofile egenskaber (høj log Kow) der udskilles med fæces. Lægemidler som indtages peroralt, (dvs gennem munden som tablet el. anden doseringsform), og kun delvis absorberes fra tarmen vil også udskilles med afføringen, se Figur 3.1. Mange lægemidler vil derfor, dog ofte i begrænset grad, udskilles med afføringen. Da der her er tale om meget begrænsede koncentrationer i fæces vil dette ikke blive vurderet yderligere her. Et lægemiddelstof kan ofte gennemgå flere metaboliseringsveje og blive udskilt med både urin og fæces, ligesom der er ofte er en fraktion af det indtagne stof der ikke optages eller ikke undergår metabolisme. Det der findes i fæces vil derfor ofte være en fraktion af den indtagne dose i form af både det indtagne stof og et par hovedmetabolitter. Tabel 3.2 viser for de valgte stoffer den fraktion der normalt regnes for at genfindes i fæces.
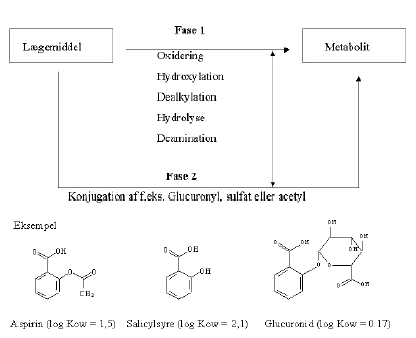
Figur 3.1 Fase I reaktionen kan være en oxidation, reduktion eller hydrolyse af lægemiddel-molekylet. Produktet er oftest et mere reaktivt og polært stof end udgangsstoffet. Den reaktive gruppe i molekylet vil ofte være en hydroxylgruppe, som samtidig vil være det sted en konjugation foregår. Konjugationen udgør fase II, hvor en større gruppe påhæftes, f.eks. en glucuronyl, sulfat eller acetyl gruppe som oftest vil resultere i en vandopløselig og inaktiv metabolit. (Rang og Hale, 1991) Børn contra voksne. Børn og unges omdannelse af lægemidler i kroppen adskiller sig ofte fra voksnes grundet biokemiske og fysiologiske forskelle. Der er derfor generelt grund til at være varsom med at give børn unødvendigt medicin og derfor ikke udsætte dem for tilfældig eksponering heraf. Det skyldes bl.a at der i de første leveår foregår en livlig aktivitet i flere organers struktur og størrelse såsom centralnervesystemet, reproduktionsorganer og andre hormonsystemer der er mere sensitive overfor lægemiddelindtagelse end hos voksne. Ser vi på lister over lægemiddelstoffer bør primært hormoner, midler mod hjertesygdomme og cancermidler derfor undgås at blive indtaget utilsigtet af børn. Normaliseret i forhold til dets vægt, er mindre børns lever og nyrer dog større end ved voksne, og eliminationen af stoffer i leveren foregår derfor relativt hurtigere. Både nedbrydning og udskillelse foregår hurtigere i mindre børn. Den større metaboliseringsrate i børn kan derfor resultere i øget følsomhed over for de stoffer der omdannes til aktive metabolitter der kan have toksiske effekter (f.eks. visse cancermidler). I nogle tilfælde vil den hurtige elimination i og udskillelse fra kroppen dog modvirke de toksiske effekter. Forekomst af metabolitter i fæces fra nettolisten. Furosemid (ATC C03CA01). Ca. 60-70 % absorberes fra tarmen således at ca. 33% udskilles via galden med afføringen som konjugeret glucuronidfurosemid. Østrogen (ATC G03CA). De naturlige østrogener metaboliseres og kunjugeres i tarmen, leveren og nyrerne, og de udskilles gennem nyrerne og fæces (ca. 40%) som glucuronider og sulfater. Konjugerede østrogener er også biologiske aktive fordi de let hydrolyseres til det frie østrogen i mave-tarm kanalen. Gestoden (ATC G03D). Biotilgængelighden er ca. 85%. Udskilles gennem fæces i højere grad end østrogen som glucuronider og sulfatkonjugater. De konjugerede stoffer er også biologisk aktive - se ovenfor. Desogestrel (ATC G03D). Biotilgængelighden er ca. 85%. Udskilles gennem fæces i højere grad end østrogen som glucuronider og sulfatkonjugater. De konjugerede stoffer er også biologisk aktive - se ovenfor. Amlodipin (ATC C08CA01). Biotilgængeligheden er 60-65%. Metaboliseres i leveren til inaktive metabolitter hvorved ca. 50 % udskilles med afføringen som uabsorberes stof eller inaktive metabolitter. Ibuprofen (ATC M01AE01). Absorberes fuldstændigt fra mave-tarm kanalen og metaboliseres i leveren til inaktive metabolitter. 5% udskilles med afføringen. Budesonid (ATC R03BA02). Oral biotilgængeligehed er på kun 11% hvorimod det absorberes bedre via luftvejene. Metaboliseres i leveren til inaktive metabolitter såsom 6-?hydroxybudesonide og 16-hydroxyprednisolone. Ca 20% udskilles via afføringen mere ved peoral indtagelse. Citalopram (ATC N06AB04).Biotilgængeligheden er ca. 80%. Metaboliseres i leveren til delvis aktive metabolitter. 88% udskilles med afføringen. Terbutalin (ATC R03AC03) Biotilgængeligheden efter peroralt indgift er op til 40%. 20% udskilles med afføringen Zopiclon (ATC N05CF01). Biotilgængeligheden er ca. 80%. Metaboliseres i leveren via CYP3A4. ca 25 % udskilles via galden med afføringen som inaktive eller delvis aktive metabolitter såsom zopiclone N-oxide og N-desmethylzopiclon. Ketoconazol (ATC D01AC08) Absorberes i meget varierende grad fra mave-tarmkanalen (20-70%). Absorptionen øges i forbindelse med måltid. Metaboliseres i leveren til inaktive metabolitter og op til 85% kan udskilles med fæces. Omeprazol (ATC A02BC01) Biotilgængeligheden er ca. 50% og udskilles i begrænset grad med afføringen (20%) som inaktive metabolitter som eksempelvis omeprazol sulfone. Digoxin (ATC C01AA05) Absorberes ved peroralt indgift 70-85%. Ikke absorberet medicin udskilles med fæces (op til 30%) som aktivt stof. Insulin (ATC A10AB01 ) Insulin metaboliseres hurtigt til inaktive metaboliter i lever, nyrer og muskelvæv. Da insulin kun kan injiceres vil der ikke findes insulin i fæces. Lidt insulin vil forekomme i urin som uomdannet stof. Erythromycin (ATC J01FA01) Op til 80% af stoffet udskilles med fæces som både aktive og inaktive metabolitter og ikke-absorberet stof. Ciclosporin (ATC L04AA01). Ca 90 % af dosen udskilles som metabolitter via galden med fæces. I de eksponeringsscenarier der evalueres her er der typisk tale om børn som indtager en jordfraktion. Ved sammenligning mellem koncentrationen af lægemiddel i jord/fæces og den terapeutiske dosis for voksne, er der alene gennem indtagelse af jord ikke tegn på at der opnås doser af lægemiddelrester som kan give effekter på børn. I den sammenhæng kan det overvejes om det er ønskeligt at sammenligne følsomme gruppers, i dette tilfælde børns, eksponering til stoffer som de kun i yderst sjældne tilfælde ville blive behandlet med. Det gælder f.eks. digoxin og cancermidler, der kan være lægemidler som raske børn ikke bør udsættes for - en slags "nul tolerance" stoffer, som børn slet ikke bør eksponeres for. Ved indtagelse af jordrester på grønsager og rodfrugter kan andre følsomme grupper med meget lav eller ingen tolerance overfor visse lægemidler blive eksponeret. Et klassisk eksempel er problemerne ved eventuel forekomst af penicillin, men også f.eks. artificielle gestagener af 19-nortesterontypen som skal undgås i den tidlige graviditet på grund af mulig risiko for virilisering af pigefostre. Stabilitet under kompostering. Der er ingen tilgængelige oplysninger i litteraturen om lægemidlers stabilitet i fæces under langtidsopbevaring. Et enkelt studie har dog undersøgt det nærtbeslægtet problemstilling, om antibiotika har effekt på den anaerobe nedbrydning under biogas produktion (Sanz et al., 1996). Dette arbejde viste at, bortset fra makrolidet erythromycin, havde 15 forskellige antibiotika med forskellige virkningsmekanismer en hæmmende effekt på den anaerobe nedbrydning og på methan produktion. Tetracyklinerne og kloramfenikol havde endog stor effekt. Til forskel fra betingelserne for dette projekt var temperaturen i beholderen i det omtalte studie 30°C under hele forsøget. Indenfor dette projekts rammer vil omsætningen af stofferne derfor kun blive behandlet i overordnede vendinger. Fæces tænkes opbevaret i ca. 1 år og tilsat flis for at hæmme dannelse af anaerobe forhold i en beholder der er afskærmet for lys. Det forudsættes at temperaturen i beholderen under opbevaringen ikke overstiger 20 °C. Under sådanne forhold må det formodes at fæces tørrer mere og mere ud. De generelt højlipofile lægemidler, formodes derfor at sorbere til fæces og med resulterende lav biotilgængelig for evt. bionedbrydning, såvel som mulig fotonedbrydning. Surhedsgraden er ca. neutral (målingsinterval = 6,7 - 8,4) og derfor vil hverken sur eller basisk hydrolyse være udpræget for de fleste af stofferne. Oxidation af lægemiddelstofferene forventes derfor at være den eneste kemiske omdannelsesproces der kan finde sted. Uden at udføre laboratorieforsøg er det ikke muligt at kvantificere en evt. oxidation i beholderen. I nedenstående risikoberegninger er derfor forudsat at lægemiddelstofferne ikke nedbrydes under den 1 årige opbevaring i fæces. Binding til og optagelse fra jordmatricen efter udbringning. De undersøgte stoffer og metabolitter i nærværende undersøgelse er overvejende lipofile (se log Kow værdier for stofferne i tabel 5.2) og består ofte af flere funktionelle kemiske grupper med både base eller syre egenskaber. Sådanne stoffer kan tit have en stærk binding til jord (Tolls, 2001; Loke et al. 2002). Fordelingskoefficienten, Kd, imellem jord og vand benyttes ofte til at beskrive denne egenskab. Denne parameter er ikke rapporteret i litteraturen for de undersøgte stoffer, men det må formodes at de opfører sig på samme måde som andre miljøfremmede stoffer med tilsvarende fysisk-kemiske egenskaber. Med de pågældende kemiske strukturer må man antage at de undersøgte stoffer er hårdt bundet til jord med en tilsvarende lav biotilgængelighed. For tilsvarende lipofile stoffer har man endvidere undersøgt om stofferne ved indtagelse af jord kan frigøres i menneskets tarm og blive biotilgængelige for membrantransport i tarmen. Mange faktorer såsom galdeindholdet i tarmen, ufordøjet fødemængden kan fremme eller hæmme desorptionen af stofferne. En omfattende hollandske undersøgelse (Oomen, 2000) af højlipofile HOC's såsom PCB, og Lindan samt bly, viste at biotilgængeligheden og evt. optagelse gennem menneskets tarm og deraf resulterende toksicitet var afhængig at tilstedeværelse af jord. Hvis stofferne var sorberet på en jordfase så faldt biotilgængeligheden sammenlignet med at stofferne bare blev transporteret med føde eller væske. Dette indikerer at desorptionen af højlipofile stoffer fra jord reduceres i forhold til fra føde og flydende væsker. Konklusionen er at jord hæmmer optagelsen af miljøfremmede stoffer i tarmen. Det blev vurderet at kun op til 50% af den sorberede mængde stof på jorden, blev gjort biotilgængeligt i tarmen afhængig af fødeindhold og galdeinhold i tarmen. 3.3 Risikovurdering for medicinresterVed vurderingen af aktivstoffet i lægemidler er anvendt forholdet mellem "predicted environmental concentration" og "predicted no-effect concentration" (PEC/PNEC). Dette er et standard princip som anvendes ved risikovurdering af kemikalier (OECD, 1992; NCM, 1995; EU TGD, 1996). Som applikations- eller sikkerhedsfaktor til beregning af PNEC er brugt værdien 1000. Det er valgt at undlade at benytte den ekstra faktor 10 for små datasæt, som EUs retningslinier for vurdering af lægemidler giver mulighed for (EU, 2002). På en lang række punkter er procedurene fra de nævnte retningslinier ens. Når PEC/PNEC er over en (Risikokvotienten RQ > 1) er der potentiale for miljøeffekter og det anbefales da generelt at undersøge stofferne nærmere. Udfra de fundne PEC og PNEC data udregnes risikokvotienten som:
RQ giver en værdi for risikoen på påvirkning af organismer i det miljø hvor PEC og PNEC er bestemt. RQ udtrykker både hvor farligt et stof er og hvor megen viden der er benyttet i evalueringen. Ved fastsættelse af PNEC benyttes en sikkerhedsfaktor, der afhænger af hvor megen viden man har om det pågældende stof. Denne sikkerhedsfaktor har normalt værdien 1000, 100, 50 eller 10, hvor 10 svarer til en meget god viden om stoffets farlighed. Man kan ikke konkludere, at et stof med RQ = 10 er ti gange så farligt som et stof med RQ = 1. RQ vil for stoffer med få tilgængelige data ofte kunne mindskes ved at tilvejebringe flere økotoksikologiske data fordi sikkerhedsfaktoren der kan sænkes. Det er dog kun under forudsætning af, at der ikke fremkommer data som tyder på større giftighed! Omvendt kan man konkludere, at hvis RQ er større end 100 er det ikke tilstrækkeligt blot at fremskaffe mere viden. Den producerede viden skal samtidig afkræfte hvor farligt man på det nuværende vidensgrundlag mener at stoffet er. Til vurdering af lægemidler og andre specifikt virkende stoffer kan en tommelfingerregel være at for at kunne udelukke en effekt skal RQ være mindre end 0,1. Fastlæggelse af eksponering, PEC. Basisdata for scenarierne A, B og C er beskrevet i afsnit 2.4 og 2.5. Fæces med et indhold af medicinrester som defineret i disse scenarier udbringes derefter ved udlægning. Til beregning af lægemiddelkoncentrationen i jorden efter udspredning (PECjord) anvendes følgende formel:
Hvor Cfæces er koncentrationen i fæces, B er den fraktion af lægemiddelstoffet der nedbrydes under opbevaring (sættes til 0), L er den mængde fæces der udspredes (kg/ha). ρb er jordens densitet (1500 kg/m3) og D er pløjedybden for den udspredte fæces (1 cm). Fastlæggelse af økotoksikologi, PNEC. Predicted no effect concentration (PNEC) er den estimerede koncentration, hvorved der ikke ses effekt på nogen organismer. Den bestemmes i bedste fald ud fra kendskabet til No observed effect concentration (NOEC) data for enkelte organismer, der deles med en sikkerhedsfaktor afhængig af datakendskabet (se nedenstående). Hvis der ikke er NOEC data tilgængeligt anvendes EC50, LC50 eller estimerede data. Når der forefindes data for flere arter anvendes data for den følsomste art. Størrelsen af sikkerhedsfaktoren afhænger af den tilgængelige datamængde og kvaliteteten af de økotoksikologiske data. For at anvende sikkerhedsfaktoren 10, kræves data opnået ved kroniske test på mindst tre forskellige arter på tre trofiske niveauer. Faktoren 100 kræver EC50 eller LC50 for akut toksicitet for tre forskellige arter og en NOEC, ellers anvendes en faktor 1000 (EU TGD 1996). I nærværende beregninger er anvendt faktoren 1000. PNEC udregnes således: PNEC = L(E)C50, LOEC eller NOEC / Sikkerhedsfaktoren Haves NOEC kun som koncentration i vandigt medium, kan det tillades at oversætte denne værdi til en jordkoncentration som: NOECjord = NOECvandigtmedium * kd hvor kd (L/kg) er fordelingskoefficienten imellem vand og jord. Det forudsættes herved at jorden er 50% mættet med vand. Tabel 3.3 Beregning af PNEC for de 3 lægemiddelstoffer hvor data er tilgængelige.
1) Halling-Sørensen et al (1998) 2) Stuer-Lauridsen et al (2000) For de fleste stoffer findes der ikke økotoksikologiske data hvorfor PEC/PNEC beregning kun kan foretages på Østrogen, Iboprufen og Digoxin. Usikkerhedsfaktor 1000 anvendt jvf. EU risikovurderingsguideline (EU TGD 1996), når der er begrænsede datasæt uden NOECs. Resultatet af risikovurderingen er vist i Tabel 3.4. Der gøres opmærksom på, at hvis den anvendte LOEC for Østradiol vurderes som en NOEC kan usikkerhedsfaktoren 100 anvendes og risikokvotienterne vil da ligge mellem 4.100 og 37.600. Tabel 3.4 Beregning af risikokvotienter, RQ, for stoffer hvor fuldt datasæt forefindes. Beregning er mulig for 3 af de 12 stoffer. Resultatet for standard-familie er markeret med fed skrift.
Der er ingen tvivl om, at østradiol med det nuværende datasæt markerer sig som et stof med potentielle miljøeffekter. Selv med et komplet datasæt og en "teoretisk" sikkerhedsfaktor på 1 vil RQ overskride 1. Der skal dog gøres opmærksom på, at det er data for vandmiljø og ikke jordmiljøet som ligger til grund for beregningen. Ibuprofen ligger også omkring RQ = 1 afhængig af scenariet, hvilket indikerer potentielle effekter. Digoxin synes derimod kun at nå en kritisk RQ (0,1-1) under værst tænkelige forhold, men hører til i gruppen af mulige "nul tolerance stoffer". 3.4 Vurdering af risiko for akutte effekterDen sundhedsmæssige vurdering tager også udgangspunkt i de tre scenarier for kemisk risikovurdering. Beregningerne viser at ratioen mellem en voksendosis af det pågældende lægemiddelstoffet og indholdet i en 200 mg klump i alle tilfælde med en faktor 1000, se Tabel 3.5. I de fleste tilfælde er denne faktor på mere end en faktor 10.000, svarende til at man skal indtage mellem 200 g og 2 kg fæces for at indtage en døgndosis, og for flere af stofferne op til 10 kg jord. Det bemærkes, at der i Larsen (1998) er vurderet, at det absolut maksimale indtag af jord beregningsmæssigt kan sættes til 10 g, og at selv ved dette indtag vil TDI ikke være nær. Det er derfor i praksis ikke muligt at man via en enkelt dags eksponering i haven kan indtage hvad der svarer til en dagsdosis medicin. Tabel 3.5 Antallet af gange en voksendosis af det pågældende lægemiddelstof overtiger indholdet af stoffet i 200 mg fæces.
3.5 Diskussion af resultater3.5.1 Kemisk risikovurderingNormalt regnes PNEC systemets sikkerhedsfaktorer (10-1000)for relativt konservative. Imidlertid undtages specifikt virkende stoffer fra EU's retningslinier som omhandler industrikemikalier, idet der findes andre retningslinier for pesticider og biocider der er de typiske specifikt virkende stoffer på markedet. Disse retningslinier indeholder særlig afsnit om stoffernes virkemåde som lægger op til valg af særlige relevante test. Sådanne resultater fra specielt udvalgte følsomme test er ikke til rådighed for lægemidler i dag, og applikationsfaktorerne er derfor ikke nødvendigvis så konservative for lægemidler som for andre kemikalier. Generelt er der ikke mange data om nedbrydning af lægemidler under miljørelevante forhold. På grund af relativ lav temperatur og sorption til partikler regnes der ikke med nedbrydning under komposteringen, mens der til gengæld regnes med fuldstændig nedbrydning i jordmiljøet i løbet af 12 måneder og derfor ingen akkumulering fra år til år af lægemidler ved tilførsel af komposteret fæces. Validiteten af disse antagelser hviler på et relativt spinkelt grundlag. I virkelighedens verden vil en stor del af lægemidlerne utvivlsomt omsættes ret hurtigt kemisk og biologisk, mens en lille andel vil vise sig at modstå omsætning enten som moderstof eller metabolitter. 3.5.2 Akutte effekterDet kan konkluderes, at der med hensyn til indholdet af lægemidler ikke er nogen sundhedsmæssig risiko ved at spise i størrelsesorden 200 mg fæces indeholdende lægemiddelrester. Der skal indtages mellem 200 g og 2 kg fæces for at indtage enkelt voksen dosis. For visse særlige stoffer såsom hormoner, cancermidler, antibiotika kan man ud fra et forsigtighedsprincip ønske at følge et "nul tolerance"-princip for deres forekomst i jord for at beskytte udsatte grupper. Visse mennesker/aldersgrupper kan af forskellige grunde have en stor følsomhed for disse stoffer. Eksempler på sådanne stoffer, hvor der er vanskeligt at fastsætte "sikre" niveauer, kan være:
3.6 Delkonklusion for afsnittetEn vurdering af TDI og den forventede koncentration af tungmetaller og persistente miljøgifte, eksemplificeret ved dioxiner, i komposteret fæces giver ikke anledning til bekymring selv ved 200 mg fæces indtaget dagligt af et barn på 10 kg. Grænseværdien ved udbringning af slam ville være overskredet for cadmium og kviksølv. Indholdet af disse metaller er også nær grænseværdien for indhold i uforurenet jord. Ingen af disse grænseværdier er dog gældende for udbringning af komposteret fæces i private haver. Aktive lægemiddelstoffer, primært i form af nedbrydningsprodukter og metabolitter, udskilles med fæces og vil havne i miljøet, hvis komposteret fæces anvendes i private haver som gødning selv efter langtidsopbevaring. Nedbrydningsprodukterne og metabolitterne vil generelt have lavere aktivitet end moderstoffer. Nedbrydningen sker primært i mennesket inden udskillelse og stofferne vurderes ofte til at være meget stabile i fæces under opbevaringen pga af de fysiske forhold i opbevaringstanken. Antallet af medicinerede personer med bolig på adressen er mest betydningsfuld for de anslåede koncentrationsniveauer. Kontinuerlig medicinering for specielt livsstilssygdomme, såsom hjerte-kar sygdomme, stress- og søvnproblemer og for hormonelle tilstande har indvirkning på koncentrationsniveauet i den oplagrede fæces. Familiens gæsters og familiens antibiotikabehandlinger i løbet af året bidrager ikke væsentligt i den totale medicinmængde, der udskilles til fæcesbeholderen sammenlignet med kontinuerlig medicinering af enkeltpersoner i familien, især hvis disse har livsstilssygdomme eller kroniske lidelser. Økotoksikologiske data findes kun for meget få lægemiddelstoffer, således at det kun har været muligt at udføre en begrænset PEC/PNEC beregning i jordmiljøet for 3 lægemiddelstoffer. Kun få økotoksikologiske data på vandorganismer kan anvendes fordi fordelingskonstanten imellem jord og vand ikke kendes. Der er ingen data for relevante arter for jordmiljøet. Den acceptable risikokvotient er overskredet for 2 ud af de 3 stoffer ved et scenarie, hvor indholdet af fæces fra en standard-familie udbredes i haven. Det kan derfor ikke udelukkes, at der, for visse stoffer, vil være risici i forbindelse med udspredning af fæces i haver. På det nuværende datagrundlag kan en risiko for effekt på miljøet ikke afvises for stoffer som anvendes i store voluminer eller har lave effektkoncentrationer. Baseret på sammenligning af anbefalet dagligt indtag og de forventede koncentrationer i fæces, er det generelt usandsynligt at mennesket påvirkes væsentligt selv ved indtagelse af komposteret fæces direkte fra jorden. Stoffer, hvor man ønsker "nul tolerance", vil dog blive indtaget. Det kan være stoffer som påvirker mennesket i dets udviklingsstadier, giver allergi, har celletoksicitet, langtidseffekter og/eller hormonlignende effekter.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||