Kemisk oxidation med permanganat
2 Reaktion mellem organisk stof i jorden og permanganat
Reaktionen mellem det organiske stof i jorden og permanganat er undersøgt ved laboratorieskala batchforsøg. Forsøgene er udført med henblik på at opnå en bedre forståelse af de mekanismer, der ligger til grund for omsætning af permanganat, når det reagerer med morænelers sedimenter.
2.1 Baggrund og formål
Permanganatforbrug i jord og grundvand er typisk bestemt i batchforsøg ved forholdsvis høje permanganatkoncentrationer (5-25 g /l) i forbindelse med planlægning af fuldskalaprojekter (Dall-Jepsen, 2003; Jørgensen et al., 2003; Westergaard, 2003). Sådanne forsøg giver sandsynligvis et meget konservativt resultat for omsætningen af permanganat, bl.a. fordi selvdestruktion antages at være mere udtalt ved højere koncentrationer af permanganat. Erfaringstal udtrykker derfor kun i begrænset omfang omsætningen af permanganat og kinetikken ved lavere koncentrationer.
I litteraturen har der primært været fokus på permanganatomsætningen i sandede aflejringer, mens omsætning og kinetik i morænelerssedimenter er sparsomt belyst.
Manglende data og erfaringer kan være problematisk ved vurdering af spredningen af permanganaten, hvor fx utilsigtet spredning til recipienter og drikkevandsforsyninger kan være en følge af overdosering. Yderligere er der et økonomisk aspekt, idet der kan opnås substantielle besparelser på fuldskalaoprensninger, hvis disse kan udføres med lavere doser af permanganat.
Ved laboratorieforsøg er det vist, at der er en sammenhæng mellem koncentrationen af permanganat og mængden af organisk stof, der bliver oxideret i sedimentet for sandede materialer (Hønning og Skou, 2003). I moræneler er den forventede omsætning af permanganat større, og der er formentlig også en række andre betydende bestanddele (fx reducerede jernforbindelser), som kan omsætte permanganat.
Der er således på nuværende tidspunkt en række spørgsmål, der er uafklarede i forhold til dosering, effekt, omsætning og kinetik af permanganat, som vil blive belyst i dette kapitel ved en række laboratorieforsøg
2.1.1 Formål
Formålet med laboratorieforsøgene er, at:
- Vurdere sammenhængen mellem den observerede omsætning af organisk stof og permanganatomsætning i forsøg med morænelers sedimenter.
- Vurdere om permanganatomsætning skyldes autodestruktion eller reaktionen med organisk stof.
- Vurdere reaktionsorden for reaktionen mellem organisk stof og permanganat. Hvis det er muligt beregnes nedbrydningsrater til brug for vurderinger og modelberegninger.
2.2 Eksperimentelt
2.2.1 Forsøgsopstilling
Der er benyttet 4 sedimenter med forskellige indhold af ler og organisk kulstofindhold til forsøgene. De 4 sedimenter kommer fra 2 lokaliteter, hvor der er benyttet sediment fra både den oxiderede og reducerede zone. Sedimenterne er beskrevet i afsnit 2.3.
For hver type sediment er der benyttet 5 startkoncentrationer af MnO4-; 5 mg/L, 50 mg/L, 500 mg/L, 5 g/L og 20 g/L, svarende til 5 serier for hver sedimenttype.
Et af grundprincipperne ved denne type flaskeforsøg er, at sediment og vand skal være i fuldstændig kontakt, hvilket opnås, når der er fuldstændig vandmætning og omrøring i flasken, en såkaldt ”slurry”. Den opnås som tommelfingerregel, når vægt-volumen forholdet (g:mL) mellem sediment og væske er mindre eller lig 1:1.
Forsøgene er gennemført som laboratorieskala flaskeforsøg med 20 serier af 100 ml blue cap flasker, med 5 serier for hver type sediment. I hver af de 20 serier indgik der 11 flasker.
Til hver flaske blev der afvejet og tilsat 40 g sediment, hvorefter der blev tilsat permanganat i den ønskede koncentration til flasken var helt fyldt. Flaskerne blev vejet før og efter tilsætning af sediment og permanganat, så den eksakte mængde var kendt. Flaskerne blev herefter hensat i roterkasse i den fastsatte tid. Roterkassen kørte med 1 omdrejning i minuttet.
2.2.2 Materialer
2.2.2.1 Sedimenter
De anvendte morænelers sedimenter er hentet fra henholdsvis Dalumvej, Odense og fra Stavnsbjerggård, Hvidovre (kaldet Hvidovre i det følgende). Karakteristika for sedimenterne er beskrevet i afsnit 2.3. Lokaliteten Dalumvej er undersøgt i både laboratorium og felt og er den gennemgående lokalitet i dette projekt. Dalumvej er yderligere beskrevet i kapitel 4.
2.2.2.2 Permanganatopløsninger
Opløsninger af permanganat blev fremstillet ved opløsning af kaliumpermanganat i postevand fra M&R's laboratorium. Der er anvendt postevand til alle opløsninger frem for destilleret vand, da det har et ionindhold og carbonatbufferkapacitet, som svarer bedre til grundvand i morænelersaflejringer.
2.2.3 Forsøgsoversigt, udførelse og prøvetagning
2.2.3.1 Planlægning af forsøg
Med henblik på at fastlægge den optimale prøvetagningsfrekvens og sedimentmængde blev der udført et mindre testforsøg med sediment fra Dalumvej. Ved gennemførslen af testforsøget blev erfaringer fra tidligere forsøg med lerede sedimenter taget i anvendelse, således at der blev anvendt 80 g sediment. Ved anvendelse af 80 g sediment blev der taget højde for at vægt-volumen forholdet (g:mL) mellem sediment og væske lå omkring 1:1.
Prøvetagningsfrekvensen blev fastlagt ud fra en regnearksmodel i Excel, der antog en 2. ordens reaktion mellem permanganat og sediment. Ud fra modellen blev hovedvægten af prøveudtagene planlagt til at finde sted i de første 12 timer af forsøget.
Resultaterne fra testforsøget viste, at permanganaten blev opbrugt forholdsvis hurtigt i alle flasker med reduceret sediment og i flasker med en lav permanganat koncentration og oxideret sediment. Testforsøgene viste også, at frekvensen af udtag var passende i forhold til reaktionskinetikken.
Ud fra testforsøget blev prøvetagningsfrekvensen fastlagt og det blev besluttet at gennemføre de endelige forsøg med 40 g sediment i stedet for 80 g sediment.
2.2.3.2 Forsøgsoversigt
Der blev samlet benyttet 220 blue cap flasker til gennemførelse af forsøget. Tabel 2.1 viser hvorledes flaskerne blev benævnt i forhold til startkoncentrationen af permanganat.
Tabel 2.1: Benævnelse af de 20 serier i delforsøg 1.
| MnO4- (mg/l) |
Dalumvej oxideret |
Dalumvej reduceret |
Hvidovre Oxideret |
Hvidovre reduceret |
| 5 | A1-A11 | F1-F11 | L1-L11 | Q1-Q11 |
| 50 | B1-B11 | G1-G11 | M1-M11 | R1-R11 |
| 500 | C1-C11 | H1-H11 | N1-N11 | S1-S11 |
| 5000 | D1-D11 | I1-I11 | O1-O11 | T1-T11 |
| 20000 | E1-E11 | J1-J11 | P1-P11 | U1-U11 |
2.2.3.3 Udførelse og prøvetagning
Med hensyn til prøvetagning har forsøget kørt efter høstprincippet. Det vil sige, at flaskerne til specifikke tidspunkter er blevet taget op fra roterkassen, centrifugeret og væskefasen analyseret. Derefter er væskefasen dekanteret fra og en sedimentprøve udtaget. Flaskerne er analyseret ud fra den prøvetagningsplan, der fremgår af tabel 2.2.
Tabel 2.2: Prøvetagningsplan for delforsøg 1.
| Tid | Serie A-F-L-Q |
Serie B-G-M-R |
Serie C-H-N-S |
Serie D-I-O-T |
Serie E-J-P-U |
| 5 min | X | ||||
| 15 min | X | X | |||
| 30 min | X | X | X | X | X |
| 60 min | X | X | X | X | X |
| 2 timer | X | X | X | X | X |
| 4 timer | X | X | X | X | X |
| 8 timer | X | X | X | X | X |
| 12 timer | X | X | X | X | X |
| 24 timer | X | X | X | X | X |
| 48 timer | X | X | X | X | X |
| 4 dage | X | X | X | X | |
| 6 dage | X | X | X | ||
| 20 dage | X | X | X | X | X |
Tabel 2.2 viser, at der for de to lave startkoncentrationer er nogle udtag efter kort tid (5 min) og for de høje startkoncentrationer er der udtag efter 4 og 6 dage for at kunne følge koncentrationen af permanganat bedre. De angivne tider er for det tidspunkt, hvor batchflasken blev taget op fra roterkassen. Der kan godt være sket yderligere reaktion i de ti minutter, flaskerne har stået i centrifugen.
Ved prøveudtag er flaskerne først blevet centrifugeret i 10 minutter ved 1700 rpm, for at få en adskilt væskefase, som kunne prøvetages. Prøvetagning er foregået ved, at låget er taget af og pH målt som det første. Derefter er der udtaget 10 ml væskefase til opbevaring for senere analyser. Der er udtaget mellem 2 og 25 ml væske til analyse for permanganat, jævnfør analysemetoden angivet i bilag A.
Efter permanganat analyse er væskefasen hældt fra og en sedimentprøve udtaget og overført til pyrexrør (figur 2.1). Det udtagne sediment er tørret over nat ved 105 C og efterfølgende knust til pulver. Fra den knuste sedimentprøve er der udtaget prøver til måling af indholdet af organisk kulstof (TOC).

Figur 2.1 Prøvetagning af flasker til analyse for organisk kulstof
2.3 Resultater
2.3.1 Geologi
2.3.1.1 Sedimentkarakteristik, Dalumvej
Sedimentet fra Dalumvej kommer fra en 6” boring udført med sneglebor til 7 meters dybde. Til forsøget er der anvendt sediment fra 2 dybder, fra henholdsvis den oxiderede og den reducerede zone. Det oxiderede sediment er taget fra 3,25-3,75 meter under terræn og det reducerede sediment fra 5,00-5,75 meter under terræn. Det oxiderede sediment er beskrevet som gulbrun moræneler med enkelte små sandlinser, og det reducerede sediment er beskrevet som vådt gråt moræneler med sandlinser (Tabel 2.3).
I forsøget er pH målt på en flaske indeholdende sediment og postevand. pH er 7,33 for det oxiderede sediment og 7,19 for det reducerede sediment. Indholdet af organisk kulstof er på 2,1 g/kg TS (0,21 %) for det oxiderede sediment og 4,1 g/kg TS (0,41 %) for det reducerede sediment.
Tabel 2.3: Karakteristika for de 4 anvendte sedimenter.
| Dalumvej oxideret | Dalumvej reduceret | Hvidovre oxideret | Hvidovre reduceret | |
| Prøvedybde (m.u.t) | 3,25-3,75 | 5,00-5,75 | 1,25-2,00 | 7,50-8,00 |
| Farve | Gulbrun | grå | Brun | Grå |
| pH i postevand | 7,33 | 7,19 | 7,44 | 7,41 |
| COD (g/kg) | 3,9 | 6,0 | 5,5 | 13,7 |
| TOC (%) | 0,21 | 0,41 | 0,21 | 0,41 |
| TOC (g/kg TS) | 2,1 | 4,1 | 2,1 | 4,1 |
| Afvigelse (g/kg TS) | ±0,5 | ±1,0 | ±0,4 | ±0,7 |
2.3.1.2 Sedimentkarakteristik, Hvidovre
Sedimentet fra Hvidovre kommer fra en 4” boring udført med sneglebor til 8 meters dybde. Til forsøget er der anvendt sediment fra 2 dybder repræsenterende den oxiderede og den reducerede zone. Det oxiderede sediment er taget fra 1,25-2,00 meter under terræn og det reducerede sediment fra 7,50-8,00 meter under terræn. Det oxiderede sediment er beskrevet som brun moræneler med enkelte små sandslirer, og det reducerede sediment er beskrevet som gråt moræneler med indhold af sand og sten (Tabel 2.3).
I forsøget er pH målt i en flaske indeholdende sediment og postevand. pH er 7,44 for det oxiderede sediment og 7,41 for det reducerede sediment.
Fra de udtagne sedimentprøver er der målt indhold af organisk kulstof (TOC) på 2,1 g/kg TS (0,21 %) for det oxiderede sediment og 4,1 g/kg TS (0,41 %) for det reducerede sediment.
2.3.2 Omsætning af MnO4-
Koncentrationen af MnO4- er målt i alle flasker. Det omregnes ud fra en kendt startkoncentration af MnO4-og en kendt mængde sediment til en omsætning af MnO4- pr. kg sediment.
Sedimentets naturlige omsætning af permanganat benævnes som NOD (Natural Oxidant Demand). I tidligere udførte forsøg er omsætningen angivet som g KMnO4/kg TS (Hønning og Skou, 2003, Hønning et al., 2004). Da kun permanganaten har interesse vil omsætningen i denne rapport blive angivet som g MnO4-/kg TS. For at kunne sammenholde data med tidligere resultater kan benyttes en omregningsfaktor, hvor resultatet opgivet som MnO4- ganges med 1,33 for at få det tilsvarende resultat i KMnO4.
2.3.2.1 Maksimal omsætning for høje MnO4- koncentrationer
Resultaterne fra det sidste udtag efter 20 dage benyttes som et mål for den maksimale omsætning af permanganat. Omsætningen for de to høje startkoncentrationer (5 og 20 g MnO4-/l) er angivet i tabel 2.4. Tabellen viser, at omsætningen af permanganat er væsentligt højere i det reducerede sediment end i det oxiderede sediment. Samtidig er omsætningen af permanganat højere i sedimentet fra Hvidovre, selv om indholdet af organisk kulstof er det samme på de to lokaliteter (tabel 2.3). Resultaterne viser også, at omsætningen er signifikant højere ved den højere startkoncentration af permanganat.
Tabel 2.4: Maksimal omsætning af MnO4- ved høj startkoncentration. Omsætningen er angivet som NOD i g MnO4-/kg TS og i parentes er angivet omsætningen i % af den maksimale omsætning af MnO4- i forhold til sedimentet.
| NOD (5 g/l) |
Som KMnO4 | NOD (20 g/l) |
Som KMnO4 | |
| Dalumvej oxideret | 3,32 (23) | 4,42 | 7,28 (12) | 9,68 |
| Dalumvej reduceret | 7,68 (56) | 10,21 | 11,53 (20) | 15,33 |
| Hvidovre oxideret | 6,17 (42) | 8,21 | 11,38 (18) | 15,14 |
| Hvidovre reduceret | 13,71 (90) | 18,23 | 19,58 (35) | 26,04 |
2.3.2.2 Maksimal omsætning for lave MnO4- koncentrationer
Den maksimale omsætning for de tre lave startkoncentrationer af MnO4- er angivet i tabel 2.5. Det skal bemærkes, at permanganaten var omsat fuldstændigt i alle flasker med de tre lave startkoncentrationer efter 20 dage, og i de fleste tilfælde blev permanganaten i disse flasker omsat meget tidligt i forløbet.
Dette betyder, at den angivne maksimale omsætning ikke kan tages som udtryk for sedimentets maksimale omsætning af MnO4- ved den pågældende startkoncentration. Det er blot udtryk for, at der ikke var mere permanganat, som kunne omsættes.
Den eneste undtagelse er de to oxiderede sedimenter, hvor der er benyttet en startkoncentration på 500 mg/l. Dette er markeret med fed i tabel 2.5. I disse to tilfælde blev 100 % omsætning af MnO4- først opnået ved det sidste prøveudtag efter 20 dage. Således svarer den målte NOD til den maksimale omsætning af permanganat for de to oxiderede sedimenter ved en startkoncentration på 500 mg/l.
Tabel 2.5: Maksimal omsætning af MnO4- givet som g MnO4-/kg TS ved de tre lave startkoncentrationer af permanganat og i parentes er angivet omsætningen i % af den maksimale omsætning i forhold til sedimentet.
| NOD (5 mg/l) |
NOD (50 mg/l) |
NOD (500 mg/l) |
|
| Dalumvej oxideret | 0,01 (100) | 0,15 (100) | 1,47 (100) |
| Dalumvej reduceret | 0,01 (100) | 0,15 (100) | 1,68 (100) |
| Hvidovre oxideret | 0,01 (100) | 0,16 (100) | 1,47 (100) |
| Hvidovre reduceret | 0,01 (100) | 0,12 (100) | 1,55 (100) |
For startkoncentrationer af permanganat fra 500 mg/l og op til 20g/l, hvor der er reelle målinger af den maksimale omsætning viser resultaterne, at omsætning af permanganat stiger markant når startkoncentrationen øges. Derved kan der heller ikke angives en fast NOD værdi for en bestemt type sediment. NOD værdien er afhængig af den anvendte koncentration af MnO4-. Jo højere koncentration af MnO4-, jo højere er omsætningen af MnO4-.
2.3.3 Kinetik for MnO4-
2.3.3.1 NOD over tid
Resultaterne i afsnit 2.3.2 viste, at der var forskel på hvor meget permanganat der blev omsat i forhold til startkoncentrationen af permanganat. Dette understreges i figur 2.2, som viser omsætningen af permanganat over tid for sedimentet fra Dalumvej (figur 2.2a) og Hvidovre (figur 2.2b). Omsætningen er ikke vist for de to lave startkoncentrationer af permanganat, da permanganat blev omsat så hurtigt, at det ikke kan illustreres grafisk. Hovedparten af permanganatomsætningen sker indenfor de første 4-5 dage, og 50 % af den samlede omsætning sker indenfor de første 12 timer.
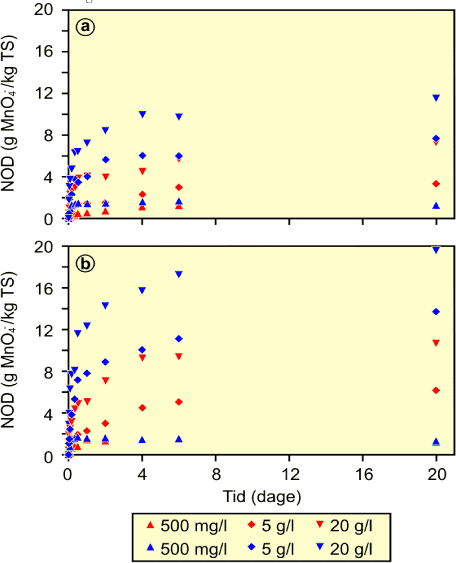
Figur 2.2: Omsætning af permanganat over tid for oxideret og reduceret sediment fra Dalumvej (a) og Hvidovre (b) givet som NOD (g MnO4-/kg TS) over tiden.
Det oxiderede sediment er angivet ved (![]() ), og det reducerede sediment er angivet ved (
), og det reducerede sediment er angivet ved (![]() ).
).

Figur 2.3: Prøveudtag efter 2 og 4 timer, for batchflasker med startkoncentration på 500 mg/l. Rækkefølgen fra venstre mod højre er Dalumvej oxideret, Dalumvej reduceret, Hvidovre oxideret og Hvidovre reduceret.
Forskellen i omsætning for de 4 sedimenttyper er illustreret på figur 2.3, der viser flaskerne efter henholdsvis 2 og 4 timer for startkoncentration på 500 mg/l. Efter 4 timer er permanganaten omsat (lys lilla og klar) i de to flasker med sediment fra Hvidovre. For Dalumvej er omsætningen af permanganat i det oxiderede sediment begrænset (mørk lilla), mens der sker en markant omsætning (lyslilla) for det reducerede sediment.
2.3.3.2 Kinetik for omsætning af permanganat
Omsætningen af permanganat antages at følge en 1. ordens reaktion. For at analysere batchforsøgene benyttes en empirisk grafisk procedure, der er videre beskrevet i bilag B. Den grafiske repræsentation af analysen er illustreret i figur 2.4, der viser den naturlige logaritme af den normerede permanganatkoncentration over tid.
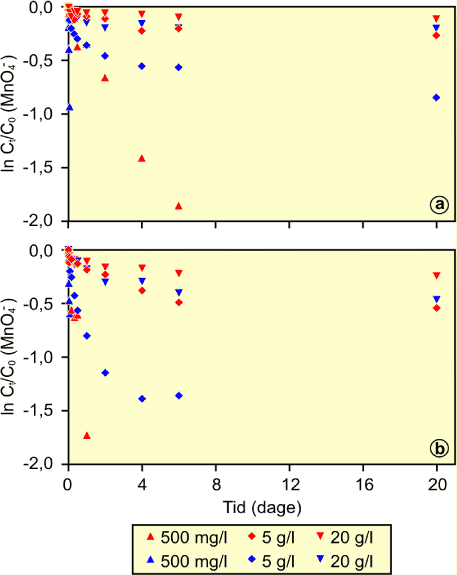
Figur 2.4: Den naturlige logaritme af Ct/C0 for oxideret og reduceret sediment fra Dalumvej (a) og Hvidovre (b) over tid. Det oxiderede sediment er angivet ved (![]() ),
og det reducerede sediment er angivet ved (
),
og det reducerede sediment er angivet ved (![]() ).
).
For at omsætningen af permanganat skal følge en 1. ordens reaktion skal de viste kurver være lineære. Figur 2.4 viser tydeligt, at omsætningen af permanganat ikke for nogen koncentrationer følger en 1. ordens reaktionskinetik over hele perioden på 20 dage.
Den grafiske analyse blev gentaget for de første 8 timer (figur 2.5). Omsætningen af permanganat i de første 1-8 timer ser ud til at følge en 1. ordens reaktion. Raterne er angivet i tabel 2.6 og er yderligere beskrevet i bilag B med tilhørende r2-værdier. Raten er meget afhængig af den anvendte koncentration af permanganat, hvor den bliver højere for en lavere permanganatkoncentration. For de høje permanganatkoncentrationer ses en tendens til, at der sker en stor omsætning af permanganat over den første time, hvorefter der sker en svag omsætning mellem 1 og 8 timer. Raterne i tabel 2. 6 er gennemsnitsrater over de første 8 timer, så raterne kan sammenlignes indbyrdes, men for de høje koncentrationer kunne man overveje at bruge en rate for omsætningen den første time efterfulgt af en anden rate for tiden mellem 1 og 8 timer.
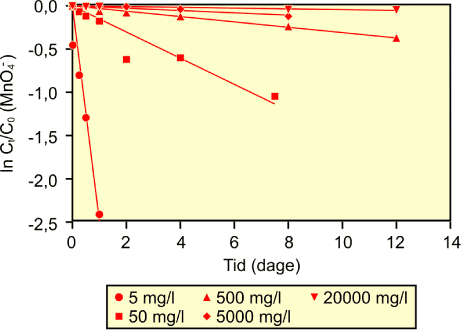
Figur 2.5: Den naturlige logaritme af Ct/C0 for oxideret sediment fra Dalumvej over tiden. Koncentrationerne angiver startkoncentration af MnO4-. Figuren er et eksempel på hvorledes kinetikkonstanterne i tabel 2.6 er fundet.
Tabel 2.6: 1. ordens kinetik konstanter givet i timer-1 for omsætningen af permanganat for op til 8 timer fra start.
| MnO4- (mg/l) |
Dalumvej oxideret | Dalumvej reduceret | Hvidovre oxideret | Hvidovre reduceret |
| 5 | 2,49 | - | 1,37 | - |
| 50 | 0,15 | >2,19 | 0,28 | >3,12 |
| 500 | 0,03 | 0,51 | 0,09 | 0,35 |
| 5000 | 0,01 | 0,04 | 0,02 | 0,06 |
| 20000 | 0,005 | 0,02 | 0,01 | 0,02 |
> Ratekonstant regnet på første prøveudtag, da MnO4- var omsat derefter.
- Ikke muligt at måle ratekonstant, da MnO4- var omsat ved første prøveudtag.
2.3.4 Organisk kulstof
2.3.4.1 Teoretisk omsætning af organisk kulstof
Naturligt forekommende reducerede bestanddele i sedimentet kan omsætte en stor del af den tilsatte permanganat. Et modelstof, C7H8O4, er foreslået som repræsentant for organisk kulstof. Den fuldstændige omsætning af det anvendte modelstof med permanganat er foreslået i Hønning og Skou (2003):
28 MnO4- + 3 C7H8O4 + 28 H+ → 28 MnO2(s) + 21 CO2 + 26 H2O
I naturlige miljøer (3,5<pH<12) vil 28 mol permanganat reagere med 3 mol modelstof, svarende til at 4 mol permanganat reagerer med 3 mol organisk kulstof. Udtrykt i masser svarer dette til, at 119 g MnO4- reagerer med 9 g organisk kulstof, hvilket giver et reaktionsforhold i g/g på 13,2:1.
Sammenholdes det målte indhold af organisk kulstof i de 4 typer sedimenter med det teoretiske reaktionsforhold kan den nødvendige mængde permanganat (NOD) til oxidation af sedimentets indhold af organisk kulstof beregnes. Disse udregninger er samlet i tabel 2.7.
Tabel 2.7: Teoretisk NOD-værdi, hvis det forudsættes, at al NOD tilskrives organisk kulstof.
| Dalumvej oxideret | Dalumvej reduceret | Hvidovre oxideret | Hvidovre reduceret | |
| TOC (g/kg TS) | 2,1 | 4,1 | 2,1 | 4,1 |
| Standard afvigelse (g/kg TS) |
±0,5 | ±1,0 | ±0,4 | ±0,7 |
| Teoretisk NOD (g/kg TS) | 27,7 | 54,1 | 27,7 | 54,1 |
| Standard afvigelse (g/kg TS) |
±6,6 | ±13,2 | ±5,3 | ±9,2 |
Udregningerne kan også vendes den anden vej. Med den kendte mængde af tilsat permanganat kan reaktionsforholdet (13,2) benyttes til at udregne hvor meget organisk kulstof der maksimalt kan oxideres af permanganaten (tabel 2.8). Det fremgår, at det kun er ved de to høje startkoncentrationer af permanganat, at man vil forvente at se en målbar reduktion i indholdet organisk kulstof.
Tabel 2.8: Teoretisk omsætning af organisk kulstof (TOC), omregnet til g/kg TS, i en flaske.
| MnO4- (mg/l) |
MnO4- (ml) |
MnO4- (mg) |
TOC omsætning (mg) |
TOC omsætning (g/kg TS) |
| 5 | 110 | 0,55 | 0,04 | 0,001 |
| 50 | 110 | 5,5 | 0,42 | 0,01 |
| 500 | 110 | 55 | 4,2 | 0,12 |
| 5000 | 110 | 550 | 41,7 | 1,16 |
| 20000 | 110 | 2200 | 166,7 | 4,63 |
2.3.4.2 Måling af organisk kulstof
Der er målt indhold af organisk kulstof på udvalgte prøver fra alle 20 analyseserier. Hovedvægten af målingerne er lagt på sedimentet fra Dalumvej. For de to sedimenter fra Hvidovre er der målt på 5 flasker fra hver af de 10 serier.
For det oxiderede sediment fra Dalumvej er der for alle permanganatkoncentrationer målt et indhold af organisk kulstof på omkring 0,8 g/kg TS, svarende til en omsætning på 1,3 g/kg TS eller 60 % af den samlede mængde organisk kulstof (tabel 2.9). Omsætningen af organisk kulstof over tiden for den høje startkoncentration af permanganat er vist i figur 2.6, der illustrerer hvorledes det organiske kulstof bliver omsat indenfor de første 24 timer i det oxiderede sediment. I det reducerede sediment fra Dalumvej er omsætningen af organisk kulstof mere afhængig af den anvendte permanganatkoncentration. Figuren viser, at omsætningen af organisk kulstof er større ved en højere koncentration af permanganat, og at omsætningen for det reducerede sediment ligeledes sker indenfor de første 10-12 timer. Omsætningen af organisk kulstof ligger mellem 45 og 65 % (tabel 2.9).
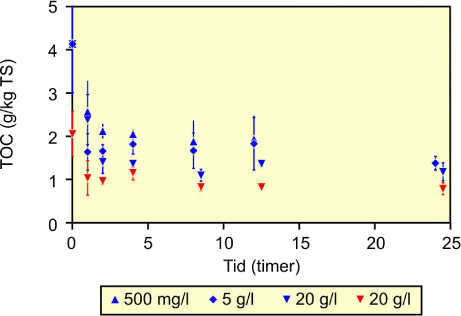
Figur 2.6: Måling af organisk kulstof på oxideret og reduceret sediment fra Dalumvej. Startkoncentrationen af permanganat i det oxiderede sediment er angivet ved
(![]() ) og i det reducerede sediment ved (
) og i det reducerede sediment ved (![]() ).
).
Målingerne på sedimentet fra Hvidovre viser, at der for de tre laveste koncentrationer af permanganat ikke er målt nogen omsætning af organisk kulstof. For det oxiderede sediment er der kun målt en omsætning af organisk kulstof for den høje startkoncentration på 20 g MnO4-/l, hvor der er målt en omsætning på 0,8 g/kg TS, svarende til 40 % af den samlede mængde organiske kulstof i sedimentet. For det reducerede sediment fra Hvidovre er der for de to høje startkoncentrationer målt en TOC omsætning på op til 1,7 g/kg TS, svarende til 40 % af den samlede mængde organiske kulstof (tabel 2.9).
Beregningerne i tabel 2.8 viste, at de høje koncentrationer af permanganat teoretisk kunne omsætte en stor del af det organiske kulstof. Resultaterne har vist, at der er omsat en stor del organisk kulstof. Spørgsmålet i denne forbindelse er hvorvidt denne omsætning kan skyldes permanganaten eller sagt på en anden måde, om omsætning af permanganat kan skyldes reaktion med det organiske kulstof. Sammenligningen er sat op for sedimenter fra Dalumvej og Hvidovre i tabel 2.9, der viser de målte omsætninger af permanganat og hvad det vil svare til i omsat organisk kulstof. For sedimentet fra Dalumvej viser tabellen, at den mængde permanganat, som er omsat, ikke kan forklare den mængde organisk kulstof, der er blevet omsat ved reaktionen. Omsætning af organisk kulstof ud fra den målte omsætning af permanganat er markant lavere end den aktuelle omsætning. For Hvidovre sedimentet er der en bedre overensstemmelse mellem den målte omsætning af organisk kulstof og den omsætning, der var forventet ud fra omsætningen af permanganat.
Tabel 2.9: Omsætning af organisk kulstof ud fra målt omsætning af permanganat for sediment fra Dalumvej og Hvidovre samt målt omsætning af organisk kulstof givet i g/kg TS.
| MnO4- (mg/l) |
NOD (g/kg TS) |
Omsætning TOC ud fra NOD (g/kg TS) |
Målt omsætning af TOC (g/kg TS) |
| Dalumvej – oxideret | Start TOC 2,1 g/kg TS | ||
| 5 | 0,01 | 0,001 | 1,3 |
| 50 | 0,15 | 0,01 | 1,3 |
| 500 | 1,47 | 0,11 | 1,3 |
| 5000 | 3,32 | 0,25 | 1,3 |
| 20000 | 7,28 | 0,55 | 1,3 |
| Dalumvej – reduceret | Start TOC 4,1 g/kg TS | ||
| 5 | 0,01 | 0,001 | 1,8 |
| 50 | 0,15 | 0,01 | 1,8 |
| 500 | 1,68 | 0,13 | 2,1 |
| 5000 | 7,68 | 0,58 | 2,5 |
| 20000 | 11,53 | 0,87 | 2,8 |
| Hvidovre – oxideret | Start TOC 2,1 g/kg TS | ||
| 5 | 0,01 | 0,001 | 0,0 |
| 50 | 0,16 | 0,01 | 0,0 |
| 500 | 1,47 | 0,11 | 0,0 |
| 5000 | 6,17 | 0,47 | 0,0 |
| 20000 | 11,38 | 0,86 | 0,8 |
| Hvidovre – reduceret | Start TOC 4,1 g/kg TS | ||
| 5 | 0,01 | 0,001 | 0,0 |
| 50 | 0,12 | 0,01 | 0,0 |
| 500 | 1,55 | 0,12 | 0,0 |
| 5000 | 13,71 | 1,04 | 1,7 |
| 20000 | 19,58 | 1,48 | 1,7 |
I sammenhæng med resultaterne i tabel 2.9 kan det diskuteres, hvorvidt det anvendte reaktionsforhold for reaktionen mellem organisk kulstof og permanganat er korrekt. I denne rapport er anvendt et modelstof C7H8O4 til at repræsentere det organiske stof i sedimentet. Anvendelsen af et modelstof er selvfølgelig en forsimpling, da det organiske stof består af mange komponenter og kan variere fra sediment til sediment. Tabellen er lavet på antagelsen af, at det organiske kulstof i sedimentet står for hovedparten af permanganatforbruget. Det kan derfor diskuteres om den målte NOD kun skyldes reaktionen med det organiske kulstof, idet sedimenter kan indeholde mange andre reaktive bestanddele, specielt i de reducerede sedimenter.
Sedimenterne fra Dalumvej og Hvidovre indeholder flere reaktive bestanddele, hvilket ses ud fra COD tallene i tabel 2.3. Ved COD analysen sker der en meget kraftig oxidation, der kan oxidere flere bestanddele og mere organisk kulstof end permanganat. Derfor er COD analysen en maksimal oxidation af alle bestanddelene i sedimentet. COD tallet kan omregnes til en tilsvarende maksimal NOD-værdi for sedimentet, der kan sammenlignes med NOD for permanganat. Dette gøres ved at gange COD tallene med 4, idet det kemiske iltforbrug (g O2/kg sediment) svarer til ca. ¼ af massen af permanganat (DS 275, 1984 og Linde-Jensen et al., 1976), hvorved det ses, at de tilsvarende NOD tal er mere end dobbelt så høje som de målte NOD-værdier. Dette viser, at der er flere bestanddele og mere organisk kulstof tilbage i sedimentet, som ikke er blevet oxideret af permanganaten. Da disse bestanddele sandsynligvis sidder forskelligt bundet på sedimentet kan det forklare, at der er en forskel på hvor meget permanganaten oxiderer og derved den målte NOD-værdi.
Ud fra de teoretiske beregninger var det forventet, at omsætningen af organisk kulstof ikke var målbar for de lavere koncentrationer af permanganat. En mulig forklaring på, at man alligevel finder en markant omsætning kunne være, at det målte initielle indhold af organisk kulstof er for højt på Dalumvej. I senere forsøg findes der koncentrationer af organisk kulstof i oxideret sediment fra de tilstødende dybder, som er betydeligt lavere (0,9 og 1,5 g/kg TS i forhold til 2,1 g/kg TS). Det samme fænomen gør sig gældende for det reducerede sediment (3,3 g/kg TS i forhold til 4,1 g/kg TS). De målte variationer i startværdien for organisk kulstof kan skyldes, at sedimentet ikke er blevet homogeniseret inden starten af forsøget. For eksempel er der i forsøgene med oxideret sediment fra Dalumvej anvendt sediment fra 3,0-4,0 meter under terræn, hvor de anvendte sedimentprøver er udtaget i 3 forskellige poser og anvendt fra pose til pose. Der er målt tre forskellige startværdier af TOC for det oxiderede sediment (0,9-2,1 g/kg TS), hvorfor variation i baggrundskoncentrationen af organisk kulstof formentlig er årsag til sløringen af den forventede årsagssammenhæng.
Version 1.0 Februar 2006, © Miljøstyrelsen.