[Forside] |
Økotoksikologisk vurdering af begroningshindrende biocider og biocidfrie bundmalinger |
Indholdsfortegnelse
2. Kobber
2.1 Kobberkoncentrationer målt ved lystbådehavne
2.2 Omdannelse og biotilgængelighed af kobber i vand og sediment
2.3 Frigivelse og binding af kobber i sedimenter
2.4 Bioakkumulerbarhed og akvatisk toksicitet
2.4.1 Bioakkumulerbarhed
2.4.2 Toksicitet over for akvatiske organismer
2.5 Vurdering af kobber
3. Sea-Nine
3.1 Fysisk-kemiske egenskaber
3.2 Biologisk nedbrydning af DCOI i det akvatiske miljø
3.2.1 Primær nedbrydning i havvand
3.2.2 Mineralisering og nedbrydningsprodukter i aerobt sediment
3.2.3 Mineralisering og nedbrydningsprodukter i anaerobt sediment
3.2.4 Omsætning og skæbne af DCOI i havnebassin
3.3 Bioakkumulerbarhed og akvatisk toksicitet
3.3.1 Bioakkumulerbarhed
3.3.2 Toksicitet over for akvatiske organismer
3.4 Risikovurdering af DCOI
4. Zinkpyrithion
4.1 Fysisk-kemiske egenskaber
4.2 Abiotisk nedbrydning
4.3 Biologisk nedbrydning af zinkpyrithion i det akvatiske miljø
4.3.1 Mineralisering og nedbrydningsprodukter i aerobt sediment
4.3.2 Mineralisering og nedbrydningsprodukter i anaerobt sediment
4.4 Toksicitet over for akvatiske organismer
4.5 Vurdering af zinkpyrithion og nedbrydningsprodukter
4.6 Risikovurdering af zinkpyrithion
5. Biocidfrie malinger
5.1 Undersøgelser af biocidfrie malinger
5.2 Udvaskningsforsøg og økotoksikologiske test
5.3 Vurdering af biocidfrie malinger
Bilag 1: Model til beregning af eksponeringskoncentrationer (PEC)
Bilag 2: Undersøgelse af mineraliseringen af DCOI og zink-pyrithion i marine sedimenter
Bilag 4: Økotoksikologiske data vedrørende DCOI
Bilag 5: Økotoksikologiske data vedrørende zinkpyrithion
Forord
Denne rapport er udarbejdet i forbindelse med projektet "Indledende vurdering af mekanisk rensning som alternativ til biocidholdig bundmaling samt vurdering af biocidholdige antibegroningsmidler med forventet reduceret miljøbelastning". Projektet er gennemført for midler fra Rådet for genanvendelse og mindre forurenende teknologi. Det samlede projekt er udført af Dansk Sejlunion, J.C. Hempel's Skibsfarve-Fabrik A/S (i det følgende refereret til som Hempel) samt VKI med Eva Bie Kjær, Hempel, som projektleder.
Den nærværende rapport er udarbejdet af VKI. Målet med denne del af projektet har været:
- Økotoksikologiske vurderinger af biociderne kobber, Sea-Nine og zinkpyrithion på baggrund af eksisterende data og nye laboratorieforsøg, og
- Økotoksikologiske vurderinger af udvaskningsvand fra paneler påført de biocidfrie malinger, der blev anvendt i projektet.
Projektet har været fulgt af en styregruppe, der har afholdt 8 styregruppemøder i løbet af projektperioden. Denne styregruppe havde følgende medlemmer:
| Frank Jensen (formand) | Miljøstyrelsen |
| Eva Bie Kjær (sekretær) | J.C. Hempel's Skibsfarve-Fabrik A/S |
| Torben Madsen | VKI |
| Steen Wintlev-Jensen | Dansk Sejlunion |
| Carl Gerstrøm | Dansk Sejlunion |
| Anders Stubkjær | Kommunernes Landsforening |
| Christian A. Jensen | Amtsrådsforeningen |
| Jens A. Jacobsen | Danmarks Miljøundersøgelser |
| Jan B. Nielsen | Miljøkontrollen |
| G. Høpner Petersen | Zoologisk Museum |
| Peter Györkös | Miljøstyrelsen |
| Alf Aagaard | Miljøstyrelsen |
| Tim Blangsted J.C. | Hempel's Skibsfarve-Fabrik A/S |
| Martin Christoffersen | J.C. Hempel's Skibsfarve-Fabrik A/S |
| Jane Dormon | J.C. Hempel's Skibsfarve-Fabrik A/S |
| Chris Dam | J.C. Hempel's Skibsfarve-Fabrik A/S |
| Torsten Rasmussen | J.C. Hempel's Skibsfarve-Fabrik A/S |
| Johs. Egede Olsen | J.C. Hempel's Skibsfarve-Fabrik A/S |
| Susanne Holm Faarbæk | J.C. Hempel's Skibsfarve-Fabrik A/S |
Ved projektets afslutning deltog desuden Pia Ølgaard Nielsen, Miljøstyrelsen.
Styregruppens medlemmer takkes for et konstruktivt samarbejde under udførelsen af projektet.
I forbindelse med udarbejdelsen af rapporten har der været taget kontakter til Nordox (kobber), Rohm and Haas (Sea-Nine) og Arch Chemicals (zinkpyrithion), der takkes for samarbejdet og en konstruktiv dialog.
Hørsholm, den 1. november 1999,
Torben Madsen, VKI
Sammenfatning
Formålet med denne undersøgelse har været at vurdere miljøfarligheden af aktivstofferne kobber, 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on, (DCOI) og zinkpyrithion og af stoffer, der udludes fra bundmalinger uden biocider.
Biotilgængeligheden af kobber er en nøgleparameter for vurderingen af metallets giftighed i vandmiljøet. Kompleksbinding af kobber til organiske stoffer reducerer normalt biotilgængeligheden, men denne binding afhænger tilsyneladende af strukturen af det organiske stof. Biotilgængeligheden af kobber i akvatiske sedimenter afhænger af metallets speciering, af sedimentet og af de eksponerede organismers fysiologi og fødevalg. Det er f.eks. vist, at vandlevende organismer lettere optager metaller, der er bundet til let fordøjelig føde, end metaller bundet til svært omsættelig føde. Biotilgængeligt kobber er meget giftigt over for vandlevende organismer. En permanent immobilisering af kobber kan kun forekomme ved binding til uforstyrrede, iltfattige sedimenter. Havnesedimenter er typisk iltfattige og har et højt indhold af sulfider, som vil binde kobber. Derfor forventes biotilgængeligheden af kobber at være lav i havnesedimenter. Kobber kan frigives ved klapning af sediment, og typisk for klapningspladserne i Danmark bliver sedimentet spredt af strøm og bølgepåvirkning. Som grundstof er kobber ikke nedbrydeligt. Kobbers potentielle giftvirkning i vandmiljøet reduceres ved binding til organiske stoffer og sedimenter, der medfører, at den aktuelle biotilgængelighed af kobber er lav. Forstyrrelser af sedimentet, og de deraf følgende ændrede iltforhold, vil imidlertid kunne remobilisere bundet kobber, og sådanne ændringer vil muligvis kunne medføre effekter over for følsomme organismer i nærheden af havneområder og klapningspladser.
DCOI omdannes hurtigt til nedbrydningsprodukter i havvand, hvor der er fundet halveringstider på 11 og 14 timer. Omdannelsen af DCOI er væsentligt hurtigere i akvatisk sediment, idet der er påvist halveringstider på mindre end 1 time. Den biologiske nedbrydning af DCOI blev undersøgt i to danske marine sedimenter med forskellig tekstur. Mineraliseringen til kuldioxid i et lerholdigt og et sandet sediment udgjorde henholdsvis 13 og 24% af den tilsatte 14C i løbet af 42 dages aerob inkubering ved 15°C. Mineraliseringen under anaerobe, sulfatreducerende forhold blev undersøgt i det lerholdige sediment og udgjorde 14% af den tilsatte 14C efter 56 dages inkubering ved 15°C. DCOI er meget giftigt over for vandlevende organismer, idet de laveste effektkoncentrationer (EC/LC50) er lavere end 10 µg/L. Den akvatiske toksicitet af det stabile nedbrydningsprodukt N-(n-octyl) malonaminsyre er flere størrelsesordener mindre, idet de laveste effektkoncentrationer (LC50) vurderes at være mellem 90 og 160 mg/L. Laboratorieforsøg med dosering af havvand og sediment med DCOI viste, at nedbrydning og sorption eliminerede den akutte akvatiske toksicitet af vandprøver over en periode på mindre end en dag. På basis af de foreliggende data for effekter på vandlevende organismer blev nul-effekt-koncentrationer (Predicted No-Effect-Concentration, PNEC) estimeret til 0,06 µg/L for DCOI og 90 µg/L for N-(n-octyl) malonaminsyre. PNEC for N-(n-octyl) malonaminsyre anses for at være repræsentativ for de øvrige nedbrydningsprodukter fra omdannelsen af DCOI. Til beregning af eksponeringskoncentrationer (Predicted Environmental Concentration, PEC) blev opstillet en model, der bygger på principper, der anbefales i EU's "Technical Guidance Document" for risikovurdering. Den anvendte model er ikke valideret over for målte koncentrationer i havnemiljøer eller sejlruter. Forudsætningerne for beregning af PEC blev defineret i form af "realistiske worst-case scenarier", der medfører, at de beregnede PEC-værdier i praksis kun sjældent vil overskrides. De højeste beregnede eksponeringskoncentrationer for DCOI var PEC (vand), der var 0,52 µg/L i en lystbådehavn og 0,006 µg/L i en befærdet sejlrute uden for havnen. For nedbrydningsprodukterne var PEC (vand) 2,2 µg/L i lystbådehavnen og 0,047 µg/L i sejlruten uden for havnen. På baggrund af værdierne for PNEC og PEC blev risikokvotienter (PEC/PNEC) for DCOI beregnet til 8,7 for lystbådehavnen og 0,1 for sejlruten uden for havnen. De beregnede risikokvotienter for summen af nedbrydningsprodukterne fra omdannelsen af DCOI var 0,02 i lystbådehavnen og 0,0005 i sejlruten uden for havnen. På grund af den korte halveringstid i vand og sediment vil DCOI sandsynligvis hurtigt blive elimineret, når lystbådene tages op af vandet ved sejlsæsonens afslutning.
Zinkpyrithion omdannes meget hurtigt ved fotolyse og biologisk nedbrydning. Undersøgelser af nedbrydningen af zinkpyrithion i to danske sedimenter viste, at mineralisering til kuldioxid i et lerholdigt og et sandet sediment udgjorde henholdsvis 2,8 og 5% af den tilsatte 14C under aerobe forhold. Mineraliseringen under anaerobe, sulfatreducerende forhold udgjorde 3,5% af den tilsatte 14C i det lerholdige sediment. Ligesom DCOI er zinkpyrithion meget giftigt over for vandlevende organismer, idet de laveste effektkoncentrationer (EC/LC50) er lavere end 10 µg/L. Giftigheden af de stabile nedbrydningsprodukter omadin sulfonsyre og pyridin sulfonsyre er flere størrelsesordener mindre, idet de laveste effektkoncentrationer (LC50) for disse forbindelser er henholdsvis 36 og 29 mg/L. Laboratorieforsøg med dosering af havvand og sediment med zinkpyrithion viste, at nedbrydning og sorption eliminerede den akutte akvatiske toksicitet af vandprøver over en periode på mindre end en dag. De foreliggende data for effekter på vandlevende organismer giver grundlag for estimering af nul-effekt-koncentrationer (PNEC) på 0,1 µg/L for zinkpyrithion og 30 µg/L for stabile nedbrydningsprodukter repræsenteret ved pyridin sulfonsyre. Ved anvendelse af de samme "realistiske worst-case scenarier" som for DCOI blev de højeste eksponeringskoncentrationer (PEC, vand) for zinkpyrithion beregnet til mellem 0,56 og 1,7 µg/L i lystbådehavnen og mellem 0,0053 og 0,022 µg/L i sejlruten uden for havnen. For summen af nedbrydningsprodukterne var PEC (sediment, porevand) mellem 1,6 og 2,7 µg/L i lystbådehavnen og mellem 0,037 og 0,042 µg/L i sejlruten. På baggrund af værdierne for PNEC og PEC blev risikokvotienter (PEC/PNEC) for zinkpyrithion beregnet til mellem 5,6 og 17 for lystbådehavnen og mellem 0,05 og 0,22 for sejlruten. Risikokvotienterne for summen af nedbrydningsprodukterne fra omdannelsen af zinkpyrithion var 0,05-0,09 for lystbådehavnen og 0,0012-0,0014 for sejlruten. De laveste risikokvotienter er baseret på PEC værdier, hvor fotolytisk omdannelse af zinkpyrithion er antaget i beregningerne. De højeste risikokvotienter er derimod baseret på PEC-værdier, hvor der helt ses bort fra fotolytisk omdannelse. Ligesom DCOI vil zinkpyrithion sandsynligvis hurtigt blive elimineret, når lystbådene tages op af vandet ved sejlsæsonens afslutning, som følge af den korte halveringstid i vand og sediment.
Effekter på vandlevende organismer af vandprøver fra udvaskningsforsøg med de biocidfrie malinger, den epoxy-baserede High Protect 35651 og den eksperimentelle silikone-holdige 86330 maling, blev undersøgt i test med den marine grønalge Skeletonema costatum og det marine krebsdyr Acartia tonsa. En tilsvarende undersøgelse blev gennemført med en organotin-baseret bundmaling, Hempel's Antifouling Nautic 76800. Vandprøver fra udvaskningsforsøget med High Protect 35651 medførte ingen hæmning af væksten af S. costatum, og kroniske effekter på A. tonsa blev kun observeret i ufortyndet udvaskningsvand (nul-effekt-koncentration, NOEC = 100 mL/L). Vandprøver fra udvaskningsforsøget med den eksperimentelle 86330 maling udviste toksicitet over for S. costatum samt i akutte og kroniske test med A. tonsa (NOEC, akut <100 mL/L; NOEC, kronisk <10 mL/L). Imidlertid er der forhold, der tyder på, at variationer af produktionsteknisk eller påføringsmæssig art kan påvirke udludningen af stoffer fra denne type maling. Disse forhold bør undersøges nærmere, inden der foretages en endelig vurdering af malingens miljøegenskaber. Udvaskningsvandet fra begge de biocidfrie malinger havde markant mindre effekt end vandprøver fra tilsvarende forsøg med den organotin-baserede Hempel's Antifouling Nautic 76800. Udvaskningsvand fra High Protect 35651 og den eksperimentelle 86330 medførte kroniske NOEC-værdier for A. tonsa, der var henholdsvis mindst 1.000 og 100 gange højere end de tilsvarende NOEC for udvaskningsvand fra den organotin-baserede maling.
Summary
The objective of this investigation was to assess the environmental hazards of the active substances, copper, 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on (DCOI) and zinc pyrithione and to assess the environmental hazards of substances that leach from antifouling paint without biocides.
The bioavailability of copper is the key parameter for the assessment of the toxicity of the metal in the aquatic environment. Sequestration of copper to organic matter normally reduces the bioavailability, however, this sequestration is apparently dependent on the composition of the organic materials. The bioavailability of copper in aquatic sediments depends on the speciation of the metal, on the sediment and on the physiology and food selection of the exposed organisms. It has been demonstrated that metals sequestrated to easily digested food are absorbed more easily by aquatic organisms than metals sequestrated to indigestible food. Bioavailable copper is very toxic to aquatic organisms. A permanent immobilization of copper may occur only by sequestration to undisturbed, anoxic sediments. Harbour sediments are usually anoxic and have a high content of sulphides that sequestrate to copper. Therefore, the bioavailability of copper in harbour sediments is expected to be low. Copper may be released by disposal of sediment, and on the Danish dumping sites the sediment is usually scattered by water current and waves. As an element, copper is not degradable. The potential toxic effect of copper to the aquatic environment is reduced by sequestration to organic compounds and sediments, which means that the actual bioavailability of copper is low. Disturbances of the sediment, and the consequent changes in the oxygen conditions, may remobilize sequestrated copper, and such changes may cause effects on sensitive organisms in the vicinity of harbour areas and dumping sites.
DCOI is rapidly transformed into metabolites in sea water, where half-lives of 11 and 14 hours were found. The transformation of DCOI is very much quicker in aquatic sediment as half-lives of less than 1 hour have been found. The biodegradation of DCOI was examined in two Danish marine sediments with different textures. The mineralization into CO2 in a clayey and sandy sediment represented 13% and 24%, respectively, of the added 14C during an aerobic incubation of 42 days at a temperature of 15°C. The mineralization under anaerobic, sulphate-reducing conditions was examined in the clayey sediment and represented 14% of the added 14C after an incubation of 56 days at a temperature of 15°C. DCOI is very toxic to aquatic organisms as the lowest effect concentrations (EC/LC50) are lower than 10 µg/L. The aquatic toxicity of the stable metabolite, N-(n-octyl) malonamic acid, is several orders of magnitude lower as the lowest effect concentrations (LC50) are estimated to be between 90 and 160 mg/L. Laboratory tests performed with sea water and sediment containing DCOI showed that degradation and sorption eliminated the acute, aquatic toxicity of water samples in less than one day. On the basis of data available regarding effects on aquatic organisms, Predicted No-Effect-Concentrations (PNEC) were estimated at 0.06 µg/L for DCOI and 90 µg/L for N-(n-octyl) malonamic acid. PNEC for N-(octyl) malonamic acid is considered to be representative of the other metabolites from the transformation of DCOI. To calculate exposure concentrations (Predicted Environmental Concentration, PEC), a model was set up that was based on principles recommended by the EU's "Technical Guidance Document" for risk assessment. The used model was not validated as regards concentrations in harbours and navigation routes. The basis of the calculation of PEC was defined by way of realistic worst-case scenarios, which means that the calculated PEC values are seldom exceeded, in practice. The highest calculated exposure concentrations for DCOI were PEC (water), which was 0.52 µg/L in a pleasure craft harbour and 0.006 µg/L in a busy navigation route outside the harbour. As for the metabolites, PEC (water) was 2.2 µg/L in the pleasure craft harbour and 0.047 µg/L in the navigation route outside the harbour. On the basis of the values for PNEC and PEC, the risk quotients (PEC/PNEC) for DCOI were calculated at 8.7 for the pleasure craft harbour and at 0.1 for the navigation route outside the harbour. The calculated risk quotients of the total amount of metabolites from the transformation of DCOI were 0.02 in the pleasure craft harbour and 0.0005 in the navigation route outside the harbour. Because of the short half-life in water and sediment, DCOI will most likely be rapidly eliminated as soon as the pleasure crafts are taken out of the water at the end of the sailing season.
By photolysis and biodegradation zinc pyrithione is transformed very rapidly. Analyzes of the degradation of zinc pyrithione in two Danish sediments showed that mineralization into CO2 in a clayey and sandy sediment represented 2.8 and 5%, respectively, of the added 14C under aerobic conditions. The mineralization under anaerobic, sulphate-reducing conditions represented 3.5% of the added 14C in the clayey sediment. Like DCOI, zinc pyrithione is very toxic to aquatic organisms as the lowest effect concentrations (EC/LC50) are less than 10 µg/L. The toxicity of the stable metabolites, omadine sulfonic acid and pyridine sulfonic acid, is several orders of magnitude lower as the lowest effect concentrations (LC50) of these compounds are 36 and 29 mg/L, respectively. Laboratory tests performed with sea water and sediment containing zinc pyrithione showed that degradation and sorption eliminated the acute, aquatic toxicity of water samples in less than one day. The available data regarding effects on aquatic organisms form the basis of an estimation of PNEC values at 0.1 µg/L for zinc pyrithione and 30 µg/L for stable metabolites represented by pyridine sulfonic acid. By using the same realistic worst-case scenarios as for DCOI, the highest exposure concentrations (PEC, water) of zinc pyrithione were calculated to be between 0.56 and 1.7 µg/L for the pleasure craft harbour and between 0.0053 and 0.022 µg/L for the navigation route outside the harbour. For the total amount of metabolites PEC (sediment, pore water) was between 1.6 and 2.7 µg/L in the pleasure craft harbour and between 0.037 and 0.042 µg/L in the navigation route. On the basis of the values for PNEC and PEC, the risk quotients (PEC/PNEC) for zinc pyrithione were calculated to be between 5.6 and 17 for the pleasure craft harbour and between 0.05 and 0.22 for the navigation route. The risk quotients of the total amount of metabolites from the transformation of zinc pyrithione were 0.05-0.09 for the pleasure craft harbour and 0.0012-0.0014 for the navigation route. The lowest risk quotients are based on PEC values, for which transformation of zinc pyrithione by photolysis is included in the calculations. The highest risk quotients are, however, based on PEC values in which transformation by photolysis is not taken into account. Like DCOI, zinc pyrithione will most likely be rapidly eliminated as soon as the pleasure crafts are taken out of the water at the end of the sailing season, in consequence of the short half-life in water and sediment.
Effects on aquatic organisms of water samples from leaching tests with paints containing no biocides, the epoxy-based High Protect 35651 and the experimental silicone-containing 86330 paint, were tested on the marine green alga, Skeletonema costatum, and on the marine crustacean, Acartia tonsa. A similar test was performed with an organotin-based antifouling paint, Hempel's Antifouling Nautic 76800. Water samples from the leaching test with High Protect 35651 caused no inhibition of growth of S. costatum, and chronic effects on A. tonsa were observed only in undiluted leachate (no-effect-concentration, NOEC = 100 mL/L). Water samples from the leaching test with the experimental 86330 paint showed toxicity to S. costatum and in acute and chronic tests with A. tonsa (NOEC, acute <100 mL/L; NOEC, chronic <10 mL/L). However, some factors seem to indicate that variations in production and in application may have an effect on the leaching of substances from this type of paint. These indications should be investigated further before a final assessment of the environmental properties of the paint is made. The leachates of both paints without biocides showed a significantly lower effect than water samples from similar tests with the organotin-based paint, Hempel's Antifouling Nautic 76800. Leachates from the paints, High Protect 35651 and the experimental 86330, caused chronic NOEC values for A. tonsa, which were at least 1,000 and 100 times higher, respectively, than the corresponding NOEC values for leachates from the organotin-based paint.
1. Indledning
Den nærværende undersøgelse omfatter økotoksikologiske egenskaber og risikovurdering med relation til aktivstoffer i bundmalinger og til kemiske forbindelser, der udludes fra biocidfrie malinger. De miljø- og sundhedsmæssige egenskaber for en række aktivstoffer i bundmaling til lystbåde og større skibe er for nylig blevet vurderet i rapporten "Kortlægning og vurdering af antibegroningsmidler til lystbåde i Danmark" (Madsen et al. 1998), der blev udarbejdet af CETOX (Center for Integreret Miljø og Toksikologi) og Danmarks Miljøundersøgelser (DMU). De tidligere vurderinger (Madsen et al. 1998) blev foretaget i løbet af en tre måneders periode, der ikke tillod en mere detaljeret gennemgang af de tilgængelige oplysninger om aktivstofferne. På baggrund af anbefalingerne i "Kortlægning og vurdering af antibegroningsmidler til lystbåde i Danmark" blev aktivstofferne kobber, 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on (DCOI) og zinkpyrithion udvalgt til en grundigere vurdering af forbindelsernes miljøfarlighed.
Vurderingen af kobber bygger på en gennemgang af tilgængelig litteratur med fokus på relationerne mellem kobbers speciering, biotilgængelighed og økotoksicitet.
Den mere sparsomme publicerede litteratur om DCOI og zinkpyrithion har gjort det nødvendigt at inddrage undersøgelser, der er udført af producenterne Rohm and Haas og Arch Chemicals. Dette materiale er blevet suppleret med nye undersøgelser af de to stoffers biologiske nedbrydelighed i danske, kystnære sedimenter under iltholdige (aerobe) og iltfrie (anaerobe) forhold. Desuden blev effekten af nedbrydning og sorption til sediment på de to biociders akvatiske giftighed belyst i laboratorieforsøg med det marine krebsdyr Acartia tonsa. Oplysningerne om biocidernes nedbrydning, fordeling og toksicitet i det marine miljø er anvendt til en risikovurdering, der bygger på to scenarier: en dansk lystbådehavn og en befærdet sejlrute. De to scenarier er defineret, således at de beregnede eksponeringskoncentrationer (Predicted Environmental Concentration, PEC) forventes at være realistisk konservative, hvorved de beregnede PEC-værdier i praksis kun sjældent vil overskrides (se bilag 1 for en nærmere beskrivelse af beregningen af PEC).
De økotoksikologiske egenskaber af en epoxy-baseret og en silikone-baseret maling uden biocider blev belyst ved undersøgelser af giftigheden af vandprøver fra udvaskningsforsøg. I disse forsøg var forholdet mellem det malede areal og væskevolumenet 13-14 gange højere, end dette forhold forventes at være i en havn med et stort antal lystbåde. De økotoksikologiske undersøgelser omfattede test med den marine grønalge Skeletonema costatum og test for akut og kronisk toksicitet over for A. tonsa.
2. Kobber
2.1 Kobberkoncentrationer målt ved lystbådehavne
2.2 Omdannelse og biotilgængelighed af kobber i vand og sediment
2.3 Frigivelse og binding af kobber i sedimenter
2.4 Bioakkumulerbarhed og akvatisk toksicitet
2.4.1 Bioakkumulerbarhed
2.4.2 Toksicitet over for akvatiske organismer
2.5 Vurdering af kobber
2.1 Kobberkoncentrationer målt ved lystbådehavne
Danmark
I Egå Marina ved Århus Bugt var kobberindholdet i havnesediment 150-600 mg/kg
tørvægt i en afstand af 5-10 m fra afløb fra befæstede arealer, faldende til 53-120
mg/kg tørvægt 30 m fra afløb (Jensen & Heslop 1997a). Til sammenligning var
kobberindholdet i sediment i Århus bugt 25-50 mg/kg tørstof. Endelig blev der i samme
undersøgelse målt vandkoncentrationer af kobber på 2,4 µg/L i Studstrup og 13 µg/L i
Marselisborg lystbådehavn, men analyserne angives at være noget usikre.
Kobberindholdet i havnesedimenter på andre lokaliteter i området er også analyseret. De højeste koncentrationer er fundet ved slæbestederne i Bønnerup havn (7.000-18.000 mg/kg tørvægt), der er en blanding af lystbåde- og fiskerihavn, og Århus Fiskerihavn (1.600-2.400 mg/kg tørvægt). Kobberkoncentrationerne i havnebassinerne var 15-70 mg/kg tørvægt i Bønnerup havn og 100-400 mg/kg tørvægt i Århus Fiskerihavn. Koncentrationerne i sediment fra Ebeltoft, Grenå og Hov Bedding var henholdsvis 280, 490 og 1.200 mg/kg tørvægt (Jensen & Heslop 1997b).
Fyns amt har målt kobberindhold i sediment fra 5 til 110 mg/kg tørvægt i havneområder (Fyns Amt 1999). Fra Lillebælt er der analyseret daterede sedimentkerner, således at den tidsmæssige udvikling af kobberindholdet kan vurderes. Målingerne på sedimentkernerne viste et signifikant stigende indhold af kobber ved Als, en stigende tendens på fire stationer, og konstante/varierende koncentrationer på fire andre stationer. Kobberindholdet i kernerne varierede fra 19 til 46 mg/kg tørvægt.
Sverige
I 1990 og 1993 blev kobberkoncentrationer i vand, sediment og vandplanter målt i Stockholms skærgård (Greger & Kautsky 1990 og 1993, cf. Bard 1997). Målingerne viste et markant højere indhold af kobber i sedimenter ved lystbådehavne og steder med stor trafik af lystbåde. Kobberkoncentrationer op til 1.300 mg/kg tørvægt blev målt i sedimenter. Forøgede kobberkoncentrationer i forhold til mindre belastede områder blev også fundet i vandplanter. Tilsvarende målinger blev foretaget ved Bullandö Marina, der ligeledes ligger i skærgården ved Stockholm (Öhrn 1995, cf. Bard 1997). Før sæsonstart i april 1993 var kobberindholdet i vandet 0,8-1,0 mg/L, mens det i juni måned var 3,0-3,8 mg/L. Kobberindholdet i sedimentet i Bullandö Marina var kun svagt forhøjet i forhold til referencestationer, hvor kobberindholdet var 30 mg/kg tørvægt.
Frankrig
Målinger udført af de franske myndigheder i Arcachon Bugten ved Atlanterhavskysten i perioden 1979-1991 viste en stigning af kobberindholdet i østers (Claisse & Alzieu 1993). Stigningen var signifikant på 2 ud af 4 stationer fra 1982 frem til 1991. Stigningen i kobberindholdet i østers falder tidsmæssigt sammen med et øget forbrug af kobberbaserede antibegroningsmidler, efter at anvendelsen af organotin TBT blev reguleret i 1982. Forøgelsen af kobberindholdet var størst og signifikant i østers fra de to inderste stationer. Stigningen var mindre og ikke signifikant på stationerne yderst i bugten, hvilket forklares med, at vandskiftet ved disse stationer er større end længere inde i bugten. De franske målinger er unikke på grund af de lange tidsserier og det omfattende måleprogram, der er gennemført. Mange forhold kan have betydning for akkumuleringen af kobber i organismer, og den direkte sammenhæng mellem en øget kobberkoncentration i vand og et øget indhold af kobber i østers er ikke angivet i de franske undersøgelser.
Baggrundskoncentrationer
Til sammenligning med de ovenfor angivne koncentrationer, angives baggrundskoncentrationen af kobber at være 25-35 mg/kg tørvægt i danske sedimenter og 0,5-1,5 mg/L i havvand (Madsen et al. 1998). Svenske undersøgelser angiver et kobberindhold på 0,3-0,8 mg/L i vand fra Østersøen og på 0,2 mg/L i vand fra Kattegat. De svenske baggrundsværdier for sediment angives at være 10-40 mg/kg tørvægt i Østersøen (Debourg et al. 1993).
I havne og tilgrænsende vandområder er der således fundet forhøjede koncentrationer af kobber i både sedimenter og vandprøver; i lystbådehavne op til en faktor 30 gange baggrundskoncentrationen i sedimenter og op til en faktor 10-15 gange baggrundskoncentrationen i vand.
2.2 Omdannelse og biotilgængelighed af kobber i vand og sediment
Biotilgængelighed
I modsætning til organiske forbindelser, der anvendes i antibegroningsmidler, er metaller ikke nedbrydelige. I vand vil kobber forekomme både opløst i vandet og bundet til partikler. Kobber kan imidlertid optræde i forskellige former (specier) afhængigt af bl.a. vandets saltholdighed, pH, indhold af organisk stof m.m. Specieringen af kobber er afgørende for, om levende organismer kan optage det (hvorvidt det er biotilgængeligt), og derved om kobber er giftigt for organismerne.
Det antages ofte, at det primært er de frie kobberioner (Cu2+), der kan passere cellemembraner og derfor udgøre den biotilgængelige og giftige del af kobber (Campbell 1995). Det er imidlertid påvist, at andre kobberioner og lipidbundet kobber også kan passere cellemembraner og altså også være biotilgængeligt (Allen 1993).
Kompleksbinding
I saltvand og ferskvand er det velkendt, at kompleksbinding af kobber til organiske stoffer er dominerende (Bruland et al. 1991), hvilket typisk reducerer biotilgængeligheden af kobber (Lewis 1995). Ligetil er det imidlertid ikke, idet der er forskel på organiske stoffers kompleksbindingsegenskaber i forhold til kobber. F.eks. har Garvey et al. (1991) vist, at humussyre reducerer giftigheden af kobber, mens fulvussyre ikke har en tilsvarende virkning. Efter alt at dømme er kompleksbindingen af kobber til organiske stoffer meget specifik (Wells et al. 1998). Det er vist, at planktonalger kan udskille organiske stoffer, der binder kobber (Moffet & Brand et al. 1986, cf. Wells et al. 1998). Planktonalger, der udsættes for forhøjede kobberkoncentrationer, kan udskille sådanne kobberbindende stoffer (ligander), hvorved biotilgængeligheden og en eventuel giftvirkning af kobber reduceres (Wangersky 1986, cf. Paulson et al. 1994). En anden effekt af de organiske ligander menes at være dannelsen af kolloider og efterfølgende aggregering, som fjerner kobber fra vandfasen og fører det til sedimentet (Wells et al. 1998).
Sedimentation, speciering og biotilgængelighed
Transporten af kobber til sedimenter vil typisk forgå via sedimentation af kobber, indbygget i eller adsorberet til partikler (mikroalger, lerpartikler m.m.). I åbne havområder vil kobbers sedimentation primært blive kontrolleret af sedimentationen af planktonalger (Wangersky 1986, cf. Paulson et al. 1994), hvortil kobber er bundet og/eller indbygget. I sedimentet vil en lang række kemiske og biologiske omdannelser af betydning for kobberspecieringen foregå, herunder oxidation/reduktion, opløsning/udfældning og kompleksbinding. Omdannelserne vil være styret af sedimenttype (bl.a. kornstørrelse og indhold af organisk stof), grave- og filtreringsaktivitet af sedimentlevende hvirvelløse dyr (bioturbation) samt iltforholdene i vandet og i sedimentet.
Specieringen af kobber i sedimenter bestemmes af dynamiske og reversible processer (Calmano et al. 1990). F.eks. kan kobber, der er bundet til reducerede forbindelser (organiske stof og sulfider), blive frigivet fra sedimentet til det overliggende vand på grund af oxidation (iltning) som følge af resuspension eller bioturbation (Petersen et al. 1997; Ciceri et al. 1992; Westerlund et al. 1986), eller der kan ske en omfordeling, således at kobber i stedet bliver bundet i oxiderede forbindelser (f.eks. jern- og manganoxider og -hydroxider). Disse forbindelser anses for at være ustabile, mens sulfider og organiske stoffer karakteriseres som mere stabile (Förstner et al. 1990; Calmano et al. 1990).
I iltfrie, anaerobe sedimenter - f.eks. i finkornede sedimenter med et højt indhold af organisk stof - vil kobber typisk være bundet til sulfider og organisk stof, hvorimod kobber ved gode iltforhold typisk vil være bundet til forbindelser som jernoxider, manganoxider og hydroxider. Metalsulfider er svært opløselige men oxideres relativt let og hurtigt ved gode iltforhold (Förstner 1985).
Biotilgængeligheden af kobber i sedimenter er et yderst komplekst fænomen, der ikke alene afhænger af specieringen og sedimentet, men også af de eksponerede organismers fysiologi og fødevalg (Slotton & Reuter 1995). Det er vist, at biotilgængeligheden kan være specifik for enkelte arter, og at der er variation inden for samme art i forhold til alder, køn og størrelse af organismen (Lewis 1995). Det er endvidere vist, at organismerne lettere optager metaller, der er bundet til let fordøjelig føde end metaller bundet til svært omsættelig føde (Wang & Fisher 1996). Fordøjelsesenzymer i tarmen sikrer en høj udnyttelse af føden (Forbes et al. 1998), hvorved optagelsen af kobber fra sedimentet kan øges.
Vurdering af biotilgængelighed
Forhøjede koncentrationer af metaller i akvatiske sedimenter er udbredt, og myndighederne skal ofte tage stilling til, om de forhøjede koncentrationer indebærer en risiko for negative virkninger på økosystemet. Desværre er problemstillingen vanskelig, idet biotilgængeligheden af metaller kan være meget varierende i forskellige sedimenter (Luoma 1989).
I forsøg på at forudsige biotilgængeligheden af metaller i sedimenter ud fra kemiske analyser, er der udviklet forskellige ekstraktions- og fraktioneringsforskrifter til analyser af kobber bundet til carbonater, manganoxider, jernoxider og organiske stoffer (f.eks. Förstner 1985). Problemet med sådanne ekstraktions- og fraktioneringsforskrifter er imidlertid at fortolke, hvilke specier der er biotilgængelige. Med udgangspunkt i undersøgelser, der viste en korrelation mellem cadmium-koncentrationen i porevandet i sedimentet og den akutte toksicitet af sediment tilsat cadmium over for en amphipod (krebsdyr der lever i små huler i sedimentet), blev det foreslået at antage, at indholdet i porevandet repræsenterede den biotilgængelige del af cadmium (Ankley et al. 1994).
I tilsvarende undersøgelser af cadmiums effekter over for andre amphipoder har Di Toro et al. (1990 cf. Ankley 1996) vist, at den akutte toksicitet af cadmium kunne forudsiges ud fra indholdet af syrelabilt sulfid (Acid Volatile Sulfide, AVS). AVS er den fraktion af sulfid i sedimentet, der kan ekstraheres med kold saltsyre og er et mål for sedimentets kapacitet til at binde metaller. Hvis bindingskapaciteten overskrides, øges koncentrationen af cadmium i porevandet og amphipoderne dør. AVS er forsøgt anvendt til at bestemme biotilgængeligheden for amphipoder af kobber i ferskvandssedimenter (Ankley et al. 1993, cf. Ankley 1996). AVS overvurderede markant biotilgængeligheden af kobber, hvilket blev forklaret med tilstedeværelsen af en anden bindingsfase end AVS.
Konceptet bygger på antagelse af, at kun indholdet i porevandet er tilgængeligt, kombineret med en ligevægtsbetragtning. Denne antagelse kan ikke forventes at gælde for sedimentædende dyr, der sluger hele sedimentpartikler, og som har fordøjelsesenzymer i tarmen til nedbrydning af organiske stoffer. Endvidere har AVS-metoden den begrænsning, at den er udviklet til kun at bestemme den aktuelt biotilgængelige fraktion af metaller, og således ikke giver et mål for den potentielt biotilgængelige fraktion, der med tiden kan blive biotilgængelig, f.eks. i forbindelse med ændring af iltforholdene
Der er således ikke fundet en enkel metode, hvormed man ud fra kemiske analyser kan vurdere, hvor stor en del af kobberet - specielt i sedimenter - der er biotilgængeligt, og det er usikkert under hvilke forhold (sedimenttype, iltforhold) og for hvilke organismer, AVS-metoden er gyldig.
2.3 Frigivelse og binding af kobber i sedimenter
Klapning
I forbindelse med resuspension af sedimenter er det vist, at en betydelig del af det bundne kobber kan blive frigivet fra sedimentet. I laboratorieeksperimenter under naturlige forhold har man fundet, at op til 2% af det partikelbundne kobber kan blive frigivet til vandet ved resuspension (Petersen et al. 1997). En undersøgelse af sedimenter på klapningspladser i Cleveland Bay før og efter en klapning konkluderer, at kobber i sedimentet er bundet i labile fraktioner, som er potentielt biotilgængelige, og som let spredes ved resuspension (Reichelt & Jones 1994).
Målt frigivelse
Det er påvist, at metaller (især kobber) kan frigives fra sedimenter til vandet over sediment med iltet overflade (Luoma 1989). Frigivelse af kobber fra sedimenter er observeret ved den nordamerikanske kyst (Boyle et al. 1981 cf. Luoma 1989), i Nordsøen (Kremling 1983, cf. Luoma 1989) og flere steder i kystnære områder (Windom et al. 1983, cf. Luoma 1989). I indhegningseksperimenter er det påvist, at kobberfrigivelsen er større fra kobberbelastede sedimenter end fra ubelastede sedimenter (Hunt & Smith 1983).
Bioturbation
Bioturbation i sedimenter kan have stor betydning for remobilisering af metaller fra sedimentet. Sedimentlevende dyr karakteriseres i forhold til deres fødesøgning. Sedimentædere sluger sand, mudder og vand uden forudgående sortering. Det organiske indhold i sediment er lavt sammenlignet med andre former for føde. Som en kompensation for dette må sedimentædere indtage store mængder sediment, nogle op til 8-10 gange deres egen kropsvægt hver dag. Sedimentædere roder typisk meget rundt i sedimentet, hvorved begravede metaller kan blive mobiliseret. Suspensionsædere lever af partikler, de filtrerer fra en vandstrøm, de danner mellem vandet over sedimentet og sedimentet, hvorved udvekslingen af stoffer over sediment-vandoverfladen øges. Samlet forøger dyrene kontakten mellem sedimentet og det overliggende vand. I betragtning af at nettodepositionen i havsedimenter kun er nogle få millimeter om året, kan dyrene være med til at bringe gammelt sediment op til overfladen og nyt sediment ned i dybere lag. Peterson et al. (1996) fandt, at bioturbationen markant kunne øge biotilgængeligheden af metaller i sedimenter via iltning af sulfidforbindelser. De fandt, at metal-sulfid komplekser var relativt ustabile for den iltning, der finder sted i forbindelse med bioturbation.
Udskiftningen af sulfidholdigt vand med iltholdigt vand vil også remobilisere sulfidbundne metaller (Emerson et al. 1984, cf. Förstner et al. 1990), da iltindholdet i vandet over sedimentet er af stor betydning for bindingen og frigivelsen af metaller fra sedimenter. I sommerperioder med dårlige iltforhold i havnen ved Corpou Christi Bay har man målt, at cadmium blev bundet til sulfider, mens man målte en frigivelse i vintermånederne med gode iltforhold (Holms et al. 1974, cf. Förstner et al. 1990). Det kan derfor ikke umiddelbart antages, at kobber, der er bundet i sulfider, ikke kan blive biotilgængeligt på længere sigt.
2.4 Bioakkumulerbarhed og akvatisk toksicitet
2.4.1 Bioakkumulerbarhed
Kobber er et mikronæringsstof, som levende organismer har brug for i små mængder. Højerestående organismer som fisk kan regulere indholdet af kobber i organismen og kan ophobe kobber til en vis grad i leveren men ikke i musklerne. Forekommer kobber i omgivelserne eller føden i meget lave koncentrationer, kan opkoncentrering derfor skyldes, at organismen udnytter kobberet som næringsstof. Fortolkningen af biokoncentreringsfaktorer (BCF-værdier) for et essentielt mikronæringsstof som kobber er derfor vanskelig, og der foreligger ikke oplysninger om koncentrationerne af kobber og de anvendte organismers krav til kobber i de citerede undersøgelser. I korttidsstudier med alger (½-2 dage) er der målt BCF-værdier på 1-40. I langtidsstudier med insekter og muslinger ligger værdierne væsentligt højere: I et 28-dages studie med myggelarver – sandsynligvis i sediment - er der fundet en BCF-værdi på 5.830; endvidere er der fundet BCF-værdier på 5.000-10.000 i muslinger over en periode på 2-3 år (AQUIRE 1999). BCF-værdier mellem 400 og 90.000 er fundet for plankton og visse lavere organismer (Debourg et al. 1993).
2.4.2 Toksicitet over for akvatiske organismer
Vandlevende organismer
Tabel 2.1 viser en oversigt over toksiciteten af kobber over for forskellige grupper af vandlevende organismer målt i enkeltartslaboratorietest. Af tabel 2.1 fremgår det, at kobber er meget giftigt med effektkoncentrationer fra få mikrogram kobber pr. liter.
Tabel 2.1
Økotoksikologiske data for effekter af kobber på organismer i vandet A.
Ecotoxicological data on effects of copper on aquatic organisms A.
| Systematisk gruppe Taxonomic group |
Effektmål |
Eksponeringstid |
Resultat |
| Alger, Algae | LC50/EC50 vækst, growth |
1t-5d, |
0,01-0,55 |
| Alger, Algae | NOEC* |
2-3d |
0,009-0,049 |
| Alger, Algae | NOEC |
19-20d |
0,01 |
| Krebsdyr, Crustaceans | LC50 |
2-4d |
0,0075-0,32 |
| Krebsdyr, Crustaceans | LC50 (opløst Cu, dissolved Cu) |
2d |
0,019-0,084 |
| Krebsdyr, Crustaceans | EC50 (forplantning, reproduction) |
7d |
0,01-0,02 |
| Krebsdyr, Crustaceans | NOEC (forplantning, reproduction) |
7-10d |
0,04-0,22 |
| Fisk, Fish | LC50 |
4d |
0,024-21 |
| Fisk, Fish | LC50 (opløst Cu, dissolved Cu) |
4d |
0,098-0,60 |
| Fisk, Fish | EC50 (anomaliteter + klækning, anormalities + hatching) |
12d |
0,075-0,19 |
| Fisk, Fish | NOEC (overlevelse + klækning, survival + hatching) |
12-42d |
0,01-0,12 |
| Insekter | LC50 |
1-10d |
23,6-0,20 |
| Bløddyr (snegle, muslinger), Molluscs | LC50 |
1-4d |
0,03-9,3 |
| Bløddyr (muslinger), Molluscs | EC50 (lukning, closing) |
1-6d |
0,04-<0,02 |
| Pighude (søpindsvin), Echinoderm | NOEC (forplantning + udvikling, reproduction + development) |
½-1t, |
0,0031-0,066 |
| Hjuldyr, Rotifers | LC50 |
1d |
0,063 |
| Hjuldyr, Rotifers | NOEC (bevægelse, movement) |
3t, |
0,006 |
| Orme, Worms | LC50 |
28d |
0,044 |
A
: AQUIRE 1999. Data af høj kvalitet er udvalgt blandt flere hundrede resultater fra AQUIRE-databasen. Resultaterne er opgivet som nominelle, totale koncentrationer af kobber, og specieringen er almindeligvis ikke angivet.A
: AQUIRE 1999. Data of high quality have been selected among several hundred results from the AQUIRE database. The results are given as nominal, total concentrations of copper, and in general, the speciation is not given.: AQUIRE 1999. Data of high quality have been selected among several hundred results from the AQUIRE database. The results are given as nominal, total concentrations of copper, and in general, the speciation is not given.* Den højeste koncentration, hvor der ikke blev observeret effekt (NOEC, No Observed Effect Concentration).
* The highest concentration at which no effects were observed (NOEC, No Observed Effect Concentration).
I Danmark er der fastsat kvalitetskrav for kobber i ferskvand og saltvand på henholdsvis 12 mg/L og 2,9 mg/L, der dog angives at bygge på et datagrundlag, som ikke er endeligt kvalitetsvurderet (Miljø- og Energiministeriet 1996). På basis af 65 enkeltartslaboratorietest med saltvandsorganismer er en PNEC-værdi for kobber beregnet til 5,6 µg/L (Hall & Anderson 1998). Der er benyttet en beregningsmetode, der er baseret på fordelingen af følsomheden af de testede organismer, og den beregnede PNEC-værdi beskytter teoretisk 95% af arterne med 95% sikkerhed. Den er dog dobbelt så høj som den laveste NOEC-værdi i tabel 2.1 (0,0031 mg/L = 3,1 µg/L).
Økosystem-undersøgelser
Effekter på naturlige planktonalger er målt ved få mikrogram kobber per liter. Kroniske effekter af kobber på planktonalger i marine modeløkosystemer er påvist fra 1 µg/L (Gustavson et al. 1999). Omfattende og veldokumenterede eksperimenter med mikroalger og kobber (Brand et al. 1986) viser, at kobber selv ved meget lave koncentrationer kan hæmme algers reproduktion. I undersøgelserne blev virkningen af kobber på 38 forskellige kloner af marine planktonalger undersøgt i vand, hvor de metalchelaterende egenskaber var kendt. Giftvirkningen af kobber på reproduktionen er i artiklen relateret til aktiviteten af frie kobberioner, og det konkluderes, at kobber kan hæmme reproduktionen af følsomme algearter selv i uforurenede havområder, hvor kobberkoncentrationen er lav (0,1-0,2 µg/L). Undersøgelserne udmærker sig bl.a. ved at relatere effekten af kobber til aktiviteten af de frie kobberioner i vandet og ikke - som i så mange undersøgelser - kun til den totale kobberkoncentration.
Svenske undersøgelser viste kobberkoncentrationer op til 3 µg/L ved lystbådehavne i områder, hvor baggrundskoncentrationen af kobber var 0,8-0,5 µg/L. Ved de aktuelle kobberkoncentrationer blev der ikke fundet effekter på planktonalger (Wängberg et al. 1995).
Bundlevende organismer
Resultater af undersøgelser med organismer, der lever i sediment eller på bunden, er samlet i tabel 2.2.
Tabel 2.2
Økotoksikologiske data for effekter af kobber på bundlevende organismer.
Ecotoxicological data on effects of copper on bottom-living organisms.
| Systematisk gruppe Taxonomic group |
Effektmål |
Eksponeringstid |
Resultat |
| InsekterA, Insects | LC50 |
10d |
0,20 mg/L |
| Insekter2, Insects | LC50 |
10d |
1.026 mg/kg TS3 |
| KrebsdyrA, Crustaceans | LC50 |
10d |
0,028 mg/L |
| Krebsdyr2, Crustaceans | LC50 |
14d |
247 mg/kg TS3 |
| OrmeA, Worms | LC50 |
28d |
0,044 mg/L |
| Krebsdyr 1, Crustaceans | LC25 |
28d |
998 mg/kg TS3 |
| Krebsdyr 1, Crustaceans | EC25 (vækst, growth) |
28d |
330 mg/kg TS3 |
| Krebsdyr2, Crustaceans | LC50 |
10d |
185 mg Cu2O/kg TS
» |
A
AQUIRE 1999; 1 Borgmann & Norwood 1997; 2 Bard 1997; 3 TS = tørstof.De tre studier, hvor koncentrationen er opgivet som mg/L kan være udført i vand uden sediment. De øvrige studier tyder på, at kobber i sediment kan forårsage effekter på sedimentlevende dyr ved koncentrationer, der overstiger 100 mg/kg (tabel 2.2). Dette er godt og vel dobbelt så meget som de højeste af de opgivne baggrundskoncentrationer, men meget lavere end koncentrationer målt i havnesedimenter.
2.5 Vurdering af kobber
Kobber er et grundstof og kan derfor ikke nedbrydes. Kobber kan "fjernes" fra vandmiljøet ved at blive bundet og begravet i sedimenter uden for organismers rækkevidde. Set i et geologisk tidsperspektiv er der tilført store mængder tungmetaller til havet, der ikke har medført alvorlige økotoksiske effekter, idet bindingen af metallerne til sedimenter har forhindret det.
I vandmiljøet vil kobber bindes til uorganiske og organiske stoffer og partikler. Disse bindingsforhold er medvirkende til forekomsten af forskellige specier af kobber. Det er usikkert hvilke specier, der er biotilgængelige, og der findes ingen sikre målemetoder til vurdering af den biotilgængelige fraktions størrelse. Endvidere er biotilgængeligheden af kobber ikke konstant og må anskues i forskellige tidsperspektiver. Således må der skelnes mellem, hvad der er aktuelt og potentielt biotilgængeligt. Den aktuelle biotilgængelighed vil typisk være betydeligt mindre end den potentielle. Desuden er biotilgængeligheden artsspecifik og kan endvidere afhænge af fysiologi, ernæring, alder, størrelse og køn af de pågældende organismer.
En permanent immobilisering af kobber kan kun ske ved binding til partikler og efterfølgende sedimentation på sedimenter med dårlige iltforhold med en permanent forekomst af sulfider. Sådanne forhold vil reelt kun findes i områder uden resuspension, dvs. uden bioturbation (makrofauna) og fiskeri med bundtrawl. Udbredelsen af sådanne sedimenttyper i Danmark er begrænset til nogle få huller i bl.a. det sydfynske øhav. Kobber, der er bundet til partikler, der sedimenterer på iltrige sedimenter med bioturbation, vil sandsynligvis forblive i de biologiske systemer i mange år. På dybt vand vil næringsstoffer og spormetaller - herunder kobber - forblive i vandfasen, idet partiklerne når at blive omsat i vandsøjlen, inden de når overfladen af sedimentet.
Havnesedimenter er typisk iltfattige og har et højt indhold af sulfider, som vil binde kobber. Derfor forventes kobber at være relativt hårdt bundet i havnesedimenter. En frigivelse fra sedimentet ved resuspension induceret af bl.a. skibenes skruer kan imidlertid ikke udelukkes. Med jævne mellemrum oprenses sedimenter i havnene og materialet klappes på udvalgte lokaliteter. Kobber kan frigives ved klapningen, og typisk for klappladserne i Danmark bliver sedimentet efterfølgende spredt af strøm og bølgepåvirkning. Stabile klappladser er vanskelige at finde i Danmark og kobber i havnesedimenter må derfor forventes at blive spredt ud over store områder i forbindelse med klapning.
Toksiciteten af kobber er afhængig af specieringen og biotilgængeligheden af kobber i vandet. Det forhold, at kobber er et mikronæringsstof i kombination med, at indholdet af metalchelaterende stoffer kan være meget variabelt i tid og rum, samt at følsomheden af forskellige arter er meget varierende, vanskeliggør sammenligningen af forskellige undersøgelser. De koncentrationer, hvor der er målt effekter i laboratorietest, ligger generelt over de oplyste baggrundskoncentrationer for kobber i miljøet, men koncentrationer målt i og nær havneområder er på niveau med eller højere end koncentrationer, hvor der er målt effekter. De organismer, der er mest følsomme for kobber, er alger og krebsdyr, og i økosystem-undersøgelser af algers følsomhed er der målt effekter ved kobberkoncentrationer, der er på niveau med baggrundskoncentrationer.
3. Sea-Nine
3.1 Fysisk-kemiske egenskaber
3.2 Biologisk nedbrydning af DCOI i det akvatiske miljø
3.2.1 Primær nedbrydning i havvand
3.2.2 Mineralisering og nedbrydningsprodukter i aerobt sediment
3.2.3 Mineralisering og nedbrydningsprodukter i anaerobt sediment
3.2.4 Omsætning og skæbne af DCOI i havnebassin
3.3 Bioakkumulerbarhed og akvatisk toksicitet
3.3.1 Bioakkumulerbarhed
3.3.2 Toksicitet over for akvatiske organismer
3.4 Risikovurdering af DCOI
Dette kapitel indeholder en økotoksikologisk vurdering af 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on (DCOI), der er aktivstoffet i Sea-Nine 211.
3.1 Fysisk-kemiske egenskaber
En oversigt over DCOI's fysisk-kemiske egenskaber er samlet i tabel 3.1.
Tabel 3.1
Fysisk-kemiske egenskaber for DCOI.
Physico-chemical properties of DCOI.
| CAS nr. CAS No. | 64359-81-5 |
| Synonymer, synonyms | 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on 4,5-dichlor-2-n-octyl-3(2H)-isothiazolon RH-5287 |
| Klassificering, classification | - |
| Molekylær formel, molecular formula | C11H17Cl2NOS |
| Molvægt, molar weight | 282,23 |
| Vandopløselighed, water solubility (20° C) | 6,5 mg/L1 |
| Damptryk, vapour pressure (25° C) | 7,4 · 10-6 mm Hg1 |
| Oktanol-vand fordelingskoefficient, octanol-water partition coefficient (log Kow) | 2,8 (målt, measured)2 |
| Organisk-stof-vand fordelingskoefficient, organic carbon-water partition coefficient (log Koc) | 3,2 (målt, measured)3 |
1
Shade et al. 1993; 2 Jacobson 1993; 3 Howard 1991. Shade et al. 1993; 2 Jacobson 1993; 3 Howard 1991.
3.2 Biologisk nedbrydning af DCOI i det akvatiske miljø
3.2.1 Primær nedbrydning i havvand
Der er udført flere undersøgelser af nedbrydningen af DCOI i det akvatiske miljø. Abiotiske processer angives at forløbe med halveringstider på 9-12,5 dage for hydrolyse og 13,4 dage for fotolyse. Biologiske processer har dog større betydning for omdannelsen af DCOI. Undersøgelser beskrevet af Shade et al. (1993) har vist, at DCOI (10 µg/L) omdannes med en halveringstid på 11 timer i havvand med 7 × 104 bakterier/mL (totalt antal bakterier ved tælling i mikroskop). Parallelle forsøg med havvandsprøver med et lavere antal bakterier (<1.000 bakterier/mL) gav længere halveringstider for DCOI (Shade et al. 1993). Disse forsøg anses ikke for at være relevante, da havvandets biologiske aktivitet har været urealistisk lav. I en ny undersøgelse blev hastigheden for omdannelsen af DCOI (10 µg/L) bestemt i havvand fra Jyllinge Lystbådehavn. Undersøgelsen viste, at 7,1% af den tilsatte DCOI var tilbage efter 72 timer ved en temperatur på 12° C (Jacobson & Kramer 1999). På baggrund af de målte koncentrationer for DCOI (Jacobson & Kramer 1999) kan den biologiske halveringstid beregnes til 14 timer ved 12° C (bilag 1, afsnit 2.4.1).
3.2.2 Mineralisering og nedbrydningsprodukter i aerobt sediment
Omdannelse af DCOI
Den aerobe halveringstid for DCOI er meget kort i marine systemer med sediment og havvand. Analyser af prøver fra laboratorieforsøg med sediment og havvand viste, at DCOI hurtigt blev omdannet til andre kemiske forbindelser. I flasker doseret med 0,05 mg/kg var mindre end 6% af den tilsatte radioaktivitet intakt DCOI ved prøvetagning på den første forsøgsdag (dag 0). Ved doseringen 1 mg/kg var ca. 3,5% af den tilsatte 14C intakt DCOI ved prøvetagning dag 1. Den ubetydelige andel af udgangsstoffet, der kunne genfindes dag 0, repræsenterede reelt en prøvetagning efter 1 time, da det tog ca. 1 time at forberede prøverne for analyse. Den meget hurtige omdannelse af DCOI gør det umuligt at beregne en eksakt halveringstid, der dog med sikkerhed er mindre end 1 time (Lawrence et al. 1991a).
Mineralisering og nedbrydningsprodukter
I løbet af forsøgsperioden på 30 dage blev [14C]DCOI delvist
mineraliseret, idet 22% (0,05 mg/kg) og 8,7% (1 mg/kg) af den tilsatte radioaktivitet blev
omdannet til 14CO2 ved 25° C. DCOI
omdannes overvejende til polære nedbrydningsprodukter og til forbindelser, der ikke
ekstraheres fra sedimentet (tabel 3.2). Sammenligning med HPLC-kromatogrammer for 15
potentielle nedbrydningsprodukter førte ikke til en entydig identifikation af de
nedbrydningsprodukter, der blev observeret i sedimentforsøgene. Det mest polære
nedbrydningsprodukt havde samme analytiske retentionstid som n-octyl malonaminsyre
(C8H17NHC(=O)CH2CO2H),
og mindst to andre nedbrydningsprodukter var lineære strukturer, hvor isothiazolon-ringen
var brudt (Lawrence et al. 1991a). Vurderet ud fra analyser af de 15 kendte
standarder dannes der flere ringformede strukturer ved den indledende, primære
nedbrydning af DCOI. Det betragtes som sandsynligt, at de nedbrydningsprodukter, der var
til stede i forsøgene efter 30 dage, var lineære forbindelser. De to
nedbrydningsprodukter, der blev fundet ved analyse af sedimentprøver efter 30 dage, var
begge mere polære end de anvendte isothiazolon-standarder. Den hurtige primære
nedbrydning af DCOI (mere end 94% omdannelse efter 1 time) tyder på en hurtig reaktion,
der involverer en kemisk ustabil binding, f.eks. N-S bindingen i isothiazolon-ringen
(Lawrence et al. 1991a).
En sikker identifikation af tre nedbrydningsprodukter blev opnået i en senere undersøgelse, hvor en mikrobiel berigelseskultur viste sig velegnet til at opnå højere koncentrationer af nedbrydningsprodukter (Mazza 1993). Kulturen var beriget efter dosering af akvatisk sediment med DCOI (5 mg/kg). En sammenligning af HPLC-kromatogrammer for nedbrydningsprodukter dannet i berigelseskulturen og i sediment viste, at nedbrydningsprodukterne var næsten identiske. Ved anvendelse af berigelseskulturen og flere analytiske metoder (bl.a. HPLC og GC/MS) blev to væsentlige nedbrydningsprodukter identificeret som N-(n-octyl) malonaminsyre og N-(n-octyl) acetamid. Desuden blev der identificeret et tredje, kvantitativt mindre betydende produkt, N-(n-octyl) b hydroxypropionamid, der sandsynligvis dannes ved anaerob nedbrydning.
Tabel 3.2
Aerob bionedbrydning af [14C]DCOI (0,05 mg/kg), polaritet og fordeling
af nedbrydningsprodukter i sediment og havvand. Data fra Lawrence et al. 1991a.
Aerobic biodegradation of [14C]DCOI (0.05 mg/kg), polarity and distribution of
metabolites in sediment and seawater. Data from Lawrence et al. 1991a.
Tid (dage) |
% af tilsat 14C, % of 14C added |
||||
DCOI |
Polære stoffer* |
Ikke-polære stoffer** |
CO2 |
Ikke-ekstraherbare stoffer |
|
0 |
5,1 |
41,1 |
1,2 |
0,0 |
62,0 |
1 |
- |
44,7 |
0,65 |
0,55 |
62,2 |
2 |
- |
27,6 |
1,3 |
3,3 |
55,3 |
5 |
- |
27,0 |
0,3 |
8,1 |
66,8 |
9 |
- |
23,9 |
0,7 |
8,2 |
59,0 |
15 |
- |
22,3 |
- |
8,4 |
56,5 |
20 |
- |
24,8 |
- |
9,1 |
78,0 |
26 |
- |
20,3 |
- |
14,2 |
67,0 |
30 |
- |
13,1 |
- |
21,9 |
63,5 |
-, ikke påvist; * mere polære end DCOI; ** mindre polære end DCOI.
-, not detected; * more polar than DCOI; ** less polar than DCOI.
Sedimentet fra de aerobe bionedbrydningsforsøg (Lawrence et al. 1991a) blev yderligere karakteriseret for bundne nedbrydningsprodukter. Sedimentprøver udtaget ved forsøgenes start og efter 30 dage blev karakteriseret ved ekstraktion med methylenchlorid/methanol, der blev fulgt af ekstraktioner med HCl og NaOH (Kesterson & Atkins 1992a). Relativt vandopløselige nedbrydningsprodukter, der ekstraheres med HCl, udgjorde <0,1% af den tilsatte radioaktivitet. Nedbrydningsprodukter i NaOH-ekstraktet blev yderligere opdelt i fulvussyre- og humussyrefraktioner, der indeholdt henholdsvis 1,2% og 5,1% af den tilsatte 14C efter 30 dage. De nedbrydningsprodukter, der ikke blev ekstraheret med disse procedurer var sandsynligvis bundet til humin eller ler og udgjorde 45% af den tilsatte 14C efter 30 dage (Kesterson & Atkins 1992a). Resultaterne viser, at de stabile nedbrydningsprodukter fra DCOI hovedsagelig var bundet til humussyre, humin og lermineraler i sedimentet.
Undersøgelser med danske sedimenter
Den aerobe bionedbrydelighed af DCOI blev undersøgt ved anvendelse af et lerholdigt sediment (0,83 µg DCOI/g) og et sandet sediment (0,033 mg/g), der begge blev inkuberet med det tilhørende havvand (bilag 2). Begge sedimenter og det tilhørende havvand blev indsamlet fra to lokaliteter i Øresund. Mineraliseringen af [2,3-14C]DCOI til 14CO2 udgjorde 13% af den tilsatte 14C i det lerholdige sediment og 24% af den tilsatte 14C i det sandede sediment efter 42 dages inkubering ved 15° C (figur 3.1-3.2). Undersøgelsen af fordelingen af 14C i det lerholdige sediment ved forsøgets afslutning efter 42 dage viste, at 48% af den tilsatte 14C var bundet til humussyrer, humin og lermineraler. Sådanne stoffer forventes at have en lav biotilgængelighed. Mere vandopløselige stoffer i testsystemets vandfase eller i form af hydrolyserbare forbindelser og fulvussyrer i sedimentet udgjorde i alt 17% af den tilsatte 14C efter 42 dage. Der blev udført forsøg med glukose for at undersøge effekten af den lave koncentration og de øvrige eksperimentelle betingelser på mineraliseringen af et let bionedbrydeligt stof. Mineraliseringen af glukose udgjorde 52% af den tilsatte 14C i det lerholdige sediment og 60% af den tilsatte 14C i det sandede sediment efter 42 dage. Metoder og resultater er udførligt beskrevet i bilag 2.
Figur 3.1 Se her
Mineralisering af [14C] DCOI (0,83 µg/g) i lerholdigt sediment og havvand fra Øresund (sediment LS). Aerobe forhold. Stiplet kurve angiver 14CO2 frigivet ved forsuring.
Mineralization of [14C] DCOI (0.83 µg/g) in clayey sediment and seawater from Øresund (sediment LS). Aerobic conditions. Dotted curve represents 14CO2 released by acidification.
Figur 3.2 Se her
Mineralisering af [14C] DCO1 (0,033 µg/g) i sandet sediment og havvand fra Øresund (sediment SS). Aerobe forhold. Stiplet kurve angiver 14CO2 frigivet ved forsuring.
Mineralization of [14C] DCO1 (0.033 µg/g) in sandy sediment and seawater from Øresund (sediment SS). Aerobic conditions. Dotted curve represents 14CO2 released by acidification.
I forsøget med det lerholdige sediment blev vand- og sedimentprøver udtaget ved inkuberingens start og efter 28 og 42 dage. Kemiske analyser af DCOI og nedbrydningsprodukter i disse prøver blev foretaget af Rohm and Haas (Spring House, Pennsylvania). Vandprøverne viste sig at have et meget lavt indhold af 14C (2,5 - 6% af tilsat 14C), der ikke muliggjorde en nærmere karakterisering af nedbrydningsprodukter. Analyserne af sedimentprøverne fra det samme forsøg viste, at DCOI omdannes til forbindelser, der er mere polære end udgangsstoffet, og at en betydelig del af den tilsatte radioaktivitet modstod ekstraktion fra sedimentet (tabel 3.3).
Tabel 3.3
Aerob bionedbrydning af [14C]DCOI til nedbrydningsprodukter og kuldioxid i havvand og lerholdigt sediment fra Øresund. HPLC analyser blev kun foretaget på sedimentprøver (sediment LS).
Aerobic biodegradation of [14C]DCOI into metabolites and carbon dioxide in seawater and clayey sediment from Øresund. HPLC analyses was only performed with sediment samples (sediment LS).
Tid (dage) |
DCOI 1 |
Polære stoffer 2 |
Ikke polære stoffer 3 |
CO2 |
Ikke ekstraherbare stoffer |
% af tilsat 14C, % of 14C added |
|||||
0 |
0,37 |
46,4 ± 6,5 |
- |
0 |
43,7 ± 4,6 |
28 |
- |
20,4 ± 0,60 |
- |
8,7 ± 0,35 |
51,0 ± 13,6 |
42 |
0,80 ± 0,92 |
18,5 ± 1,7 |
- |
13 ± 0,52 |
49,2 ± 21,9 |
1
bestemt ud fra HPLC co-kromatografi med DCOI standard; 2 mere polære end DCOI; 3 mindre polære end DCOI; SD, standardafvigelser mellem tre replikater; -, ikke påvist. bestemt ud fra HPLC co-kromatografi med DCOI standard; 2 mere polære end DCOI; 3 mindre polære end DCOI; SD, standardafvigelser mellem tre replikater; -, ikke påvist.1
determined by HPLC co-chromatography with DCOI standard; 2 more polar than DCOI; 3 less polar than DCOI; SD, standard deviations of three replicates; -, not detected. determined by HPLC co-chromatography with DCOI standard; 2 more polar than DCOI; 3 less polar than DCOI; SD, standard deviations of three replicates; -, not detected.3.2.3 Mineralisering og nedbrydningsprodukter i anaerobt sediment
Omdannelse af DCOI
Ligesom det var tilfældet under aerobe forhold, blev DCOI hurtigt omdannet til andre kemiske forbindelser. I forsøgene var kun 2,0% (0,05 mg/kg) og 2,2% (1 mg/kg) af den tilsatte radioaktivitet intakt DCOI ved prøvetagning på den første forsøgsdag (dag 0). Da den første prøvetagning reelt repræsenterede en 1 times prøve, kan det med sikkerhed konstateres, at halveringstiden for DCOI var mindre end 1 time (Lawrence et al. 1991b).
Mineralisering og nedbrydningsprodukter
[14C]DCOI (0,05 mg/kg) blev kun mineraliseret i mindre grad i det anaerobe sediment, idet dannelsen af 14CO2 udgjorde mellem 6,7 og 9,5% af den tilsatte radioaktivitet gennem hele forsøgsperioden på 365 dage (tabel 3.4). Dette niveau blev opnået efter 61 dages inkubering ved 25° C. Den relative andel, der blev mineraliseret i det parallelle forsøg med en dosering på 1 mg/kg, udgjorde mellem 5,3% og 8,2% af den tilsatte 14C i perioden fra 61 til 365 dage (Lawrence et al. 1991b). De produkter, der blev dannet fra nedbrydningen af DCOI, blev relateret til standarder af 15 potentielle nedbrydningsprodukter. Resultaterne viser, at der efter 29 dage var dannet mindst tre nedbrydningsprodukter, der er mere polære end DCOI. Selvom det ikke kan udelukkes, at ét af disse produkter ligner udgangsstoffet, anses det for mest sandsynligt, at der er tale om lineære strukturer. Desuden blev påvist to nedbrydningsprodukter med en mindre polaritet end DCOI. Disse ikke-polære stoffers identitet kan ikke fastslås med sikkerhed, da de ikke kunne relateres til nogen af de benyttede standarder. Det fremgår af tabel 3.4, at de kvantitativt væsentligste nedbrydningsprodukter fra DCOI er polære forbindelser. De polære nedbrydningsprodukter udgøres formodentlig af flere lineære forbindelser.
Tabel 3.4
Anaerob bionedbrydning af [14C]DCOI (0,05 mg/kg), polaritet og fordeling af nedbrydningsprodukter i sediment og havvand. Data fra Lawrence et al. 1991b.
Anaerobic biodegradation of [14C]DCOI (0.05 mg/kg), polarity and distribution of metabolites in sediment and seawater. Data from Lawrence et al. 1991b.
Tid (dage) |
% af tilsat 14C, % of 14C added |
||||
DCOI |
Polære stoffer* |
Ikke-polære stoffer** |
CO2 |
Ikke- |
|
0 |
2,0 |
13,3 |
0,9 |
0,0 |
47,1 |
14 |
-A |
25,3 |
2,1 |
1,1 |
41,4 |
29 |
- |
23,0 |
1,5 |
4,0 |
41,6 |
61 |
-A |
18,7 |
3,8 |
8,4 |
40,1 |
90 |
- |
18,6 |
2,5 |
7,6 |
58,5 |
120 |
- |
12,6 |
1,3 |
9,5 |
47.6 |
180 |
- |
12,6 |
2,2 |
8,5 |
48,9 |
270 |
- |
8,7 |
1,0 |
8,5 |
66,7 |
365 |
- |
*** |
*** |
6,7 |
44,0 |
-, ikke påvist (dog: A, lav konc. detekteret, formodentlig artefakt); * mere polære end DCOI; ** mindre polære end DCOI; *** prøve tabt.
-, not detected (however: A, low conc. detected, probably artifact); * more polar than DCOI; ** less polar than DCOI; *** sample lost.
Vandopløselige nedbrydningsprodukter fra omdannelsen af DCOI udgjorde mellem 3,6% og 9,3% af den tilsatte radioaktivitet gennem hele forsøgsperioden. Nedbrydningsprodukter, der var bundet til sedimentet og ikke kunne ekstraheres med methylenchlorid/methanol, udgjorde en konstant høj andel på mellem 40% og 67% af den tilsatte 14C (tabel 3.4). Yderligere ekstraktion med HCl og NaOH viste, at relativt vandopløselige nedbrydningsprodukter udgjorde <0,1%, mens fulvus- og humussyrer udgjorde henholdsvis 0,6% og 3,6% af den tilsatte 14C efter 365 dage. Nedbrydningsprodukter, der herefter fortsat var bundet til sedimentet, sandsynligvis til humin eller ler, udgjorde 30% af den tilsatte 14C (Kesterson & Atkins 1992b). Dannelsen af nedbrydningsprodukter, der bindes til humussyrer, humin og lermineraler i sedimentet er overensstemmende med resultaterne i de aerobe bionedbrydelighedsforsøg (Kesterson & Atkins 1992a).
Undersøgelser med danske sedimenter
Den anaerobe bionedbrydelighed af DCOI (0,83 µg/g) blev undersøgt ved anvendelse af det lerholdige sediment og tilhørende havvand (bilag 2), som ligeledes blev anvendt i de aerobe forsøg (jf. afsnit 3.2.2). Sediment og havvand blev inkuberet under anaerobe, sulfatreducerende forhold, der normalt er fremherskende i kystnære marine sedimenter. Mineraliseringen af [2,3-14C]DCOI til 14CO2 udgjorde 14% af den tilsatte 14C efter 56 dages inkubering ved 15° C (figur 3.3). Undersøgelsen af fordelingen af 14C i det lerholdige sediment ved forsøgets afslutning efter 56 dage viste, at 45% af den tilsatte 14C var bundet til humussyrer, humin og lermineraler. Vandopløselige stoffer i testsystemets vandfase samt hydrolyserbare forbindelser og vandopløselige fulvussyrer i sedimentet udgjorde i alt 7% af den tilsatte 14C efter 56 dage. Mineraliseringen af glukose, der var medtaget som et let bionedbrydeligt referencestof, udgjorde 59% af den tilsatte 14C efter 56 dage. Metoder og resultater er udførligt beskrevet i bilag 2.
Figur 3.3 Se her
Mineralisering af [14C] DCOI (0,83 µg/g) i lerholdigt sediment og havvand fra Øresund (sediment LS). Anaerobe forhold. Stiplet kurve angiver 14CO2 frigivet ved forsuring.
Mineralization of [14C] DCO1 (0.83 µg/g) in clayey sediment and seawater from Øresund (sediment LS). Anaerobic conditions. Dotted curve represents 14CO2 released by acidification.
Vand- og sedimentprøver fra forsøgene blev udtaget ved forsøgenes start og efter 28 og 56 dage. Kemiske analyser af DCOI og nedbrydningsprodukter i vandprøverne blev foretaget af Rohm and Haas (Spring House, Pennsylvania).
Analyserne af vandprøver udtaget ved forsøgets afslutning efter 56 dage viste, at 4,0 ± 2,4% af den tilsatte 14C var til stede i form af forbindelser, der havde samme HPLC retentionstid som DCOI. Polære forbindelser i de samme vandprøver udgjorde 13,7 ± 3,0% af den tilsatte 14C. Sedimentprøverne blev ikke analyseret, fordi de indeholdt 3-4 gange mindre radioaktivitet end sedimentprøverne fra det aerobe forsøg (tabel 3.3).
3.2.4 Omsætning og skæbne af DCOI i havnebassin
En undersøgelse af spredningen og fjernelsen af DCOI blev udført i nærheden af et nymalet skib og et andet skib, der var malet et par måneder tidligere. Begge skibe var beliggende i Korsør Havn, hvor undersøgelsen blev foretaget den 26. og 27. oktober 1998. Vandets temperatur var ca. 10° C de pågældende dage og varierede meget lidt med vanddybden (Steen et al. 1999). Vinden de pågældende dage var sydvestlig (mellem ca. 240 og 255° den 26. oktober og ca. 200° den 27. oktober), vindhastigheden var på ca. 8-10 m/s med vindstød op til 15 m/s (den 26. oktober) og lidt højere den 27. oktober (Danmarks Meteorologiske Institut 1999). Havneudmundningen i Korsør Havn er placeret i nordøstlig retning, hvorfor vandet i havnen de pågældende dage må forventes at være blevet presset ud.
Koncentrationen af DCOI i vandfasen blev målt langs to transekter: den ene vinkelret på skibenes retning og den anden i nordøstlig retning, dvs. i vindretningen. De fleste prøver blev taget den 26. oktober. Prøverne blev taget over en forholdsvis kort periode (ca. 5 timer), og de målte koncentrationer kan derfor kun antages at gælde for pågældende dag. De højeste målte koncentrationer af DCOI var <300 ng/L tæt ved skibssiden (£ 1 m) og aftog til <50 ng/L i ca. 30 m’s afstand fra skibet. Koncentrationen af DCOI i en afstand på 2 m fra bådene (langs transekten vinkelret på bådene) varierede meget lidt med dybden, hvorfor den vertikale opblanding blev anset for at være fuldstændig.
Steen et al. (1999) har udført modelberegninger, hvor Korsør Havn er modelleret som en én-dimensional kasse, hvor strømmen ind og ud af havnen blev negligeret og hvor dispersionskoefficienten blev varieret mellem ca. 0,004-0,03 m2/s. Dette interval angives at være yderpunkterne i det forventede variationsinterval for dispersionskoefficienten i havnen. Ud over spredningen er der antaget en første ordens forsvindingskinetik for DCOI. Simuleringerne blev udført med tre forskellige hastighedskonstanter for denne første ordens proces: 0 dag-1, 1 dag-1, og 1 time-1. Som følge af vindforholdene de pågældende dage må det antages, at dispersionen har været høj i havnebassinet, hvorfor værdien på 0,03 m2/s vurderes at være den mest realistiske. Til sammenligning kan det nævnes, at den horisontale dispersionskoefficient i danske kystvande typisk varierer mellem 0,04 og 5 m2/s (Harremoës & Malmgren-Hansen 1989). For de to transekter blev den bedste overensstemmelse mellem de målte og beregnede DCOI koncentrationer opnået ved anvendelse af en forsvindingshastighedskonstant på mellem 1 time-1 og 1 dag-1.
Med hastighedskonstanten 1 time-1 opnås en god overensstemmelse mellem målte og beregnede værdier tæt ved skibene for den ene transekt, mens koncentrationerne for den anden transekt underestimeres ved afstande større end ca. 8 m. For begge transekter er de beregnede koncentrationer lavere end de målte koncentrationer i større afstand fra skibene (ca. 30 m). Med antagelse om en forsvindingshastighedskontant på 1 dag-1 er de beregnede koncentrationer højere end de målte tæt ved skibene for begge transekter men lavere end de målte koncentrationer længere væk (ca. 60 m). Der er således noget, der tyder på, at forsvindingshastighedskonstanten for DCOI tæt ved skibene er højere end den tilsvarende konstant længere væk fra skibene. På denne baggrund vurderes forsvindingshastighedskonstanten for hele havnebassinet at være mellem 1 time-1 og 1 dag-1, hvilket svarer til en halveringstid på mellem ca. 0,69 og 16,6 timer. Denne halveringstid inkluderer både biologisk og abiotisk omdannelse samt processer som binding til suspenderet materiale, sedimentation, eventuel vertikal opblanding og eventuelle ufuldstændigheder i beregningen af fortyndingen i havnebassinet.
3.3 Bioakkumulerbarhed og akvatisk toksicitet
3.3.1 Bioakkumulerbarhed
Der foreligger undersøgelser af bioakkumulering af DCOI i fisk, men ikke i andre typer organismer (f.eks. muslinger). Bioakkumulerbarheden af DCOI i fisk er undersøgt i laboratorieforsøg over 28 dage med anvendelse af [14C]DCOI. Der er gennemført to undersøgelser med tilhørende kemiske analyser af vand- og vævsprøver (Forbis et al. 1985; Derbyshire et al. 1991). I alle forsøg blev [14C]DCOI kontinuerligt tilsat til et gennemstrømningssystem. Kemiske analyser viste, at koncentrationen af DCOI i den sidste del af forsøgene var væsentligt lavere end den nominelle koncentration (f.eks. 4,5% og 0,55% af tilsat 14C efter henholdsvis 21 og 28 dage (Leak 1986), mens DCOI knapt kunne måles i det andet forsøg (Derbyshire et al. 1991). Det antages, at hovedparten af den tilbageværende 14C aktivitet i vandet repræsenterede et eller flere polære nedbrydningsprodukter.
De fundne BCF-værdier (målt som radioaktivitet) var nogenlunde ens i de to studier. BCF var 130-200 for muskelvæv, 700-1100 for indre organer og 600 for hele fisken (Forbis et al. 1985; Derbyshire et al. 1991). De kemiske analyser viste, at kun 1% af radioaktiviteten i fiskene var intakt DCOI (Leak 1986). I forbindelse med undersøgelsen af Derbyshire et al. (1991) blev der anvendt både HPLC og TLC til identifikation af 14C-mærkede stoffer, der var akkumuleret i fiskenes væv. Det blev sandsynliggjort, at der var tale om stoffer uden isothiazolon-ringstruktur, og at stofferne var indbygget i fiskenes protein. Resultaterne tyder på, at DCOI blev omdannet i vandet, hvorefter det hovedsageligt var polære, og sandsynligvis lineære, forbindelser, der blev optaget i fiskene. Denne antagelse bekræftes af undersøgelserne af bionedbrydningen af DCOI (jf. afsnit 3.2.2; Lawrence et al. 1991a). Det anses derfor for sandsynligt, at de målte BCF-værdier snarere bør relateres til nedbrydningsprodukter af DCOI, men da kun få af disse er identificeret, kan betydningen af den konstaterede bioakkumulering af mærket 14C ikke vurderes.
3.3.2 Toksicitet over for akvatiske organismer
Vandlevende organismer
Toksiciteten af DCOI er undersøgt i standardlaboratorietest med en række vandlevende organismer, der findes i ferskvand og saltvand:
Ferskvand:
- Selenastrum capricornutum, grønalge (Forbis 1990)
- Daphnia magna, krebsdyr (Burgess 1990; Ward & Boeri 1990)
- Oncorhynchus mykiss, regnbueørred (Shade et al. 1993)
- Lepomis macrochirus, "bluegill sunfish" (Shade et al. 1993)
Saltvand:
- Skeletonema costatum, grønalge (Debourg et al. 1993)
- Mysidopsis bahia, mysis, krebsdyr (Boeri & Ward 1990)
- Penaeus aztecus, "brown shrimp", krebsdyr (Heitmuller 1977)
- Cyprinodon variegatus, "sheepshead minnow", fisk (Shade et al. 1993)
- Paralichthys olivaceus, japansk flynder, fisk (Kawashima 1997a)
- Pagrus major, "red sea bream", fisk (Kawashima 1997b)
- Crassostrea virginica, østers (Roberts et al. 1990)
Endvidere er forsøg med en musling og protozoer refereret af henholdsvis Shade et al. (1993) og Debourg et al. (1993). Der har i nogle af forsøgene været problemer med at holde eksponeringskoncentrationen konstant, og ikke alle resultater er beregnet ud fra målte koncentrationer (se nedenfor). Betydningen af dette er en overvurdering af effektkoncentrationerne – og dermed en undervurdering af stoffets giftighed.
Resultaterne, der er samlet i bilag 4, viser, at der ikke var stor forskel på følsomheden af ferskvands- og saltvandsorganismer. Tabel 3.5 viser en oversigt over effekter på de forskellige grupper af organismer.
Tabel 3.5
Økotoksikologiske data for effekter af DCOI på vandlevende organismer (se bilag 4 for detaljerede data).
Ecotoxicological data for effects of DCOI on aquatic organisms (see Appendix 4 for detailed data).
| Systematisk gruppe Taxonomic group |
Effektmål |
Eksponeringstid |
Resultat |
| Alger, Algae | EC50 |
4-5 |
0,0139-0,036 |
| Krebsdyr, Crustaceans | EC/LC50 |
2-4 |
0,0047-1,312 |
| Krebsdyr, Crustaceans | NOEC* (forplantning, |
21 |
0,00063 |
| Fisk, Fish | LC50 |
4 |
0,0027-0,030 |
| Fisk, Fish | NOEC (tidl. |
35 |
0,006 |
| Bløddyr (snegle, muslinger), Molluscs | EC/LC50 |
2-4 |
0,0019-0,850 |
| Protozoa | 100% effekt |
? |
5 |
* Den højeste koncentration, hvor der ikke blev observeret effekt (NOEC, No Observed Effect Concentration).
* The highest concentration at which no effects were observed (NOEC, No Observed Effect Concentration).
Resultaterne fra de udførte algetest (Forbis 1990) er beregnet på baggrund af den nominelle koncentration. Rapporten fra en af testene viser, at koncentrationen af DCOI faldt gennem hele forsøgsperioden: Der var kun 67% af den nominelle koncentration tilbage efter 48 timer, og ved afslutningen af testen efter 72 timer var det kun muligt at måle stoffet i glas med den højeste koncentration (Forbis 1990). De opgivne EC50-værdier er derfor for høje.
En 21-dages reproduktionstest med dafnier (Ward & Boeri 1990) er udført på en måde, der gør det vanskeligt at drage sikre konklusioner. Dette skyldes anvendelsen af forskellige koncentrationer af et opløsningsmiddel i forbindelse med tilsætning af DCOI samt, at der er stor variation i data. Den opgivne NOEC-værdi repræsenterer den laveste testede koncentration, men som testen er gennemført kan det ikke udelukkes, at der har været effekter af DCOI ved denne koncentration, da effekten sløres af en utilsigtet virkning af opløsningsmiddel. Da resultatet af denne test er den laveste NOEC, der er fundet ved undersøgelserne, er det denne værdi, der lægges til grund for beregningen af PNEC for DCOI.
N-(n-octyl) malonaminsyre
Den akutte akvatiske giftighed af N-(n-octyl) malonaminsyre, der er et væsentligt nedbrydningsprodukt fra omdannelsen af DCOI (jf. afsnit 3.2.2) er undersøgt i test med fisk og dafnier. Toksiciteten af N-(n-octyl) malonaminsyre er undersøgt i statiske forsøg, og beregningerne er baseret på målte middelkoncentrationer af stoffet. Effektkoncentrationer for N-(n-octyl) malonaminsyre er angivet for dafnier (48 t): EC50 = 260 mg/L, NOEC = 16 mg/L (Sword & Muckerman 1994b), og regnbueørreder (96 t): LC50 = 250 mg/L, NOEC = 160 mg/L (Sword & Muckerman 1994a). I dafnie-forsøget er der stor variation i data, og grundlaget for beregningen af resultatet er ikke klart defineret. Dafnier, der lå på bunden af glassene synes ikke at være medregnet som "ubevægelige", hvilket de burde ifølge den anvendte metodebeskrivelse. Det vurderes, at den faktiske EC50 ligger i intervallet 90-160 mg/L, snarere end på 260 mg/L, som opgivet i rapporten (Sword & Muckerman 1994b).
Selv med ovenstående forbehold må det dog konkluderes, at toksiciteten af N-(n-octyl) malonaminsyre er adskillige størrelsesordener mindre end toksiciteten af DCOI.
Der er i forbindelse med undersøgelserne af N-(n-octyl) malonaminsyre gennemført QSAR-beregninger for toksiciteten af dette og nogle stoffer med lignende struktur, som er væsentlige nedbrydningsprodukter fra den mikrobielle omdannelse af DCOI. Resultaterne er vist i tabel 3.6.
Tabel 3.6
QSAR-beregninger af toksicitet og potentiel bioakkumulerbarhed for sandsynlige nedbrydningsprodukter fra omdannelsen af DCOI.
QSAR calculations of the toxicity and the potential bioaccumulation of four probable metabolites from the transformation of DCOI.
| Stof, substance | Beregnet EC50 (48 t), dafnier |
Beregnet EC50 |
Beregnet oktanol-vand fordelings- |
| [mg/L] * | [mg/L] ** | [log Kow] ** | |
| N-(n-octyl) malonaminsyre | 172 |
199 |
1,9 |
| N-(n-octyl) acetamid | 102 |
115 |
2,0 |
| N-(n-octyl) oxaminsyre | 140 |
160 |
1,9 |
| N-(n-octyl)-b -hydroxypropionamid | 261 |
Ikke bestemt |
Ikke bestemt |
* Efter Sword & Muckerman 1994b. ** Personlig komm., Andrew Jacobson, Rohm & Haas Company.
* From Sword & Muckerman 1994b. ** Personal comm., Andrew Jacobson, Rohm & Haas Company.
Det fremgår af resultaterne i tabel 3.6, at de sandsynlige nedbrydningsprodukter fra omdannelsen af DCOI hverken er særligt toksiske eller bioakkumulerbare i akvatiske organismer.
Sedimentlevende organismer
Der foreligger resultater af en 10-dages-test med det marine, sedimentlevende krebsdyr, amphipoden Ampelisca abdita: LC50 = 320 mg/kg og NOEC = 6,9 mg/kg tørvægt (Putt 1994). Testen er gennemført med 14C-mærket DCOI, og koncentrationerne er målt som radioaktivitet. Ved afslutning af testen var ca. 90% af 14C-aktiviteten tilknyttet sedimentet, mens den resterende del fordelte sig i forholdet ca. 8:2 mellem porevand og overliggende vand. Der blev ikke udført kemiske analyser, og forfatterne gør opmærksom på, at den målte radioaktivitet sandsynligvis skyldes nedbrydningsprodukter og ikke DCOI.
Algesamfund
Akutte og kroniske effekter af DCOI er undersøgt på naturlige fytoplankton- (planktonalger) og epipsammonsamfund (mikroalger, der lever på sandkorn). Akutte og kroniske effekter af DCOI på fytoplanktonsamfund er fundet ved en koncentration af DCOI på 0,0003 mg/L (den laveste koncentration, hvor der blev observeret effekter, Lowest Observed Effect Concentration, LOEC) (Arrhenius 1997). Den akutte effekt af DCOI var en stimulering af algernes aktivitet, mens den kroniske effekt var en adaptation til DCOI over få dage. Hæmning af fotosyntesen skete ved højere koncentrationer (EC50: 0,05-0,1 mg/L (95% konfidensinterval)). I undersøgelsen konkluderes det, at effekten af DCOI stadig var markant ved forsøgets afslutning efter 7 dage. Epipsammon samfund var yderst tolerante for DCOI og effektkoncentrationerne var flere størrelsesordener højere end for fytoplankton.
Effekter af nedbrydning af DCOI på akvatisk toksicitet
Der er udført laboratorieundersøgelser, hvor effekterne af nedbrydning på giftigheden over for akvatiske organismer blev undersøgt for en række antibegroningsmidler, der omfattede DCOI, Irgarol 1051 og Diuron (Callow & Finlay 1995, Callow & Willingham 1996). I disse undersøgelser blev stofferne inkuberet i havvand, i havvand tilsat marine bakterier samt i steriliseret havvand. Ændringer i toksiciteten som følge af nedbrydning af aktivstofferne blev undersøgt over for marine bakterier (tælling af kolonidannende bakterier), kiselalger (Amphora coffeaeformis) og krebsdyr (Artemia salina). Nedbrydningsforsøgene var startet med koncentrationer af stofferne, der gav ca. 80% effekt på algerne (EC80 = 0,5 mg/L for DCOI), således at et eventuelt fald i opløsningernes toksicitet kunne følges. Resultaterne viste, at toksiciteten stort set ikke faldt i steriliseret havvand, og at omdannelsen af aktivstofferne til nedbrydningsprodukter med lav giftighed var hurtigst i det bakterieberigede havvand. Testen med kiselalger viste f.eks., at toksiciteten af DCOI blev reduceret væsentligt (fra ca. 80 til ca. 20% hæmning) efter to uger i naturligt og bakterieberiget havvand, og at prøver, der var inkuberet i 4, 6 og 8 uger i de to typer havvand gav 10% eller ingen signifikant hæmning (Callow & Finlay 1995). Halveringstiden for toksiciteten af DCOI blev beregnet til 8,5 dage i havvand og 3 dage i bakterieberiget havvand (Callow & Finlay 1995).
Relationen mellem nedbrydning og sorption af DCOI og den akutte giftighed over for det marine krebsdyr Acartia tonsa blev undersøgt i dette projekt. Undersøgelserne blev udført i systemer af det sandede sediment og tilhørende havvand fra Øresund (bilag 2), der også blev anvendt til bionedbrydningsforsøg. Sediment-havvand-systemerne blev tilsat DCOI i koncentrationen 100 µg/kg. Vandfase og sediment blev adskilt 20 min efter dosering, og anvendelse af vandfasen i test med A. tonsa medførte en dødelighed svarende til 35% af forsøgsorganismerne. Stationær inkubering i mørke ved 20-25° C medførte, at der ikke var dødelige effekter på A. tonsa efter 1 dag (figur 3.4). Tilsvarende resultater blev opnået, når sediment-vand-systemerne blev inkuberet i lys med en intensitet svarende til 340 µmol/m2 × s. Målinger som VKI har foretaget i Øresund viser, at den gennemsnitlige lysintensitet i perioden fra maj til oktober 1998 var 420 µmol/m2 × s i en dybde på ca. 1 meter. Den anvendte lysintensitet var således ca. 80% af den gennemsnitsværdi, der er beregnet ud fra målinger i 1998. Resultaterne med A. tonsa viser, at DCOI bindes til sediment eller omdannes til nedbrydningsprodukter med en væsentlig lavere giftighed end udgangsstoffet. De anvendte metoder er udførligt beskrevet i bilag 3. Et parallelt forsøg blev udført med zinkpyrithion (jf. afsnit 4.4).
Figur 3.4 Se her
Effekter af nedbrydning af DCOI (100 µg/kg) doseret til sediment og havvand på den akutte toksicitet over for Acartia tonsa (forsøg udført i mørke).
Effects of degradation of DCOI (100 µg/kg) dosed to sediment and seawater on the acute toxicity to Acartia tonsa (test performed in the dark).
3.4 Risikovurdering af DCOI
Beregning af eksponeringskoncentrationer (PEC)
Til beregning af eksponeringskoncentrationer (PEC, Predicted Environmental Concentration) blev opstillet en model, der bygger på principper, der normalt anvendes til eksponeringsvurderinger (EC 1996). Eksponeringsvurderingerne blev foretaget for to scenarier:
- En lystbådehavn (med udgangspunkt i forholdene i Jyllinge Lystbådehavn)
- En befærdet sejlrute (med udgangspunkt i forholdene ved Kronprins Frederiks Bro, Frederikssund)
Modellen og de to scenarier er udførligt beskrevet i bilag 1. For udgangsstoffet og de væsentligste nedbrydningsprodukter blev følgende eksponeringskoncentrationer beregnet for hvert af de to scenarier:
- PEC (vandsøjle)
- PEC (sediment)
- PEC (sediment-porevand)
De tre eksponeringskoncentrationer blev defineret som "steady-state" koncentrationen i det pågældende delmiljø; dvs. den koncentration, som de beregnede koncentrationer nærmer sig med tiden, når der simuleres en kontinuerlig frigivelse af udgangsstoffet til vandmiljøet. Det er søgt at udføre beregningerne af PEC ved anvendelse af "realistiske worst-case scenarier", hvilket betyder, at de anvendte parametre i modellen bygger på realistisk konservative antagelser, der medfører, at de beregnede PEC-værdier i praksis kun sjældent vil overskrides. Den anvendte model er ikke valideret over for målte koncentrationer i havnemiljøer eller sejlruter. Flere af de antagelser, der indgår i simuleringen, har afgørende betydning for resultatet af beregningerne:
- Baggrundskoncentrationerne for både udgangsstoffet og nedbrydningsprodukterne blev antaget at være nul.
- 70% af lystbådene blev antaget at være påført maling indeholdende DCOI.
- Frigivelseshastigheden af DCOI fra bundmaling blev beregnet til 13 mg/m2/dag i havn og 25 mg/m2/dag ved sejlads (bilag 1).
- Den primære biologiske omdannelse af DCOI til det formodede nedbrydningsprodukt N-(n-octyl) malonaminsyre blev antaget at forløbe med en halveringstid på 14 timer i overfladevand ved en temperatur på 12° C.
Den biologiske halveringstid for DCOI på 14 timer, der antages i simuleringen, er fastsat på baggrund af en eksperimentelt bestemt halveringstid i havvand ved 12° C (Jakobson & Kramer 1999). Det er valgt at benytte halveringstiden for DCOI i havvand, og ikke i havvand og sediment, fordi resultatet af simuleringen er eksponeringskoncentrationer ved en kontinuerlig frigivelse af DCOI til havvand efter opnået "steady state". Når lystbådene tages op af vandet ved sejlsæsonens afslutning, vil DCOI sandsynligvis hurtigt blive elimineret, da DCOI enten omdannes i vandfasen eller bindes til sedimentet, hvor det omdannes med en meget kort halveringstid (jf. afsnit 3.2.2 og 3.2.3).
De beregnede eksponeringskoncentrationer for DCOI og nedbrydningsprodukter er ca. 50 gange højere inden for lystbådehavnen end i den befærdede sejlrute udenfor (tabel 3.7).
Tabel 3.7
Beregnede eksponeringskoncentrationer (PEC) for DCOI og nedbrydningsprodukter ved "steady-state".
Calculated exposure concentrations (PEC) for DCOI and metabolites at steady-state.
| Scenarie Scenario |
Stof Substance |
PEC (vand) |
PEC (sediment, porevand) |
PEC (sediment, bundet) |
mg/L |
mg/L |
mg/kg |
||
| Lystbåde- havn Pleasure craft harbour |
DCOI | 0,52 |
0,0015 |
0,12 |
| N-(n-octyl) malanominsyre | 1,98 |
0,83 |
2,32 |
|
| N-(n-octyl) beta hydroxy- propionamid |
0,020 |
0,14 |
0,43 |
|
| N-(n-octyl) acetamid | 0,050 |
0,084 |
2,42 |
|
| Andre forbindelser, Other compounds | 0,10 |
|||
| Sejlrute Navigation route |
DCOI | 0,0061 |
0,00002 |
0,0014 |
| N-(n-octyl) malanominsyre | 0,040 |
0,011 |
0,031 |
|
| N-(n-octyl) beta hydroxypropionamid | 0,00071 |
0,0019 |
0,0058 |
|
| N-(n-octyl) acetamid | 0,0018 |
0,0013 |
0,039 |
|
| Andre forbindelser, Other compounds | 0,0040 |
Beregning af nul-effekt-koncentration (PNEC)
Nul-effekt-koncentrationer (PNEC, Predicted No-Effect Concentration) er estimeret for DCOI og N-(n-octyl) malonaminsyre. De øvrige stabile nedbrydningsprodukter fra omdannelsen af DCOI antages at have tilsvarende akvatisk toksicitet som N-(n-octyl) malonaminsyre.
De foreliggende undersøgelser af den akvatiske giftighed af DCOI anses for repræsentative, og datamaterialet omfatter langtidsstudier med fisk og krebsdyr. Algetesten kan fortolkes både som en korttidstest og en langtidstest (EC 1996).
For DCOI foreligger der tre NOEC-værdier fra langtidstest (fisk, krebsdyr og alger), der omfatter den gruppe organismer, der var mest følsom i korttidstest (fisk). På den baggrund beregnes PNEC ved division af den laveste NOEC-værdi, der er 0,00063 mg/L for krebsdyr (Ward & Boeri 1990), med en omregningsfaktor på 10 (EC 1996). Dette giver en PNEC på 0,00006 mg/L = 0,06 mg/L for DCOI. Som tidligere anført i afsnit 3.3.2 kan der ikke afledes en entydig NOEC fra langtidstesten med krebsdyr (Ward & Boeri 1990). Udelades denne undersøgelse, foreligger der resultater fra et enkelt langtidsstudium med fisk, hvor NOEC var 0,006 mg/L. I dette tilfælde anvendes en omregningsfaktor på 100, hvorved PNEC beregnes til 0,00006 mg/l = 0,06 µg/L, der er identisk med den ovenfor beregnede værdi.
Beregning af PNEC for N-(n-octyl) malonaminsyre baseres på den laveste effektkoncentration. Da der primært er tale om data fra korttidstest, anvendes en omregningsfaktor på 1.000 over for den laveste effektkoncentration. For N-(n-octyl) malonaminsyre er den lavest rapporterede LC50 = 250 mg/L for regnbueørred, mens værdien for dafnier (EC50 = 260 mg/L), som omtalt ovenfor, kan diskuteres. Til beregning af PNEC for N-(n-octyl) malonaminsyre anvendes her en LC50-værdi på 90 mg/L (over for dafnier), fordi denne vurderes at være den faktiske effektkoncentration i de udførte forsøg (jf. afsnit 3.3.2). Herved fås en PNEC på 0,09 mg/L = 90 µg/L. Den beregnede PNEC for N-(n-octyl) malonaminsyre antages at være repræsentativ for de øvrige nedbrydningsprodukter fra omdannelsen af DCOI. De to beregninger af PNEC er vist i tabel 3.8.
Tabel 3.8
Beregning af PNEC for DCOI og N-(n-octyl) malonaminsyre.
Calculation of PNEC for DCOI and N-(n-octyl) malonamic acid.
| Stof, substance | Laveste effektkoncentration Lowest effect concentration |
Værdi, value |
Omregnings- |
PNEC |
| DCOI | Langtidstest, long-term test NOEC krebsdyr NOEC crustaceans |
|
|
|
| N-(n-octyl) malonaminsyre N-(n-octyl) malonamic acid |
Korttidstest, short-term test EC50 krebsdyr EC50 crustaceans |
|
|
|
Risikokvotient
På baggrund af de ovenfor beregnede værdier for PEC (vand) for DCOI og de angivne nedbrydningsprodukter i tabel 3.7 samt PNEC-værdier for DCOI og N-(n-octyl) malonaminsyre kan der beregnes risikokvotienter Rq = (PEC/PNEC) som angivet i tabel 3.9.
Tabel 3.9
Beregning af risikokoefficienter (Rq) for DCOI og dets nedbrydningsprodukter
Calculation of risk quotients (Rq) for DCOI and its metabolites
Stof |
PNEC |
Lystbådehavn |
Sejlrute |
||
[µg/L] |
PEC |
Rq |
PEC |
Rq |
|
| DCOI | 0,06 |
0,52 |
8,7 |
0,0061 |
0,10 |
| Nedbrydningsprodukter Metabolites |
90 * |
2,2 |
0,02 |
0,047 |
0,0005 |
* N-(n-octyl) malonaminsyre
* N-(n-octyl) malonamic acid
De angivne risikokvotienter er beregnet ud fra "realistiske worst-case scenarier" (bilag 1), der bl.a. bygger på en antagelse om, at 70% af lystbådene er påført en bundmaling, som indeholder DCOI. Ud fra antagelserne i simuleringen og de beregnede PEC-værdier vurderes det, at der inden for lystbådehavnen er en risiko for kronisk økotoksiske effekter, idet DCOI antages at blive tilført konstant ved udludning fra bundmaling. Risikokvotienten for DCOI uden for lystbådehavnen er mindre end 1, og her skønnes risikoen for økotoksiske effekter af DCOI at være lav.
Både inden for og uden for lystbådehavnen vurderes der at være en meget lav risiko for økotoksiske effekter af nedbrydningsprodukter fra omdannelsen af DCOI.
4. Zinkpyrithion
4.1 Fysisk-kemiske egenskaber
4.2 Abiotisk nedbrydning
4.3 Biologisk nedbrydning af zinkpyrithion i det akvatiske miljø
4.3.1 Mineralisering og nedbrydningsprodukter i aerobt sediment
4.3.2 Mineralisering og nedbrydningsprodukter i anaerobt sediment
4.4 Toksicitet over for akvatiske organismer
4.5 Vurdering af zinkpyrithion og nedbrydningsprodukter
4.6 Risikovurdering af zinkpyrithion
4.1 Fysisk-kemiske egenskaber
En oversigt over zinkpyrithions fysisk-kemiske egenskaber er samlet i tabel 4.1.
Tabel 4.1:
Fysisk-kemiske egenskaber for zinkpyrithion (Olin 1997).
Physico-chemical properties of zinc pyrithione (Olin 1997).
| CAS nr., CAS No. | 13463-41-7 |
| Synonymer, Synonyms | Bis(1-hydroxy-2[1H]- pyridinethionato-O-S)-(T4)zink, Zink Omadine |
| Klassificering (to produkter) Classification (two products) |
T, R22, R23, R41, R38 + Xn, R20/22, R36/38 |
| Molekylær formel, Molecular formula | C10H8N2O2S2Zn |
| Molvægt, Molar weight | 317,68 |
| Vandopløselighed, Water solubility | 6,0 mg/L |
| Damptryk (25° C), Vapour pressure (25° C) | Ikke fordampeligt, fast stof Not volatile, solid substance |
| Oktanol/vand fordelingskoefficient (log Kow), Octanol/water partition coefficient (log Kow) | 0,97 |
| Organisk-stof/vand fordelingskoefficient (log Koc), Organic matter/water partition coefficient (log Koc) | 2,9-4,0 |
4.2 Abiotisk nedbrydning
Fotolyse
Zinkpyrithion omdannes meget hurtigt ved fotolyse. Undersøgelser udført under sterile forhold med en lys:mørke cyklus på 12:12 timer har vist, at koncentrationen af [pyridin-2,6-14C]zinkpyrithion i en pH 9 buffer blev reduceret til 33% af den tilsatte radioaktivitet i løbet af 15 min under belysning. Data fra dette forsøg viste desuden, at mindre end 5% af den tilsatte 14C forekom som zinkpyrithion efter 1 times eksponering med lys. Tilsvarende resultater blev opnået, når fotolyse af zinkpyrithion blev undersøgt ved anvendelse af kunstigt havvand. Her udgjorde udgangsstoffet 45% af den tilsatte radioaktivitet efter 15 min, mens 1,3% af den tilsatte dosis forekom som zinkpyrithion efter 24 timer. De beregnede halveringstider for den fotolytiske omdannelse af zinkpyrithion var 13 min i pH 9 buffer og 17,5 min i kunstigt havvand (Reynolds 1995a).
Hydrolyse
Hydrolyse af [pyridin-2,6-14C]zinkpyrithion er blevet undersøgt i vandige opløsninger ved pH 5, 7 og 9, og i kunstigt havvand ved pH 8,2. Generelt var zinkpyrithion hydrolyse-stabil ved alle de undersøgte pH-værdier (Reynolds 1995b).
4.3 Biologisk nedbrydning af zinkpyrithion i det akvatiske miljø
Omdannelse af zinkpyrithion
Forsøg med ferskvands- og saltvandssediment har vist, at omdannelsen af zinkpyrithion i akvatiske systemer foregår med en hurtig indledende rate efterfulgt af en langsommere rate. Dette er et resultat af fordelingen af pyrithion mellem den vandige fase og sedimentet, hvor nedbrydningen forløber med forskellig hastighed i de to delmiljøer. Den resulterende to-fasede omdannelse er observeret både i ferskvand og saltvand, og både under aerobe og anaerobe forhold (Ritter 1996, 1999a-e). Halveringstiderne for fjernelsen af zinkpyrithion fra vandfasen via nedbrydning og sorption til sedimentet var mellem 0,5 og 0,6 timer. Både for aerobe og anaerobe systemer medførte denne fjernelse, at <5% af den tilsatte dosis var tilbage i vandfasen efter 6 timer. Fjernelsen af sorberet pyrithion i den efterfølgende anden fase forløb med en halveringstid på henholdsvis 4 dage under aerobe forhold og 19 timer under anaerobe forhold (Ritter 1999a-e).
Zinkpyrithion reagerer ved transchelatering i tilstedeværelse af metaller, hvorved zinkpyrithion omdannes til kobber(II) pyrithion og andre mere stabile metal-pyrithion-komplekser. Den langsommere, sekundære omdannelsesrate i forsøg, der udføres ved en lav koncentration af zinkpyrithion (0,05 µg/g), skyldes sandsynligvis bindingen af metal-pyrithion-komplekser til sedimentet (Ritter 1999a-e). I tidligere undersøgelser, hvor der blev anvendt en højere koncentration af zinkpyrithion (3 µg/g), kan den sekundære omdannelsesrate skyldes, at den lavere vandopløselighed af kobber(II) pyrithion er hastighedsbegrænsende for omdannelsen (Ritter 1996; Smalley & Reynolds 1996).
Zinkpyrithion omdannes til én-ringede, heterocykliske nedbrydningsprodukter som omadin sulfonsyre og pyridin sulfonsyre. Flere andre nedbrydningsprodukter, der er identificeret af Arch Chemicals, er kendt af VKI, men betegnes her som NP1-NP5.
4.3.1 Mineralisering og nedbrydningsprodukter i aerobt sediment
Den aerobe bionedbrydelighed af zinkpyrithion (3 µg/g) blev undersøgt ved anvendelse af vand og sediment, der var indsamlet fra havne i saltvand og ferskvand, hvor der foretages vedligeholdelse af både (Ritter 1996). Senere undersøgelser med saltvand og sediment er udført for både zinkpyrithion og kobberpyrithion, der blev tilsat i en lavere koncentration på 0,05 µg/g (Ritter 1999a, b, d). I disse undersøgelser forløb nedbrydningen med samme hastighed og resulterede i de samme nedbrydningsprodukter, uanset om pyrithionen blev tilsat som zink- eller kobberkomplekset. Resultaterne fra de nyeste forsøg tillægges den største betydning, da den lavere koncentration af udgangsstoffet medfører mere realistiske sorptions- og nedbrydningsmekanismer.
Mineralisering og nedbrydningsprodukter
Mineraliseringen af [pyridin-2,6-14C]zinkpyrithion (0,05 µg/g) til 14CO2 i saltvand og sediment udgjorde 0,44% af den tilsatte 14C efter 84 dages inkubering ved 25° C (Ritter 1999a,b,d). En tilsvarende lav mineralisering blev observeret i de tidligere forsøg, hvor zinkpyrithion blev tilsat i en koncentration på 3 µg/g (Ritter 1996). I ferskvand og sediment var mineraliseringen af zinkpyrithion større, idet 12% af den tilsatte 14C blev omdannet til 14CO2 efter 30 dage ved 25° C (Ritter 1996).
Det første trin i den aerobe nedbrydning af zinkpyrithion er dannelsen af det tilhørende disulfid, der betegnes som omadin disulfid. I undersøgelser, der blev udført med zinkpyrithion i koncentrationen 3 µg/g (Ritter 1996), blev omadin disulfid dannet som et af de væsentligste nedbrydningsprodukter. Omadin disulfid har næsten samme kemiske struktur som zinkpyrithion og er påvist at være meget giftigt over for vandlevende organismer (tabel 4.7). Tilstedeværelsen af omadin disulfid var kun midlertidig, da den videre omdannelse af dette nedbrydningsprodukt medførte, at omadin disulfid udgjorde 2,8% af den tilsatte radioaktivitet efter 30 dage i eksperimentet med saltvand og sediment (i eksperimentet med ferskvand og sediment var koncentrationen af omadin disulfid under detektionsgrænsen på ca. 0,3 ng/g efter 30 dage). Påvisningen af omadin disulfid i forsøgene, hvor zinkpyrithion blev tilsat i 3 µg/g, skyldes sandsynligvis desorptions- og nedbrydningskinetikken ved den anvendte koncentration, der betragtes som miljømæssigt urealistisk. I de nye forsøg, hvor koncentrationsniveauet var 0,05 µg/g (Ritter 1999a,b,d), blev omadin disulfid ikke påvist, og omadin disulfid må derfor opfattes som et midlertidigt nedbrydningsprodukt i den biologiske omdannelse af zinkpyrithion til én-ringede, heterocykliske forbindelser. På baggrund af de forsøg, der er udført med en koncentration på 0,05 µg/g, vurderes de væsentligste produkter fra den aerobe nedbrydning af zinkpyrithion at være omadin sulfonsyre, pyridin sulfonsyre og to andre nedbrydningsprodukter, der benævnes NP1 og NP2 (tabel 4.2). NP2 blev kun påvist ved ekstraktion af sedimentet med base. Det er dog endnu ikke afklaret, hvorvidt dette nedbrydningsprodukt blev dannet i sedimentet før ekstraktion eller ved en kemisk reaktion i det basiske ekstrakt. Data fra undersøgelser af omdannelsen af kobberpyrithion i anaerobe akvatiske systemer tyder på, at NP2 sandsynligvis var tilstede i sedimentet inden ekstraktionen (Ritter 1999a-e).
Tabel 4.2
Aerob bionedbrydning af [14C]zinkpyrithion til nedbrydningsprodukter og kuldioxid i havvand og sediment (data fra Ritter 1999a,b,d).
Aerobic biodegradation of [14C]zinc pyrithione into degradation products and carbon dioxide in seawater and sediment (data from Ritter, 1999a,b,d).
% af tilsat dosis, % of added dose |
|||||||
Tid (dage) |
Zink- |
NP1 |
Omadin sulfonsyre |
Pyridin sulfon- |
NP2 |
Ikke ekstra- |
CO2 |
0 |
49,1 |
16,2 |
- |
- |
20,5 |
6,2 |
- |
1 |
9,8 |
25,8 |
- |
- |
40,7 |
14,2 |
0,01 |
3 |
11,7 |
36,0 |
- |
- |
22,0 |
22,2 |
0,02 |
7 |
1,5 |
41,5 |
4,2 |
4,5 |
17,3 |
24,8 |
0,05 |
14 |
1,6 |
26,4 |
17,2 |
6,8 |
13,5 |
28,5 |
0,08 |
21 |
3,0 |
5,6 |
33,7 |
10,2 |
10,5 |
31,8 |
0,16 |
30 |
1,1 |
7,2 |
35,3 |
11,8 |
8,2 |
27,8 |
0,23 |
42 |
1,8 |
8,0 |
28,6 |
11,9 |
8,0 |
34,3 |
0,33 |
63 |
1,2 |
- |
28,9 |
17,4 |
7,9 |
29,7 |
0,39 |
84 |
2,0 |
1,7 |
31,7 |
24,7 |
4,4 |
30,4 |
0,44 |
-, ikke påvist, not detected.
En betydelig del af nedbrydningsprodukterne var bundet til sedimentet og modstod ekstraktion med acetonitril efterfulgt af to ekstraktioner med 0,1 N KOH. Andelen af disse ikke-ekstraherbare 14C-mærkede nedbrydningsprodukter blev forøget i løbet af de første 14 dage og udgjorde ca. 30% af den tilsatte 14C i perioden fra 14 dage til eksperimentets afslutning efter 84 dage. Den totale genfindelse af den tilsatte radioaktivitet varierede mellem 93 og 99% (Ritter 1999a,b,d).
Undersøgelser med danske sedimenter
Den aerobe bionedbrydelighed af zinkpyrithion (0,037 µg/g) blev undersøgt i sediment og havvand fra de samme to lokaliteter i Øresund som ved undersøgelsen af DCOI, der omfattede et lerholdigt og et sandet sediment (jf. afsnit 3.2.2 og bilag 2). Mineraliseringen af [pyridin-2,6-14C]zinkpyrithion til 14CO2 udgjorde 2,8% af den tilsatte 14C i det lerholdige sediment og 5,0% af den tilsatte 14C i det sandede sediment efter 42 dages inkubering ved 15° C (figur 4.1-4.2). Undersøgelsen af fordelingen af 14C ved forsøgenes afslutning efter 42 dage viste, at nedbrydningsprodukter fra omdannelsen af zinkpyrithion primært var vandopløselige forbindelser. I testsystemet med det sandede sediment blev 65% af den tilsatte 14C genfundet i systemets vandfase, mens 22% var bundet til hydrolyserbare forbindelser og fulvussyrer i sedimentet. I forsøget med det lerholdige sediment blev 32% af den tilsatte 14C genfundet i vandfasen, mens sedimentet indeholdt 38% i form af hydrolyserbare forbindelser og fulvussyrer. Sammenlignet hermed udgjorde nedbrydningsprodukter bundet til humussyrer, humin og lermineraler en mindre andel på mellem 3,6% (sandet sediment) og 16% (lerholdigt sediment) af den tilsatte radioaktivitet. Resultaterne af de kemiske analyser (tabel 4.2) viser, at den resterende 14C ved forsøgets afslutning var nedbrydningsprodukter og ikke intakt zinkpyrithion. Nedbrydningsprodukterne vurderes at have en høj biotilgængelighed, da radioaktiviteten især forekom i form af vandopløselige forbindelser. Metoder og resultater er udførligt beskrevet i bilag 2.
Figur 4.1 Se her
Mineralisering af [14C] zinkpyrithion (0,037 mg/g) i lerholdigt sediment og havvand fra Øresund (sediment LS) Aerobe forhold. Stiplet kurve angiver 14CO2 frigivet ved forsuring.
Mineralization of [14C] zinkpyrithione (0.037 m g/g) in clayey sediment and seawater from Øresund (sediment LS) Aerobic conditions. Dotted curve represents 14CO2 released by acidification.
Figur 4.2 Se her
Mineralisering af [14C] zinkpyrithion (0,037 mg/g) i sandet sediment og havvand fra Øresund (sediment SS) Aerobe forhold. Stiplet kurve angiver 14CO2 frigivet ved forsuring.
Mineralization of [14C] zinkpyrithione (0.037 mg/g) in sandy sediment and seawater from Øresund (sediment SS) Aerobic conditions. Dotted curve represents 14CO2 released by acidification.
Vand- og sedimentprøver fra forsøgene blev udtaget ved forsøgenes start og efter 28 dage. Kemiske analyser af zinkpyrithion og nedbrydningsprodukter blev foretaget af Arch Chemicals (Cheshire, Connetticut). Disse analyser viser, at zinkpyrithion hovedsageligt blev omdannet til omadin sulfonsyre, pyridin sulfonsyre og NP1 i begge sedimenter (tabel 4.3).
Tabel 4.3 Se her
Aerob bionedbrydning af [14C]zinkpyrithion til nedbrydningsprodukter og
kuldioxid i saltvand og sediment fra Øresund.
Aerobic biodegradation of [14C]zinc pyrithione into metabolites and carbon
dioxide in seawater and sediment from Øresund.
4.3.2 Mineralisering og nedbrydningsprodukter i anaerobt sediment
Den anaerobe bionedbrydelighed af zinkpyrithion (3 µg/g) blev undersøgt ved anvendelse af vand og sediment, der var indsamlet fra de samme ferske og marine lokaliteter som i de aerobe forsøg (Ritter 1996). Senere undersøgelser med saltvand og sediment er udført med både kobberpyrithion og zinkpyrithion, der blev tilsat i en koncentration på 0,05 µg/g (Ritter 1999a,c,e). De nyeste resultater fra forsøg udført i koncentrationen 0,05 µg/g (Ritter 1999a,b,d) tillægges den største betydning for vurderingen af zinkpyrithions skæbne under anaerobe forhold.
Mineralisering og nedbrydningsprodukter
I lighed med resultaterne fra de aerobe bionedbrydningsforsøg var mineraliseringen af [pyridin-2,6-14C]zinkpyrithion til kuldioxid ubetydelig i anaerobt marint sediment. Dannelsen af 14CO2 udgjorde 0,9% af den tilsatte 14C efter 182 dages inkubering ved 25°C (Ritter 1999a,b,d).
I de tidligere undersøgelser, hvor zinkpyrithion blev tilsat i en koncentration på 3 µg/g, blev omadin disulfid dannet som midlertidigt nedbrydningsprodukt, mens et usymmetrisk disulfid af NP3 og 2-mercaptopyridin N-oxid var til stede gennem hele forsøgsperioden på 91 dage (Smalley & Reynolds 1996). Dannelsen af disse to-ringede nedbrydningsprodukter i betydende mængder (>10% af den tilsatte radioaktivitet) skyldes formodentlig den gældende sorptions- og nedbrydningskinetik ved den anvendte koncentration. I de nye forsøg, hvor koncentrationen af zinkpyrithion var 0,05 µg/g, blev hverken omadin disulfid eller det usymmetriske disulfid påvist (Ritter 1999a,b,d). Det væsentligste nedbrydningsprodukt fra den anaerobe omdannelse af zinkpyrithion tilsat i koncentrationen 0,05 µg/g var NP3, mens lavere koncentrationer af tre andre én-ringede heterocykliske forbindelser (pyridin sulfonsyre, NP4 og NP5) blev dannet som følge af den videre omdannelse af NP3 (tabel 4.4). Små mængder af NP1 blev dannet umiddelbart efter forsøgets start (<1% af tilsat 14C; dag 3), men dette nedbrydningsprodukt blev omdannet til andre forbindelser og kunne ikke påvises efter 14 dage (Ritter 1999a,b, d).
Tabel 4.4
Anaerob bionedbrydning af zinkpyrithion til nedbrydningsprodukter og kuldioxid i saltvand og sediment (data fra Ritter 1999a,b,d).
Anaerobic biodegradation of zinc pyrithione into metabolites and carbon dioxide in seawater and sediment (data from Ritter 1999a,b,d.).
% af tilsat dosis, % of added dose |
|||||||
Tid (dage) |
Zink- |
NP3 |
NP4 |
Pyridin sulfon- |
NP5 |
Ikke ekstra- |
CO2 |
0 |
30,1 |
21,2 |
2,1 |
1,0 |
5,2 |
7,4 |
- |
1 |
4,7 |
62,0 |
3,5 |
- |
6,8 |
5,8 |
- |
3 |
0,3 |
74,5 |
3,0 |
0,1 |
3,1 |
7,9 |
- |
7 |
0,1 |
78,1 |
1,5 |
0,8 |
2,7 |
9,1 |
- |
14 |
- |
54,5 |
5,9 |
3,3 |
8,2 |
14,8 |
- |
22 |
- |
38,0 |
8,8 |
1,4 |
5,4 |
18,2 |
0,1 |
30 |
- |
32,9 |
7,4 |
2,0 |
4,7 |
19,2 |
0,3 |
63 |
- |
14,3 |
8,5 |
2,2 |
5,5 |
29,4 |
0,6 |
90 |
1,8 |
13,7 |
3,4 |
2,2 |
4,0 |
34,3 |
0,3 |
182 |
- |
2,3 |
7,9 |
4,3 |
1,2 |
52,7 |
0,9 |
-, ikke påvist, not detected.
En betydelig del af nedbrydningsprodukterne var bundet til sedimentet og modstod ekstraktion med acetonitril og alkali. Koncentrationen af ikke-ekstraherbare, sediment-bundne nedbrydningsprodukter blev gradvist forøget gennem forsøget og udgjorde 53% af den tilsatte 14C efter 182 dage. Den totale genfindelse af den tilsatte radioaktivitet varierede mellem 90 og 102% (Ritter 1999a,b,d).
Undersøgelser med danske sedimenter
Den anaerobe bionedbrydelighed af zinkpyrithion (0,037 mg/g) blev undersøgt ved anvendelse af det lerholdige sediment og tilhørende havvand (bilag 2), som ligeledes blev anvendt i de aerobe forsøg (jf. afsnit 4.3.1). Sediment og havvand blev inkuberet under anaerobe, sulfatreducerende forhold, der normalt er fremherskende i kystnære marine sedimenter. Mineraliseringen af [pyridin-2,6-14C]zinkpyrithion til 14CO2 udgjorde 3,5% af den tilsatte 14C efter 56 dages inkubering ved 15°C (figur 4.3). Sammenlignet med forsøgene, der blev udført under aerobe forhold, var der en større andel af de anaerobt dannede nedbrydningsprodukter, som var bundet til humussyrer, humin og lermineraler i sedimentet. Denne andel udgjorde 39% af den tilsatte 14C efter 56 dages inkubering af det lerholdige sediment og tilhørende havvand. Mere vandopløselige nedbrydningsprodukter i systemets vandfase eller bundet til hydrolyserbare forbindelser og fulvussyrer udgjorde dog en væsentlig andel på i alt 35% af den tilsatte radioaktivitet. Ligesom i de aerobe forsøg blev zinkpyrithion omdannet til nedbrydningsprodukter (tabel 4.5), hvoraf flere vurderes at have en høj biotilgængelighed. Metoder og resultater er udførligt beskrevet i bilag 2.
Figur 4.3 Se her
Mineralisering af [14C] zinkpyrithion (0,037 mg/g) i lerholdigt sediment og havvand fra Øresund (sediment LS) Anaerobe forhold. Stiplet kurve angiver 14CO2 frigivet ved forsuring.
Mineralization of [14C] zinkpyrithione (0.037 mg/g) in clayey sediment and seawater from Øresund (sediment SS) Anaerobic conditions. Dotted curve represents 14CO2 released by acidification.
Vand- og sedimentprøver fra forsøgene blev udtaget ved forsøgets start og efter 28 dage. Kemiske analyser af zinkpyrithion og nedbrydningsprodukter i disse prøver blev foretaget af Arch Chemicals (Cheshire, Connetticut). Resultaterne af de udførte analyser viser, at de kvantitativt væsentligste nedbrydningsprodukter under anaerobe, sulfatreducerende forhold var de énringede, heterocykliske forbindelser NP3 og NP5 (tabel 4.5).
Tabel 4.5 se her
Anaerob bionedbrydning af [14C] zinkpyrithion til nedbrydningsprodukter og kuldioxid i saltvand og sediment fra Øresund.
Anaerobic biodegradation of [14C]zinc pyrithione into metabolites and carbon dioxide in seawater and sediment from Øresund.
4.4 Toksicitet over for akvatiske organismer
Zinkpyrithion
Toksiciteten af det aktive stof zinkpyrithion er undersøgt ved standardlaboratorietest med en række vandlevende organismer, der findes i ferskvand (grønalgen Selenastrum capricornutum, krebsdyret Daphnia magna, fiskene regnbueørred (Oncorhynchus mykiss) og "fathead minnow" (Pimephales promelas)) og saltvand (krebsdyret Mysidopsis bahia og fisken "sheepshead minnow" (Cyprinodon variegatus) samt østers (Crassostrea virginica)) (Boeri et al. 1993, 1994a-e, 1999; Ward et al. 1994a). Desuden blev fem arter af ferskvandsfisk anvendt sammen i en enkelt test (Olin 1997). Pimephales promelas blev også benyttet i denne test, og resultatet for denne art var i overensstemmelse med resultatet i standardtesten. P. promelas var i øvrigt den mest følsomme af de fem arter. På grund af zinkpyrithions manglende stabilitet ved lyspåvirkning blev forsøgene gennemført med dæmpet lys og alle forsøg - undtagen algetest - foregik med konstant udskiftning af testopløsningen (gennemstrømning). Herved lykkedes det at holde eksponeringskoncentrationen næsten konstant i alle forsøgene - selv i algetesten (Ward et al. 1994a), hvor mediet ikke kan udskiftes, og alle resultater er beregnet ud fra målte koncentrationer.
Resultaterne, der er samlet i bilag 5, viser, at der ikke var stor forskel på følsomheden af ferskvands- og saltvandsorganismer. Alger er tilsyneladende den taksonomiske gruppe, der er mindst følsom over for zinkpyrithion. Tabel 4.6 viser en oversigt over zinkpyrithions toksicitet over for forskellige grupper af organismer.
Der er gennemført langtidsstudier med krebsdyr (dafnier og små rejer) samt fisk (den mest følsomme, Pimephales promelas, i korttidstest). I krebsdyrstudierne er forplantningen undersøgt, og i fiskestudiet er udviklingen fra æg til småfisk fulgt. Det fremgår af resultaterne i tabel 4.6, at fisk også er den mest følsomme gruppe i langtidstest, om end resultaterne med krebsdyr og fisk er af samme størrelsesorden; laveste NOEC er 0,0023 mg/L for krebsdyr og 0,0012 mg/L for fisk.
Tabel 4.6
Økotoksikologiske data for effekter af zinkpyrithion på vandlevende organismer. Alle koncentrationer er målte koncentrationer, forsøgene med dyr blev udført med gennemstrømning (se bilag 5 for detaljerede data).
Ecotoxicological data for effects of zinc pyrithione on aquatic organisms. All concentrations are measured concentrations, tests with animals were flow through tests (see Appendix 5 for detailed data).
| Systematisk gruppe Taxonomic group |
Effektmål |
Eksponerings- |
Resultat |
| Alger, algae | EC50 |
5 |
0,028 |
| Alger, algae | NOEC* |
5 |
0,0078 |
| Krebsdyr, crustaceans |
EC50 |
2-4 |
0,0036-0,0063 |
| Krebsdyr crustaceans |
NOEC |
21 |
0,0023-0,0027 |
| Fisk, fish | LC50 |
4 |
0,0026-0,4 |
| Fisk, fish | NOEC |
32 |
0,0012 |
| Østers, oyster | EC50 (skalafsætning) |
4 |
0,022 |
*: Den højeste koncentration, hvor der ikke blev observeret effekt (NOEC, No Observed Effect Concentration).
*: The highest concentration at which no effects were observed (NOEC, No Observed Effect Concentration).
Nedbrydningsprodukter
Toksiciteten af tre nedbrydningsprodukter er undersøgt i laboratoriet. Resultaterne af disse test er opsummeret i tabel 4.7 sammen med resultaterne af de tilsvarende test med zinkpyrithion.
Tabel 4.7
Oversigt over resultater af test af toksiciteten af zinkpyrithion samt tre nedbrydningsprodukter for vandlevende organismer. Alle er korttidstest og resultaterne er opgivet som LC50 eller EC50. For zinkpyrithion og omadin sulfonsyre er der tale om målte koncentrationer.
Summary of results from aquatic toxicity tests with zinc pyrithione and three metabolites. All are short term tests and the results are expressed as LC50 or EC50. Measured concentrations for zinc pyrithione and omadine sulfonic acid.
| Systematisk gruppe Taxonomic group |
Zinkpyrithion |
Omadin disulfid* |
Omadin sulfon |
Pyridin sulfon |
| Alger, algae | 0,028 |
0,14 |
36 |
29 |
| Krebsdyr, crustaceans |
0,0036-0,0063 |
0,0064-0,013 |
>127-71 |
72- >122 |
| Fisk, fish | 0,0026-0,4 |
0,03-1,1 |
59- > 137 |
57- >127 |
| Østers, oyster | 0,022 |
0,160 |
99 |
86 |
*: Data fra Olin 1997, Data from Olin 1997.
For alle fire stoffer gælder, at de er testet på 1 ferskvandsalge (Selenastrum capricornutum), 1 ferskvandskrebsdyr (Daphnia magna) og 1 saltvandskrebsdyr (Mysidopsis bahia) samt 2 ferskvandsfisk (Pimephales promelas og Oncorhyncus mykiss) og 1 saltvandsfisk (Cyprinodon variegatus), hvortil kommer en skalafsætningstest med østersarten Crassostrea virginica (saltvand). Pyridin sulfonsyre er endvidere anvendt i langtidstest med fisken Pimephales promelas (Boeri et al. 1999).
I algetesten med omadin sulfonsyre faldt koncentrationen af stoffet under testen. De koncentrationer, der er benyttet til beregning af effektkoncentrationen, er målt ved testens start, og den reelle EC50 er sandsynligvis noget lavere end den værdi, der angives i tabel 4.7 (EC50: 36 mg/L) (Boeri et al. 1994g). I de øvrige test (Ward et al. 1994b, c, d; Boeri et al. 1994f, h, i) er resultaterne beregnet som gennemsnittet af koncentrationen ved start og slut af testen. Anvendes denne beregningsmetode på resultaterne fra algetesten fås EC50 = 23 mg/L.
Resultaterne viser, at mens zinkpyrithion og omadin disulfid var meget giftige (L(E)C50 i størrelsesordenen 3-300 µg/L) for vandlevende organismer, var omadin sulfonsyre og pyridin sulfonsyre (der er en-ringede heterocykliske forbindelser) væsentligt mindre giftige (størrelsesordenen >20 mg/L) (Olin 1977). Pyrindin sulfonsyre gav ingen effekter ved en koncentration på 0,01 mg/L i et langtidsstudie med fiskeæg og -larver (Boeri et al. 1999). Alger var den gruppe organismer, der var mest følsom for de to sidste stoffer. Der var ikke for nogen af stofferne gennemgående forskelle i følsomheden af ferskvands- og saltvandsorganismer.
Effekter af nedbrydning af zinkpyrithion på akvatisk toksicitet
Et parallelt forsøg, som dét, der blev beskrevet for DCOI (jf. afsnit 3.3.2), blev udført for at undersøge relationen mellem nedbrydning af zinkpyrithion og den akutte giftighed over for Acartia tonsa. Undersøgelserne blev udført på samme måde som for DCOI ved anvendelse af sediment-havvand-systemer, der blev tilsat zinkpyrithion i koncentrationen 25 µg/kg. Vandfase og sediment blev adskilt 20 min efter dosering, og anvendelse af vandfasen i test med A. tonsa medførte en dødelighed svarende til 100% af forsøgsorganismerne. Resultaterne af undersøgelsen viste, at stationær inkubering i mørke eller lys (340 µmol/m2 · s) ved 20-25°C medførte, at der ikke var dødelige effekter på A. tonsa efter 1 dag (figur 4.4). Den hurtige detoksificering viser, at zinkpyrithion hurtigt blev bundet til sedimentet eller omdannet til nedbrydningsprodukter med en væsentlig lavere giftighed end udgangsstoffet, ligesom det var tilfældet for DCOI (jf. afsnit 3.3.2). De anvendte metoder er udførligt beskrevet i bilag 3.
Figur 4.4 Se her
Effekter af nedbrydning af zinkpyrithion (25 µg/kg) doseret til sediment og havvand på den akutte toksicitet over for Acartia tonsa (forsøg udført i mørke).
Effects of degradation of zinc pyrithione (25 µg/kg) dosed to sediment and seawater on the acute toxicity to Acartia tonsa (test performed in the dark).
4.5 Vurdering af zinkpyrithion og nedbrydningsprodukter
Zinkpyrithion omdannes meget hurtigt i akvatiske systemer. Tabel 4.2 og 4.4 viser, at efter inkubation i mindre end 1 døgn udgjorde den intakte zinkpyrithion mindre end halvdelen af den tilsatte radioaktivitet (dag 0). Zinkpyrithion antages at blive omdannet via det strukturelt lignende omadin disulfid, der hurtigt omdannes til én-ringede heterocykliske forbindelser under miljørealistiske forsøgsbetingelser. De gennemførte forsøg med zinkpyrithion viste, at de kvantitativt vigtigste nedbrydningsprodukter var omadin sulfonsyre og pyridin sulfonsyre under aerobe forhold og NP3, NP4, NP5 og pyridin sulfonsyre under anaerobe forhold (Tabel 4.2-4.5). De en-ringede heterocykliske forbindelser vurderes alle at være svært nedbrydelige og stabile i akvatiske miljøer. Den biologiske nedbrydning af zinkpyrithion fører til en kvantitativt betydelig dannelse af nedbrydningsprodukter, der bindes til sedimentet. Dette fremgår af, at ca. 30% af den tilsatte radioaktivitet var bundet til sedimentet ved afslutningen af det aerobe bionedbrydningsforsøg efter 84 dage, mens ca. 50% af den tilsatte 14C kunne genfindes i sedimentet i det anaerobe forsøg efter 182 dage (Ritter 1999a, b, d).
Den akvatiske toksicitet er undersøgt for omadin sulfonsyre og pyridin sulfonsyre, der begge var væsentligt mindre giftige (L(E)C50 i størrelsesordenen mg/L) end zinkpyrithion og omadin disulfid (L(E)C50 i størrelsesordenen µg/L). Baseret på stoffernes kemiske struktur anses det for sandsynligt, at toksiciteten af de øvrige en-ringede nedbrydningsprodukter vil være på samme niveau som toksiciteten af omadin sulfonsyre og pyridin sulfonsyre. På denne baggrund vurderes det, at de kendte stabile nedbrydningsprodukter fra omdannelsen af zinkpyrithion under aerobe og anaerobe forhold vil have en akvatisk giftighed, der er mellem 1.000 og 10.000 gange lavere end giftigheden af zinkpyrithion (jf. tabel 4.7). De sedimentbundne nedbrydningsprodukter er endnu ikke identificeret. Da disse nedbrydningsprodukter ikke kunne ekstraheres fra sedimentet med acetonitril og KOH, vurderes de at have en lav biotilgængelighed og dermed en lav giftighed over for akvatiske organismer.
4.6 Risikovurdering af zinkpyrithion
Beregning af eksponeringskoncentrationer (PEC)
Eksponeringskoncentrationer (PEC, Predicted Environmental Concentration) blev beregnet for en lystbådehavn (Jyllinge Lystbådehavn) og en befærdet sejlrute ved anvendelse af internationalt accepterede principper (EC 1996) som beskrevet for DCOI (jf. afsnit 3.4). Modellen og de to scenarier er udførligt beskrevet i bilag 1. For udgangsstoffet og de væsentligste nedbrydningsprodukter blev følgende eksponeringskoncentrationer beregnet:
- PEC (vandsøjle)
- PEC (sediment)
- PEC (sediment-porevand)
De tre eksponeringskoncentrationer blev defineret som "steady-state" koncentrationen i det pågældende delmiljø; dvs. den koncentration, som de beregnede koncentrationer nærmer sig med tiden, når der simuleres en kontinuerlig frigivelse af udgangsstoffet til vandmiljøet. Den anvendte model er ikke valideret over for målte koncentrationer i havnemiljøer eller sejlruter. Eksponeringskoncentrationerne blev beregnet ud fra følgende antagelser:
- Baggrundskoncentrationerne for både udgangsstoffet og nedbrydningsprodukterne blev antaget at være nul.
- 70% af lystbådene blev antaget at være påført maling indeholdende zinkpyrithion.
- Frigivelseshastigheden af zinkpyrithion fra bundmaling blev beregnet til 21 mg/m2/dag i havn og 41 mg/m2/dag ved sejlads.
- Den gennemsnitlige fotolytiske halveringstid for zinkpyrithion blev beregnet til 9,8 timer for Jyllinge Lystbådehavn og 6,6 timer for sejlrute ved Kronprins Frederiks Bro (jf. bilag 1). Det var ikke muligt at kvantificere, hvor meget tilstedeværelsen af bådene og skyggevirkninger fra molekajen påvirker mængden af sollys, der rammer vandoverfladen, hvorfor der er foretaget beregninger med og uden inddragelse af fotolyse.
- Den primære biologiske omdannelse af zinkpyrithion til én-ringede, heterocykliske forbindelser blev antaget at forløbe med en halveringstid på 12 timer i overfladevand ved en temperatur på 25°C.
Den halveringstid for zinkpyrithion, der antages i simuleringen, svarer til en væsentligt langsommere omdannelse af zinkpyrithion end den initielle fjernelse af stoffet fra vandfasen i undersøgelser med havvand og sediment (jf. afsnit 4.3). Sammenlignet med fjernelsen af zinkpyrithion fra vandfasen (Ritter 1999a-e) anvendes en længere halveringstid i simuleringen, fordi akvatiske systemer med sediment giver mulighed for sorption og normalt har et større potentiale for biologisk nedbrydning sammenlignet med nedbrydningspotentialet i pelagialet i havvand. Anvendelsen af en halveringstid for omdannelsen af zinkpyrithion, der svarer til den forventede omdannelse i overfladevand, skyldes, at resultatet af simuleringen er eksponeringskoncentrationer ved en kontinuerlig frigivelse af zinkpyrithion efter opnået "steady-state". Når lystbådene tages op af vandet ved sejlsæsonens afslutning, vil zinkpyrithion sandsynligvis hurtigt blive elimineret, da stoffet enten omdannes i vandfasen eller vil bindes til sedimentet, hvor det omdannes med en meget kort halveringstid (jf. afsnit 4.2 og 4.3).
De beregnede eksponeringskoncentrationer for zinkpyrithion og nedbrydningsprodukter er ca. 50 gange højere inden for lystbådehavnen end i den befærdede sejlrute udenfor (tabel 4.8).
Tabel 4.8a
Beregnede eksponeringskoncentrationer (PEC) for zinkpyrithion og nedbrydningsprodukter ved "steady-state". Fotolyse inkluderet.
Calculation of PEC for zinc pyrithione and metabolites at steady-state. Photolysis included.
| Scenarie Scenario |
Stof Substance |
PEC (vand) |
PEC (sediment, porevand) |
PEC (sediment, bundet) |
| mg/L | mg/L | mg/kg | ||
| Lystbådehavn Pleasure craft harbour |
Zinkpyrithion, Zinc pyrithione | 0,56 |
0,00056 |
0,089 |
| NP3 | 1,22 |
0,25 |
0,68 |
|
| NP4 | 0,099 |
0,19 |
0,078 |
|
| Pyridin sulfonsyre, Pyridine sulfonic acid | 0,0080 |
0,068 |
0,040 |
|
| NP1 | 0,15 |
0,091 |
0,062 |
|
| Omadin sulfonsyre, Omadine sulfonic acid | 0,012 |
0,48 |
0,47 |
|
| Andre forbindelser, Other compounds | 0,11 |
- |
- |
|
| Sejlrute Navigation route |
Zinkpyrithion, Zinc pyrithione | 0,0053 |
0,00001 |
0,00090 |
| NP3 | 0,027 |
0,0028 |
0,0076 |
|
| NP4 | 0,0027 |
0,0022 |
0,00089 |
|
| Pyridin sulfonsyre, Pyridine sulfonic acid | 0,00040 |
0,00077 |
0,00045 |
|
| NP1 | 0,0032 |
0,0011 |
0,00077 |
|
| Omadin sulfonsyre, Omadine sulfonic acid | 0,00046 |
0,0059 |
0,0058 |
|
| Andre forbindelser, Other compounds | 0,0032 |
- |
- |
Tabel 4.8b
Beregnede eksponeringskoncentrationer (PEC) for zinkpyrithion og nedbrydningsprodukter ved "steady-state". Fotolyse ikke inkluderet.
Calculation of PEC for zinc pyrithione and metabolites at steady-state. Photolysis not included.
| Scenarie Scenario |
Stof Substance |
PEC (vand) |
PEC (sediment, porevand) |
PEC (sediment, bundet) |
mg/L |
mg/L |
mg/kg |
||
| Lystbådehavn Pleasure craft harbour |
Zinkpyrithion, Zinc pyrithione | 1,7 |
0,0013 |
0,21 |
| NP3 | 0,00006 |
0,54 |
1,5 |
|
| NP4 | 0,20 |
0,43 |
0,18 |
|
| Pyridin sulfonsyre, Pyridine sulfonic acid | 0,016 |
0,15 |
0,090 |
|
| NP1 | 0,45 |
0,24 |
0,17 |
|
| Omadin sulfonsyre, Omadine sulfonic acid | 0,036 |
1,3 |
1,3 |
|
| Andre forbindelser, Other compounds | 0,24 |
- |
- |
|
| Sejlrute Navigation route |
Zinkpyrithion, Zinc pyrithione | 0,022 |
0,00002 |
0,0027 |
| NP3 | 0,00001 |
0,0072 |
0,019 |
|
| NP4 | 0,0059 |
0,0061 |
0,0025 |
|
| Pyridin sulfonsyre, Pyridine sulfonic acid | 0,00088 |
0,0022 |
0,0013 |
|
| NP1 | 0,013 |
0,0042 |
0,0028 |
|
| Omadin sulfonsyre, Omadine sulfonic acid | 0,0019 |
0,022 |
0,021 |
|
| Andre forbindelser, Other compounds | - |
- |
- |
Beregning af nul-effekt-koncentration (PNEC)
Nul-effekt-koncentrationer (PNEC, Predicted No-Effect Concentration) er estimeret for zinkpyrithion og pyridin sulfonsyre. De øvrige stabile nedbrydningsprodukter fra omdannelsen af zinkpyrithion antages at have samme akvatiske toksicitet som pyridin sulfonsyre.
De foreliggende undersøgelser af den akvatiske giftighed af zinkpyrithion anses for repræsentative, og datamaterialet omfatter langtidsstudier med krebsdyr og den mest følsomme organismegruppe fisk. Algetesten kan fortolkes både som en korttidstest og en langtidstest (EC 1996).
For zinkpyrithion fortolkes data som omfattende tre NOEC-værdier fra langtidstest (krebsdyr, alger og fisk), der omfatter den gruppe organismer, der var mest følsom i korttidstest (fisk). På den baggrund beregnes PNEC ved division af den laveste NOEC-værdi, der er 0,0012 mg/L for fisk, med en omregningsfaktor på 10 (EC 1996). Dette giver en PNEC på 0,0001 mg/L = 0,1 mg/L for zinkpyrithion.
Resultatet af den langtidstest med fisk og pyridin sulfonsyre, der er gennemført (Boeri et al. 1999), anses ikke for anvendelig til beregning af PNEC. Dette skyldes, at der kun blev anvendt én koncentration (0,01 mg/L), hvor der ikke blev målt nogen effekter. Resultatet viser således ikke noget om i hvilket koncentrationsområde, effekter kan forventes. Beregninger af PNEC for pyridin sulfonsyre baseres derfor på den laveste effektkoncentration i tabel 4.7. Algetesten anses for at være den eneste, der kan betragtes som en langtidstest, og den alene giver ikke tilstrækkeligt grundlag for at basere beregningerne på NOEC (EC 1996). Der er således tale om data fra korttidstest, og der anvendes en omregningsfaktor på 1.000 over for den laveste effektkoncentration. For pyridin sulfonsyre anvendes EC50-værdien på 28,9 mg/L for alger (pyridin sulfonsyre), hvilket giver PNEC på 0,03 mg/L = 30 µg/L. Den beregnede PNEC for pyridin sulfonsyre antages at være repræsentativ for de øvrige stabile nedbrydningsprodukter fra omdannelsen af zinkpyrithion.
De to beregninger af PNEC er vist i tabel 4.9.
Tabel 4.9
Beregning af PNEC for zinkpyrithion og pyridin sulfonsyre.
Calculation of PNEC for zinc pyrithione and pyridine sulfonic acid.
| Stof, substance | Laveste effekt- koncentration Lowest effect concentration |
Værdi, value |
Omregningsfaktor |
PNEC |
| Zinkpyrithion, Zinc pyrithione |
Langtidstest, long-term test NOEC fisk NOEC fish |
|
|
|
| Pyridin sulfonsyre, pyridine sulfonic acid |
Korttidstest, short-term test EC50 alger EC50 algae |
|
|
|
Risikokvotient
I situationen, hvor fotolytisk omdannelse af zinkpyrithion indgår i beregningen af PEC, beregnes risikokvotienten ud fra PEC (vand) for zinkpyrithion og de angivne nedbrydningsprodukter i tabel 4.8. PEC (sediment, porevand) for nedbrydningsprodukterne er højere end den tilsvarende PEC (vand), når fotolytisk omdannelse negligeres. Derfor anvendes i dette tilfælde PEC (vand) for zinkpyrithion og PEC (porevand) for nedbrydningsprodukterne til beregning af risikokvotienten. Idet der anvendes PNEC-værdier for zinkpyrithion og pyridin sulfonsyre, beregnes risikokvotienter (Rq = PEC/PNEC) som angivet i tabel 4.10.
Tabel 4.10
Beregning af risikokoefficienter (Rq) for zinkpyrithion og dets nedbrydningsprodukter.
Calculation of risk quotients (Rq) for zinc pyrithione and its metabolites.
Stof |
PNEC |
Lystbådehavn Pleasure craft harbour |
Sejlrute Navigation route |
||
|
PECA |
RqA |
PECA |
RqA |
|
| Zinkpyrithion Zinc pyrithione |
0,1 |
0,56 |
5,6 |
0,0053 |
0,05 |
| Nedbrydnings-produkter Metabolites |
30 |
1,6 |
0,05 |
0,037 |
0,0012 |
A
, øverste værdi, fotolyse inkluderet; nederste værdi; fotolyse ikke inkluderet., øverste værdi, fotolyse inkluderet; nederste værdi; fotolyse ikke inkluderet.A, upper value, photolysis included; lower value; photolysis not included.
De angivne risikokvotienter er beregnet ud fra "realistiske worst-case scenarier" (bilag 1), der bl.a. bygger på en antagelse om, at 70% af lystbådene er påført en bundmaling, som indeholder zinkpyrithion. Ud fra antagelserne i simuleringen og de beregnede PEC-værdier vurderes det, at der inden for lystbådehavnen er en risiko for kroniske økotoksiske effekter, idet zinkpyrithion antages at blive tilført konstant ved udludning fra bundmaling. Risikokvotienten for zinkpyrithion uden for lystbådehavnen er mellem 0,05 og 0,22, og her skønnes risikoen for økotoksiske effekter af zinkpyrithion at være lav. Risikokvotienten uden for lystbådehavnen er sandsynligvis tættest på 0,05, hvor fotolyse er inddraget i beregningen af PEC, da der ikke forventes større skyggevirkninger på en almindelig sejlrute.
Inden for lystbådehavnen vurderes der at være en lav risiko for økotoksiske effekter af de stabile nedbrydningsprodukter fra omdannelsen af zinkpyrithion, og denne risiko skønnes at være meget lav i områder uden for lystbådehavnen.
5. Biocidfrie malinger
5.1 Undersøgelser af biocidfrie malinger
5.2 Udvaskningsforsøg og økotoksikologiske test
5.3 Vurdering af biocidfrie malinger
5.1 Undersøgelser af biocidfrie malinger
Pilotforsøg med mekanisk rensning af to biocidfrie bundmalinger blev gennemført af Dansk Sejlunion og Hempel i sejlsæsonen 1998 (Dansk Sejlunion & Hempel 1999).
Biocidfrie bundmalinger bliver defineret og fortolket forskelligt i forskellige officielle sammenhænge. I nærværende rapport gælder definitionen: En biocidfri bundmaling indeholder ikke aktive stoffer (=biocider), der er tilsat med henblik på at forhindre begroning via disse stoffers toksiske virkning. Eksempler på biocider som har været anvendt eller fortsat anvendes i bundmalinger i Danmark er TBT, kobber, Diuron, Irgarol, Nopcocide, Seanine (aktiv stof DCOI), Zincpyrithion, etc.
Den begroningshindrende effekt opnås istedet som resultat af en meget glat overflade, hvorpå begroningen har svært ved at hænge fast (svarende til en "slip-let" effekt, ofte baseret på silikone). Som biocidfrie alternativer overvejes også meget hårde epoxy malinger, som forventes at få en kraftig begroning; men som tillader gentagne mekaniske afrensninger uden at malingens overflade ødelægges.
De to malingtyper var en eksperimentel silikoneholdig maling, 86330, og en epoxy-baseret maling, High Protect 35651, der er et kommercielt produkt beregnet til forebyggelse mod osmose. De miljømæssige egenskaber af de to biocidfrie malinger blev undersøgt ved økotoksikologiske laboratorietest af vandprøver fra udvaskningsforsøg med malede paneler. De økotoksikologiske test omfattede den marine grønalge Skeletonema costatum og det marine krebsdyr Acartia tonsa. Da effekter af stoffer, der udludes fra malingerne, kun er undersøgt i test med to vandlevende organismer, er der anvendt en opstilling, som sikrer en "worst-case" situation i udvaskningsforsøget.
Forholdet mellem det malede areal og den omgivende vandmængde i udvaskningsforsøget blev fastlagt efter beregninger ud fra forholdene i Jyllinge Lystbådehavn. På baggrund af vurderinger fra Dansk Sejlunion (personlig kommunikation med Steen Wintlev-Jensen, Dansk Sejlunion) er det antaget, at bådene i havnen udgøres af 360 sejlbåde med et samlet nedsænket bundareal på 6840 m2 (360 × 19 m2) og 60 motorbåde med et samlet nedsænket bundareal på 1320 m2 (60 × 22 m2). Jyllinge Lystbådehavn har et areal på ca. 31.500 m2 og en gennemsnitlig vanddybde på 2,3 m, hvorefter vandmængden i havnen kan beregnes til 70.450 m3 (jf. bilag 1, tabel A.1). Ud fra disse antagelser er forholdet mellem det malede bundareal på havnens lystbåde og vandmængden i havnen beregnet til 0,11 m2:1 m3. Forholdet mellem det malede areal og det samlede væskevolumen i udvaskningsforsøgene var 1,5 m2:1 m3. Den malede overflade pr. volumenenhed var således 13-14 gange større i udvaskningstesten, end dette forhold ville være, hvis bådene i Jyllinge Lystbådehavn var malet med samme maling.
5.2 Udvaskningsforsøg og økotoksikologiske test
Testmalinger
Laboratorieforsøgene omfattede to biocidfrie malinger (1 og 2 nedenfor) samt Hempel's Antifouling Nautic 76800, der er en organotin-baseret bundmaling til storskibsfart. Testmalingerne i undersøgelsen var følgende:
En eksperimentel 86330 maling (silikone-holdig)
High Protect 35651 (epoxy-baseret)
Hempel's Antifouling Nautic 76800 (organotin-baseret)
Udvaskningsforsøg
Udvaskningsforsøgene blev udført i helstøbte glasakvarier med 38 liter filtreret havvand. Fire paneler, der var påført testmaling på begge sider, blev nedsænket i hvert akvarium, således at kun den malede del af panelerne var i kontakt med havvandet. Den malede overflade på ét panel var 150 cm2. Vandet i akvarierne blev kontinuert beluftet med en svag strøm af atmosfærisk luft, og fordampet væske blev erstattet en gang om ugen. Akvarierne blev dækket med sort plastic og blev placeret ved 20° C. Vandprøver fra akvarierne blev indsamlet efter 0, 6, 13, 20 og 34 dage. Den første dag af udvaskningsforsøget (dag 0) blev udtaget 0,5 liter fra hvert akvarium efter 3 timer, mens der til de øvrige tidspunkter blev udtaget 9 liter fra hvert akvarium. Ved hver udtagning af 9-liters vandprøver blev ét panel fjernet fra akvarierne, således at forholdet mellem det malede areal og væskevolumnet forblev uændret gennem udvaskningsforsøget.
Økotoksikologiske test
Toksiciteten af vandprøverne blev bestemt ved væksthæmningstest med den marine grønalge Skeletonema costatum, der blev udført i overensstemmelse med procedurerne i OECD Guideline for Testing of Chemicals No. 201 "Alga Growth Inhibition Test" (OECD 1984). Algetesten blev udført med vandprøver, der var udtaget efter 0, 6, 13, 20 og 34 dages udvaskning. Resultaterne fra denne test blev anvendt til at vælge vandprøver til undersøgelse af kroniske effekter over for krebsdyr og bestemmelse af potentielt bioakkumulerbare stoffer.
På baggrund af resultaterne fra algetesten blev toksiciteten af vandprøver, der var udtaget efter 13 og 34 dage, bestemt ved test med det marine krebsdyr Acartia tonsa. Giftigheden over for A. tonsa blev undersøgt ved screeningstest for akut toksicitet (ISO 1998) og ved test for kronisk toksicitet, der blev udført som beskrevet af Danmarks Miljøundersøgelser (1986) og Johansen & Møhlenberg (1987). Forekomsten af hydrofobe, potentielt bioakkumulerbare stoffer i udvaskningsvandet blev bestemt i overensstemmelse med OECD Guideline for Testing of Chemicals No. 117 "Partition Coefficient (n-octanol/water), High Performance Liquid Chromatography (HPLC) Method" (OECD 1989).
De anvendte materialer og metoder er udførligt beskrevet i rapporten "Ecotoxicological tests of leachates of antifouling paints" (Bjørnestad et al. 1999), der også indeholder en detaljeret beskrivelse af undersøgelsens resultater. De følgende afsnit sammenfatter de vigtigste resultater.
Væksthæmningstest med alger
Toksicitetstesten med S. costatum viste, at udvaskningsvandet fra High Protect 35651 ikke hæmmede algernes vækst. Derimod afgav både Hempel's Antifouling Nautic 76800 og den eksperimentelle 86330 maling stoffer til det omgivende vand, der medførte en hæmning af algernes vækst (tabel 5.1).
Tabel 5.1
Hæmning af væksten for Skeletonema costatum ved test af udvaskningsvand i en koncentration på 900 mL/L.
Inhibition of growth of Skeletonema costatum of leachates in a concentration of 900 mL/L.
| Testmaling Test paint |
Væksthæmning (%) |
||||
dag 0 |
dag 6 |
dag 13 |
dag 20 |
dag 34 |
|
| Kontrol Control |
< 1 |
< 1 |
< 1 |
< 1 |
< 1 |
| High Protect 35651 | < 1 |
< 1 |
< 1 |
< 1 |
< 1 |
| Eksperimentel 86330 | 2 |
48 |
100 |
100 |
100 |
| Hempel's Antifouling Nautic 76800 | 100 |
100 |
100 |
100 |
100 |
Da resultaterne med den eksperimentelle 86330 maling (tabel 5.1) var overraskende, har Hempel's laboratorium gennemført yderligere udvaskningstest med anvendelse af den metode, der er beskrevet ovenfor (personlig kommunikation med Susanne Holm Faarbæk, Hempel). I disse forsøg blev der indsamlet udvaskningsvand efter 20 dage, hvorefter toksiciteten af de kodede vandprøver blev bestemt af VKI. Vandprøver fra to uafhængige udvaskningsforsøg med den eksperimentelle 86330 medførte en hæmning af S. costatum på henholdsvis 78% og 100%. Udvaskningsvand fra en anden maling, 97003-057, hvis sammensætning er meget lig den eksperimentelle 86330, medførte ingen hæmning af algevæksten. Imidlertid kunne forsøget med 97003-057 malingen ikke reproduceres, da en ny laboratoriebatch af malingen, 97003-128, medførte en 90% hæmning af S. costatum (personlig kommunikation med Susanne Holm Faarbæk, Hempel).
Mens de yderligere udvaskningsforsøg med den eksperimentelle 86330 maling generelt bekræfter resultaterne i tabel 5.1, tyder de divergerende resultater for 97003 malingen på, at variationer af produktionsteknisk eller påføringsmæssig art har stor indflydelse på udludningen af stoffer fra den malede overflade. Det har ikke været muligt at nå til en afklaring af disse forhold i forbindelse med denne undersøgelse.
Toksicitetstest med Acartia tonsa
Vandprøver fra udvaskningsforsøget med High Protect 35651 medførte ingen akut toksicitet over for A. tonsa i screeningstest. Derimod viste den kroniske toksicitetstest, at ufortyndede vandprøver fra udvaskningsforsøget med High Protect 35651 hæmmede udviklingen af Acartia nauplier, mens der ikke blev observeret nogen hæmning, når vandprøverne blev fortyndet 10 gange (100 mL/L) (figur 5.1). Da der heller ikke blev observeret effekter på ægproduktionen ved en koncentration på 100 mL/L, var NOEC (NOEC, No Observed Effect Concentration) lig med 100 mL/L for udvaskningsvandet fra High Protect 35651.
I modsætning til High Protect 35651 var udvaskningsvandet fra forsøget med den eksperimentelle 86330 maling akut toksisk over for A. tonsa, idet dødeligheden af voksne Acartia var 100% for ufortyndede vandprøver udtaget efter henholdsvis 20 og 34 dage. Udvaskningsvand, der blev fortyndet 10 gange (100 mL/L), medførte en dødelighed på henholdsvis 40% (20 dage) og 20% (34 dage). I den kroniske toksicitetstest var der ingen udvikling af nauplier til copepoditter og voksne ved påvirkning med udvaskningsvand fortyndet til 100 mL/L (vandprøve udtaget efter 13 dage) og 10 mL/L (vandprøve udtaget efter 34 dage) (figur 5.2-5.3). På baggrund af disse resultater konkluderes det, at NOEC var mindre end 10 mL/L for udvaskningsvandet fra den eksperimentelle 86330 maling.
Figur 5.1 Se her
Udvikling af nauplier, copepoditter og voksne i udvaskningsvand fra High Protect
35651, dag 13.
Development of nauplii, copepodites and adults in leachate from High Protect 35651, day
13.
Figur 5.2 Se her
Udvikling af nauplier, copepoditter og voksne i udvaskningsvand fra den eksperimentelle 86330 maling, dag 13.
Development of nauplii, copepodites and adults in leachate from the experimental 86330 paint, day 13.
Figur 5.3 Se her
Udvikling af nauplier, copepoditter og voksne i udvaskningsvand fra den eksperimentelle 86330 maling, dag 34.
Development of nauplii, copepodites and adults in leachate from the experimental 86330 paint, day 34.
Vandprøver fra udvaskningsforsøget med Hempel's Antifouling Nautic 76800 havde en høj akut toksicitet over for A. tonsa, idet vandprøven, der blev udtaget efter 20 dage og fortyndet 100 gange (10 mL/L), medførte en dødelighed på 100%. Der var ingen udvikling af nauplier til copepoditter og voksne ved påvirkning med udvaskningsvand fortyndet til 0,1 mL/L (vandprøve udtaget efter 13 dage). På baggrund af disse resultater konkluderes det, at NOEC var mindre end 0,1 mL/L for vandprøver fra udvaskningsforsøget med Hempel's Antifouling Nautic 76800.
NOEC-værdier for akutte og kroniske effekter er angivet i tabel 5.2.
Tabel 5.2
NOEC-værdier bestemt i test med Acartia tonsa (NOEC, No observed effect
concentration).
NOEC values determined in tests with Acartia tonsa (NOEC, No observed effect
concentration).
Dag for prøvetagning af
udvasknings- |
NOEC |
NOEC |
NOEC |
|
| Kontrol Control |
34 |
1.000 |
1.000 |
1.000 |
| High Protect 35651 | 34 |
1.000 |
100 |
100 |
| Eksperimentel 86330 | 34 |
<100 |
<10 |
10 A |
| Hempel's Antifouling Nautic 76800 | 34 |
<1 |
<0,1 A |
- |
A
, test udført med udvaskningsvand udtaget efter 13 dage; -, ikke bestemt.A, test perfomed with leachate taken after 13 days, -, not determined., test udført med udvaskningsvand udtaget efter 13 dage; -, ikke bestemt.
A, test perfomed with leachate taken after 13 days, -, not determined.
n-Oktanol-vand-fordelingskoefficient
n-Oktanol-vand-fordelingskoefficienten (log Kow) anvendes normalt som et udtryk for kemiske stoffers iboende evne til at bioakkumuleres i vandlevende organismer. Stoffer, hvor log Kow >3, anses for at være potentielt bioakkumulerbare. Den gennemførte undersøgelse var en kvalitativ test, hvor log Kow blev bestemt for stoffer i udvaskningsvand, men hvor koncentrationen af stofferne ikke blev bestemt.
Seks forbindelser med log Kow >3 blev påvist i en vandprøve fra udvaskningsforsøget med High Protect 35651 ved neutral pH. Imidlertid var der nogen analytisk usikkerhed, da disse forbindelser gav små arealer i HPLC-kromatogrammer, og fire forbindelser blev kun påvist i én af to analyser. Ved pH 2 blev fundet 12 forbindelser med log Kow >3. Selvom resultaterne bør fortolkes med forsigtighed, påviser undersøgelsen tilstedeværelsen af potentielt bioakkumulerbare stoffer i udvaskningsvandet fra High Protect 3565. Af disse stoffer vurderes hovedparten at have en log Kow mellem 3 og 4.
Fire forbindelser med log Kow >3 blev påvist i en vandprøve fra udvaskningsforsøget med den eksperimentelle 86330 maling ved neutral pH. Ved pH 2 blev påvist 12-15 forbindelser med log Kow >3. Resultaterne viser, at der udvaskes potentielt bioakkumulerbare stoffer til det omgivende vand i udvaskningsforsøg med den eksperimentelle 86330. Ligesom det var tilfældet med High Protect 3565, vurderes hovedparten af disse stoffer at have en log Kow mellem 3 og 4.
Undersøgelserne af log Kow har således vist, at der kan udvaskes potentielt bioakkumulerbare forbindelser fra både High Protect 35651 og den eksperimentelle 86330. Det vurderes dog, at de udvaskede stoffer har et lavt bioakkumuleringspotentiale, da de fleste af stofferne havde en log Kow <3-4, og da der ikke blev påvist forbindelser med log Kow >5. Stoffer med log Kow mellem 3 og 4 vil typisk have en biokoncentreringsfaktor på 100-575 (Veith & Kosian 1983).
5.3 Vurdering af biocidfrie malinger
De gennemførte udvaskningsforsøg blev udført med et forhold mellem det malede areal og det omgivende væskevolumen, der var mindst 13-14 gange større end den tilsvarende ratio i Jyllinge Lystbådehavn (jf. afsnit 5.1). For begge biocidfrie malinger, High Protect 35651 og den eksperimentelle 86330, havde vandprøver fra udvaskningsforsøg markant mindre effekt end vandprøver fra tilsvarende forsøg med den kommercielle maling Hempel's Antifouling Nautic 76800. Det fremgår af tabel 5.2, at udvaskningsvand fra High Protect 35651 og den eksperimentelle 86330 medførte NOEC-værdier for A.tonsa, der var henholdsvis mindst 1.000 og 100 gange højere end NOEC for udvaskningsvand fra Hempel's Antifouling Nautic 76800.
Vandprøver fra udvaskningsforsøget med High Protect 35651 medførte ingen hæmning af S. costatum, og kroniske effekter på A. tonsa blev kun observeret ved ufortyndet udvaskningsvand (NOEC = 100 mL/L).
Vandprøver fra udvaskningsforsøget med den eksperimentelle 86330 maling var toksiske over for S. costatum samt i akutte og kroniske test med A. tonsa (NOEC, akut <100 mL/L; NOEC, kronisk <10 mL/L). Imidlertid er der forhold omkring udludningen af stoffer fra denne type maling, som ikke er fuldt belyst (jf. resultater med S. costatum). Disse forhold bør undersøges nærmere, inden der foretages en endelig vurdering af malingens miljøegenskaber.
6. Konklusion
Følgende konklusioner kan afledes af denne undersøgelse:
Biotilgængeligt kobber er meget giftigt over for vandlevende organismer. Kobbers potentielle giftvirkning i vandmiljøet reduceres ved binding til organiske stoffer og sedimenter, der medfører, at den aktuelle biotilgængelighed af kobber er lav. Forstyrrelser af sedimentet, og de deraf følgende ændrede iltforhold, vil imidlertid kunne remobilisere bundet kobber, og sådanne ændringer vil muligvis kunne medføre effekter over for følsomme organismer i nærheden af havneområder og klapningspladser.
DCOI omdannes hurtigt til nedbrydningsprodukter i havvand, hvor der er fundet halveringstider på mellem 11 og 14 timer. Omdannelsen af DCOI er væsentligt hurtigere i akvatisk sediment, idet der er påvist halveringstider på mindre end 1 time. DCOI er meget giftigt over for vandlevende organismer, idet de laveste effektkoncentrationer (EC/LC50) er lavere end 10 µg/L. Den akvatiske toksicitet af det stabile nedbrydningsprodukt N-(n-octyl) malonaminsyre er flere størrelsesordener mindre, idet de laveste effektkoncentrationer (LC50) vurderes at være mellem 90 og 160 mg/L.
På baggrund af "realistiske worst-case scenarier" er risikokvotienter (PEC/PNEC) for DCOI beregnet til 8,7 for lystbådehavnen og 0,1 for sejlruten. Ud fra antagelserne i beregningerne vurderes det, at der inden for lystbådehavnen er en risiko for kronisk økotoksiske effekter, idet DCOI antages at blive tilført konstant ved udludning fra bundmaling. Risikokvotienten for DCOI uden for lystbådehavnen er mindre end 1, og her skønnes risikoen for økotoksiske effekter at være lav. De beregnede eksponeringskoncentrationer (PEC) bygger på realistisk konservative forudsætninger, som medfører, at værdierne for PEC i praksis kun sjældent vil overskrides. Når bådene tages op af vandet ved sejlsæsonens afslutning, vil DCOI sandsynligvis hurtigt blive elimineret, da DCOI enten omdannes i vandfasen eller bindes til sedimentet, hvor det omdannes med en meget kort halveringstid.
Zinkpyrithion omdannes meget hurtigt ved fotolyse og biologisk nedbrydning. Zinkpyrithion er meget giftigt over for vandlevende organismer, idet de laveste effektkoncentrationer (EC/LC50) er lavere end 10 µg/L. Giftigheden af de stabile nedbrydningsprodukter omadin sulfonsyre og pyridin sulfonsyre er flere størrelsesordener mindre, idet de laveste effektkoncentrationer (LC50) for disse forbindelser er henholdsvis 36 og 29 mg/L.
Ved anvendelse af de samme "realistiske worst-case scenarier" som for DCOI er risikokvotienter (PEC/PNEC) for zinkpyrithion beregnet til: 5,6-17 for lystbådehavnen og 0,05-0,22 for sejlruten. De laveste risikokvotienter er baseret på PEC-værdier, hvor fotolytisk omdannelse af zinkpyrithion er antaget i beregningerne, mens de højeste risikokvotienter bygger på beregninger, hvor der helt ses bort fra fotolytisk omdannelse. Ud fra antagelserne i beregningerne vurderes det, at der inden for lystbådehavnen er en risiko for kronisk økotoksiske effekter, idet zinkpyrithion antages at blive tilført konstant ved udludning fra bundmaling. Risikokvotienten for zinkpyrithion uden for lystbådehavnen er under 1, og her skønnes risikoen for økotoksiske effekter at være lav. Risikokvotienten uden for lystbådehavnen er sandsynligvis tættest på 0,05, hvor fotolyse er inddraget i beregningen, da der ikke forventes vedvarende skygge på en almindelig sejlrute. Som beskrevet for DCOI medfører de realistisk konservative forudsætninger, at de beregnede PEC-værdier i praksis kun sjældent vil overskrides. Zinkpyrithion vil sandsynligvis hurtigt blive elimineret, når lystbådene tages op af vandet ved sejlsæsonens afslutning, som følge af stoffets korte halveringstid i vand og sediment.
Vandprøver fra udvaskningsforsøget med High Protect 35651 medførte ingen hæmning af væksten af S. costatum, og kroniske effekter på A. tonsa blev kun observeret i ufortyndet udvaskningsvand (nul-effekt-koncentration, NOEC = 100 mL/L). Vandprøver fra udvaskningsforsøget med den eksperimentelle 86330 maling udviste toksicitet over for S. costatum samt i akutte og kroniske test med A. tonsa (NOEC, akut <100 mL/L; NOEC, kronisk <10 mL/L). Imidlertid er der forhold, der tyder på, at variationer af produktionsteknisk eller påføringsmæssig art kan påvirke udludningen af stoffer fra denne type maling. Disse forhold bør undersøges nærmere, inden der foretages en endelig vurdering af malingens miljøegenskaber. Udvaskningsvandet fra begge de biocidfrie malinger havde markant mindre effekt end vandprøver fra tilsvarende forsøg med den organotin-baserede Hempel's Antifouling Nautic 76800. Udvaskningsvand fra High Protect 35651 og den eksperimentelle 86330 medførte kroniske NOEC-værdier for A. tonsa, der var henholdsvis mindst 1.000 og 100 gange højere end de tilsvarende NOEC for udvaskningsvand fra den organotin-baserede maling.
7. Referencer
Allen, H.E. (1993): The significance of trace metal speciation for water, sediment and soil quality criteria and standards. The Science of the Total Environment, Suppl. 1993.
Ankley, G.T., N.A. Thomas, D.M. Di Toro, D.J. Hansen, J.D. Mahony, W.J. Berry, R.C. Schwartz & R.A. Hoke (1994): Assessing potential bioavailability of metals in sediments: A proposed approach. Environmental Management, 18, 331-337.
Ankley, G.T. (1996): Evaluation of metal/acid-volatile sulfide relation-ships in the prediction of metal bioaccumulation by benthic macrovertebrates. Environ. Toxicol. Chem., 15, 2138-2146.
Arch Chemicals (1999a): Results of mysid test. Modtaget fra P. Turley.
Arch Chemicals (1999b): Analytical protocol. Modtaget fra J.C. Ritter.
AQUIRE (1999): Aquatic toxicity information retrieval. US EPA, National Health and Environmental Effects Laboratory, Mid-Continent Ecology Division. On-line available via Internet. http:\\www.epa.gov\ecotoxy.
Arrhenius, Å. (1997): Effects of 4,5-dichloro-2-n-octyl-4-isothiazoline-3-one, the active ingredient of the new antifouling agent Sea-nine TM211 Biocide, on marine microalgal communities. Master thesis. University of Göteborg, Göteborg, 20 pp.
Bach, H., D. Rasmussen, J.A. Farr & N. Nyholm (1986): "Beregninger af chemical fate for stoffer udledt til Stenungsund recipienten". VKI, Rapport til Statens Vandvårsverk (Sverige).
Bard, J. (1997): Supplement 1 to the ecotoxicological evaluation of copper in antifouling paints, copper, cuprous oxide, cuprous thiocyanate. Rapport til Kemikalieinspektionen i Sverige, 40 pp.
Bjørnestad, E., T. Madsen, C. Helweg, H.B. Rasmussen, C. Seierø, H. Enevoldsen & F. Pedersen (1999): Ecotoxicological tests of leachates of antifouling paints. VKI rapport nr. 11324/100 udarbejdet til Hempel's Marine Paints A/S.
Boeri, R.L. & T.J. Ward (1990): Acute flow-through toxicity of RH-287 to the mysid, Mysidopsis bahia. Rohm and Haas report No. 89RC-0305. EnviroSystems Division, Resource Analysts, Incorporated, Hampton, New Hampshire 03842.
Boeri, R.L., J.P. Magazu & T.J. Ward (1993): Acute toxicity of zinc omadine (zinc bis-1-oxide-2(1H)-pyridinethionate) to the mysid, Mysidopsis bahia. Study report. U.S. EPA-FIFRA, Guideline 72-3(b). T.R. Wilbury Study Number 23-OL, pp. 1-28. Arch Chemicals.
Boeri, R.L., J.P. Magazu & T.J. Ward (1994a): Acute toxicity of zinc omadine (zinc bis-1-oxide-2(1h)-pyridinethionate) to the fathead minnow, Pimephales promelas. Study report. U.S. EPA-FIFRA, Guideline 72-1. T.R. Wilbury Study Number 19-OL, pp. 1-29. Arch Chemicals.
Boeri, R.L., J.P. Magazu & T.J. Ward (1994b): Acute toxicity of zinc omadine to the rainbow trout, Oncorhynchus mykiss. Study report. U.S. EPA-FIFRA, Guideline 72-1. T.R. Wilbury Study Number 20-OL, pp. 1-28. Arch Chemicals.
Boeri, R.L., J.P. Magazu & T.J. Ward (1994c): Acute toxicity of zinc omadine (zinc bis-1-oxide-2(1H)-pyridinethionate) to the sheepshead minnow, Cyprinodon variegatus. Study report. U.S. EPA-FIFRA, Guideline 72-3(b). T.R. Wilbury Study Number 22-OL, pp. 1-30. Arch Chemicals.
Boeri, R.L., J.P. Magazu & T.J. Ward (1994d): Acute toxicity of zinc omadine (zinc bis-1-oxide-2(1H)-pyridinethionate) to the daphnid, Daphnia magna. Study report. U.S. EPA-FIFRA, Guideline 72-2. T.R. Wilbury Study Number 21-OL, pp. 1-28. Arch Chemicals.
Boeri, R.L., J.P. Magazu & T.J. Ward (1994e): Acute flow-through mollusc shell deposition test with zinc omadine (zinc bis-1-oxide-2(1H)-pyridinethionate). Study report. U.S. EPA-FIFRA, Guideline 72-3(c). T.R. Wilbury Study Number 24-OL, pp. 1-27. Arch Chemicals.
Boeri, R.L., P.L. Kowalski & T.J. Ward (1994f): Acute toxicity of omadine sulfonic acid (pyridine-N-oxide-2-sulfonic acid) to the sheepshead minnow, Cyprinodon variegatus. Study report. U.S. EPA-FIFRA, Guideline 72-3. T.R. Wilbury Study Number 36-OL, pp. 1-27. Arch Chemicals.
Boeri, R.L., P.L. Kowalski & T.J. Ward (1994g): Growth and reproduction test with omadine sulfonic acid (pyridine-N-oxide-2-sulfonic acid) and the freshwater alga, Selenastrum capricornutum. Study report. Guidelines referenced FIFRA 122-2. T.R. Wilbury Study Number 39-OL, pp. 1-28. Arch Chemicals.
Boeri, R.L., P.L. Kowalski & T.J. Ward (1994h): Acute toxicity of omadine sulfonic acid (pyridine-N-oxide-2-sulfonic acid) to the mysid, Mysidopsis bahia. Study report. U.S. EPA-FIFRA, Guideline 72-3 (b). T.R. Wilbury Study Number 37-OL, pp. 1-28. Arch Chemicals.
Boeri, R.L., P.L. Kowalski & T.J. Ward (1994i): Acute flow-through mollusc shell deposition test (pyridine-N-oxide-2-sulfonic acid) with omadine sulfonic acid. Study report. U.S. EPA-FIFRA, Guideline 72-3. T.R. Wilbury Study Number 38-OL, pp. 1-27. Arch Chemicals.
Boeri, R.L., J.P. Magazu & T.J. Ward (1999): Early life-stage toxicity of zinc pyrithione and pyridine-2-sulfonic acid (persistent terminal degradant) to the fathead minnow, Pimephales promelas. Study report. OECD 210 guideline. T.R. Wilbury. Study number 1678-OL, pp. 69. Arch Chemicals.
Borgman, U. & W.P. Norwood (1997): Toxicity and accumulation of zinc and copper in Hyalella azteca exposed to metal spiked sediments. Can. J. Fish. Aquat. Sci., 54, 1046-1054.
Brand, L.E., W.G. Sunda & R.R.L. Guillard (1986): Reduction of marine phytoplankton reproduction by copper and cadmium. J. Exp. Mar. Biol. Ecol., 96, 225-250.
Bruland, K.W., J.R. Donat & D.A. Hutchins (1991): Interactive influences of bioactive trace metals on biological production in oceanic waters. Limnol. Oceanogr., 36, 1555-1577.
Burgess, D. (1990): Acute flow-through toxicity of RH-287 technical to Dapnia magna. Rohm and Haas report No. 89RC-0017. ABC Laboratory, Inc., Columbia, Missouri 65205.
Burns, L.A., D.M. Cline & R.R. Lassiter (1981): Exposure analysis modelling system (EXAMS): User manual and system documentation. EPA – Environmental Resarch Laboratory, Athens.
Calkins, J., (1975): Measurements of the penetration of solar UV-B into various natural waters". In: climatic impact assessment program, 1975. Monograph 5, U.S. Department of Transportation, Washington D.C.
Callow, M.E. & J.A. Finlay (1995): A simple method to evaluate the potential for degradation of antifouling biocides. Biofouling, 9, 153-165.
Callow, M.E. & G.L. Willingham (1996): Degradation of antifouling biocides. Biofouling, 10, 239-249.
Calmano, W., W. Ahlf & U. Förstner (1990): Exchange of heavy metals between sediment components and water. NATO ASI Series, Vol. G.23. Metal speciation in the environment. Broekaert, J.A.C., Gücer, S., Adams; F. (eds). Springer-Verlag, Berlin.
Campbell, P.G.C (1995): Interactions between trace metals and aquatic organisms: A critique of free-ion activity model. A. Tessier and D.R. Turner (eds). Metal speciation and bioavailability in aquatic systems.. John Wiley and Sons Ltd.
Ciceri, G., S. Maran, W. Martinotti & G. Queirazza (1992): Geochemical cycling of heavy metals in a marine coastal area: Benthic flux determination from pore water profiles and in situ measurements using benthic chambers. Hydrobiol., 235/236, 501-517.
Claisse, D. & C.I. Alzieu (1993): Copper contamination as a result of antifouling paint regulations? Mar. Poll. Bulletin, 26, 395-397.
Danmarks Meterologiske Institut (1999): Vejrinformationsdata fra Danmarks Metrologiske Institut.
Danmarks Miljøundersøgelser (1986): A novel life-cycle test with copepods. M. Chen & F. Møhlenberg.
Dansk Sejlunion & Hempel (1999): Indledende vurdering af mekanisk rensning som alternativ til biocidholdig bundmaling samt vurdering af biocidholdige antibegroningsmidler med forventet reduceret miljøbelastning. Endeligt rapportudkast til Miljøstyrelsen, juni 1999.
Danmarks Statistik (1996): Statistisk Årbog.
Debourg, C., A. Johnson, C. Lye, L. Törnqvist & C. Unger (1993): Antifouling products. Pleasure boats, commercial vessels, nets, fish cages and other underwater equipment. KEMI Report No. 2/93. The Swedish National Chemicals Inspectorate. Solna.
Derbyshire, R.L., A.H. Jacobson, M.L. O’Dowd & M.A. Santangelo (1991): Metabolism of RH-5287 in bluegill sunfish. Rohm and Haas Company Technical Report No. 34-90-71, Rohm and Haas Company, Spring House, PA.
DHI (1994): Roskilde vig og bredning: Spildevandsundersøgelse. August 1994.
EC (1996): Technical Guidance Document in support of commission directive 93/67/EEC on risk assessment for new notified substances and commission regulation (EC) No 1488/94 on risk assessment for existing substances. Part II Environmental risk assessment. Brussels.
European Chemicals Bureau (1997): EUSES – The European Union system for the evaluation of substances. Joint Reserach Centre European Commission Environment Institute, European Chemicals Bureau, Ispra.
Fenn, R. (1999): Photolysis of zinc pyrithione in natural sunligth. Study conducted by Arch Chemicals Inc., 1999.
Forbes, T.L., V.E. Forbes, A. Giessing, R. Hansen & L.K. Kure (1998): Relative role of porewater versus ingested sediment in bioavailability of organic contaminants in marine sediments. Environ. Toxicol. Chem., 17, 2453-2462.
Forbis, A.D. (1990): Acute toxicity of RH-287 to Selenastrum capricornutum Printz. Final report #37740. U.S. EPA-FIFRA, 40 CFR, Part 158.150, Guideline 122-2. ABC Laboratories, Columbia, Missouri 65205. Rohm and Haas.
Forbis, A.D., L. Georgie & B. Bunch (1985): Uptake, depuration and bioconcentration of 14C-RH-5287 by bluegill sunfish (Lepomis macrochirus). Rohm and Haas Company Technical Report No. 310-86-33, ABC Labs, Inc., Columbia, MO.
Förstner, U. (1985): Chemical forms and reactivities of metals in sediments. Leschber, R., R.D. Davis & P. L’Hermite (eds). Chemical methods for assessing bio-available metals in sludges and soils. Elsevier Applied Science, London, pp. 1-30.
Förstner, U., W. Ahlf, W. Calmano, M. Karsten & J. Schoer (1990): Assessment of metal mobility in sludges and solid wastes. NATO ASI Series, Vol. G.23. Metal speciation in the environment. Broekaert, J.A.C., S. Gücer & F. Adams (eds). Springer-Verlag, Berlin.
Fredenslund, F., M. Severinsen & M. Bugge Andersen (1995): Evaluation of the SimpleBox model for Danish conditions. Miljøprojekt nr. 307, Miljøstyrelsen, København.
Fyns Amt (1999): Upublicerede data (Søren Larsen).
Garvey J.E., Owen H.A. and Winner R.W. (1991): Toxicity of copper to the green algae, Chlamydomonas reinhardtii (Chlorophyceae), as affeced by humic substances of terrestrial and freshwater origin. Aquatic Toxicology, 19, 89-96.
Gustavson, K., S. Petersen, B. Pedersen, F. Stuer-Lauridsen & S.Å. Wängberg (1999): Pollution-induced community tolerance (PICT) in coastal phytoplankton communities exposure to copper. Hydrobiologia (in press).
Hall, L.W. & R.D. Anderson (1998): A deterministic ecological risk assessment for copper in European saltwater environments. Rohm and Haas Company. Biocides Technical Report No. 98-23.
Heitmuller, T. (1977): Acute toxicity of C-9211 to brown shrimp (Penaeus aztecus). Toxicity test report. EG&G, Bionomics, Marine Research Laboratory, Route 6, Box 1002, Pensacola, Florida 32507.
Harremoës P. & A. Malmgren-Hansen (1989): Lærebog i vandforurening. Polyteknisk Forlag.
Hempel (1999a): Telefax dateret 21. april 1999 fra Martin Wiese Christoffersen (Hempel).
Hempel (1999b): Telefax dateret 16. september 1999 fra Eva Bie Kjær (Hempel).
Hempel (1999c): Telefax dateret 30. september 1999 fra Eva Bie Kjær (Hempel).
Howard, P.H. (1991): Handbook of environmental fate and exposure data for organic chemicals. Vol. III, Pesticides, Lewis Publ. 684 pp.
Hunt, C.D. & D.L. Smith (1983): Remobilization of metals from polluted marine sediments. Can. J. Fish. Aquat. Sci., 40, 132-142.
ISO (1998): Water quality - determination of acute lethal toxicity to marine copepods (Copepoda, Crustacea). ISO/FDIS 14669.
ISO (1999): Draft standard for calculation method (ISO 15184-4). Udsendt til medlemmer af ISO/TC35/SC9/WG27, general test methods for paints and varnishes - determination of leaching rates from antifouling paints. Date 24 June 1999.
Jacobson, A. (1993). RH-5287: Octanol:water partition coefficient. Rohm and Hass Company, Research Laboratories, Pennsylvania.
Jacobson, A. & V. Kramer (1999): Additonal information on water-sediment partitioning and half-life of DCOI in a harbor. Note prepared for VKI. Rohm and Haas Company, Research Laboratories, Pennsylvania.
Jensen, C.A. & J.A. Heslop (1997a): Undersøgelse af miljøproblemer ved brug af bundmalinger på lystbåde. Århus Amt.
Jensen, C.A. & J.A. Heslop (1997b): Nye analyseresultater fremlagt i forbindelse med denne rapport.
Johansen, K. & F. Møhlenberg (1987): Impairment of egg production in Acartia tonsa exposed to tributyltin oxide. Ophelia 27, 1327-1341.
Karman, C.C:, E.A. Vik, H.P.M. Schobben, G.D. Øfjord & H.P. van Dokkum (1996): Charm III Main Report. TNO-MEP R96/355. Institute of Environmental Sciences, Energy Research and Process Innovation (TNO-MEP), Department of Ecological Risk Studies, Den Helder (Netherlands).
Kawashima, Y. (1997a): Acute toxicity test of RH-287 with Japanese flounder. Test report. Kurume Research Laboratories, Chemical Biotesting Center, Chemicals Inspection & Testing Institute, Japan.
Kawashima, Y. (1997b): Acute toxicity test of RH-287 with Red Sea bream. Test report. Kurume Research Laboratories, Chemical Biotesting Center, Chemicals Inspection & Testing Institute, Japan.
Kesterson, A. & R. Atkins (1992a): Supplemental study on the aerobic aquatic metabolism of 13/14C RH-5287. PTRL East, Inc., Kentucky. Submitting laboratory: Rohm and Haas Company, Pennsylvania.
Kesterson, A. & R. Atkins (1992b): Supplemental study on the anaerobic aquatic metabolism of 13/14C RH-5287. PTRL East, Inc., Kentucky. Submitting laboratory: Rohm and Haas Company, Pennsylvania.
Kronprins Frederiks Bro (1996): Statistikker over brooplukninger og passager af fartøjer i 1995).
Kronprins Frederiks Bro (1998): Statistikker over brooplukninger og passager af fartøjer i 1997).
Kronprins Frederiks Bro (1999): Statistikker over brooplukninger og passager af fartøjer i 1998).
Lawrence, L.J., B. Lawrence, S. Jackson & A. Kesterson (1991a): Aerobic aquatic metabolism of 13/14C RH-5287. PTRL East, Inc., Kentucky. Submitting laboratory: Rohm and Haas Company, Pennsylvania.
Lawrence, L.J., B. Lawrence & A. Kesterson (1991b): Anaerobic aquatic metabolism of 13/14C RH-5287. PTRL East, Inc., Kentucky. Submitting laboratory: Rohm and Haas Company, Pennsylvania.
Leak, T. (1986): Characterization of RH-5287 in fish tissues and water from a bioconcentration study. Technical report No. 310-86-32. Rohm and Haas Company, Independence Mall West, Philadelphia, Pennsylvania 19105.
Lewis, A.G. (1995): Copper in water and aquatic environments. Int. Copper Association, Ltd. New York.
Luoma, S.N. (1989): Can we determine the biological availability of sediment-bound trace elements? Hydrobiol. 176/177, 379-396
Madsen, T. and P. Kristensen (1997): Effects of bacterial inoculation and nonionic surfactants on degradation of polycyclic aromatic hydrocarbons in soil. Environ. Toxicol. Chem., 16, 631-637.
Madsen, T., K. Gustavson, L. Samsøe-Petersen, F. Simonsen, J. Jacobsen, S. Foverskov & M.M. Larsen (1998): Kortlægning og vurdering af antibegroningsmidler til lystbåde i Danmark. Miljøprojekt nr. 384. Miljøstyrelsen, København, 108 pp.
Madsen, T. (1999). Biodegradation of a pyrethroid insecticide in freshwater pond sediment. In prep.
Mazza, L.S. (1993): Supplemental study on the aerobic aquatic metabolism of RH-5287. Rohm and Haas Company, Research Laboratories, Pennsylvania.
Miljø- og Energiministeriet (1996): Bekendtgørelse nr. 921 af 8. oktober 1996 om kvalitetskrav for vandområder og krav til udledning af visse farlige stoffer til vandløb, søer eller havet.
OECD (1984): Alga, growth inhibition test. Guideline for testing of chemicals, No. 201.
OECD (1989): Partition coefficient (n-octanol/water), high performance liquid chromatography (HPLC) method. Guideline for testing of chemicals, No. 117.
Olin (1997): Evaluation of the safety and efficacy of Zinc omadine industrial fungicide. Technical summary submitted by Olin. Arch Chemicals.
Paulson, A.J., H.C. Curl & J.F. Gendron (1994): Partitioning of Cu in estuarine waters, II. Control of partitioning by the biota. Marine Chemistry, 45, 81-93.
Petersen, W., E. Willer & C. Willamowski (1997): Remobilization of trace elements from polluted anoxic sediments after resuspension in oxic water. Water, Air and Soil Pollution, 99: 515-522.
Peterson, G.S., G.T. Ankley & E.N. Leonard (1996): Effect of bioturbation on metal-sulfide oxidation in surficial freshwater sediments. Environ. Toxicol. Chem., 15, 2147-2155
Putt, A.E. (1994): RH-287 Technical - acute toxicity to amphipods (Ampelisca abdita) during a 10-day sediment exposure under static conditions. Rohm & Haas Report No. # 94RC-0092. Springborn Laboratories, Inc., Wareham, Massachusetts 02571-1075.
Reichelt, A.J. & G.B. Jones (1994): Trace metals as tracers of dredging activity in Clevaland Bay - field and laboratory studies.
Reynolds, J.L. (1995a): Aqueous photolysis of [pyridine-2,6-14C]zinc omadine in pH 9 buffer and artificial sea water. XenoBiotic Laboratories, Inc., Plainsboro, NJ. Arch Chemicals.
Reynolds, J.L. (1995b): Hydrolysis of [pyridine-2,6-14C]zinc omadine. XenoBiotic Laboratories, Inc., Plainsboro, NJ. Arch Chemicals.
Ritter, J.C. (1996): Aerobic aquatic metabolism of [pyridine-2,6-14C]zinc omadine. Central Analytical Laboratory, Cheshire, CT. Arch Chemicals.
Ritter, J.C. (1999a): Summary of the aerobic and anaerobic aquatic metabolism of [pyridine-2,6-14C]copper omadine and [pyridine-2,6-14C]zinc omadine in marine water and sediment. Olin Research Centre, Cheshire, CT. Arch Chemicals.
Ritter, J.C. (1999b): Aerobic aquatic metabolism of [pyridine-2,6-14C]copper omadine® in marine water and sediment. Olin Research Research Centre, Cheshire, CT. Arch Chemicals.
Ritter, J.C. (1999c): Anaerobic aquatic metabolism of [pyridine-2,6-14C]copper omadine® in marine water and sediment. Olin Research Research Centre, Cheshire, CT. Arch Chemicals.
Ritter, J.C. (1999d): Supplemental aerobic aquatic metabolism of [pyridine-2,6-14C]zinc omadine® in marine water and sediment. Olin Research Research Centre, Cheshire, CT. Arch Chemicals.
Ritter, J.C. (1999e): Supplemental anaerobic aquatic metabolism of [pyridine-2,6-14C]zinc omadine® in marine water and sediment. Olin Research Research Centre, Cheshire, CT. Arch Chemicals.
Roberts Jr., M.H., P.F. de Lisle, M.A. Vogelbein & R.C. Hale (1990): Acute toxicity of RH-287 to the American oyster, Crassostrea virginica in static natural and synthetic estuarine waters. Rohm and Haas Report No. 89RC-0037.
Roskilde Amt og Frederiksborg Amt (1997): Overvågning af Roskilde Fjord, 1996.
Salomons, W., N.M. de Rooij, H. Kerdijk & J. Bril (1987): Sediments as a source for contaminants? Hydrobiol., 149, 13-30.
Schwarzenbach, R.P., P.M. Gschwend & D.M. Imboden (1993): Environmental organic chemistry. John Wiley & Sons, Inc.
Shade, W.D., S.H. Hurt, A.H. Jacobson & K.H. Reinert (1993): Ecological risk assessment of a novel marine antifoulant. Environmental toxicology and risk assessment: 2nd Volume, ASTM STP 1216. J.W. Gorsuch, F.J. Dwyer, C.G. Ingersoll & T.W. La Point (eds.), American Society for Testing and Materials, Philadelphia, 1993.
Slotton, D.G. & J.E. Reuter (1995): Heavy metals in intact and resuspended sediments of a California reservoir, with emphasis on potential bioavailbility of copper and zinc. Mar. Freshwater Res., 46, 257-265.
Smalley, J.D. & J.L. Reynolds (1996): Anaerobic aquatic metabolism of [pyridine-2,6-14C]zinc omadine in fresh water and seawater. XenoBiotic Laboratories, Inc., Plainsboro, NJ. Arch Chemicals.
Steen, R.J.C.A., J. Jacobsen, F. Ariese & A.G.M. van Hattum (1999): Monitoring Sea-NineÒ 211 antifouling agent in a Danish harbor. IvM, Vrije Universiteit, Report number E99/10.
Sword, M.C. & M. Muckerman (1994a): Static acute toxicity of N-(n-octyl) malonamic acid to rainbow trout (Oncorhynchus mykiss). Rohm & Haas Report No. #93RC-0166. ABC Laboratories, Columbia, Missouri 65202.
Sword, M.C. & M. Muckerman (1994b): Static acute toxicity of N-(n-octyl) malonamic acid to Daphnia magna. Rohm & Haas Report No. #93RC-0165. ABC Laboratories, Columbia, Missouri 65202.
Syracuse Research Corporation (1996): LOGKOW software program. Syracuse Research Corporation, New York.
Sørensen, J., B.B. Jørgensen & N.P. Revsbech (1979). A comparison of oxygen, nitrate, and sulfate respiration in coastal marine sediments. Microbial Ecology, 5, 105-115.
Turley, P.A. & N.P. Skoulis (1997): A review of the aquatic fate and toxic effects of zinc omadine. Arch Chemicals.
U.S: EPA (1999): GCSOLAR. Program from U.S. EPA.
Zafirioiu, O.C. (1977): Marine organic photochemistry previewed. Marine Chemistry 5, 497-522.
Zehnder, A.J.B., B. Huser & T.D. Brock (1979). Measuring radioactive methane with the liquid scintillation counter. Appl. Environ. Microbiol., 37, 897-899.
Zepp, R.G. & D.M. Cline (1977): Rates of direct photolysis in aquatic environment. Env. Sci.Techn., 11, 359-366.
Veith, G.D. & P. Kosian (1983): Estimating bioconcentration potential from octanol/water partition coefficients. D. Mackay, S. Paterson, S.J. Eisenreich & M.S. Simons (eds.), Physical behavior of PCBs in the Great Lakes. Ann Arbor Science, Ann Arbor, MI, USA.
Wang, W. & N:S. Fisher (1996): Assimilation of trace elements and carbon by the mussel Mytilius edulis: Effects of food composition. Limnol. Oceanogr., 41, 197-207.
Wängberg S.-Å., S. Alexanderson & M. Hellgren (1995): Båtbottonfärgernas bidrag til kobberförekomsten i den akvatiske miljö. Upföljning av KemI´s beslut om båtbottonfärger, med hjælp av PICT-undersökning på microalgesamhällen. KemI-rapport.
Ward, T.J. & R.L. Boeri (1990): Chronic toxicity of RH-287 to the daphnid, Daphnia magna. Study report. EnviroSystems Study No. 9031-RH. Rohm and Haas Report No. 9ORC-0050. EnviroSystems Division, Resource Analysts, Incorporated, Hampton, New Hampshire 03842.
Ward, T.J., J.P. Magazu & R.L. Boeri (1994a): Growth and reproduction test with zinc omadine (zinc bis-1-oxide-2(1H)-pyridinethionate) and the freshwater alga, Selenastrum capricornutum. Study report. Guidelines referenced FIFRA 122-2. T.R. Wilbury Study Number 25-OL. Page 1-29. Arch Chemicals.
Ward, T.J., P.L. Kowalski & R.L. Boeri (1994b): Acute toxicity of omadine sulfonic acid (pyridine-N-oxide-2-sulfonic acid) to the fathead minnow, Pimephales promelas. Study report. U.S. EPA-FIFRA, Guideline 72-1. T.R. Wilbury Study Number 33-OL, pp. 1-28. Arch Chemicals.
Ward, T.J., P.L. Kowaski & R.L. Boeri (1994c): Acute toxicity of omadine sulfonic acid (pyridine-N-oxide-2-sulfonic acid) to the rainbow trout, Oncorhynchus mykiss. Study report. U.S. EPA-FIFRA, Guideline 72-1. T.R. Wilbury Study Number 34-OL, pp. 1-28. Arch Chemicals.
Ward, T.J., P.L. Kowaski & R.L. Boeri (1994d): Acute toxicity of omadine sulfonic acid (pyridine-N-oxide-2-sulfonic acid) to the daphnid, Daphnia magna. Study report. U.S. EPA-FIFRA, Guideline 72-2. T.R. Wilbury Study Number 35-OL, pp. 1-26. Arch Chemicals.
Wells, M.L., P.B. Kozelka & K.W. Bruland (1998): The complexation of "dissolved" Cu, Zn, Cd and Pb by soluble and colloidal organic matter in Nraragansett Bay, RI. Mar. Chem., 62, 203-217.
Westerlund, S.F.G., L.G. Anderson, P.O.J. Hall, Å. Iverfeldt, M.M. Rutgers van der Loeff & B. Sundby (1986): Benthic fluxes of cadmium, copper, nickel, zinc and lead in the coastal environment. Geochimica et Cosmochimica Acta, 50, 1289-1296.
Bilag 1. Model til beregning af eksponeringskoncentrationer (PEC)
1. Indledning
I dette bilag beskrives den eksponeringsmodel, der blev anvendt til beregning af eksponeringskoncentrationer PEC (Predicted Environmental Concentration) af DCOI og zinkpyrithion (ZPT) samt deres vigtigste nedbrydningsprodukter.
Den opstillede model benytter modelleringsprincipper, der generelt anvendes ved bestemmelse af PEC. Talrige modeller til eksponeringsberegninger er beskrevet i litteraturen. Her kan bl.a. nævnes:
- SimpleBox, som er en "multi-compartment" model baseret på fugacitetsprincippet (Fredenslund et al. 1995). Modellen anvendes i Technical Guidance Document (TGD) til generisk risikovurdering af enkeltstoffer (EC 1996). Den er således også inkorporeret i EDB-modellen EUSES, som er en "elektronisk" udgave af TGD (European Chemicals Bureau 1997).
- EUSES har endvidere inkluderet et modul til estimering af PEC for antibegroningsmidler.
- CHARM-modellen, som anvendes ved risikovurderinger af offshore-kemikalier (Karman et al. 1996).
- EXAMS, som er et interaktivt computerprogram til simulering af skæbnen af miljøfremmede stoffer i akvatiske økosystemer (Burns et al. 1981).
2. Opstilling af beregningsmodel
Generelt består eksponeringsvurderinger af følgende elementer:
- Opstilling af scenarier, der beskriver de miljøparametre, som har betydning for emissionen og skæbnen af stofferne
- Bestemmelse af emissionen af kemikalier
- Beregning af PEC i relevante delmiljøer
- Følsomhedsanalyse, hvor PEC’s relative afhængighed af de parametre, som indgår i standardscenerierne, samt PEC’s relative afhængighed af stofparametrene, beregnes
Disse elementer blev også anvendt i nærværende eksponeringsberegninger.
2.1 Scenarier
Der er opstillet 2 standardscenarier til beregning af eksponeringskoncentrationer (PEC):
- Lystbådehavn. Som standard lystbådehavn er Jyllinge Lystbådehavn valgt. Denne lystbådehavn er valgt som en realistisk "worst-case", idet havnen har et højt antal både i forhold til havnens vandvolumen og et lavt vandskifte. Det samlede havneareal medtages i scenariet, og det antages, at der er total opblanding i hele havneområdet.
- Stærkt befærdet sejlrute. Som standard befærdet sejlrute er passagen ved Kronprins Frederiks Bro (ved Frederikssund) valgt; dels fordi den er relativt stærkt befærdet med lystbåde, og dels fordi der er optællinger af hvor mange både, der passerer under Kronprins Frederiks Bro. Scenariet omfatter en vandsøjle med en længde i sejlretningen på 1 m og en bredde svarende til bådenes bredde. Der antages fuldstændig opblanding i vandsøjlens dybderetning.
Begge standardscenarier er således placeret i Roskilde Fjord.
Hvert scenarie blev karakteriseret m.h.t.:
- Vandskifte
Netto vandudvekslingen mellem Roskilde Fjord og udløbet ved Isefjord blev antaget at svare til netto ferskvandstilførslen til fjorden, som er angivet til at være ca. 1,25 × 10-4 m3 × s-1 pr. m af fjordens længde (Harremoës & Malmgren-Hansen 1989). Da Roskilde Fjord er ca. 38 km lang (Harremoës & Malmgren-Hansen 1989), tilføres i alt ca. 410.400 m3 vand/dag. Med et overfladeareal på ca. 125 km2 svarer dette til en netto vandudveksling på 0,003 m3/m2/dag. Netto vandudvekslingen er således meget lav. DHI (1994) angiver således også, at vandstanden i Roskilde Fjord primært er bestemt af vindforhold og tidevandsvariationer. Vandstandsvariationerne er bestemmende for strømforholdene og dermed for fjordens vandskifte. De største vandstandsvariationer induceres af vinden, men tidevandet er bestemmende for de regelmæssige minimale variationer og dermed for hvilket mindste vandskifte, der forekommer på kort sigt. Ved Hundested i nord er tidevandets normale størrelse ca. 20 cm, hvilket er tilsvarende den daglige variation ved roligt vejr, som er observeret af brovagten ved Kronprins Frederiks Bro ved Frederikssund. I bunden af fjorden ved Roskilde er tidevandsvariationen nede på 6 – 7 cm (DHI 1994). På grund af vinden er almindeligt forekommende variationer over længere perioder dog langt større.
- For Jyllinge Lystbådehavn er det primært nordvestlige vinde, der kan give op til 1 m højvande og sydøstlige og sydlige vinde, der kan give 0,5-1,0 m lavvande. Vandstandsdata (for årene 1996, 1997, 1998) for en station ved Værebro Å, som løber ud i Roskilde Fjord nogle kilometer nord for Jyllinge Lystbådehavn, giver en gennemsnitlig samlet daglig ændring i vandstanden på ca. 0,6 m/dag (0,6 m3/m2/dag). Vandstandsdata er erhvervet fra Ivar Thorstein Hansen, Roskilde Amt. Dette tal er benyttet som udtryk for vandudvekslingen i Jyllinge Lystbådehavn.
- For passagen ved Frederikssund er forskellen mellem daglig minimum og maksimum vanddybde (i perioder uden kraftig blæst, hvor forskellene kan være mere betydelige) angivet af brovagten på broen til at være ca. 0,2 m. Derudover vil vindforhold bidrage til vandskiftet. Det er ikke lykkedes at få eksakte data for variationen af vanddybden under Kronprins Frederiks bro, men vandskiftet vil sandsynligvis som minimum være på niveau med vandskiftet i Jyllinge Lystbådehavn og ved Værebro. Derfor er der ligeledes antaget en vandudveksling på ca. 0,6 m3/m2/dag for passagen ved Frederikssund.
For begge scenarier er det antaget, at stofkoncentrationen i det vand, der transporteres ind i det betragtede vandområde, er ubetydelig.
- Vanddybde.
- Indhold og karakterisering af suspenderet materiale. Det suspenderede materiale blev karakteriseret m.h.t. indhold af organisk materiale. Det suspenderede materiale blev endvidere antaget at have et tilstrækkeligt højt indhold af mineraler, så det kunne antages at være negativt ladet.
- Salinitet.
- Temperatur. Temperaturen er her sat til 12,5oC, svarende til den gennemsnitlige lufttemperatur i perioden april - september (bådsæsonen er typisk fra slutningen af april frem til begyndelsen af oktober).
- pH.
- Antal m2 bundareal af skibe, som er i vandområdet, pr. tidsenhed.
- Procentdelen af skibene, der har bundmaling med det undersøgte antibegroningsmiddel (P).
- Sedimentets vandhold. Bortset fra et lavere indhold af organisk kulstof i sedimentet blev sammensætningen af det øverste sedimentlag antaget at være identisk med sammensætningen af det suspenderede materiale. Sedimentet blev antaget at være anaerobt.
Antal både i det betragtede vandområde.
|
Gennemsnitlig opholdstid for bådens tyngdepunkt i vandområdet:
- For lystbådehavnen blev det antaget, at alle bådene er i havnen. Dansk Sejlunion oplyser, at pladserne er fyldt op fra ca. medio maj til ultimo september. I sommerferieperioden (1. juli – 15. august) er ca. 1/3 af bådene væk, og der er stort set ingen gæster i havnen, da dens beliggenhed er uhensigtsmæssig for turister på vej gennem Roskilde Fjord (personlig korrespondance med Steen Wintlev, Dansk Sejlunion). En antagelse om, at alle bådpladserne hele tiden er fyldt op, vil således overestimere den samlede udludning af antibegroningsmidler til havnen.
- Dansk Sejlunion (personlig korrespondance med Steen Wintlev-Jensen, Dansk Sejlunion) oplyser endvidere, at passagen ved Frederikssund sker med relativt lille hastighed på grund af det snævre farvand og de mange både. Sejlhastigheden ved passage skønnes at være ca. 3-4 knob, hvilket svarer til 5,5 – 7,4 km/time. Opholdstiden af en båds tyngdepunkt i den betragtede vandsøjle er således på ca. 5,6 × 10-6 – 7,5 × 10-6 dage.
I tabel B1.1 er der givet en oversigt over de parametre, hvormed de to scenarier er karakteriseret. Disse parametre er anvendt i basisberegningerne.
Tabel B1.1 Se her
Opstilling af standardscenarie.
Standard scenario.
2.2 Emission af antibegroningsmidler
Hastigheden, hvormed antibegroningsmidlet frigives til vandmiljøet, udtrykkes som :
U = [frigivet masse pr. areal pr. tidsenhed].
Måling af realistiske frigivelseshastigheder af antibegroningsmidler er behæftet med store problemer, da frigivelseshastigheden er afhængig af en række faktorer, som
- tiden efter påføringen af malingen. Frigivelseshastigheden er ofte fundet at aftage som funktion af tiden, pga. den faldende koncentration af stofferne i malingen
- tykkelse af malingslaget
- afgivelse af andre stoffer i malingen
- ydre omstændigheder som, hvorvidt båden ligger stiller eller ej, strømforhold/vandskifte, temperatur m.v. Frigivelseshastigheden er typisk højere, når båden sejler, end når den ligger i havn.
Der foreligger et udkast til standard (ISO 1999), hvorefter frigivelseshastigheden af antibegroningsmidler kan beregnes. Frigivelseshastigheden bestemmes ud fra et estimat over malingens levetid, hvor det simpelt antages, at al begroningsmiddel frigives i løbet af levetiden. Der regnes med en højere frigivelsesrate i de første 14 dage, efter at malingen er påført båden. Efter 14 dage antages frigivelsesraten at være konstant. Standarden tager ikke højde for, at frigivelsen under sejlads sandsynligvis er højere, end når båden ligger i havn, og vil derfor sandsynligvis overestimere frigivelseshastigheden, når båden ligger i havn og under-estimere frigivelseshastigheden ved sejlads. Udkastet til standarden foreslår endvidere typiske filmtykkelser og levetider for forskellige malinger (ISO 1999). Tykkelsen af det afslidte filmlag på 6 måneder (svarende til en sejlsæson) kan ud fra standardforslagets foreslåede filmtykkelser og levetider, beregnes til 42 mm (opløselig matrix), 38 mm (uopløselig matrix), 45 mm (tinbaseret selvpolerende maling) og 50 mm (tinfri selvpolerende maling). Disse lagtykkelser er i god overensstemmelse med, at Hempel har estimeret det gennemsnitlige afslidte filmlag til 42 mm pr. sejlsæson for lystbåde i Danmark (Hempel 1999c). Hempel har baseret beregningerne på hvor meget bundmaling, der sælges til det danske marked pr. år samt antallet af lystbåde/motorbåde over 6 m (svarende til dem, der males) samt deres gennemsnitlige bundareal.
Til simulering af den forøgede frigivelseshastighed ved sejlads antages det, at 60 mm af filmlaget slides af ved 6 måneders konstant sejlads. Til simulering af den lavere frigivelseshastighed, når båden ligger i havn, antages det, at 30 mm af filmlaget slides af, hvis båden konstant ligger i havn i 6 måneder. Disse antagelser svarer til, at bådene er ude at sejle i ca. 2 måneder af en sejlsæson og ligger i havn i de resterende 4 måneder, samt at frigivelseshastigheden er dobbelt så stor ved sejlads sammenlignet med, når båden ligger stille.
Ud fra fortrolige oplysninger fra Hempel (Hempel 1999b) omkring indhold af antibegroningsmidler, tørstofindhold, massefylde kan den gennemsnitlige frigivelseshastighed for de to typer antibegroningsmidler beregnes. Resultatet af disse beregninger er angivet i tabel B1.2.
Tabel B1.2
Beregnede gennemsnitlige frigivelseshastigheder.
Calculated average release rates.
Antibegroningsmiddel |
Frigivelseshastighed (U) (mg/m2/dag) |
|
I havn |
Ved sejlads |
|
| DCOI | 13 |
25 |
| ZPT | 21 |
41 |
Den samlede frigivelse af aktivstoffet til vandmasserne pr. tidsenhed udtrykkes i modellen ved:
 |
hvor
N er antallet af skibe, der er i vandområdet pr. dag [både/dag]
A er det gennemsnitlige våde bundareal [m2/båd]
t er opholdstiden for bådenes tyngdepunkt i det betragtede vandområde [dage]
P er procentdelen af skibene, som er malet med det betragtede antibegroningsmiddel [%]
2.3 PEC-Model
Modellen deles op i følgende dele:
- Massebalance i vandsøjlen
- Massebalance i sedimentet
Omsætning i vandsøjlen
Følgende forhold i vandsøjlen blev taget i betragtning:
- Nedbrydningshastigheden af udgangsstoffet og den følgende dannelse af nedbrydningsprodukter. Aerobe forhold i vandsøjlen blev antaget. Temperaturens indflydelse på nedbrydningshastigheden blev inkluderet ved antagelse om, at nedbrydningshastigheden halveres, når temperaturen falder med 10°C (og omvendt). I modelperioden er temperaturen ikke så lav, at nedbrydningen stopper.
- Abiotisk omsætning. Fotolytisk nedbrydning af ZPT er inkluderet. Hydrolyse er ikke vurderet at være en betydningsfuld reaktion for de to undersøgte stoffer (se hovedrapporten). Fotolytisk nedbrydning er ligesom andre reaktioner temperaturafhængig, men temperaturens indflydelse er lavere end for andre reaktioner. Schwarzenbach et al. (1993) angiver således, at en ændring i temperaturen på 10°C kun ændrer reaktionshastigheden med en faktor på mellem 1,15 og 1,5. Temperaturens indflydelse på den fotolytiske nedbrydning er derfor negligeret i nærværende arbejde.
- En første ordens nedbrydningskinetik blev antaget for samtlige nedbrydningsreaktioner.
- Der blev ikke skelnet mellem opløst stof og stof bundet til opløst organisk materiale (DOC).
- Bindingen til det suspenderede materiale blev udtrykt ved en lineær adsorption.
- Lineær sedimentation af det suspenderede materiale blev antaget.
- Resuspension af sedimenteret materiale. Resuspensionshastigheden blev i beregningerne antaget til at være konstant.
Følgende forhold i sedimentet blev taget i betragtning:
- Sedimentation af suspenderet materiale fra det øvre vandlag.
- Resuspension af sediment til det øvre vandlag.
- En første ordens anaerob nedbrydning. Sedimentet blev antaget at være anaerobt, hvorfor kun anaerob nedbrydning blev inddraget.
- Kun det sediment, som dannes i simuleringsperioden, blev betragtet. Dette sedimentlag blev antaget at være fuldstændigt homogent blandet.
En massebalance for vandsøjlen og sedimentet for både udgangsstoffet og de vigtigste nedbrydningsprodukter blev opstillet.
Følgende tre PEC (Predicted Environmental Concentration) blev beregnet:
- PEC(vandsøjle)
- PEC(sediment)
- PEC(sediment-porevand)
De tre koncentrationer blev sat lig med "steady-state" koncentrationen, dvs. den koncentration, som de beregnede koncentrationer nærmer sig med tiden, når der simuleres en kontinuer frigivelse af stoffet til vandmiljøet.
For alle stoffer blev baggrundsniveauet antaget at være 0.
2.4 Data for aktivstoffer
2.4.1 DCOI
Aerob nedbrydning
Figur B1.1 viser det forsimplede nedbrydningsmønster, som blev antaget for DCOI. DCOI blev i første omgang antaget at blive nedbrudt til N-(n-octyl) malonaminsyre, som under frigivelse af CO2 omdannes til N-(n-octyl) acetamid samt til N-(n-octyl) b hydroxypropionamid. Disse to nedbrydningsprodukter antages at blive omdannet til en lang række forskellige organiske forbindelser, som er samlet under "Andre nedbrydningsprodukter". Halveringstiden for denne pseudo-reaktion er antaget at være den samme for N-(n-octyl) acetamid og N-(n-octyl) b hydroxypropionamid. Disse nedbrydningsprodukter vil i et vist omfang blive mineraliseret under dannelse af CO2 (halveringstid for denne omdannelse er antaget ens for alle "andre nedbrydningsprodukter").
Halveringstiden for omdannelsen af DCOI til N-(n-octyl) malonaminsyre blev bestemt på baggrund af et forsøg, hvor fjernelsen af DCOI blev målt i havvand fra Jyllinge Lystbådehavn over en periode på 72 timer ved 12° C (Jacobson & Kramer 1999). Ved at minimere summen af arealerne af de relative rest af DCOI (RRSQ), der angives af Jacobson & Kramer (1999), ved anvendelse af følgende ligning:
![]()
hvor
i er en numerisk reference til observationen
yi(observeret) er den målte nedbrydning (%)
yi(estimeret) er den estimerede nedbrydning (%) ved antagelse af første ordens kinetik og ved antagelse af, at yi(estimeret) til tiden 0 = yi(observeret) til tiden 0
kan halveringstiden beregnes til 12,8 timer (for replikat 1) og 15,3 timer (for replikat 2) med en gennemsnitlig halveringstid på 14,1 timer (ved 12° C). De øvrige halveringstider blev estimeret ud fra de kvantiteter, som på baggrund af eksperimentelle undersøgelser (Mazza 1993) blev vurderet til at være til stede efter 30 dages aerob nedbrydning (se figur B1.1).
De estimerede halveringstider for den aerobe omdannelse af DCOI ved 25° C er givet i tabel B1.3.
Tabel B1.3
Estimerede halveringstider (dage) ved 25°C for aerob nedbrydning af DCOI.
Estimated half-lives (days) at 25°C of aerobic degradation of DCOI.
| Udgangs- stoffer |
Nedbrydningsprodukter |
|||||
DCOI |
N-(n- |
N-(n- |
N-(n- |
Andre nedbryd- nings- produkter |
14 CO2CO2 |
|
| DCOI | - |
0,2 |
- |
- |
- |
- |
| N-(n-octyl) malonamin- syre |
- |
- |
95 |
32,7 |
19,7 |
- |
| N-(n-octyl) b hydroxypro- pionamid |
- |
- |
- |
- |
19,7 |
- |
| N-(n-octyl) acetamid | - |
- |
- |
- |
19,7 |
- |
| Andre nedbrydnings- produkter | - |
- |
- |
- |
- |
66,5 |
| 14CO2 | - |
- |
- |
- |
- |
- |
Anaerob nedbrydning
Den anaerobe nedbrydning af DCOI blev antaget at følge det samme reaktionsmønster som den aerobe nedbrydning. Nedbrydningshastighederne blev dog antaget at være langsommere for den anaerobe nedbrydning.
Omdannelsen af DCOI ved aerobe og anaerobe forsøgsbetingelser er vist som funktion af tiden i figur B1.2. Data fra hovedrapportens tabel 3.2 (aerobe forhold) og 3.4 (anaerobe forhold; koncentrationer normeret til 100%) er anvendt. Det skal bemærkes, at tidsaksen for afbildningen af de anaerobe forsøg er 4,5 gange længere end tidsaksen for de aerobe forsøg. Det fremgår af figur B1.2, at der herved er en rimelig overensstemmelse mellem de målte koncentrationer for de aerobe hhv. de anaerobe forsøg. Det blev derfor antaget i beregningerne, at halveringstiderne for reaktionerne under anaerobe forhold er 4,5 gange længere end under aerobe forhold.
Figur B1.1 Se her
Nedbrydning af DCOI.
Degradation of DCOI.
Figur B1.2 Se her
Nedbrydningsforløb af DCOI ved aerobe og anaerobe forhold.
Degradation of DCOI under aerobic and anaerobic conditions.
Stofegenskaber
Udvalgte egenskaber for DCOI og dets nedbrydningsprodukter er givet i tabel B1.4. DCOI og de tre nedbrydningsprodukter blev antaget ikke at forefindes på ioniseret form ved pH = 7.
Tabel B1.4
Egenskaber for DCOI og dets nedbrydningsprodukter.
Properties of DCOI and its metabolites.
Stof |
Molvægt (g/mol) |
LogKOW |
LogKOC |
| DCOI | 282 |
2,8** |
3,2 |
| N-(n-octyl)malonaminsyre | 215 |
2,00* |
1,75* |
| N-(n-octyl) betahydroxypropionamid | 201 |
1,77* |
1,789* |
| N-(n-octyl) acetamid | 171 |
2,74* |
2,756* |
*
Beregnet vha. KowWin (Syracuse Research Corporation 1996).* Calculated by means of KowWin (Syracuse Research Corporation 1996).
Calculated by means of KowWin (Syracuse Research Corporation 1996).
** Målt (data angivet i hovedrapporten), measured (data stated in the main report).
2.4.2 Zinkpyrithion (ZPT)
Bionedbrydning
Figur B1.3 angiver de forenklede biologiske nedbrydningsveje for ZPT, som blev simuleret i eksponeringsberegningerne. Det er en stærk forenkling i forhold til de meget komplicerede nedbrydningsveje for ZPT.
Følgende forkortelser er benyttet:
|
ZPT |
|
PT |
|
OMDS |
|
OMSo |
|
PSoA |
Andre énringede, heterocykliske nedbrydningsprodukter karakteriseres med betegnelserne NP1-NP5 (jf. hovedrapporten, kapitel 4). Identiteten af NP1-NP5 er kendt af VKI.
To hovednedbrydningsveje er antaget:
1) Primært under aerobe forhold:
ZPT ® OMDS ® NP1 ® OMSo + andre forbindelser
2) Primært under anaerobe forhold:
ZPT® NP3 + OMDS ® NP4 ® PSoA + andre forbindelser
Det blev antaget, at OMDS, NP3, PSoA og OMSo omdannes videre til andre forbindelser, der mineraliseres i mindre omfang.
Halveringstiden for den primære reaktion (ZPT ® PT® OMDS + NP3) blev sat til 0,5 dage. De øvrige halveringstider blev estimeret ud fra de kvantiteter, som blev fundet i de aerobe og anaerobe nedbrydningsforsøg, hvor stofkoncentrationerne blev målt som funktion af tiden (disse forsøg er omtalt i hovedrapporten).
De estimerede halveringstider for den aerobe og anaerobe nedbrydning er givet i tabel B1.5 og B1.6. Målte og beregnede koncentrationer er gengivet i figur B1.4.
Tabel B1.5
Modelsimulering af aerob biologisk nedbrydning af zinkpyrithion. Estimerede
halveringstider (dage) ved 25°C.
Model simulation of aerobic biodegradation of zinc pyrithione. Estimated half-lives (days)
at 25°C.
Udgangs- |
Nedbrydningsprodukter |
|||||||
ZPT |
OMDS |
NP4 |
PSoA |
NP1 |
OMSo |
Andre forbind- elser |
CO2 |
|
| ZPT | - |
0,5 |
- |
- |
- |
- |
- |
- |
| NP3 | - |
- |
- |
- |
- |
- |
50 |
- |
| OMDS | - |
- |
4,0 |
- |
2,0 |
- |
4,0 |
- |
| NP4 | - |
- |
- |
15,0 |
- |
- |
- |
- |
| PSoA | - |
- |
- |
- |
- |
- |
250 |
- |
| NP1 | - |
- |
- |
- |
- |
15,0 |
- |
- |
| OMSo | - |
- |
- |
- |
- |
- |
80 |
- |
| Andre forbind- elser |
- |
- |
- |
- |
- |
- |
- |
2000 |
| CO2 | - |
- |
- |
- |
- |
- |
- |
- |
Tabel B1.6
Modelsimulering af anaerob biologisk nedbrydning af zinkpyrithion. Estimerede
halveringstider (dage) ved 25°C.
Model simulation of anaerobic biodegradation of zinc pyrithione. Estimated half-lives
(days) at 25°C.
Udgangs- |
Nedbrydningsprodukter. |
||||||||
ZPT |
NP3 |
OMDS |
NP4 |
PSoA |
NP1 |
OMSo |
Andre forbind- |
CO2 |
|
| ZPT | - |
0,5 |
30 |
- |
- |
- |
- |
- |
- |
| NP3 | - |
- |
- |
50 |
- |
- |
- |
50 |
- |
| OMDS | - |
- |
- |
4,0 |
- |
2,0 |
- |
4,0 |
- |
| NP4 | - |
- |
- |
- |
15,0 |
- |
- |
- |
- |
| PSoA | - |
- |
- |
- |
- |
- |
- |
5,0 |
- |
| NP1 | - |
- |
- |
- |
- |
- |
15,0 |
- |
- |
| OMSo | - |
- |
- |
- |
- |
- |
- |
80 |
- |
| Andre forbind- elser |
- |
- |
- |
- |
- |
- |
- |
- |
6000 |
| CO2 | - |
- |
- |
- |
- |
- |
- |
- |
- |
Fotolyse
Som nævnt tidligere inkluderes fotolytisk nedbrydning af ZPT i modelsimuleringerne. ZPT antages at blive omdannet til NP3 ved den fotolytiske nedbrydning.
Den fotolytiske halveringstid for ZPT i dagslys ved middagstid er blevet bestemt til:
- 1,78 min uden skydække
- 3,74 min med skydække
Forsøgene blev foretaget i september ved en nordlig breddegrad på
ca. 42o, hvor nedbrydningshastigheden af ZPT i saltvand blev fulgt (Fenn 1999).
Forsøgene foregik i buede rør. En førsteordenshastighedskonstant kP kan
beregnes til 0,18 min-1 (uden skydække) og 0,08 min-1 (med
skydække). Til korrektion for at rørene er buede, er der anvendt en faktor på 2,2.
Den målte fotolytiske hastighedskonstant ved skyfri himmel er antaget til at kunne beskrives ved (se Schwarzenbach et al. 1993):
![]()
hvor
F er det såkaldte quantum yield, som her er antaget uafhængig af bølgelængden [-]. F angiver, hvor stor en del af de molekyler, som er exciteret af lyset, der omdannes til et andet stof.
![]() er den specifikke hastighed for
lysabsorption [tid-1]. Denne er beregnet af (Schwarzenbach et al. 1993):
er den specifikke hastighed for
lysabsorption [tid-1]. Denne er beregnet af (Schwarzenbach et al. 1993):
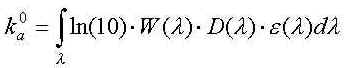
l er bølgelængde [nm].
W(l) er lysintensiten ved de forskellige bølgelængder [milliEinstein/cm2/tid/nm]. Lysintensiteten ved breddegraden 40o og efterår er hentet fra Zepp & Cline (1977).
D(l) er forholdet mellem den gennemsnitlige banelængde for lyset og den dybde af et vandelement, som kan antages fuldstændigt opblandet [-]. D(l ) er her antaget lig med 1 for alle bølgelængder.
e (l) er den såkaldte molære ekstinktionskoefficient [(mol/l- 1/cm]. Værdier for disse er for ZPT taget fra (Fenn 1999).
Der er taget hensyn til kuvettens lysafbøjning.
F blev herved bestemt til 0,07.
Det amerikanske program GCSOLAR (U.S. EPA 1999) blev herefter anvendt til beregning af den fotolytiske halveringstid. Programmet anvender de såkaldte attenuationkoefficienter, a1 , der benyttes til at beregne, hvor meget vandet absorberer lyset, som funktion af dybden.
Attenuationkoefficienten for vandet ved Kronprins Frederiks bro, er bestemt ud fra målte sigtedybder ved 2 stationer i nærheden af broen (Roskilde Amt og Frederiksborg Amt, 1997). Den mindste sigtedybde i sommerperioden er på ca. 2,5 m. Ved anvendelse af data fra Calkins (1977) er følgende sammenhæng mellem sigtedybden og attenuation-koefficienten a ved sigtedybder under 4 m fundet:
a [m-1] = 3,05 - 0,57× Sigtedybden [m].
Attenuationkoefficienten for Jyllinge Lystbådehavn er fundet ud fra litteraturdata i kystnære område (Zafirioiu 1977). Værdierne angives her som funktion af bølgelængde og med en minimum og maximum værdi. De højeste værdier er anvendt i nærværende beregninger.
GCSOLAR tager ikke højde for skydækkets indflydelse på fotolysehas-tigheden. Det amerikanske program EXAMS (Burns et al. 1981), som også kan anvendes til simulering af fotolysen af stoffer, tager højde for skydækkets indflydelse på fotolysehastigheden. Ved brug af EXAMS er det beregnet, at halveringstiden i forhold til halveringstiden ved klar himmel bliver ca. 50% højere ved et skydække på 60%, som er det gennemsnitlige skydække i Danmark i månederne april-september (Danmarks Statistik 1996).
GCSOLAR kan beregne den gennemsnitlige fotolytiske halveringstid for hver af årstiderne: Forår, sommer, efterår og vinter og ved forskellige breddegrader (dog kun breddegrader delelige med 10). Den gennemsnitlige fotolytiske halveringstid for ZPT i årstiderne forår, sommer, efterår samt breddegraderne 50o og 60o blev fundet til 9,8 timer for Jyllinge Lystbådehavn (6,5 timer, hvis der intet skydække er) og 6,6 timer for Kronprins Frederiks Bro (4,4 timer, hvis der intet skydække er).
Den fotolytiske nedbrydning er svagt afhængig af temperaturen. Der er dog ikke inkluderet en temperaturafhængighed af den fotolytiske nedbrydning i nærværende beregninger.
Den fotolytiske halveringstid er bestemt for et åbent vandområde, hvor der er taget hensyn til skydække og den faldende lysintensitet ned gennem vandsøjlen, men hvor der er ikke taget hensyn til, at de både, der er i havnen, samt molen vil afskære en vis del af sollyset. Der er derfor udført beregninger, dels hvor der er taget højde for den fotolytiske nedbrydning og dels hvor den fotolytiske nedbrydning er negligeret. De aktuelle forhold vil sandsynligvis ligge et sted mellem de to betragtninger, men det er ikke umiddelbart muligt at kvantificere, hvor stor betydning skyggepåvirkningen fra bådene og molen har på den mængde lys, der rent faktisk rammer vandoverfladen. For den befærdede sejlrute under Kronprins Frederiks bro vil der lige under broen være begrænset sol-lysadgang, medens der i den øvrige del af sejlruten ikke vil være større skyggevirkninger.
Stofegenskaber
Stofegenskaberne for zinkpyrithion og dets nedbrydningsprodukter er angivet i tabel B1.7.
De forskellige énringede, heterocykliske nedbrydningsprodukter har en lav beregnet log KOW, hvilket indikerer en høj vandopløselighed. Sulfonsyrerne forventes også at være meget stærke syrer, hvorfor de sandsynligvis er fuldt dissocieret ved den herskende pH i de to vandområder. Bindingen til sediment og suspenderet materiale for disse to forbindelser forventes derfor at være lav. De beregnede KOC-værdier er dog anvendt til beregning af bindingen til suspenderet materiale og til sedimentet.
Tabel B1.7
Egenskaber for zinkpyrithion og dets nedbrydningsprodukter.
Properties of zinc pyrithione and its metabolites.
Stof |
LogKOW |
LogKOC |
| ZPT | 0,97** |
2,9-4,0 |
| NP3 | 1,50* |
1,728* |
| OMDS | -2,35* |
3,355* |
| NP4 | -2,36* |
0,912* |
| PSoA | -2,35* |
1,072* |
| NP1 | -4,50* |
1,131* |
| OMSo | -4,49* |
1,291* |
| Andre forbindelser | -3,0*** |
1,1*** |
*
Beregnet vha. KowWin (Syracuse Research Corporation 1996).* Calculated by means of KowWin (Syracuse Research Corporation 1996).
** Målt (data angivet i hovedrapporten), measured (data stated in the main report).
*** Fiktivt sat, fictive Beregnet vha. KowWin (Syracuse Research Corporation 1996).
* Calculated by means of KowWin (Syracuse Research Corporation 1996).
** Målt (data angivet i hovedrapporten), measured (data stated in the main report).
*** Fiktivt sat, fictive
Figur B1.3 Se her
Nedbrydningningsveje for zinkpyritihion (både aerobt og anaerobt).
Degradation paths of zinc pyrithione (both aerobically and anaerobically).
Figur B1.4a Se her
Beregnede og målte stofkoncentrationer for zinkpyrithion og dets
nedbrydningsprodukter. Aerobe forsøgsbetingelser.
Calculated and measured concentrations of zinc pyrithione and its metabolites. Aerobic
experimental conditions.
Figur B1.4b Se her
Beregnede og målte stofkoncentrationer for zinkpyrithion og dets nedbrydningsprodukter. Anaerobe forsøgsbetingelser.
Calculated and measured concentrations of zinc pyrithione and its metabolites. Anaerobic experimental conditions.
3. Beregningsresultater
I tabel B1.8 er de beregnede PEC-værdier for de to scenarier og de forskellige stoffer angivet. Koncentrationerne er som tidligere nævnt "steady-state" koncentrationer.
Det fremgår af tabel B1.8, at de højeste beregnede koncentrationer findes for lystbådehavnen. De beregnede koncentrationer er her ca. 100 gange højere end de koncentrationer, der beregnes for den befærdede sejlrute.
For udgangsstofferne er følgende "steady-state" koncentrationer for vandfasen - PEC(vand) - beregnet:
|
0,52 mg/L (lystbådehavn) 0,006 mg/L (befærdet sejlrute) |
|
0,56 mg/L (lystbådehavn, fotolyse inkluderet) 1,7 mg/L (lystbådehavn, fotolyse ikke inkluderet) 0,005 mg/L (befærdet sejlrute, fotolyse inkluderet) 0,022 mg/L (befærdet sejlrute, fotolyse ikke inkluderet) |
Tabel B1.8a
Beregningsresultater for DCOI.
Calculation results of DCOI.
|
|
PEC (vand) |
PEC (sediment, porevand) |
PEC (sediment, bundet) |
| mg/L | mg/L | mg/kg | ||
| DCOI | Lystbåde- |
0,52 |
0,0015 |
0,12 |
| N-(n-octyl) malanominsyre | 1,98 |
0,83 |
2,32 |
|
| N-(n-octyl) beta hydroxypropionamid | 0,020 |
0,14 |
0,43 |
|
| N-(n-octyl) acetamid | 0,050 |
0,084 |
2,42 |
|
| Andre forbindelser | 0,10 |
|||
| DCOI | Sejlrute |
0,0061 |
0,00002 |
0,0014 |
| N-(n-octyl) malanominsyre | 0,040 |
0,011 |
0,031 |
|
| N-(n-octyl) beta hydroxypropionamid | 0,00071 |
0,0019 |
0,0058 |
|
| N-(n-octyl) acetamid | 0,0018 |
0,0013 |
0,039 |
|
| Andre forbindelser | 0,0040 |
Tabel B1.8b
Beregningsresultater for ZPT.
Calculation results of ZPT.
| Forbind- |
Sce- |
Med fotolyse |
Uden fotolyse |
||||
PEC (vand) |
PEC (sedi- |
PEC (sedi- |
PEC (vand) |
PEC (sedi- |
PEC (sedi- |
||
| mg/L | mg/L | mg/kg | mg/L | mg/L | mg/kg | ||
| ZPT | Jyl- |
0,56 |
0,00056 |
0,089 |
1,7 |
0,0013 |
0,21 |
| NP3 | 1,22 |
0,25 |
0,68 |
0,00006 |
0,54 |
1,5 |
|
| NP4 | 0,099 |
0,19 |
0,078 |
0,20 |
0,43 |
0,18 |
|
| PSoA | 0,0080 |
0,068 |
0,040 |
0,016 |
0,15 |
0,090 |
|
| NP1 | 0,15 |
0,091 |
0,062 |
0,45 |
0,24 |
0,17 |
|
| OMSo | 0,012 |
0,48 |
0,47 |
0,036 |
1,3 |
1,3 |
|
| Andre for- bind- elser |
0,11 |
- |
- |
0,24 |
- |
- |
|
| ZPT | Sejl- |
0,0053 |
0,00001 |
0,00090 |
0,022 |
0,00002 |
0,0027 |
| NP3 | 0,027 |
0,0028 |
0,0076 |
0,00000 |
0,0072 |
0,019 |
|
| NP4 | 0,0027 |
0,0022 |
0,00089 |
0,0059 |
0,0061 |
0,0025 |
|
| PSoA | 0,00040 |
0,00077 |
0,00045 |
0,00088 |
0,0022 |
0,0013 |
|
| NP1 | 0,0032 |
0,0011 |
0,00077 |
0,013 |
0,0042 |
0,0028 |
|
| OMSo | 0,00046 |
0,0059 |
0,0058 |
0,0019 |
0,022 |
0,021 |
|
| Andre for- bind- elser |
0,0032 |
- |
- |
- |
- |
- |
|
4. Følsomhedsanalyse
Beregningsresultaterne er bl.a. betinget af de værdier, som de forskellige parametre er tildelt.
En følsomhedsanalyse af følgende parametres betydning for de beregnede koncentrationer af udgangsstofferne (DCOI og ZPT) er udført:
- Havnescenarier. Der er udført supplerende PEC-beregninger for 5 lystbådehavne (se afsnit 4.1)
- Temperaturen. Temperaturen blev varieret mellem 5oC og 15oC, da det vurderes at være en typisk variation for temperaturen i månederne maj – september (se afsnit 4.2)
- Vandskiftet. Vandskiftet blev varieret mellem 0 m3/m2/d svarende til ingen vandudskiftning og 1 m3/m2/d, som vil kunne finde sted under visse forhold (se afsnit 4.2)
- Sedimentationshastighed. Sedimentationshastigheden blev varieret mellem 0,7 m/d svarende til, at netto sedimentationen er næsten 0 og op til 1,5 m/d (se afsnit 4.2)
- Udludningshastighed. Den samlede udludningshastighed blev varieret mellem 50% og 200% af den samlede udludningshastighed, som blev anvendt i basisberegningerne (se afsnit 4.2)
4.1 Havnescenarier
Der er udført supplerende beregninger for 5 andre lystbådehavne. Karakteriseringen af disse er givet i tabel B1.9. Disse data er indhentet af Hempel og videregivet til VKI.
Vandudvekslingen i havnene er sat til 0,6 m3/m2/dag for alle havne undtagen for Svendborg og for Horsens havn. For Horsens Lystbådehavn er vandudvekslingen sat til 0,8 m3/m2/dag. Svendborg Lystbådehavn står på pæle i Svendborg Sund. Strømforholdene er derfor antaget til at være tilsvarende strømforholdene i Svendborg Sund. En gennemsnitlig strømhastighed på 0,5 m/s er antaget for Svendborg Lystbådehavn, hvilket svarer til amplituden i den kraftige periodiske hastighedsvariation, som tidevandet bevirker i Svendborg Sund (Harremoës & Malmgren-Hansen 1989).
Tabel B1.9 Se her
Havnescenarie (udarbejdet af Hempel).
Harbour scenario (prepared by Hempel).
De beregnede "steady-state" koncentrationer i disse havnescenarier er givet i tabel B10.
Tabel B1.10
Beregnede "steady-state" koncentrationer.
Calculated steady-state concentrations.
| Havn | Antal både pr havnevolumen i forhold
til antal både pr. havnevolumen i Jyllinge Lystbådehavn |
PEC, vand (ZPT) |
PEC, vand (DCOI) |
|
Med |
Uden fotolyse |
|||
| Jyllinge | 1,0 |
0,56 |
1,70 |
0,52 |
| Grenå | 0,2 |
0,11 |
0,28 |
0,08 |
| Horsens | 0,7 |
0,49 |
1,14 |
0,35 |
| Rungsted | 0,3 |
0,02 |
0,08 |
0,02 |
| Egå Marina | 0,5 |
0,29 |
0,81 |
0,25 |
| Svendborg | 0,5 |
<0,01 |
<0,01 |
<0,01 |
Det fremgår af tabel B1.10, at Jyllinge Lystbådehavn resulterer i de højeste beregnede koncentrationer. Den primære grund til dette er, at der er forholdsmæssigt flere både i Jyllinge Lystbådehavn i forhold til det vandvolumen, der skal fortynde det frigivne kemikalie (se tabel B1.10). Det anvendte scenarie er således et konservativt scenarie som forudsat ved udpegningen af Jyllinge Lystbådehavn.
4.2 Følsomhedsanalyse af øvrige parametre
Tabellerne B1.11a og B1.11b viser forholdet mellem den beregnede koncentration af udgangsstoffet i vandfasen efter ændring af parameter og den beregnede koncentration i standardscenariet.
Det fremgår af tabellerne B1.11a og B1.11b, at inden for den variation, der er tillagt de enkelte parametre, er det den samlede udludningshastighed, som forårsager de største variationer i de beregnede koncentrationer. Sedimentationshastigheden har kun en meget lille betydning for de beregnede koncentrationer af udgangsstofferne.
Tabel B1.11a
Følsomhedsanalyse af PEC (vand) for DCOI. Tallene angiver forholdet mellem den beregnede koncentration af udgangsstoffet i vandfasen efter ændring af parameter og den beregnede koncentration i standardscenariet.
Sensitivity analysis of PEC (water) of DCOI. The figures indicate the relation between the calculated concentration of the basic substance in the water phase, after changing the parameter, and the calculated concentration in the standard scenario.
Parameter |
Jyllinge Lystbådehavn |
|
PEC (vand) |
PEC (vand) |
|
| Standardscenarie | 1,0 |
1,0 |
| Temperatur 5°C | 1,5 |
1,6 |
| Temperatur 15°C | 0,9 |
0,9 |
| Ingen vandskifte | 1,2 |
1,1 |
| 167% forøget vandskifte | 0,9 |
0,9 |
| 70% mindre sedimentationshastighed | 1,0 |
1,0 |
| 150% højere sedimentationshastighed | 1,0 |
1,0 |
| 50% lavere udludning | 0,5 |
0,5 |
| 200% højere udludning | 2,0 |
2,0 |
Tabel B1.11b
Følsomhedsanalyse af PEC (vand) for ZPT. Tallene angiver forholdet mellem den beregnede koncentration af udgangsstoffet i vandfasen efter ændring af parameter og den beregnede koncentration i standardscenariet.
Sensitivity analysis of PEC (water) of ZPT. The figures indicate the relation between the calculated concentration of the basic substance in the water phase, after changing the parameter, and the calculated concentration in the standard scenario.
Scenarie |
Parameter |
Med fotolyse |
Uden fotolyse |
PEC (vand) |
PEC (vand) |
||
Jyllinge Lystbådehavn |
Standardscenarie | 1,0 |
1,0 |
| Temperatur 5°C | 1,1 |
1,4 |
|
| Temperatur 15°C | 1,0 |
0,6 |
|
| Ingen vandskifte | 1,1 |
1,6 |
|
| 167% forøget vandskifte | 0,9 |
0,6 |
|
| 70% mindre sedimentationshastighed | 1,0 |
1,2 |
|
| 150% højere sedimenta-tionshastighed | 1,0 |
1,0 |
|
| 50% lavere udludning | 0,5 |
0,5 |
|
| 200% højere udludning | 2,0 |
4,0 |
|
Befærdet sejlrute |
Standardscenarie | 1,0 | 1,0 |
| Temperatur 5°C | 1,2 | 1,5 | |
| Temperatur 15°C | 0,9 | 0,9 | |
| Ingen vandskifte | 1,1 | 1,2 | |
| 167% forøget vandskifte | 0,9 | 0,9 | |
| 70% mindre sedimentationshastighed | 1,0 | 1,0 | |
| 150% højere sedimentationshastighed | 1,0 | 1,0 | |
| 50% lavere udludning | 0,5 | 0,5 | |
| 200% højere udludning | 2,0 | 2,0 |
Udtrykkes lysintensiteten ved overfladen som I0 og lysintensiteten i dybden z som I, beskrives sammenhængen mellem I og I0 : log10(I/I0) = -a × z Udtrykkes lysintensiteten ved overfladen som I0 og lysintensiteten i dybden z som I, beskrives sammenhængen mellem I og I0 : log10(I/I0) = -a × z
Bilag 2. Undersøgelse af mineraliseringen af DCOI og zinkpyrithion i marine sedimenter
1. Indledning
Mineraliseringen af 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on (DCOI) og zinkpyrithion blev undersøgt i laboratorieforsøg med kystnære, marine sedimenter. Forsøgene blev udført under aerobe og anaerobe forhold ved anvendelse af testkoncentrationer i ng/g, der antages at give en miljørealistisk omdannelseskinetik. I de anaerobe eksperimenter blev sulfatreducerende forhold etableret ved tilsætning af sulfat. Kystnære, marine sedimenter indeholder betydelige mængder af sulfat (Sørensen et al. 1979). Glukose blev medtaget i forsøgene for at undersøge mineraliseringen af et let bionedbrydeligt stof i lav koncentration og under de givne eksperimentelle betingelser.
2. Materialer og metoder
Sediment og havvand
Sedimentprøver og tilhørende havvand blev indsamlet fra to lokaliteter i Øresund. De to sæt af sediment og vandprøver kan beskrives som angivet nedenfor.
Lerholdigt sediment (LS)
- Lokalitet: Øresund, 55° 50'642N - 12° 40'854E; dybde (sediment), 22 m; dybde (vand), 20 m.
- Tekstur: grovsand (0,25-2 mm), 0,9%; finsand (0,063-0,25 mm), 26,4%; silt og ler (<0,063 mm), 65,8%; organisk stof, 6,9%.
- Antal bakterier (vand): 3,1 × 103 pr. mL.
- Antal bakterier (sediment): 1,5 × 105 pr. g.
Sandet sediment (SS)
- Lokalitet: Øresund, 55° 50'030N - 12° 37'534E; dybde (sediment), 4 m; dybde (vand), 2 m.
- Tekstur: grovsand, 91,5%; finsand, 7,3%; silt og ler, 1,0%; organisk stof, 0,2%.
- Antal bakterier (vand): 2,1 × 103 pr. mL.
- Antal bakterier (sediment): 4,8 × 104 pr. g.
Antallet af bakterier i havvand og sediment blev bestemt som kimtal ved indstøbning af en kendt mængde af prøven i Bacto Marine Agar 2216 (Difco). Sediment (ca. 1,6 g) blandes med 9 mL fosfatbuffer og behandles herefter som en vandprøve. Kimtallet bestemmes som antallet af kolonier, der er vokset frem efter 72 timers inkubering ved 21° C. Sediment og vandprøver blev opbevaret adskilt i mørke ved 4° C indtil anvendelsen.
Kemikalier
[2,3-14C]DCOI (Lot Nos. 853.0208 og 853.0209; 15,9 mCi/mmol, 56,44 µCi/mg, radiokemisk renhed 98,6%) blev leveret af Rohm and Haas Research Laboratories (Spring House, Pennsylvania). [14C]zinkpyrithion (Lot. No. 3228-143; 157,63 mCi/mmol, 0,50 mCi/mg) og [UL-14C]D-glukose (Lot 48H9476 Sigma; 212,5 mCi/mmol, 1,18 mCi/mg, opløst i ethanol:vand, 9:1) blev leveret af Arch Chemicals (Cheshire, Connetticut). Alle øvrige kemikalier var kommercielt tilgængelige og af analytisk renhed.
Aerobe bionedbrydnings-forsøg
De aerobe bionedbrydningsforsøg blev udført med både sediment LS og SS. Stamopløsninger af [14C]DCOI (i methanol), [14C]zink-pyrithion (i dimethyl sulfoxid) og [14C]glukose (i deioniseret vand) blev tilsat til 300-mL glasflasker med 10 g sediment (vådvægt) og 50 mL havvand, der forinden var blevet beluftet med atmosfærisk luft i ca. 20 timer. For [14C]DCOI blev stamopløsningen tilsat til forsøgsflasker med 0,5 g tørret sediment, og methanolen blev tilladt at fordampe, inden yderligere sediment og vand blev tilført. De øvrige stoffer blev tilsat ved at blande stamopløsningen med sedimentet, hvorefter der blev tilsat havvand. De resulterede koncentrationer af de tre modelstoffer er angivet i tabel B.1. To glasrør blev anbragt i forsøgsflaskerne, et med 1N KOH (3 mL) for absorption af 14CO2 og et med ethylenglykol for opsamling af andre gasformige forbindelser. Flaskerne blev lukket med gummipropper og aluminiumskruelåg og blev stillet mørkt ved 15° C.
Mineralisering af stofferne blev fulgt ved at bestemme 14C-aktiviteten, der var opsamlet i glasrørrene. Hver uge blev udtaget prøver til væske-scintillationstælling, og forsøgsflaskerne blev stillet mørkt uden låg i ca. 10 min. for udskiftning af flaskernes gasfase med atmosfærisk luft. Herefter blev indholdet i glasrørrene erstattet med frisk KOH eller ethylenglykol. Ved afslutningen af forsøget efter 42 dage blev CO2 i vandfasen frigjort efter forsuring af sediment-vand-systemet til pH 1-2 ved tilsætning af koncentreret svovlsyre.
Anaerobe bionedbrydningsforsøg
De anaerobe bionedbrydningsforsøg blev kun udført med sediment LS. På samme måde
som i de aerobe forsøg blev stamopløsninger af de tre modelstoffer tilsat til 117-mL
serumflasker med 30 g sediment (vådvægt) og 30 mL havvand. De resulterede
koncentrationer af de tre modelstoffer er angivet i tabel B.2.1. Inden anvendelsen var
havvandet blevet forbehandlet ved tilsætning af en fosfatbuffer (27 mg KH2PO4
og 112 mg Na2HPO4 × 12H2O pr.
liter) for stabilisering af pH og en redox-indikator (1,0 mg resazurin pr. liter) for at
kunne kontrollere, at anaerobe betingelser var til stede gennem forsøget. De enkelte
serumflasker blev tilsat sulfid
(0,5 g Na2S× 9H2O/kg) som reducerende
middel, mens sulfat (Na2SO4; 25 mM i vandfasen) blev tilsat som
elektronacceptor for etablering af sulfatreducerende forhold, der er karakteriske for
marine sedimenter. Et glasrør med 1N KOH (3 mL) blev anbragt i serumflaskerne for
absorption af 14CO2. Under hele den ovennævnte procedure blev
serumflaskerne omhyggeligt beluftet med iltfri N2-gas, indtil de blev lukket
med 1-cm butylgummipropper og aluminiumlåg. Forsøgsflaskerne blev stillet mørkt ved 15° C.
Mineralisering af stofferne blev fulgt ved at bestemme 14C-aktiviteten (fra 14CO2), der var opsamlet i glasrøret med KOH. Udtagning af KOH til væskescintillationstælling blev foretaget efter 14, 28 og 56 dage, hvorefter væsken i glasrøret blev erstattet af frisk KOH. Da en del af kulstoffet ved mineralisering af modelstofferne kan omdannes til methan, blev 14CH4 bestemt ved at indsprøjte 2-mL gasprøver i scintillationsglas, der var modificerede, så lågene kunne holde et septum (Zehnder et al. 1979). Inden anvendelsen blev der boret et hul i skruelåget til hvert scintillationsglas og indsat et butylgummi-septum. Scintillationsglassene blev fyldt med 20 mL af en væskescintillations-cocktail (Insta gel II plus, Packard), der viste sig at kunne absorbere ca. 2/3 af den tilsatte methan i pilotforsøg. Ved afslutningen af forsøget efter 56 dage blev CO2 i vandfasen frigjort efter forsuring af sediment-vand-systemet til pH 1-2 ved tilsætning af koncentreret svovlsyre.
Tabel B2.1
Aerob og anaerob mineralisering. Initielle koncentrationer af modelstoffer.
Aerobic and anaerobic mineralization. Initial concentrations of model substances.
Modelstof |
Testtype |
Initiel koncentration |
| [14C]DCOI | Aerobe forhold |
0,83 |
| [14C]DCOI | Aerobe forhold |
0,033 |
| [14C]DCOI | Anaerobe forhold |
0,83 |
| [14C]Zinkpyrithion [14C]Zinc pyrithione |
Aerobe forhold |
0,037 |
| [14C]Zinkpyrithion [14C] Zinc pyrithione |
Aerobe forhold |
0,037 |
| [14C]Zinkpyrithion [14C] Zinc pyrithione |
Anaerobe forhold |
0,037 |
| [14C]Glukose [14C]Glucose |
Aerobe forhold |
0,025 |
| [14C]Glukose [14C]Glucose |
Aerobe forhold |
0,025 |
| [14C]Glukose [14C]Glucose |
Anaerobe forhold |
0,025 |
Genfindelse af resterende 14C
Efter afslutningen af de aerobe og de anaerobe forsøg blev den resterende 14C i vand og sediment bestemt ved følgende procedurer. I forsøget, hvor [14C]DCOI blev tilsat i koncentrationen 0,033 µg/g, og i forsøgene med [14C]glukose blev den resterende radioaktivitet bestemt efter væskescintillationstælling af delprøve fra vandfasen og afbrænding af 0,1-g sedimentprøver ved overskud af ilt. I de øvrige forsøg blev den resterende 14C i sedimentet bestemt ved ekstraktioner med 6N HCl efterfulgt af 1N NaOH, hvorefter det ekstraherede sediment blev afbrændt under overskud af ilt (Madsen & Kristensen 1997; Madsen 1999). Denne metode giver mulighed for at bestemme de fraktioner af 14C, der er bundet i form af hydrolyserbare forbindelser, humus- og fulvussyrer eller til humin/lermineraler
Kemiske analyser
DCOI og nedbrydningsprodukter fra omdannelsen af DCOI blev analyseret og karakteriseret af Rohm and Haas (Andrew Jacobson, Rohm and Haas Research Laboratories, Spring House, Pennsylvania). Vandprøver blev behandlet med fast-fase-ekstraktion (SPE) ved anvendelse af acetat:methanol (1:1) før analyse på HPLC. Sedimentprøver blev ekstraheret to gange med acetonitril: 0,01 N HCl (4:1) efterfulgt af ekstraktion med dichlormethan for analyse på HPLC.
Zinkpyrithion og dets nedbrydningsprodukter blev bestemt af Arch Chemicals (James C. Ritter, Department of Ecotoxicology, Cheshire, Connetticut). Sedimentprøver blev ekstraheret med acetonitril efterfulgt af to ekstraktioner med 1,0 N KOH. Herefter blev vandprøver og ekstrakter fra sediment derivatiseret før analyse på HPLC (Arch Chemicals 1999b).
3. Resultater
Den kumulerede udvikling af 14CO2 fra mineraliseringen af DCOI og zinkpyrithion er vist i figurerne 3.1-3.3 (afsnit 3.2) og 4.1-4.3 (afsnit 4.3). Den totale mineralisering og fordelingen af den resterende radioaktivitet ved forsøgenes afslutning er vist i tabel B2.2-B2.4. Mængden af 14C i absorbere med ethylenglykol (aerobe forsøg) udgjorde <0,1% af den tilsatte radioaktivitet.
Tabel B2.2 Se her
Mineralisering af DCOI i sediment og havvand under aerobe eller anaerobe forhold. Fordeling og genfindelse af 14C efter inkubering i 42 dage (aerobe forsøg) eller 56 dage (anaerobe forsøg).
Mineralization of DCOI in sediment and sea water under aerobic or anaerobic conditions. Distribution and retrieval of 14C after an incubation of 42 days (aerobic test) or 56 days (anaerobic test).
Tabel B2.3 Se her
Mineralisering af zinkpyrithion i sediment og havvand under aerobe eller anaerobe forhold. Fordeling og genfindelse af 14C efter inkubering i 42 dage (aerobe forsøg) eller 56 dage (anaerobe forsøg).
Mineralization of zinc pyrithione in sediment and sea water under aerobic or anaerobic conditions. Distribution and retrieval of 14C after an incubation of 42 days (aerobic test) or 56 days (anaerobic test).
Tabel B2.4
Mineralisering af D-glukose i sediment og havvand under aerobe eller anaerobe forhold. Genfindelse af 14C efter inkubering i 42 dage (aerobe forsøg) eller 56 dage (anaerobe forsøg)
Mineralization of D glucose in sediment and sea water under aerobic or anaerobic conditions. Retrieval of 14C after incubation of 42 days (aerobic test) or 56 days (anaerobic test)
| Sediment/ testtype Sediment/ test type |
CO2 |
Vandfase |
Sediment B |
Total gen-findelse |
| SS, aerob, SS, aerobic |
59,6 ± 2,0 |
6,0 ± 0,75 |
12,5 ± 0,89 |
78,1 |
| LS, aerob, LS, aerobic |
52,3 ± 0,76 |
4,6 ± 0,48 |
25,5 ± 0,39 |
82,4 |
| LS, anaerob, LS, anaerobic |
58,5 ± 1,9 A |
3,1 ± 0,38 |
17,3 ± 0,10 |
78,9 |
A
, heraf <0,01% som 14CH4; B, forbrænding af ikke-ekstraheret sediment; SD, standardafvigelser mellem fire replikater., heraf <0,01% som 14CH4; B, forbrænding af ikke-ekstraheret sediment; SD, standardafvigelser mellem fire replikater.A, hereof <0.01% as 14CH4; B, incineration of non-extracted sediment; SD, standard deviations between four replicates.
Bilag 3. Undersøgelse af effekten af nedbrydning og sorption på den akvatiske toksicitet af DCOI og zinkpyrithion
1. Indledning
Effekten af nedbrydning og sorption på toksiciteten af 4,5-dichlor-2-n-octyl-4-isothiazolin-3-on (DCOI) og zinkpyrithion blev undersøgt i laboratorieforsøg med det marine krebsdyr Acartia tonsa. Da især zinkpyrithion nedbrydes fotolytisk, blev forsøgene udført både i mørke og ved konstant eksponering med lys.
2. Materialer og metoder
Denne undersøgelse blev udført med det sandede sediment (SS) og tilhørende havvand, som er beskrevet i bilag 2.
DCOI (Lot No. 14-SS-18F; renhed, 99,86%) blev leveret af Rohm and Haas Research Laboratories (Spring House, Pennsylvania). Zinkpyrithion (Lot. No. J116659; renhed, 98,9%) blev leveret af Arch Chemicals (Cheshire, Connectticut).
DCOI og zinkpyrithion blev tilsat fra stamopløsninger i henholdsvis methanol (50 µL) og dimethyl sulfoxid (50 µL) til 55-mL serumflasker med 0,5 g tørret sediment. Methanolen fra DCOI- stamopløsningen blev tilladt at fordampe. Herefter tilsattes 7 g sediment (vådvægt) og 35 mL af det tilhørende havvand, der forinden var opsaltet til en saltholdighed på 3,2%. De initielle koncentrationer var 0,1 µg/g for DCOI og 0,025 µg/g for zinkpyrithion. Som gasfase i testsystemet blev tilført ren oxygen, hvorefter serumflaskerne blev lukket med teflonbeklædte gummisepta og alumimiumlåg. En serie af serumflasker blev inkuberet i mørke, mens en parallel serie flasker blev inkuberet i konstant lys. Begge serier af testflasker blev inkuberet ved en temperatur på 20 ± 2° C. De lyseksponerede serumflasker blev inkuberet med bunden i vejret og med en afstand på 5 cm til lysstofrør (Pope FID 18W/33; i alt 14 stk.), der var monteret med ca. 1,8 cm's mellemrum. Den gennemsnitlige lysintensitet i afstanden 5 cm fra lyskilden blev målt til 458 ± 32 µmol/m2 × s i luft, der omregnes til 342 µmol/m2 × s i vand. Målinger, som VKI har foretaget i Øresund, har vist, at den gennemsnitlige lysintensitet i ca. 1 m's dybde (0,6-1,4 m) var 548 µmol/m2 × s i 1997 og 420 µmol/m2 × s i 1998 (målinger både i 1997 og 1998 blev foretaget i perioden 9. maj til 30. september i døgnets lyse timer).
Tre replikate serumflasker fra bioassays blev høstet efter 0, 1, 2, 4, 7 og 14 dage. Før prøvetagning blev flaskerne rystet, hvorefter de blev placeret i mørke i 20 min. for at bundfælde sedimentet. Den vandige fase fra hver replikat blev forsigtigt overført til centrifugeglas, og supernatanten efter centrifugering (1.500 rpm i 15 min.) blev opbevaret i fryser indtil anvendelsen i test med A. tonsa.
Den akutte toksicitet over for A. tonsa blev undersøgt ved anvendelse af proceduren ISO/FDIS 14669 med den modifikation, at testen blev udført i mørke for at hindre fotolytisk omdannelse af zinkpyrithion. Kontroller i denne undersøgelse omfattede:
- Supernatant (t = 0 d) fra testsystem uden biocid
- Supernatant (t = 0 d) fra testsystem uden biocid, tilsat 50 µL methanol som i test
- Supernatant (t = 0 d) fra testsystem uden biocid, tilsat 50 µL dimethyl sulfoxid som i test
- Supernatant (t = 14 d) fra testsystem uden biocid, inkuberet i mørke som i test
- Supernatant (t = 14 d) fra testsystem uden biocid, eksponeret med lys som i test
- Havvand fra Øresund (sediment SS; jf. bilag 2) opsaltet til 3,2%
- Havvand fra Kattegat opsaltet til 3,2%
Yderligere oplysninger om toksicitetstesten med A. tonsa er angivet i rapporten "Ecotoxicological tests of leachates of antifouling paints" (Bjørnestad et al. 1999).
Effekten af doseringen med biocider på antallet af bakterier i testsystemet blev bestemt som kimtal (jf. bilag 2). Antallet af kim i en ubehandlet kontrolprøve var 9,1 × 105 pr. mL efter 1 dags inkubering, mens de tilsvarende antal var 1,5 × 105 og 1,4 × 105 pr. mL i prøver doseret med hhv. DCOI og zinkpyrithion.
Bilag 4. Økotoksikologiske data vedrørende DCOI
Tabel B4.1 Se her
Økotoksikologiske data vedrørende DCOI.
Ecotoxicological data regarding DCO1.
Bilag 5. Økotoksikologiske data vedrørende zinkpyrithion
Tabel B5.1 Se her
Økotoksikologiske data vedrørende zinkpyrithion.
Ecotoxicological data regarding zinc pyrithione