|
AOX udredning, litteraturstudium 6. Dannelse af halogenerede forbindelser ved chlorering
6.1 ChloreringsprocessenUnder anvendelse af chlorgas eller hypochlorit, som er standard for desinfektion i svřmmebade (afsnit 4), virker chlor som et kraftigt oxidationsmiddel, under alle omstćndigheder via hypochlorit efter [27]: Cl2 + H2O ® HOCl + H+ + Cl- I naturlige vandtyper findes i reglen et lavt indhold af bromid, hvorved ogsĺ dannes hypobromit: HOCl + Br- ® HOBr + Cl- Begge stoffer kan oxidere organisk stof, idet der samtidig indfřres chlor- eller bromatomer i de organiske molekyler [28,29] (figur 6.1.1).
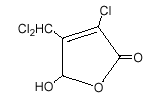
Figur 6.1.1 Phenoler, som de viste, ligner strukturmćssigt de humusstoffer, som er en del af det naturlige organiske stof i vand. Som det ses, dannes ved chloreringen en blanding af en rćkke chlororganiske stoffer, foruden chlorid, vand og kuldioxid, ligesom der kan dannes bromerede organiske stoffer. Det er chloreringsbetingelserne, der primćrt bestemmer, hvor langt reaktionen forlřber, og hvilke stoffer der dannes. Kun en mindre mćngde af den tilsatte mćngde chlor ender som organisk bundet chlor, mens det meste bliver reduceret til chlorid [30]. Undersřgelser af vand fra et fransk drikkevandsbehandlingsanlćg viste, at det organiske chlor for denne vandtype ikke sad i den aromatiske struktur, men snarere i alifatiske forbindelser eller alkylkćder af mere komplekse forbindelser [31]. De to almindelige oxidationsmidler chlor og chloramin har forskellige mekanismer [30], idet chlor kan oxidere organiske forbindelser og bindes i de organiske molekyler, men ogsĺ ende som uorganisk chlorid (se ovenfor), mens chlor fra chloramin altid vil ende i de organiske molekyler. 6.2 Eksempler pĺ organiske stoffer dannet ved chloreringsprocessenUndersřgelser af dannelse af disinfection by-products, DBP, i svřmmebade ved pilotforsřg [32] har vist, at de to vćsentligste parametre for dannelse af trihalomethaner, THM, og chloraminer er antal personer, der har badet, samt dosis af chlordesinfektionsmiddel tilsat. Desuden viste massebalancestudier, at en stor del (40-60%) af det organiske stof og chlor, som blev tilsat, ikke kunne findes som eksempelvis THM, men formodentlig fandtes som chlorerede syrer af forskellig art i vandet. I en Japansk undersřgelse [33] af svřmmebassinvand fra 30 svřmmehaller og 16 friluftsbade blev TOX og indholdet af trihalomethaner, THM, bestemt (Tabel 6.2.1). Tabel 6.2.1
Yderligere information om sammensćtning og styrende faktorer for dannelse af DBP ved chlorering kan findes i undersřgelser med relation til drikkevand. I Standard Methods findes et afsnit om halogenerede forbindelser: 5710 Formation of Trihalomethanes and Other Disinfection By-Products [34]. Her anfřres, at fřlgende forbindelser kan dannes ved chloring: trihalomethaner, halogenerede eddikesyrer og halogenerede nitriller ved reaktion med naturligt forekommende stoffer som humussyrer og fulvussyrer. Det anfřres, at det naturlige indhold af bromid i vandet vil fřre til dannelse af bromerede forbindelser. Med et forhold mellem chorid:bromid pĺ 40:1 vil der dannes lige store molćre mćngder af organisk chlor og brom. Er der mindre mćngder bromid tilstede, vil der i forbindelser med mere end et halogenatom vćre mulighed for alle tćnkelige kombinationer af chlor og brom, eksempelvis trihalomethanerne: chloroform (CHCl3), dichlorbrommethan (CHCl2Br), chlordibrommethan (CHClBr2) og bromoform (CHBr3). I Standard Methods 5710 anfřres det, at koncentrationen af halogenerede forbindelser generelt stiger med reaktionstiden, men der er undtagelser: hvis pH er hřj vil der ikke dannes trichloreddikesyre, ligesom di-halo-eddikesyre hurtigt nĺr et maksimum og derefter begynder at hydrolysere. Nogle forbindelser, som bromerede eddikesyrer, er ustabile og vil nedbrydes ved opbevaring. Standard Methods 5710 anfřrer de mest almindelige desinfektionsbiprodukter som vist i tabel 6.2.2. Tabel 6.2.2
Figur 6.2.1 Standard Methods 5710 anfřrer tillige metoder til bestemmelse af Disinfection By-Products Formation Potential og Trihalomethane Formation Potential, hvor vandprřver behandles under specificerede betingelser i en specificeret periode med en kendt mćngde chlor, og de dannede produkter derefter bestemmes. I en undersřgelse af dannelse af DBP blev 33 specifikke forbindelser dćkkende 4 trihaloemethaner, THM, 9 halogenerede eddikesyrer, HAA’s, 4 halogenerede acetonitriller, 2 haloketoner, chloropicrin,13 aldehyder og bromate bestemt sammen med sumparametrene TOX, TOCl og TOBr [37]. Undersřgelsen blev gennemfřrt pĺ ultrarent vand tilsat fulvussyrer til 3 mg/L TOC, med og uden indhold af bromid i 0,1 mg/L, samt med fire almindeligt anvendte desinfektionsmidler: chloramin, chlordioxid, chlor og ozone. Indholdet af TOX var střrst efter behandling med chlor (tabel 6.2.3). Derudover viser tabellen, at kun 50% af TOX blev identificeret ved chlorbehandling og endnu mindre for de řvrige desinfektionsmidler. Tabel 6.2.3
THAA, total halogeneret eddikesyre, TTHM, total trihalomethan, identificeret som % af TOX vist. Information om dannelse af chlorerede organiske forbindelser kan endvidere fĺs i litteraturen om stoffer dannet ved chlorering af trćmasse i celluloseindustrien. I et review over en rćkke gennemfřrte undersřgelser vedrřrende chlorblegning af papirmasse med chlor [38] findes en gennemgang af de pĺviste chlorerede forbindelser. Der skelnes traditionelt i denne type af undersřgelser imellem AOX, der bestemmes i et vandigt ekstrakt, EOX, der bestemmes efter ekstraktion med et oplřsningsmiddel, og endelig ikke-ekstraherbare organiske forbindelser. Afhćngigt af trćtypen udgjorde den udvaskelige del, AOX, mindre end 10% og den ekstraherbare del, EOX, ca. 50% af total organisk chlor. Mere end 80% af EOX var lipofilt og havde en log POW, som var střrre end 4, hvilket angiver, at der var tale om bioakkumulerbare forbindelser. Endvidere var der en del af EOX med log POW střrre end 6,2. Strukturundersřgelser med NMR-teknik viste, at der var et meget lavt indhold af aromatiske forbindelser i de undersřgte ekstrakter. Der blev identificeret linolsyre med op til 4 chloratomer. Chlorering af vand med indhold af organisk stof anvendes desuden udbredt for udlřb fra renseanlćg [39], isćr hvor vandet skal anvendes til kunstvanding af markafgrřder eller til f.eks. infiltration med henblik pĺ grundvandsdannelse. I chloreret spildevand blev identificeret nogle af indholdsstofferne [39]: chlorerede alkoholer, ketoner og syrer, mens der ved chlorering af overfladevand og modelhumusstoffer mest dannedes THM og halogenerede eddikesyrer, HAA. I behandlet overfladevand fra forskellige lokaliteter i USA blev forholdet mellem TOX og specifikke forbindelser undersřgt [40]. Det viste sig, at forholdet var nćsten konstant, nĺr det beregnedes pĺ basis af vandets indhold af organisk kulstof: 220 µg TOX dannet pr. mg TOC ved chlorering ved pH 7,0 ved et Cl2-C forhold pĺ 4-5 (mg /mg forhold) og en behandlingstid pĺ 72 timer. Endvidere viste det sig, at uafhćngigt af kilden udgjorde CHCl3 omtrent 20% af TOX, trichloreddikesyre 18% og dichloreddikesyre 6 % af TOX, mens trichloracetone og dichloracetonitril udgjorde mindre end 1 %. Tilsammen udgjorde disse forbindelser 44% af det mĺlte TOX, hvilket svarer til resultaterne af tidligere undersřgelser. I de tilfćlde, hvor yderligere forbindelser er identificeret med avancerede analyser, udgjorde den del, som er identificeret hřjst omkring 50 %. Forholdet mellem TOX og THM afhang af den řvrige vandbehandling og lĺ imellem 29% og 44% THM i forhold til TOX. I en anden undersřgelse af behandlet drikkevand fra 10 lokaliteter i USA [41] omfattende flod-, sř- og grundvand bestemtes indhold af trichloreddikesyre, TCA, pĺ 4 – 54 µg/L med en medianvćrdi pĺ 30 µg/L. TOX blev mĺlt til 146 – 566 µg Cl/L med en medianvćrdi pĺ 350 µg Cl/L. TCA-indholdet udgjorde mellem 2 og 10 % af TOX- indholdet, med en medianvćrdi pĺ 6 %. Der kunne etableres en linećr regression mellem TCA- og TOX-koncentrationerne med regressionskoefficient, R = 0,861. I Tama River, der udmunder i Tokyo, er der mĺlt dannelse af THM og TOX pĺ 8 lokaliteter op ad floden [42]. Ved behandling med 10 mg/L chlor i 24 timer var dannelses potentialerne henholdsvis 22 – 64 for THM og 112-200 µg/L for TOX. I Galilća sřen i Israel, der har hřjt indhold af bromid (1,9 mg/l), pĺvistes bromerede organiske forbindelser ved chlorering [28]. 3 bromerede haloeddikesyrer blev pĺvist i hřje koncentrationer. THM og haloeddikesyrer udgjorde 75 % af TOX, og over 85 % af TOX var bromerede forbindelser. Tribromeddikesyre kunne omdannes til bromoform, ligesom det ses for dannelsen af chloroform fra trichloreddikesyre. I atomkraftvćrker i USA, der ligeledes benytter chlorering til deres křlevand [43], er der identificeret THM, chlor- og bromphenoler og TOX (alternativ, nu forćldet, metode med adsorption pĺ XAD i stedet for pĺ aktivt kul). I chloreret křlevand fra flodvand eller havvand identificeredes 21 chlor- og bromphenoler med indtil 3 halogenatomer, samt 2 nitro- og 1 ethoxybromphenol. Totalindholdet at chlorphenoler var ca. 1 µg/L, af THM 0,5-2,8 µg/L og af TOX 2-4 µg/L. Den vćsentligste forskel pĺ havvand og ferskvand var, at der isćr var bromerede forbindelser i havvand, formodentlig pĺ grund af det hřjere indhold af uorganisk brom i havvand. 6.3 Styrende faktorer for dannelse af halogenerede organiske stoffer ved chloreringI en gennemgang af forskellige desinfektionsmidlers effektivitet og DBP-dannelse konstateredes, at dannelsen af flygtige THM og af ikke-flygtigt TOX, NPTOX, giver en fordeling med 1,5 – 11 gange mere NPTOX end THM [30]. I artiklen fremhćves, at den traditionelle regulering af chlordesinfektionsprocessen for drikkevand ved hjćlp af THM-indholdet ikke er hensigtsmćssig, fordi THM kun udgřr en mindre del af de chlorerede organiske forbindelser, som řnskes undgĺet. Eksempelvis danner chloraminer mindre THM, men ikke mindre TOX. Til gengćld er chloraminer mindre effektive til desinfektion. Dette perspektiveres af, at forfatteren anser NPTOX for at vćre den mest betćnkelige del af DBP pĺgrund af hřj carcinogen effekt (sammenlign med den kraftige carcinogene effekt af MX, som vil findes i NPTOX-fraktionen), mens den flygtige del af TOX, PTOX, hovedsageligt vil vćre THM. Det bemćrkes tillige, at ved chlorbehandling falder dannelsen af THM moderat med faldende pH, mens dannelsen af TOX stiger voldsomt. Selv om TOX-dannelsen ved chlordesinfektion ikke i sig selv er reguleret, er det altsĺ god praksis at kontrollere TOX-dannelsen ud over THM-dannelsen. I en undersřgelse af chlorering af ikke-nitrificeret spildevand med indhold af ammonium dannedes chloraminer og ikke-flygtigt organisk halogen, mens der i nitrificeret spildevand, uden ammonium, dannedes store mćngder af TOX og THM [39]. Undersřgelserne viste, at ved tilstedevćrelsen af ammonium opnĺedes et gennemsnitligt forhold TOX/DOC pĺ 7,5 µg Cl/mg C og lave indhold af THM og HAA. Ved chlorering af nitrificeret spildevand opnĺedes et gennemsnitligt forhold TOX/DOC pĺ 49 µg Cl/mg C. Forskellene i dannelse af DPB pĺ de forskellige typer af spildevand skyldes formodentlig, at ammonium i vandet reagerer med tilsat chlor, hvormed chloreringseffekten reduceres [30]. En lavere dannelse af DBP i vand med hřjt indhold af ammonium kan altsĺ vćre samtidig med en lavere desinfektionseffekt. Undersřgelsen af behandlet overfladevand [40] viste, at der var en god relation mellem bĺde potentialet for dannelsen af THM (THMFP) og for dannelsen af TOX (TOXFP) og vandets indhold af organisk stof bestemt som TOC eller som UV-absorption ved 254 nm pĺ en sur prřve. Eksempelvis var korrelationen mellem TOXFP og TOC bestemt pĺ 59 prřver: TOXFP [µg Cl/L] = 152 (+13,8) TOC [mg C/l] + 222(+ 217), R = 0,825, Et indhold af TOC pĺ 10 mg C/L forudsiges at kunne fřre til et indhold af TOX pĺ 1742+355 µg Cl/L. Korrelationen mellem THMFP og TOC bestemt pĺ 59 prřver var: THMFP [µg /L] = 54 (+4,8) TOC [mg C/l] + 46,6(+ 76,5), R = 0,828, Et indhold af TOC pĺ 10 mg C/L forudsiges at kunne fřre til et indhold af THM pĺ 587+125 µg/L. Tilsvarende er effekten af procesfaktorer som organisk stof indhold i vandet (TOC), det organiske stofs sammensćtning (karakteriseret ved absorption af ultraviolet lys, UV, ved 254 nm), pH, chlordosis, temperatur og tid beskrevet i sćt af ligninger for forskellige DBP [44]. Det skal bemćrkes, at denne type generaliseringer skal anvendes med varsomhed, idet betingelser, der ligger uden for det datasćt anvendt i opstillingen af ligningerne, kan gřre ligningerne upĺlidelige. Et eksempel pĺ ligning for dannelse af chloroform (CHCl3) og trichloreddikesyre (TCAA) er vist nedenfor: CHCl3 (µg/L) = 0,278*(TOC*UV-254)0,616*(Cl2)0,391*(T)1,15*(t)0,265*(pH-2,6)0,8*(Br + 1)-2,23 TCAA (µg/L) = 87,182*(TOC)0,355*(UV-254)0,901*(Cl2)0,881*(t)0,264*(pH)-1,732*(Br + 1)-0,679 Ligningerne beskriver, at bĺde chloroformdannelse og dannelse af trichloreddikesyre stiger med stigende indhold af organisk stof i rĺvandet, med chlordosis, med reaktions-tid og med temperaturen (indgĺr kun for chloroform). Chloroformdannelsen stiger med pH, mens TCAA-dannelsen falder med pH. Bromid mindsker dannelsen af de fuldt chlorerede DBP, fordi der i stedet dannes de analoge bromerede stoffer. Den parameter, som primćrt er variabel med henblik pĺ nedbringelse af dannelsen af DBP, er altsĺ mćngde og art af det organiske stof. Chlordosis kan ikke nedbringes under den effektive vćrdi, pH og temperatur kan ikke justeres uden gener for brugerne, og reaktionstid kan kun nedbringes ved at řge dimensionerne i behandlingsanlćgget. I undersřgelsen af behandlet overfladevand [40] sĺs det, at traditionel vandbehandling med flokkulering og bundfćldning reducerede TOC og dermed THMFP og TOXFP med 50 %. I drikkevandsbehandlingsanlćg i Frankrig [31] er undersřgt fordelingen pĺ forskellige molekylfraktioner med gelfiltrering, gel permeation kromatografi, GPC, fřr og efter chlorering (tabel 6.3.1). Tabel 6.3.1
Tabel 6.3.2
Hovedfraktionen af TOX var lavmolekylćre forbindelser (tabel 6.3.1), MW < 1000, hvor de fleste af disse forbindelser kunne ikke analyseres ved almindelig GC og kunne ikke ekstraheres med konventionelle teknikker [31], hvilket er typisk for polćre forbindelser. Dette forklarer, hvorfor det normalt ikke er muligt at redegřre for al TOX ved specifikke analyser. Chlorering af 22 forskellige aminosyrer og nogle veldefinerede oligo- og polypeptider (proteiner) har vist [31,45], at frie aminosyrer og proteiner krćvede hřj chlordosis, hvor chlor behovet varierede fra 2,5 – 16 mol Cl2/mol stof. De frie aminosyrer viste sig at have lavt THMFP, men et hřjt TOXFP. Forfatteren anfřrer, at da aminosyrekoncentrationen i drikkevand kan variere fra fĺ nanomol til adskillige hundrede nanomol pr. liter, mĺ det forventes, at disse forbindelser udgřr en betydelig del af chlorbehovet i forbindelse med behandling af drikkevand. Til nćrmere at anslĺ TOX-dannelsespotentialet af det organiske stof i vand er foreslĺet UV-spektrofotometri [46], idet der mĺles pĺ det fald i UV-absorbans af naturlige organiske forbindelser (NOM), der sker ved chlorering. Faldet i UV-absorbans afbildet imod břlgelćngden kaldes et differential UV-spektrum. Mens konventionelle UV-spektre af NOM stort set kun viser en jćvnt faldende kurve uden megen reel information, viser differential UV-spektre af NOM et bemćrkelsesvćrdigt billede typisk for en bred vifte af vandtyper og chloreringsbetingelser med et maksimum ved 272 nm. Střrrelsen af faldet i absorbans er en indikator for potentialet for TOX-dannelse ved chloreringen, idet UV-mĺlingen reelt foretages pĺ den del af molekylet, der ogsĺ reagerer med chlor. Fordi den indledende reaktion mellem chlor og NOM medfřrer, at hovedparten af den tilfřrte chlor bliver inkorporeret i det organiske molekyle, giver viden om graden af tidligere chlorering mĺlt ved differential UV-spektrofotometri mulighed for at forudsige potentialet for fortsat DPB-dannelse, for eksempel i vand under konstant chlorering i et svřmmebad. Dette understřttes af den registrerede stigning i dannelse af TOX og THM i japanske svřmmebade efter vandudskiftning og dermed tilfřrsel af frisk organisk stof (se tidligere i dette afsnit). Sammenfattende kan siges om de forbindelser, der dannes ved chlorering af vand, samt om processerne, at
|