Kortlægning og miljø- og sundhedsmæssig vurdering af fluorforbindelser i imprægnerede produkter og imprægneringsmidler
10 Dyreforsøg og in vitro tests
- 10.1 Toxicokinetic og metabolisme
- 10.2 Toksikologi
- 10.2.1 Akut toksicitet
- 10.2.2 Påvirkninger på leveren
- 10.2.3 Toksikologisk mekanisme
- 10.2.4 Toxicogenomic
- 10.2.5 Påvirkninger på cellemembraner
- 10.2.6 Påvirkning af energiproduktionen i mitochondrier
- 10.2.7 Påvirkning af intercellulær kommunikation
- 10.2.8 Påvirkning af fosterudvikling mv.
- 10.2.9 Hormonforstyrrelser
- 10.2.10 Mutagenitet
- 10.2.11 Cancer
- 10.2.12 Cocktail-effekter
- 10.3 Struktur-aktivitetsrelationer
10.1 Toxicokinetic og metabolisme
10.1.1 Optagelse
PFOS og PFOA (som ammoniumsalt) optages let og hurtigt i rotters mavetarmkanal og lunger, og toksiske koncentrationer af PFOA optages gennem kaniners hud (Lau et al., 2004; Kennedy et al., 2004; Hinderliter et al., 2006). Ca. 93% af en oral dosis af PFOA givet til rotter, blev absorberet, og de højeste blodniveauer blev nået 1-2 timer efter dosering (Hundley et al. 2006). Også en oral dosis af 8:2 FTOH absorberes let i rotter, men hudsabsorberingen var ubetydelig. Den maksimale koncentration i blodet forekom 1 time efter oraldosering, og den aftog hurtigt med en halveringstid på mindre end 5 timer (Fasano et al., 2006).
10.1.2 Bioomdannelse
PFOA og PFOS betragtes begge som værende metabolisk inaktive (Clark et al., 1973). Andre perfluoralkylsyrer med kortere eller længere alkylkæde har lignende egenskaber. Deres forstadier og funktionelle derivativer vil slutteligt blive omdannet til deres basissyrer. For eksempel omdannes 8:2 fluortelomeralkoholen og dens phosphater let til PFOA, PFNA og andre stofskifteprodukter i mus og rotter (Hagen et al., 1981; Kudo et al., 2005; Fasano et al., 2006; Henderson og Smith, 2007; D’Eon og Mabury, 2007). Omdannelsen i rotteleverceller katalyseres af cytochrom P-450 enzymsystemer (Martin et al., 2005).
Omkring 20% af en oraldosis på100 ppm EtFOSE omdannes i hanrotter til PFOS (Thomford et al., 2002). Rottelevers microsomale fraktion nedbryder også EtFOSE via de-alkylering til PFOSE og videre til PFOSA og sluttelig til PFOS (Xu et al., 2004).
10.1.3 Akkumulering
PFOA og PFOS binder til proteiner og akkumulerer – mere eller mindre afhængig af dyrearter og køn – i forskellige kropsvæv, hovedsagelig i blod, lever og nyrer i udsatte dyr (i alt 88% i hanrotter), men også i lunger, hjerte, hud, testikler (3% i hanrotter) og hjerne (Vanden Heuvel et al., 1992; Austin et al., 2003; Hundley et al., 2006). Akkumuleringen i fedtvæv og muskler er minimal.
Kudo og medarbejdere (2001) undersøgte PFCA’er med forskellig kædelængde (C7 - C10) i hanrottelever. Resultatet viste, at jo længere en kæde, desto mere af forbindelsen blev akkumuleret i leveren.
10.1.4 Eliminering
Er PFOA en gang absorberet i kroppen, elimineres PFOA som den frie carboxylsyre hovedsageligt med urinen og i mindre omfang i fæces. Derfor er eliminering via nyrerne kritisk for detoksificering af disse stoffer (Vanden Heuvel et al., 1991).
Den biologiske halveringstid for PFOA i hanrotter efter intravenøs administration var 5,6 dage. Det var 70 gange længere tid end den tilsvarende halveringstid i hunrotter, som var 2 timer. Forskellen skyldes hovedsageligt forskellen i nyreudskillelsen, som blev markant reduceret af probenezid, hvad der tyder på, at PFOA udskilles af organiske anionbærere. Kastrering af hanrotter forårsagede en stigning på 14 gange i nyreudskillelsen, så den blev sammenlignelig med hunrotter. Stigningen blev reduceret igen ved behandling med testosteron. Behandling med estradiol øgede også nyreudskillelsen, og i hunrotter fik fjernelse af æggestokke nyreklaringen til at stige (Kudo et al., 2002). Elimineringen af PFOA øges med alderen i hunrotter, men ikke i hanrotter (Hinderliter et al., 2006).
Perfluorcarboxylsyrer (PFCA) med en kortere kulstofkædelængde end PFOA elimineres hurtigere i urinen. Rækkefølgen var PFHpA (0,10/0,05 dage) > PFOA (5,6/0,08 dage) > PFNA (30/2,4 dage) > PFDA (40/59 dage) for han/hunrotter (Kudo et al., 2001; Ohmori et al., 2003). Kønsforskelle i udskillelsen var mest markant for PFOA.
Den kønsrelaterede eliminering af PFOA varierer mellem dyrearter (Hundley et al., 2006). I hamstre er det modsat, hvad det er i rotter. Han- og hunhamstre udskiller henholdsvis 99% og 58% af en dosis på 5 dage. I mus og kaniner var der ingen forskel for kønnene, og mus havde en langsom udskillelse som hanrotter, og kaniner havde en hurtig udskillelse som hunrotter. I hunde var plasmahalveringstiden af PFOA ca. 20 dage i hanhunde og det halve i hunhunde.
The elimination halveringstider i han- og hun Cynomolgus aber for PFOA var henholdsvis 33 dage og 21 dage, og urinen var den vigtigste udskilningsrute (Butenhoff et al., 2004a). PFOS har en langsommere udskillelseshastighed, og halveringstiden af PFOS i Cynomolgus aben var ca. 200 dage (Seacat et al., 2002a; Andersen et al., 2006).
Efter en oraldosering af 8:2 FTOH blev hovedparten af det 14C-mærkede stof udskilt med fæces, og 37-55% forekom som 8:2 FTOH. En mindre del (1%) blev udskilt som PFOA i urinen (Fasano et al., 2006).
10.2 Toksikologi
10.2.1 Akut toksicitet
Den akutte dødelige toksicitet er moderat svarende til en klassificering som sundhedsskadelig. PFOS er mere toksisk end PFOA. Oral rotte LD50 for PFOS er 250 mg/kg lgv (3M, 1999), og for PFOA er oral rotte LD50 mellem 430 og 1800 mg/kg (Kennedy et al., 2004). For PFOA og PFDA er LD50 for rotter udsat intraperitonealt henholdsvis 189 og 41 mg/kg. Således er PFDA meget mere toksisk og har senvirkninger (Olson og Anderson, 1983). Generelt stiger toksiciteten af de testede perfluorkemikalier med længden af alkylkæden.
10.2.2 Påvirkninger på leveren
Toksikologiske undersøgelser har vist, at leveren er det primære målorgan for POFS og PFOA, og kropsvægttab, forøget levervægt, levercellehypertrofi og ændret fedtstofskifte med reduktion i serum-cholesterol er tidlige udtryk i forsøgsdyr (Kennedy et al. 2004; Seacat et al. 2003).
Det ikke-observerede uønskede bivirkningsniveau (NOAEL) for leverpåvirkninger i hanrotter, der blev eksponeret for PFOS i føden i 14 uger, var 5 mg/kg/dag (Seacat et al., 2003). NOAEL og LOAEL for leverpåvirkninger af PFOA i hanrotter, der blev udsat via foderet i 13 uger, var henholdsvis 0,06 og 0,64 mg/kg/d (Perkins et al., 2004). En anden gentagen-dosis undersøgelse bestemte en LOAEL på 0,3-1 mg/kg for PFOA i hanrotter, og forgrenede isomere af PFOA havde lavere toksicitet end linære isomere (Loveless et al., 2006).
PFDA, der har en længere kæde end PFOA, var mere toksisk i rotter, hamster, mus og marsvin (van Rafelgheim et al., 1987; Kawashima et al., 1995). Rotter ser ud til at tolerere noget højere leverkoncentrationer af PFOS end aber, fordi NOAEL i en 6 måneder lang abeundersøgelse var 0,15 mg/kg/d (Seacat et al., 2002a). PFOA med en LOAEL på 3 til 10 mg/kg/d er markant mindre levertoksisk i aber end PFOS, og angrebspunktet er forskelligt (Butenhoff, 2002a). Den eneste effekt i aben ved de anførte doser var leverforstørrelse.
10.2.3 Toksikologisk mekanisme
PFOA og PFOS fremkalder hepatomegaly, som er karakteriseret ved en subcellulær proliferation af cellebestanddele som fx ”smooth endoplasmic reticulum”, mitochondrier, men mest udpræget peroxisomer. De observerede ændringer i leveren kunne være resultatet af processen: ”peroxisom proliferation”, en velkendt toksikologisk mekanisme i gnavere. Den kan forårsage fedtlever, blokering af energiproduktionen (oxidative phosphorylation) i mitochondrier, og reduktion af cirkulerende skjoldbruskkirtlens hormoner. Induktion af ”peroxisom proliferation” og forekomst af godartede levertumorer er forbundet med aktivering af hormon receptoren: Peroxisome proliferator-activated receptor-a (PPARa). Dette er en af de tre isoformer af PPAR, som koder med separate gener og udtrykkes forskelligt i forskellige væv, og findes i alle pattedyrsarter, der er undersøgt til dags dato. Ligander for PPAR er i stor udstrækning blevet udviklet til behandling af forskellige sygdomme, deriblandt forstyrrelser af fedstofskiftet og sukkersyge. Nogle cholesterol-dæmpende præparater, opløsningsmidler og miljømæssige kemikalier er ligander for PPARa og kan forårsage ”peroxisom proliferation”, for eksempel clofibrate, ftalater, chloroform, perchlorethylen, trichlorethylen, HFC-123 og MTBE. Mennesker udviser ikke samme tegn på leverforgiftninger af disse kemikalier, som er fundet i gnavermodeller (Peraza et al., 2006).
Denne PPAR-receptor er højst sandsynligt endemålet for PFOA og PFOS i både gnavere og mennesker (Vanden Heuvel et al., 2006). Polyfluorsyrer er analoge ligander til naturlige langkædede fedtsyrer og kan fortrænge dem i biokemiske processer og i receptorer som f.eks. PPARa. Aktiveringen via PFOA og PFOS er mere selektiv men mindre kraftig. PFOA er mere egnet end PFOS ved aktiveringen af PPARa, og mus er mere modtagelige end mennesker (Takacs og Abbott, 2007).
PFOA nedsætter immunsystemets effektivitet gennem tilførsel af PPAR og forstærker den IgE-formidlede overfølsomhedsreaktion på ovalbumin, og på denne måde kan det provokere astma (Fairley et al., 2007).
Perfluorcarboxylsyrer (PFCA), især PFOA, PFNA og PFDA, er meget kraftige peroxisome proliferators i gnaverlevere og påvirker mitochondriale, microsomale og cytosoliske enzymer og proteiner, der er involverede i fedtmetabolismen (Ikeda et al., 1985; Vanden Heuvel, 1996; Upham et. al., 1998; Kudo et al., 2000).
PFOS er mindre reaktiv som peroxisome proliferator i gnavere, og EtFOSE har ingen indvirkning (Berthiaume og Wallace, 2002). PFBA har en mindre indvirkning på indikatorer af ”peroxisom proliferation” (Ikeda et al., 1985).
Forskellene mellem dyrearter er store for PFDA. ”Peroxisom proliferation” var størst i mus og næsten fraværende i marsvin. Dog var akkumuleringen af små fedtdråber i leverceller mere udtalte i hamstere og marsvin end i rotter og mus, der blev eksponeret for PFDA (van Rafelgheim et al., 1987).
Stigning i hepatisk fedtsyre b-oxideringsaktivitet (acyl-CoA oxidase) er en biokemisk målestok af ”peroxisom proliferation”. Kudo og medarbejdere (2001) undersøgte PFCAer med forskellig kædelængde (C7 - C10) i mænds lever. Resultatet indikerede, at leverkoncentrationen og ikke kædelængden var afgørende, men jo længere kæde, desto mere af forbindelsen blev akkumuleret i leveren. I mus med mangel på vitamin A havde PFOA en stærkere indvirkning og forårsagede en stigning på 3-6 gange i ß-oxideringen af fedtsyrer (Sohlenius et al., 1995).
I en in vitro test blev forskellige perfluorkemikalier testet for interferens med det leverfedtsyrebindende protein (L-FABP). Det kraftigste kemikalie var PFOS, fulgt af EtFOSA, EtFOSE og PFOA (Luebker et al., 2002). Denne interferens kan bidrage til toksiciteten af disse kemikalier.
10.2.4 Toxicogenomic
Toxicogenomic analyse er i stand til at forudsige toksicitet og patologiske reaktioner, klassificere kemikalier, og belyse toksicitetsmekanismer. En sådan analyse viste, at PFOA og PFOS havde ”peroxisome proliferator-activated receptor-a (PPARa)” agonist-lignende indvirkninger på gener der koder for enzymer involveret i fedtstofskiftet og fedtsyrebalancen (Shipley et al., 2004; Martin et al., 2007). Det resulterer f.eks. i
- Nedregulering af gener for cholesterol biosyntesen,
hvad der betyder et in vivo fald i serum cholesterol, og - forstyrrelse af gener for metabolisme af skjoldbruskkirtelhormoner,
som betyder en formindskelse af skjoldbruskkirtelhormonniveau i
serum in vivo.
Guruge et al. (2006) brugte en microarray-teknik til at undersøge reguleringen af gener i lever fra hanrotter, der var behandlet med overdoser af PFOA. Over 500 genudtryk blev ændret markant. De fleste kategorier af inducerede opregulerede gener var de, som var involveret i transport og metabolisme af fedtstoffer, især fedtsyrer. Andre inducerede gener var involverede i cellekommunikation, binding, vækst, apoptose, veje for hormonregulering, proteolyse og peptidolyse og signaltransduktion.
I lungen og leveren på PFOA-eksponerede musefostre blev ekspressionen af gener relateret til fedtsyreomsætningen ændret (Rosen et al., 2007). Det var især tydeligt i lever fra foster, og også gener forbundet med fedtstoftransport, ketogenese, glucosemetabolisme, lipoproteinmetabolisme, cholesterol-biosyntese, steroidmetabolisme, galdesyresyntese, phospholipid metabolisme, retinol metabolisme, proteosom aktivering og betændelse. De fleste ændringer var forbundet med PPARa receptoren.
10.2.5 Påvirkninger på cellemembraner
Til trods for dens lipofobiske karakter kan PFOS og i mindre grad PFOA fordele sig i model bi-lag og cellemembraner, hvor det forårsager ændringer i membranstruktur og funktion med øget fluiditet. Interaktion med lungeoverfladestoffer, som f.eks. dipalmitoylphoshatidylcholin (DPPF), kan være en mekanisme, ved hvilken PFOS forårsager perinatal dødelighed i dyrestudier (Xie et al., 2007). Orienteringen af PFAS-molekylerne i membranerne er med den funktionelle gruppe bundet til membranproteiner og med fluorkulstof halen stikkende ud som hår (Roon et al. 2006).
Nogle af de observerede effekter af perfluorforbindelser kan skyldes forandringer i cellemembranens fluiditet, som er en målestok for den relative mobilitet af cellemembranens phospholipid bi-lag. Denne selektivt permeable cellemembran danner den første barriere, som beskytter cellen fra eksogene påvirkninger. Påvirkninger på status af gennemtrængelighed af cellemembranenen kunne spille en vigtig rolle i formidlingen af de uønskede bivirkninger af nogle forureningsstoffer. I nogle in vitro analysesystemer øgede PFOS – men ikke den kortere kæde PFBS og PFHxS – på en doseringsafhængig måde markant membranfluiditeten fra fiskeleukocyter og reducerede mitochondriernes membranpotential bestemt af flowcytometri (Hu et al., 2003).
PFOA, PFOS og EtFOSE forårsagede en lille stigning i mitochondrenes indermembran, svarende til en ændring i membranfluiditeten af et overfladeaktivt stof (Starkov og Wallace, 2002).
10.2.6 Påvirkning af energiproduktionen i mitochondrier
PFOS, PFOA, PFOSA, PFOSAA, EtFOSA, EtFOSE og EtFOSAA havde alle evnen til at forstyrre mitochondrial respiration in vitro. PFOSA var den kraftigste hæmmer af oxidative phosphorylering (Schnellmann og Manning, 1990; Starkov og Wallace, 2002).
I laboratorietests stopper N-acetylperfluoroctansulfonamider (PFOSAA, EtFOSAA) energiomsætningen i mitochondrier ved at forårsage “the mitochondrial permeability transition”. PFOA havde en lille påvirkning, mens PFOS og EtFOSE ingen påvirkning havde (O’Brien og Wallace, 2004).
10.2.7 Påvirkning af intercellulær kommunikation
”Gap junction intercellular communication” (GJIC) er den vigtigste måde, som intracellulære signaler overføres på, og det er således vigtigt for normal cellevækst og cellefunktion. Brist i denne kommunikation kan føre til fosterbeskadigelse, nervesygdom, barnløshed, sukkersyge, autoimmune forstyrrelser, cancer og andre sygdomme (Trosko et al., 1998).
Upham og medarbejdere (1998) viste, at perfluorcarboxylsyrer med kulstofskædelængde på 7-10 hurtigt og reversibelt in vitro kan hæmme ”gap junction intercellular communication” på en dosis-afhængig måde. Den langkædede PFDA hæmmer kraftigere end PFOA.
I forskellige testsystemer (in vitro og in vivo) hæmmer både PFOS, PFOSA, og PFHxS – men ikke PFBS - ”gap junction intercellular communication” dosis-afhængigt, og denne hæmning indtraf hurtigt og var reversibel (Hu et al., 2002).
Cellepåvirkninger, som f.eks. cellemembranskrøbelighed og ”gap junction communication”, er to af de hypotetiske forklaringer på påvirkninger af disse fluorforbindelser.
10.2.8 Påvirkning af fosterudvikling mv.
PFOA og PFOS kan krydse moderkagebarrieren i gnavere og kan konstateres i moderkage, fostervand og foster. Koncentrationen af PFOA i fosterblodplasma på dag 21 i drægtighedsperioden var ca. halvdelen af koncentrationen i moderdyrets plasma. Overførsel med moderdyrets mælk sker også efter fødslen, men koncentrationen af disse fremmedstoffer i mælk fra gnavere er ca. ti gange lavere end i blod (Hinderliter et al., 2005).
PFOA og PFOS kan påvirke fosterudviklingen i rotter og mus in vivo. PFOS er mere toksisk end PFOA. Disse påvirkninger inkluder reduktion i fostervægt, ganespalte, anasarka, forsinket knogledannelse af skelettet og hjerteabnormiteter, så vel som dalende neonatal overlevelse efter in utero eksponering, gennemsnitligt efterfødselsvægt, ændret mælkekirteludvikling, forkortet svangerskabsperiode, ikke fuldt udviklet lunger med tung vejrtrækning og markant forsinkelse i kønslig modning. De strukturelle abnormiteter blev kun fundet i de højeste dosisgrupper (³ 30 mg/kg/d), hvor de gravide moderdyr havde markante reduktioner i vægtforøgelse og fødeindtagelse samt forøget dødelighed blandt ungerne (Case et al., 2001; Butenhoff et al., 2004b; Kennedy et al., 2004; Grasty et al., 2005; Luebker et al., 2005b; Lau et al., 2003, 2004, 2006; Thibodeaux et al., 2003; White at al., 2007). Samtidig eksponering til PFOS forstærker påvirkningerne (Fuentes et al., 2007).
I et flergenerations undersøgelse af forplantningen i rotter var NOAEL-værdien for PFOS 0,1 mg/kg/d (Luebker et al., 2005a). Ved dette lave moderdosisniveau reducerede the længere kædede forbindelse PFDA dog fødselsvægten markant i mus (Harris og Birnbaum, 1989).
Høje doser af EtFOSE forårsagede reduceret moderlegemsvægt og fostervægt hos gnavere og havde påvirkninger, som var lig med dens metabolit PFOS. Både PFBS og PFHxS er blevet også undersøgt for påvirkninger af udvikling og reproduktion. Eksponering af moderen til PFBS-kaliumsalt gav ikke nogen skadelig påvirkning af fosterudviklingen, og der blev ikke noteret nogen markante ændringer i en flergenerations undersøgelse af rotter ved doser så høje som 1 g/kg. PFHxS er kun undersøgt i et screeningssystem ved lavere doser uden nogen observerede påvirkninger (Lau et al., 2004).
Lignende påvirkninger, som de der blev nævnt for gnavere, kan forekomme i kaniner, der blev eksponeret til PFOS og EtFOSE under svangerskabet. Ikke-effekt niveau (NOAEL) for PFOS i rotter var 0,1 mg/kg/d (Case et al., 2001).
Det er postuleret at, gentagne påvirkninger af lungeoverfladestoffer, som f.eks. dipalmitoylphoshatidylcholin (DPPC), kan være en mekanisme, ved hvilken PFOS forårsager perinatal dødelighed i dyrestudier (Xie et al., 2007).
10.2.9 Hormonforstyrrelser
Polyfluorkemikalier kan optræde som hormonforstyrrende stoffer. Eksponering af voksne rotter til PFOA (25 mg/kg lgv med mavesonde) sænkede testosteronniveauet i testiklerne, forøgede østradiolniveauet i blodserum og formindskede den relative vægt af de accessoriske kønsorganer (Cook et al., 1992; Biegel et al., 1995; Biegel, 1997; Shi et al., 2007). Dette kunne forklares ved PFOA’s induktion af enzymet leveraromatase, som omdanner testosteron til estradiol. Andre undersøgelser viser ikke sådanne påvirkninger, for eksempel i en 6-måneders oralundersøgelse i aber, hvor daglige doser af PFOA op til 20 mg/kg/dag ikke forårsagede ændringer i sexhormonniveauer (Butenhoff, 2002a).
Nogle polyfluorkemikalier har østrogene påvirkninger i cellekulturtestsystemet ”E-screen assay” (Soto et al., 1995). Fluortelomeralkoholer 6:2 FTOH og 8:2 FTOH forårsager for eksempel MCF-7 brystcancercellespredning og opregulerer østrogen receptoren, men PFOS, PFOA og PFNA har ingen østrogenpåvirkning i denne test (Maras et al., 2006; Vanparys et al., 2006).
Påvirkningerne af hormonniveauerne i gnavere afspejles i ændringer i testiklerne, hvor eksponering til perfluoroctanoat resulterer i Leydig celle hyperplasi og til sidst udvikling af Leydig celle kirtelsvulster (Biegel et al., 1995). En undersøgelse af påvirkninger af testiklerne i voksne rotter, der blev eksponeret til perfluordodecansyre (PFDoA) viste også en reduceret genekspression af mange gener, der er involveret i transport af cholesterol og produktion af steroider og dermed et reduceret serumtestosteronniveau (Shi et al., 2007). Det ser således ud, at eksponering til PFAS-stoffer kan påvirke udvikling og funktion af Leydig-celler alvorligt i den voksne rotte. Leydig-celler i testiklerne er hovedstederne for testosteron-biosyntesen.
Dette er ret alvorligt, fordi Leydig celle hyperplasi er almindelig blandt sterile mænd (Holm et al., 2003), der, som gruppe, også viser lavere testosteronniveauer sammenlignet med normale kontrolgrupper (Andersson et al., 2004). Nedsat testikelfunktion er blevet forbundet med ”testicular dysgenesis syndrom (TDS)” (Skakkebaek et al., 2001). TDS-hypotesen angiver, at in utero eksponering for hormonforstyrrende stoffer kan ødelægge testikeludviklingen og føre til reduceret testikelfunktion hos den voksne, med symptomer rangerende fra en moderat reduceret sædkvalitet til testikelcancer. Den bedste dyremodel for TDS består af rotter, der blev eksponeret for langkædede ftalater i en kritisk tidsperiode under udviklingen, hvilket resulterer i testis dysgenese med Leydig celle hyperplasi og gruppering af Leydig cellerne i centrum af testiklerne, hvilket resulterer i reducerede testosteronniveauer og nedsat frugtbarhed hos voksne (Sharpe, 2006; Hallmark et al., 2007).
Den nedsatte Leydig cellefunktion afspejler sig i en reduceret ekspression af gener, der er involveret i transport af cholesterol og steroidogenesis (Liu et al., 2005). Dette har slående ligheder til den rapporterede påvirkning af PFAS-eksponering; det ser dog ud, som om PFAS-forbindelser, i modsætning til ftalater, kan forårsage påvirkningerne hos den voksne.
PFOS påvirkede neuroendocrinsystemet i rotter, når hanrotter blev injiceret intraperitonealt med 0, 1 og 10 mg PFOS/kg lgv i to uger (Austin et al., 2003). Parringslysten blev påvirket, serum corticosteron niveauet blev forøget, og serumleptinkoncentrationen og norepinephrinkoncentrationen i hypothalamus blev formindsket.
10.2.10 Mutagenitet
PFOA var ikke-mutagen i Ames testen med fem stammer af Salmonella typhimurium og en enkel stamme af Saccharomyces cerevisiae (Griffith og Long, 1980). Adskillige andre mutagenitetsundersøgelser af PFOA, offentliggjort af kontraktlaboratorier, understøtter inaktiviteten af PFOA (Kennedy et al., 2004). PFDA er også negativ i Ames testen og adskillige andre testsystemer. PFDA var dog aktiv i et chromosomafvigelsestest ved tilstedeværelse af S-9 mix og i et S-fase DNA syntesetest (Godin et al., 1992).
Polyfluorkemikalier kan alligevel forøge den genotoksiske effekt af andre kemikalier, da PFOS øger gentoksiciteten af cyclophosphamid i micronucleus-testen (Jernbro et al., 2007). Se Figur 10.1:
Figur 10.1: Gentoksicitet af cyclophosphamid (CPP) + PFOS i micronucleus-testen (Efter Jernbro et al., 2007)
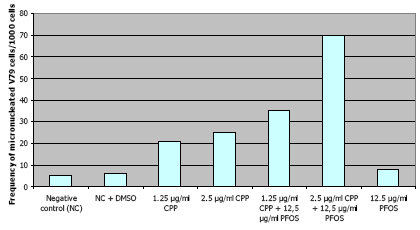
Ingen testresultater til belysning af en eventuel genotoksisk effekt af andre polyfluorerede kemikalier blev fundet i den tilgængelige litteratur.
10.2.11 Cancer
I dyreundersøgelser med CD-rotter, en stamme som har en lav spontan forekomst af disse svulster, fremkaldte PFOA en dosis-afhængig stigning i Leydig celle adenomer (Biegel et al., 1995; Liu et al., 1996). Svulsterne kan være et resultat af hormonændringer, fordi en reduceret aromatase aktivitet og en langvarig stigning i serumøstradiol blev observeret (Biegel et al., 2001). Ikke desto mindre klassificerer USA's Miljøstyrelse PFOA som et kræftfremkaldende stof i dyr (US EPA 2002).
Et færdiggjort to-årigt rottefodringsforsøg med PFOS er kun blevet rapporteret kort (Seacat et al., 2002b). En beskeden leversvulstreaktion blev observeret i højdoseringsgruppen på 20 ppm PFOS anvendt som kaliumsalt.
En dosis i foderet på 100 ppm EtFOSE forårsagede en stigning af levercelle adenomer i hunrotter og skjoldbruskkirtel adenomer i hanrotter (Thomford et al., 2002). Man regner med at omkring 20% af en oraldosis af EtFOSE metaboliseres til PFOS.
10.2.12 Cocktail-effekter
Da eksponering til polyfluorforbindelser er allestedsnærværende for mennesker, tilføjes denne eksponering til alle andre eksponeringer, som mennesker kan opleve. Dette rejser spørgsmålet om mulige blandingseffekter, om perfluorforbindelserne kan forøge skaderne fra andre eksponeringer.
Blandingseffekter er allerede påvist in vitro og in vivo for østrogene forbindelser (Silva et al., 2002; Tinwell og Ashby, 2004) og for anti-androgener (Birkhoj et al., 2004; Metzdorff et al., 2007), men der er meget få undersøgelser af blandingseffekter af forbindelser med forskellige effektudtryk.
For polyfluorstoffer er der flere rapporter om samvirkninger. Kudo og Kawashima (1997) fandt, at fiskeolie i foderet hindrer PFOA i at fremkalde fedtlever i mus. Co-administration af PFOS og dioxin (TCDD) resulterede f. eks. i en øget cytochrom P450 A1A-ekspression i sammenligning med TCDD alene (Hu et al., 2003).
Det blev ovenfor vist, at gentoksiciteten af cyclophosphamid i micronucleustesten med hamsterlunge V79-celler steg mange gange ved samtidig eksponering for PFOS (Jernbro et al., 2007). Derfor kan polyfluorerede kemikalier potentielt øge den kræftfremkaldende effekt af andre kemikalier.
10.3 Struktur-aktivitetsrelationer
De fleste toksikologiske oplysninger er om PFOS og PFOA, hvorimod viden om andre polyfluorkemikalier er sparsom. Kvalitativt ved vi, at PFOS og PFOS-derivater ser ud til at være mere toksiske end PFOA og derivativer. Yderligere stiger persistensen og toksiciteten af perfluorsyrer generelt med kædelængden, og stoffer med forgrenet kæde er mindre toksiske end linære stoffer. For tiden ser der ud til at være utilstrækkelige baggrundsdata til at foretage forudsigelser på baggrund af kvantitative struktur-aktivitets sammenhænge (QSAR) for disse stoffer, men det kan måske blive muligt på et senere tidspunkt.
Det er endnu sværere at lave teoretiske forudsigelser for egenskaberne af de mere komplekse telomere og andre komplekse polyfluorforbindelser, der anvendes i forbrugerprodukter. De tilhører forskellige kemiske klasser og kan i sidste ende nedbrydes eller metaboliseres til perfluorerede syrer. Kvalitativt vil det være muligt med nogen sikkerhed at forudsige hvilken perfluorsyre, som den kemiske forbindelse er forstadie til, og OECD har lavet et forsøg i deres liste over stoffer (Kapitel 1.1.4) for at indikere mulige længder (eller omfang af længder) af den fluorerede kulstofskæde, der kan opstå som et resultat af nedbrydningen.
Version 1.0 Oktober 2008, © Miljøstyrelsen.