Livscyklusvurdering af 3 typer metalmaling
12. Detaljeret livscyklusvurdering af TGIC-hærder og b-Hydroxyalkylamid
12.1 TGIC
12.1.1 Fremstilling af TGIC
12.1.2 Miljøpåvirkninger ved fremstilling af TGIC
12.2-Hydroxyalkylamid
12.2.1 Fremstilling af b-hydroxyalkylamid
12.2.2 Miljøpåvirkninger ved fremstilling af b-Hydroxyalkylamid
12.3 Miljøvurdering
12.3.1 Ressourceforbrug
12.3.2 Ydre miljø
12.3.3 Arbejdsmiljø
12.3.4 Samlet konklusion vedrørende valg af hærder
12.3.5 Følsomhedsvurdering
Stoffet "triglycidyl isocyranurat" (TGIC) er almindeligt anvendt som hærder ved fremstillingen af pulvermaling, men har vist sig at medføre en række arbejdsmiljøproblemer der på det seneste har medført en omklassificering efter EUs mærkningsregler således, at produktet fra 31 maj 1998 skal klassificeres som T- mærket . TGIC er rimeligt godt undersøgt og der ligger en række data og undersøgelser vedrørende arbejdsmiljøeffekter og ydre miljø effekter til brug for livscyklusvurderingen.
b-hydroxyalkylamid er et muligt alternativ til TGIC der tilsyneladende ikke medfører de samme miljø- og arbejdsmiljøproblemer.
Det er disse 2 stoffer der sammenlignes i det følgende
12.1 TGIC
Der er ikke fundet nogen "færdige" livscyklusvurderinger for TGIC, og det har derfor været nødvendigt at foretage en mere detaljeret vurdering af de enkelte procestrin som vist i det følgende.
12.1.1 Fremstilling af TGIC
TGIC produceres af CIBA-GEIGY Aktiengesellschaft Basel / Switzerland. Fremstillingen omfatter de trin der vist i figur 12.1 nedenfor.
Figur 12.1 viser samtidig hvilke mængder af de forskellige råvarer der skal anvendes for at fremstille 1000 kg TGIC. Disse mængder er beregnet støkiometrisk i bilag 1.1 ud fra reaktionsligningerne som er beskrevet i det følgende.
Ammoniak NH3
Fig. 12.1 Procestræ for fremstilling af TGIC /14/, /15/ Se her
Ammoniak fremstilles normalt ud fra nitrogen og brint. Nitrogen findes i luft og brint fås ved reformering af naturgas /15/.
Den resulterende kemiske reaktion for ammoniaksyntesen er:
(12.1) N2 + 3 H2 « 2 NH3
Fremstillingen sker via 8 enhedsoperationer som vist i figur 12.2.
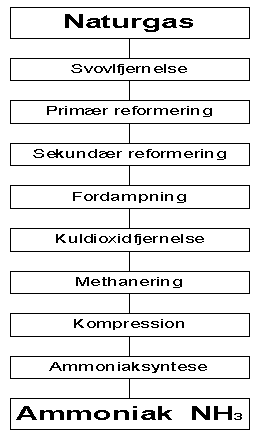
Fig. 12.2 Ammoniaksyntese baseret på naturgas /15/
Anvendelsen af naturgas beror på hvilke råmateriale der er adgang til . Produktionen i USA er for 95% vedkommende baseret på naturgas og i Europa er 72% af produktionen baseret på naturgas. Alternative råmaterialer for fremstilling af H2 ved reformering er naphta og kul.
Brint kan dog også fremstilles ved hydrolyse af vand.
Kuldioxid CO2
Urea CH4N2O
Kuldioxid fås mest som biprodukt fra forbrændingsprocesser /18/.
Urea fremstilles normalt ved "Basaroff reaktionen" /15/.
(12.2) 2 NH3 + CO2 « NH2 COONH4
(12.3) NH2 COONH4 « CH4N2O + H2O
Forbruget af råmaterialer er primært NH3 og CO2 og hjælpestoffer som damp og vand.
Emissioner fra fremstilling af urea er primært NH3 og støv. Formaldehyd, methanol og andre farlige stoffer kan emitteres til luft hvis der anvendes additiver. FormalinTM, brugt som et formaldehyd additiv kan indeholde op til 15% methanol. NH3 emitteres under selve syntesen som ukontrolleret fordampning og ved afgivelse fra det faste urea under oplagring. Støv afgives under alle fremstillingsprocesserne. Der er ikke nogen pålidelige målinger af gasformige formaldehyd emissioner /19/.
Under fremstillingen opstår der spildevand (reaktion (12.3)). Spildevandet renses for indeholdet af hovedsageligt urea og NH3. For eksempel vil produktion af 1200 ton urea om dagen som en normal dagsproduktion, medføre 360 ton spildevand om dagen.. Normalt fjernes NH3 fra spildevandet ved tilsætning af kaustisk soda hvorved det afdamper og kan opsamles. Urea nedbrydes til ammoniumcarbamat der fjernes ved stripning. /15/.
Cyranursyre C3H3N3O3
Cyranursyre fremstilles fra urea der smeltes ved en temperatur omkring 300° C (12.4). Processen kræver flere timers opvarmning for fuldstændig omdannelse af urea til cyranursyre. NH3 er det eneste biprodukt /15/, /18/.
(12.4) 3 CH4N2O ® C3H3N3O3 +3 NH3
Miljøpåvirkningen er væsentligst energiforbruget til smelteprocessen og afdampning af NH3.
Chlor Cl2
Chlor fremstilles ved elektrolyse af natrium chlorid.
(12.5) Na+ + Cl- ® Na-Hg + ½ Cl2
Elektroderne til processen kan indeholde Hg /15/, men i dag dominerer processer hvor titan eller ædelmetaller anvendes som elektroder.
Propylen
Calciumcarbonat CaCO3
Propylen fremstilles ud fra mineralolie.
Brydning af calciumcarbonat medfører emissioner fra energiforbrug og anvendelse af eksplosiver.
Allylchlorid C3H5Cl
Syntesen af allylchlorid sker ved en temperatur på 300-600 ° C og er baseret på en reaktion mellem propylen og chlor /15/.
(12.6) C3H6 + Cl2 ® C3H5Cl + HCl
Ved reaktionen dannes HCl som biprodukt.
Hypochlorsyre
HOCl
Hypochlorsyre er et almindeligt anvendt rengøringskemikalie. Hypochlorsyre fremstilles ud fra chlor og calciumcarbonat /18/.
(12.7) 2 Cl2 + 2 H2O + 2 CaCO3 ® 2 HOCl + Ca Cl2 + Ca (HCO3)2
Epichlorhydrin C3H5ClO
Reaktionen giver biprodukter i form af saltene calciumchlorid og calciumhydrogencarbonat.
Bruttoreaktionen er vist nedenfor /15/, /18/.
Triglycidyl isocyanurat C12H15N3O6
(12.8) 2 C3H5Cl + 2 HOCl ® 2 C3H5ClO + 2HCl
TGIC fremstilles ved reaktion mellem cyranursyre og epichlorhydrin /15/.
(12.9) C3H3N3O3 + 3 C3H5ClO ® C12H15N3O6 + 3 HCl
Den dannede TGIC vil ikke være 100% ren, idet den indeholder rester af epichlorhydrin i PPM området.
Som biprodukt ved reaktionen dannes saltsyre.
12.1.2 Miljøpåvirkninger ved fremstilling af TGIC
Kvalitative miljøpåvirkninger
Det har ikke været muligt at opgøre alle emissioner idet datakvaliteten og omfang af data er varierende. For nogle stoffer har det ikke været muligt at finde oplysninger om emissioner og energiforbrug overhovedet.
I tabel 12.1 er givet en kvalitativ oversigt over råvareforbrug, energiforbrug og emissioner.
Tabel 12.1 Kvalitative miljøbelastninger /14/, /15/, /8/, /19/ valitative miljøbelastninger /14/, /15/, /8/, /19/ Se her
Sundhedseffekter
I nedenstående tabel 12.2 er vist faremærkning af de stoffer som indgår i fremstillingen af TGIC samt om der ved fremstilling anvendes farlige processer.
Tabel 12.2 Sundhedseffekter og farlige reaktioner /14/, /15/, /18/ Se her
I maj 1996 har EU komissionen vedtaget en opstramning af faremærkningen for TGIC, således at den inden den 31 maj 1998 skal mærkes som:
T; R46,R23/25, R41, R43, R48/22, R52/53 (100% TGIC)
Kvantitative miljøbelastninger
I det følgende er foretaget en opsummering af alle fundne kvantitative data for miljøbelastninger omregnet til 1 ton TGIC.
Hovedkilden til LCA data er BUWAL /8/. Data i denne rapport omfatter en række stoffer hvor alle data er "terminerede" , dvs. de omfatter alle miljøbelastninger fra fremstillingen af stoffet og alle de tilhørende råvarer m.m.
Den eneste undtagelse er, at rapporten ikke opgør ressourceforbruget til energi, dvs. mængden af olie, naturgas, kul og uran anvendt til at fremstille energien der anvendes i produktionsprocesserne. Denne undtagelse er blevet bekræftet af firmaet Ökoscience AG i Zürich der har været konsulent ved udarbejdelsen af BUWAL /8/.
Derfor er ressourceforbruget til energi beregnet ud fra oplysningerne om energiforbrug i BUWAL/8/ kombineret med nøgletallene i UMIPTOOL for ressourceforbrug ved forskellige brændselstyper.
Emissioner fra energiforbrug er generelt inkluderet i BUWALs tal, men for urea og ammoniak, der ikke findes i BUWAl, er emissioner fra elektricitetsforbrug beregnet ved hjælp af emissionsfaktorer fra BUWAL kombineret med oplysninger om elforbrug fra USEPA /19/.
I tabel 12.4 for ressourceforbrug er angivet et tal på 836 kg calciumcarbonat. Dette tal er en sum af den mængde der dannes støkiometrisk ved produktionen af hypochlorit (808 kg), mængden der forbruges ved produktionen af chlor jf. BUWAL (28,28 kg) og mindre mængder brugt ved energiproduktionen.
De kemiske reaktioner for fremstilling af TGIC som er beskrevet i afsnit 12.1.1 viser
at der rent støkiometrisk dannes en række biprodukter der enten kan ende som emissioner
eller som råmaterialer i andre produktioner.
Generelt er biprodukter ikke medregnet som emissioner i de følgende tabeller medmindre
dette bekræftes af andre kilder.
Der er ikke fundet nogen data om luftemissioner, emissioner til vand og affald fra produktion af: TGIC , epichlorhydrin , allylchlorid , hypochlorsyre og cyranursyre. De reelle emissioner vil derfor sandsynligvis være større end angivet.
Energiforbrug
Energiforbruget til fremstilling af 1 ton TGIC er beregnet i bilag 2.2. Resultatet er sammenfattet i nedenstående tabel 12.3.
Tabel 12.3 Energiforbrug /14/, /15/, /8/
| Produktionstrin | Forbrug pr. ton TGIC |
| Ammoniak Urea Calciumcarbonate Chlor Propylen Hypochlorsyre Allylchlorid Epichlorhydrin Cyanursyre TGIC |
23,3 GJ5 0,3 GJ6 1,5 GJ7 30,4 GJ8 29,5 GJ ingen data ingen data ingen data ingen data ingen data |
| I alt | 85,0 GJ |
Ressourceforbrug
Ressourceforbruget ved fremstilling af TGIC er beregnet i bilag 2.3. Det har været muligt at finde aktuelle forbrugstal i håndbogslitteraturen og kun forbruget af CaCO3 ved fremstilling af HOCl er beregnet støkiometrisk.
Tabel 12.4 Ressourceforbrug /14/, /15/, /8/
| Ressource | Forbrug pr ton TGIC9 |
| naturgas rå olie vand aluminium jern kul brunkul calciumcarbonate ler natriumchlorid biomasse uran |
2.701 kg 1.613 kg 44.852 kg 0,5 kg 0,1 kg 2.976 kg 722 kg 836 kg 0,04kg 1.711 kg 46 kg 0,1 kg |
Emissioner og affald
Emissioner til luft, vand og affald fra fremstilling af TGIC er beregnet i bilagene 2.4-2.6. Der er kun fundet oplysninger om emissioner fra nogle af procestrinene. For Urea er der anført en negativ emission af CO2 som skyldes forbruget af CO2 i processen for fremstilling af Urea. Mængden er beregnet støkiometrisk.
Tabel 12.5 Emissioner /14/, /15/, /8/, /19/
| Parameter | Emission pr. ton TGIC10 |
| Emissioner til luft: | |
| Støv CO SO2 TOC NH3 CO2 HC Nox H2S HCl |
8,2 kg 5,0 kg 24,0 kg 78,0 kg 7,8 kg 3.165,0 kg 18,0 kg 17,0 kg 0,004kg 0,26 kg |
| Emissioner til Vand: | |
| SS (suspenderet stof) DS (opløste salte) COD BOD DOC Syrer SO42- Cl- Olie Metaller Kulbrinter |
3,0 kg 1,0 kg 0,1 kg 0,01 kg 0,03 kg 0,54 kg 10,0 kg 59,0 kg 0,1 kg 0,14 kg 0,01 kg |
| Fast affald: | |
| Uspec. Volumenaffald | 250 kg |
12.2 b-Hydroxyalkylamid
Der er heller ikke for b-hydroxyalkylamid fundet nogen "færdige" livscyklusvurderinger. Det har derfor også her været nødvendigt at foretage en mere detaljeret vurdering af de enkelte procestrin i fremstillingen.
12.2.1 Fremstilling af b-hydroxyalkylamid
b-hydroxyalkylamid produceres hovedsageligt af EMS-Chemie Aktiengesellschaft i Schweiz. Fremstillingen omfatter de trin der vist i Figur 12.3 nedenfor.
Benzen
C6H6
Fig. 12.3 Procestræ for fremstilling af b-hydroxyalkylamid /14/, /15/, /20/, /21/, /22/ Se her
Benzen fremstilles primært af råolie eller naphta. Ved produktionen opstår luftemissioner, spildevand og affald /8/.
Cyclohexan
C6H12
Stort set al cyclohexan produceres industrielt ved hydrering af benzen udvundet af råolie. En lille del fremstilles dog ved superfraktionering af naphta fra råolie /14/.
Benzen kan hydreres katalytisk til cyclohexan i enten væske- eller dampfasen ved tilstedeværelse af brint og med nikkel, platin eller palladium som katalysator.
(12.10) C6H6 + 3 H2 ® C6 H12
Reaktionen er stærkt exoterm og udføres typisk ved 20-30 MPa og max 300° C.
Ammoniak
NH3
Cyclohexan bruges til at fremstille adipinsyre, som indgår i syntesen af b -hydroxyalkylamid.
Ammoniak fremstilles normalt ud fra nitrogen og brint. Nitrogen findes i luft og brint fås ved reformering af naturgas /15/.
Den resulterende kemiske reaktion for ammoniaksyntesen er:
(12.11) N2 + 3 H2 « 2 NH3
Fremstillingen sker via 8 enhedsoperationer som vist i figur 12.4.
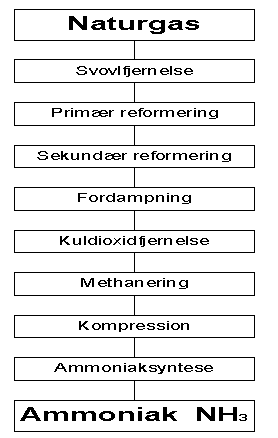
Fig. 12.4 Ammoniaksyntese baseret på naturgas /15/
Anvendelsen af naturgas beror på hvilke råmateriale der er adgang til . Produktionen i USA er for 95% vedkommende baseret på naturgas og i Europa er 72% af produktionen baseret på naturgas. Alternative råmaterialer for fremstilling af H2 ved reformering er naphta og kul.
Brint kan dog også fremstilles ved hydrolyse af vand.
Ammoniakken benyttes til fremstilling af salpetersyre og diethanolamin.
Salpetersyre
HNO3
Salpetersyre er nødvendig til fremstilling af adipinsyre /14/, /15/.
Industriel fremstilling af salpetersyre sker hovedsageligt ved oxidation af ammoniak ved hjælp af oxygen fra atmosfærisk luft. Herved dannes nitrogen, som absorberes i vand og derved danner salpetersyre. Det samlede reaktionsforløb er:
(12.12) NH3 + 2O2 ® HNO3 + H2O
Reaktionen, der katalyseres af platin eller platin/rhodium katalysatorer, foregår ved en temperatur på 800 - 900° C.
Adipinsyre
C6H10O4
Der sker luftemission, fordi der ikke er økonomi i at absorbere mere end 97 - 98% af den NO, der indblæses i vandet for at danne salpetersyre.
Adipinsyre bruges til fremstilling af alkyl esteren dimethyladipat, som indgår i syntesen af b-hydroxyalkylamid. Adipinsyre fremstilles af cyclohexan i to hovedtrin ved oxidationsprocesser.
I første trin oxideres cyclohexan til ketonen cyclohexanon og alkoholen cyclohexanol (12.13). Denne keton -alkohol blanding omdannes herefter til adipinsyre ved oxidation med salpetersyre ved tilstedeværelse af enten en krom eller kobolt og/eller kobber katalysator (12.14).
(12.13) 3 C6H12 + 3O2 ® 3 C6H12O2 3 C6H12O2 ® 2 C6H12O + C6H10 O + H2O + O2
(12.14) 2 C6H12O + C6H10O + 4 HNO3 ® 3 C6H10O4 +N2O +2NO
Methanol
CH3OH
Adipinsyre er et meget anvendt råstof bl.a. til fremstilling af polyester, nylon-6,6 m.m. Ved processen sker emission af mange forskellige forbindelser, bl.a. CH4, NOx, CO2 /13/ hvorved der opstår en del miljøproblemer.
Methanol fremstilles ved oxidation af methan udvundet af naturgas /8/. Produktionen af methanol medfører en del luftemission, spildevand og affald.
Dimethyladipat C8H14O4
Esteren dimethyladipat fremstilles industrielt ved en reaktion mellem adipinsyre og methanol med en lille mængde svovlsyre som katalysator.
(12.15) C6H10O4 + 2 CH4O ® C8H14O4 + 2 H2O
Ethylen
C2H4
Der har ikke kunnet fremskaffes oplysninger om luftemission, spildevand og affald fra denne proces.
Ethylen er den organiske forbindelse, der i dag produceres i størst mængde. Det er den vigtigste byggesten i den petrokemiske industri. Ved siden af anvendelser til fremstilling af opløsningsmidler, overfladeaktive midler, belægninger, blødgøringsmidler og antifrostvæsker, anvendes ethylen hovedsageligt til fremstilling af polymerer såsom plastic, kunstharpiks, fibre og elastomerer.
I dag fremstilles ethylen næsten udelukkende ved pyrolyse af kulbrinter, der udvindes af naturgas og/eller mineralolie. Ethylen kan også produceres ved dehydrering af ethanol.
Ethylenoxid
C2H4O
Der er en del miljøproblemer forbundet med produktion af ethylen på grund af de store produktionsmængder og fordi der ved produktionen sker luftemissioner (bl.a. CO2, HC, NOx) og opstår spildevand og affald /8/.
Ethylenoxid bruges til fremstilling af dimethanolamin, som indgår i syntesen af b -hydroxyalkylamid.
Ethylenoxid fremstilles industrielt ved en direkte oxidationsproces. Reaktionen er en katalytisk oxidation af ethylen med ilt ved brug af en sølvbaseret katalysator.
(12.16) 7 C2H4 + 6 O2 ® 6 C2H4O + 2 CO2 + 2 H2O
Diethanolamin C4H11NO2
Ved reaktionen danner den rene proces kuldioxid og vand som biprodukter.
Ethanolaminerne er de vigtigste aminoalkoholer. De fremstilles industrielt ved en reaktion med ethylenoxid og ammoniak. Di- og triethanolaminer produceres på samme måde ved gentagelse af reaktionen /14/, /15/.
(12.17) NH3 + C2H4O ® C2H7NO (7.17) C2H7NO + C2H4O® C4H11NO2
b-hydroxyalkylamid C14H30N2O6
Der har ikke kunnet fremskaffes oplysninger om luftemission, spildevand og affald fra denne proces.
Fremstilling af hærderen b-hydroxyalkylamid foregår ved en reaktion af dimethyladipat og en blanding af diethanolamin og natriumhydroxid (katalysator). Det blev i 1992 opdaget, at b-hydroxyalkylamid kan fungere som hærder og samme år blev reaktionsprocessen udviklet /20/, /22/. Processen er:
(12.18) C8H14O4 + 2 C4H11NO2 ® C14H30N2O6 + 2 CH3OH
Kvalitative miljøpåvirkninger
12.2.2 Miljøpåvirkninger ved fremstilling af b -Hydroxyalkylamid
Det har ikke været muligt at opgøre alle emissioner, idet datakvaliteten og omfang af data er varierende. For nogle stoffer har det ikke været muligt at finde oplysninger om emissioner og energiforbrug overhovedet.
I tabel 12.6 er givet en kvalitativ oversigt over råvareforbrug, energiforbrug og emissioner.
Tabel 12.6 Kvalitative miljøbelastninger /8/, /14/, /15/, /19/
| Procestrin | Råvare- forbrug |
Energi- for- brug |
Luftemis- sioner |
Spilde- vand |
Af- fald |
| Benzen C6H6 |
mineralolie, naturgas, vand | +++ | støv, CO, SO2, CO2, HC, NOx, H2S, HCl | støv, COD, BOD, DOC, syrer, chlorid, NH3,
olie, metal- ler |
+ |
| Cyclohexan C6H12 | - | + | ingen data | ingen data | ingen data |
| Hydrogen H2 |
naturgas, vand | ++ | støv, CO2, CO, HC, NOx, HCl | olie, støv, DOC, syrer, metaller, HC | + |
| Ammoniak NH3 | vand, luft | ++ | CO, SO2, VOC, NH3, CO2 | ingen data | ingen data |
| Salpetersyre HNO3 |
luft | + | NOx | ingen data | ingen data |
| Adipinsyre C6H10O4 |
luft | ingen data | CO, CO2, NOx, CH4, N2O | ingen data | ingen data |
| Methanol CH3OH | naturgas, vand | +++ | støv, CO, CO2, SO2, CO2, HC, NOx, HCl | støv, BOD, DOC, syrer, olie, metaller, HC | +++ |
| Dimet- hyladipat C8H14O4 |
ingen data | ingen data | ingen data | ingen data | ingen data |
| Ethylene C2H4 | naturgas, mineral olie, vand | +++ | CO2 | olie, støv | + |
| Ethylenoxid C2H4O | ingen data | ingen data | CO2 | ingen data | ingen data |
| Diethanolamin C4H11NO2 | ingen data | ingen data | ingen data | ingen data | ingen data |
| b-Hydroxy- alkylamid C14H30N2O6 |
ingen data | ingen data | ingen data | ingen data | ingen data |
Sundhedseffekter
I nedenstående tabel 12.7 er vist faremærkning af de stoffer som indgår i fremstillingen af b-hydroxyalkylamid samt om der ved fremstilling anvendes farlige processer.
Datakvaliteten er varierende, da stofferne enten ikke er udforsket eller sparsomt publiceret. Der er ikke medtaget stoffer, hvor ingen data foreligger.
Tabel 12.7 Sundhedseffekter og farlige reaktioner /14/, /15/, /18/
| Stof | Farlige reaktioner | Sundheds- effekter |
Symbol |
| b-Hydroxy- alkylamid C14H30 N2O6 |
ingen | ingen (lav systemisk toksicitet) | ingen krav om mærkning |
| Dimet- hyladipat C8H14O4 |
ingen data | farlig ved indånding, indtagelse eller hudkontakt, kan medføre irritation | ingen data |
| Methanol CH3OH | eksplosive reaktioner med baser og stærke iltningsmidler | giftig ved indånding, indtagelse og optagelse gennem huden, skader på synet, hovedpine, neurotoksisk | F; R11 T; R23/25 |
| Adipinsyre C6H10O4 | reaktion med baser | øjenirritation | Xi; R36 |
| Salpetersyre HNO3 | exoterm reaktion med baser, organiske forbindelser etc. | øjen - og lungeirritation, stærkt ætsende | O; R8 C; R35 |
| Ammoniak NH3 | farlige reaktioner med chlor, hydrogenchlorid, kuldioxid etc. | irriterer øjne og hud, lungeskade, giftig | R10 T; R23 |
| Cyclohexan C6H12 |
eksplosive reaktioner (dampe) | irriterer øjne og hud, narkotisk virkning, lever - og nyreskader | F; R11 |
| Hydrogen H2 | kan danne eksplosive blandinger med mange luftarter, bl.a. oxygen (knaldgas) | narkotisk virkning ved længere tids påvirkning, erstatter oxygen | Fx; R12 |
| Benzen C6H6 | eksplosive reaktioner med stærke iltningsmidler | giftig ved indånding, indtagelse og optagelse gennem huden, neurotoksisk, carcinogen ved længere tids påvirkning, hudreaktioner | Carc1; R45 F; R11 T; R48/23/24/25 |
| Diethano- lamin C4H11NO2 |
ingen data | øjen - og hudirritation | Xi; R36/38 |
| Ethylenoxid C2H4O | eksplosiv sammen med baser, syrer og aminer | mutagen, carcinogen, giftig, øjen -, hud - og lungeirritation, narkotisk virkning | Carc2; R45 Mut2; R46 Fx; R12; T; R23 Xi;R36/37/38 |
| Ethylen C2H4 |
eksplosive reaktioner med chlor | narkotisk virkning | Fx; R12 |
Kvantitative miljøbelastninger
I det følgende er foretaget en opsummering af alle fundne kvantitative data for miljøbelastninger omregnet til 1 ton b-hydroxyalkylamid .
Hovedkilden til LCA data er BUWAL /8/. Data i denne rapport omfatter en række stoffer hvor alle data er "terminerede" , dvs. de omfatter alle miljøbelastninger fra fremstillingen af stoffet og alle de tilhørende råvarer m.m.
Den eneste undtagelse er, at rapporten ikke opgør ressourceforbruget til energi, dvs. mængden af olie, naturgas, kul og uran anvendt til at fremstille energien der anvendes i produktionsprocesserne. Denne undtagelse er blevet bekræftet af firmaet Ökoscience AG i Zürich der har været konsulent ved udarbejdelsen af BUWAL /8/.
Derfor er ressourceforbruget til energi beregnet ud fra oplysningerne om energiforbrug i BUWAL/8/ kombineret med nøgletallene i UMIPTOOL for ressourceforbrug ved forskellige brændselstyper.
Emissioner fra energiforbrug er generelt inkluderet i BUWALs tal, men for urea og ammoniak, der ikke findes i BUWAl, er emissioner fra elektricitetsforbrug beregnet ved hjælp af emissionsfaktorer fra BUWAL kombineret med oplysninger om elforbrug fra USEPA /19/.
De kemiske reaktioner for fremstilling af b-hydroxyalkylamid
som er beskrevet i afsnit 12.2.1 viser at der rent støkiometrisk dannes en række
biprodukter der enten kan ende som emissioner eller som råmaterialer i andre
produktioner.
Generelt er biprodukter ikke medregnet som emissioner i de følgende tabeller medmindre
dette bekræftes af andre kilder.
Der er ikke fundet nogen data om luftemissioner, emissioner til vand og affald fra produktion af: ethylenoxid, cyclohexan, adipinsyre, salpetersyre, diethanolamin og dimethyladipat. De reelle emissioner vil derfor sandsynligvis være større end angivet i de følgende tabeller.
Energiforbrug
Energiforbruget til fremstilling af b-hydroxyalkylamid er beregnet i bilag 3.2. Der er fundet oplysninger om energiforbrug til nogle af delkomponenterne i litteraturen, men det har ikke været muligt at finde data om alle energiforbrugende processer.
Tabel 12.8 Energiforbrug /8/,/14/
| Produktionstrin | Forbrug pr. ton b-hydroxyalkylamid |
| Ammoniak benzen ethylen cyclohexan hydrogen (cyclohexan) methanol salpetersyre adipinsyre dimethyl adipat ethylen oxid diethanolamin b-hydroxyalkylamid |
12 GJ11 18 GJ 28 GJ ingen data 5,912 15 GJ ingen data ingen data ingen data ingen data ingen data 1,3 GJ13 |
| I alt | 80,4 GJ |
Ressourceforbrug
Ressourceforbruget ved fremstilling af b-hydroxyalkylamid er angivet i bilag 3.3. Der er fundet oplysninger om ressourceforbrug ved nogle af delkomponenterne i litteraturen, men det har ikke været muligt at finde data om alle processer. Tabel 12.9 indeholder også ressourceforbrug ved energiproduktion til de forskellige processer, i det omfang dette energiforbrug er kendt (se tabel 12.8).
Tabel 12.9 Ressourceforbrug /8/, /14/
| Ressource | Forbrug pr ton b-hydroxyalkylamid14 |
| naturgas rå olie vand aluminium jern kul brunkul calciumcarbonate ler natriumchlorid biomasse uran |
4.379 kg 2.390 kg 1.951 kg 0,8 kg 0,1 kg 3.924 kg 108 kg 0,2 kg 0,05kg 1,2 kg 6,9 kg 0,01kg |
Emissioner og affald
Emissioner til luft, vand og affald fra fremstilling af b-hydroxyalkylamid er beregnet i bilagene 3.4 -3.6. Der er ikke fundet oplysninger om emissioner fra alle processer.
Tabellerne indeholder også emissioner til luft, vand og affald for energiproduktion til de forskellige processer, i det omfang dette energiforbrug er kendt (se tabel 12.8).
Tabel 12.10 Emissioner /8/,/19/
| Parameter | Emission kg pr. ton b-hydroxyalkylamid15 |
| Emissioner til luft: | |
| Støv CO SO2 TOC NH3 CO2 HC Nox H2S HCl CH4 N2O |
1,5 18 11 5,1 0,4 2.589 57 22 0,006 0,01 0,06 132,0 |
| Emissioner til Vand: | |
| SS (suspendert stof) DS (opløste salte) COD BOD DOC Syrer Cl- NH3 Olie Metaller Kulbrinter |
0,2 6,9 0,1 0,03 0,03 0,07 0,04 0,005 0,2 0,09 0,2 |
| Fast affald: | |
| Uspec. Volumenaffald | 611 |
12.3 Miljøvurdering
Ved eventuel udskiftning af TGIC-hærderen med b-hydroxyalkylamid i pulvermaling kan der ske ændringer af miljøbelastningerne i alle livscyklusfaser fordi sammensætningen af malingen ændres.
For at kunne sammenligne forskellene er det vigtigt at definere den funktionelle enhed.
Funktonel enhed
Som udgangspunkt vælges en "funktionel enhed" på 1 tons pulvermaling, idet der ikke foreligger undersøgelser der talmæssigt dokumenterer forskelle i levetid for maling baseret på de 2 typer hærdere. Ud fra accelererede test, hvor malingerne afprøves under ekstreme betingelser, er der dog noget der tyder på en mindre holdbarhed af maling baseret på b-hydroxyalkylamid.
Ifølge oplysninger fra TEKNOS SCHOU A/S vil forbruget af b-hydroxyalkylamid være ca. 0,77 x forbruget af TGIC når alle andre parametre er uændrede. Alle andre parametre vil i praksis være uændrede ved hovedparten af malingerne (ca. 80% af recepterne).
Den eneste ændring der regnes med i det følgende er således at der til 1 tons pulvermaling skal bruges 0,77 x 37 = 29 kg b-hydroxyalkylamid i stedet for 37 kg TGIC.
Manglende oplysninger
Ved sammenligningen af miljøbelastningerne i det følgende skal der iøvrigt tages forbehold for at der for begge typer hærdere mangler oplysninger om ressourceforbrug og emissioner for en del procestrin som beskrevet i de foregående afsnit.
12.3.1 Ressourceforbrug
Udskiftning af TGIC med b-hydroxyalkylamid medfører en ændring i ressourceforbruget som det fremgår af tabel 12.4 og tabel 12.9. I nedenstående figur 12.5 er det normaliserede og vægtede ressourceforbrug sammenstillet for de 2 typer af hærdere.
Det der sammenlignes i figuren er ressourceforbruget til fremstilling af den mængde hærder der indgår i 1 tons pulvermaling, dvs. henholdsvis 37 kg TGIC og 29 kg b -hydroxyalkylamid. Enheden er derfor ressourcforbrug pr. tons pulvermaling.
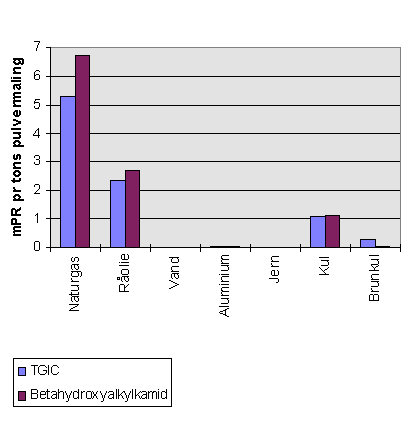
Fig. 12.5 Sammenligning af ressourceforbrug ved fremstilling af 2 hædere
Som det fremgår af figuren er ressourceforbruget gennemgående større ved b -hydroxyalkylamid, hvilket bl.a. skyldes at der anvendes naturgas og mineralolie både som råmateriale og til energifremstilling.
For TGIC er der også et forbrug af naturgas og råolie, men primært til fremstilling af energi. Herudover er de væsentligste råmaterialer til fremstilling af TGIC, NaCl og CaCO3 som findes i rigelige mængder.
Betydningen af det forøgede ressourceforbrug ved at skifte fra TGIC til b -hydroxyalkylamid skal dog vurderes i forhold til størrelsen af ressourceforbruget fra andre råvarer og de øvrige livscyklusfaser.
Fig. 12.6 viser det samlede ressourceforbrug i henholdsvis råvare-, fremstillings- og brugsfasen for pulvermaling. For råvarefasen er der ingen direkte oplysninger om det samlede ressourceforbrug, og i figuren er det derfor skønnet ud fra energiforbruget fundet i screeningen (kapitel 10).
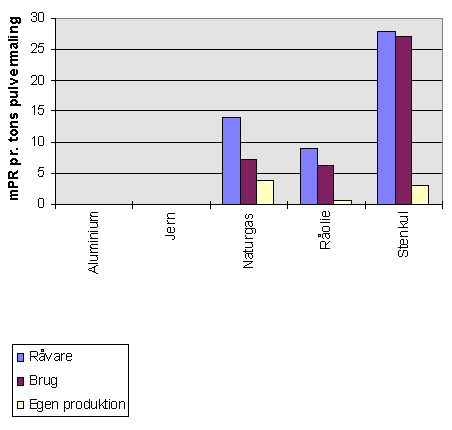
Fig. 12.6 Ressourceforbrug for pulvermaling over livscyklus
Sammenlignes fig. 12.5 og 12.6 ses det at forøgelsen af ressourceforbruget ved at skifte fra TGIC til b-hydroxyalkylamid er lille også i forhold til det samlede ressourceforbrug over pulvermalingens livsforløb.
12.3.2 Ydre miljø
I nedenstående fig. 12.7 er de vægtede miljøeffekter ved fremstilling af hærderne opgjort på grundlag af tallene i tabel 12.5 og 12.10.
Fig. 12.7 Vægtede miljøeffekter Se her
Figur 12.7 viser at b-hydroxyalkylamid medfører en væsentlig større drivhuseffekt pr. tons pulvermaling end TGIC.
En nærmere vurdering viser at dette skyldes udledningen af ca. 132 kg N2O pr. tons b-hydroxyalkylamid under fremstillingen af Adipinsyre (se afsnit 12.2.1).
I nedenstående fig. 12.8 er de potentielle miljøeffekter vist når man forsøgsvist udelader N2O-emissionen. Miljøeffekterne er nu mere ens selvom der stadig er forskelle (bemærk den ændrede skala i forhold til fig. 12.7).
Fig. 12.8 Vægtede miljøeffekter escl. emission af N2O ved betahydroxyalkylamid Se her
Umiddelbart vil den større drivhuseffekt ved at anvende b-hydroxyalkylamid dog skulle sættes i forhold til drivhuseffekten som forårsages af andre råvarer og livscyklusfaser som vist i nedenstående fig. 12.9.
Fig. 12.9 Ydre miljøbelastninger for pulvermaling over livscyklus ved brug af TGIC som hærder Se her
I fig. 12.9 er der for råvarefasen kun medtaget miljøbelastninger fra henholdsvis TiO2(sulfatmetoden) ogTGIC, idet miljøbelastningerne fra øvrige råvarer ikke kendes.
Fig. 12.9 viser, at bidraget til drivhuseffekten fra disse 2 stoffer i råvarefasen er lille sammenlignet med bidraget fra brugsfasen (energiforbrug) og at drivhuseffekten totalt er en mindre miljøbelastning end f.eks. farligt affald set over pulvermalings livscyklus.
I nedenstående fig 12.10 er TGIC erstattet af b-hydroxyalkylamid som hærder
Fig. 12.10 Ydre miljøbelastninger for pulvermaling over livscyklus ved
brug af beta-hydroxyalkylamid som hærder Se her
Ved at sammenligne figur 12.9 og fig. 12.10 ses det at den forøgelse af drivhuseffekten på knapt 200 mPEM pr. tons pulvermaling som skift af hærderen til b -hydroxyalkylamid medfører, er af relativt lille betydning for det ydre miljø, totalt set.
Derimod har det væsentlig betydning at udskiftning af TGIC til b-hydroxyalkylamid medfører at mængden af farligt affald pr. tons pulvermaling falder til 0 ved fremstilling og brug af pulvermaling, idet dette affald udelukkende består af uhærdet pulvermaling, der i dag skal klassificeres som farligt affald pga. TGIC-hærderens sundhedsskadelige egenskaber. Denne omklassificering forudsætter dog at alt TGIC fjernes fra pulvermaling og erstattes af b-hydroxyalkylamid.
Mængden af farligt affald fra bortskaffelsen af pulveraffald ændres derimod ikke, idet dette primært er affald fra schredder processen, der er mindre veldefineret i sammensætningen (afsnit 7.1.2).
Som nævnt i afsnit 12.1.1 vil TGIC endvidere iflg. producenten aldrig være 100% ren, idet den vil indeholde små rester af epichlorhydrin (i ppm-området). De præcise mængder kendes ikke, men i afsnit 7 er der ud fra grundstofanalyser beregnet en forventet HCl-emission på 1,5 kg/tons pulvermaling ved schredning og omsmeltning af malede emner.
Det antages at en del af denne emission skyldes rester af epichlorhydrin i TGIC-hærderen.
b-hydroxyalkylamid anvender ikke chlorholdige råmaterialer og vil derfor ikke give HCl emission ved forbrænding af pulvermaling.
12.3.3 Arbejdsmiljø
Ved fremstilling af pulvermaling med TGIC er der fundet en arbejdsmiljøbelastning på grund af TGIC. TGIC er jf. tabel 12.2 mærket med risikosætningen R 43, hvilket betyder at stoffet medregnes til allergifremkaldende stoffer i beregning af arbejdsmiljøeffekterne efter UMIPTOOL.
TGIC vil endvidere skulle T-mærkes som et giftigt stof fra 31 maj 1998.
b-hydroxyalkylamid er ikke mærket som farligt stof jf. tabel 12.7.
Det betyder at den allergifremkaldende arbejdsmiljøeffekt må forventes at forsvinde fuldstændigt ved skift fra TGIC til b-hydroxyalkylamid.
Under brugsfasen af pulvermaling optræder de samme allergieffekter af TGIC som under fremstillingsfasen, jf. afsnit 8.
Der må derfor forventes samme positive effekt af at udskifte TGIC med b -hydroxyalkylamid i brugsfasen som i fremstillingsfasen.
12.3.4 Samlet konklusion vedrørende valg af hærder
Som det fremgår af ovenstående er der både fordele og ulemper ved at udskifte TGIC med b-hydroxyalkylamid.
Fordelene er:
- Fjernelse af arbejdsmiljøbelastninger (som skyldes at TGIC er et allergifremkaldende og kommende T-mærket stof) i fremstilling og brug af pulvermaling
- Omklassificering af pulveraffald fra farligt affald til almindeligt affald forudsat at alt TGIC erstattes af b-hydroxylakylamid
- reduktion af udledningerne af chlorforbindelser ved bortskaffelse af pulvermaling
Ulemperne er:
- en lille forøgelse af ressourceforbruget (naturgas, olie og kul)
- en lille forøgelse af drivhuseffekten (pga. N2O)
Udover disse "objektive" informationer skal også medregnes mere subjektive hensyn i valget af hærder, som f.eks. at TEKNOS SCHOU A/S generelt ønsker at undgå T-mærkede stoffer i produktionen.
Ud fra dette kan det anbefales at TEKNOS SCHOU A/S udskifter TGIC-hærderen med b-hydroxyalkylamid, men at der samtidig startes en dialog med råvareleverandøren EMS chemie om mulighederne for at reducere N2O-emissionen ved rensning eller lignende.
12.3.5 Følsomhedsvurdering
Ovenstående konklusion er selvfølgelig behæftet med usikkerhed, fordi der mangler data for en del af processerne.
F.eks. mangler der i visse tilfælde oplysninger om hvilke specifikke stoffer der emitteres, idet bl.a. BUWAL angiver nogle emissioner som "uspecificerede partikler" eller "uspecificerede metaller". For disse kan der ikke beregnes bidrag til toxicitet mv..
Der er dog ingen tvivl om, at de viste arbejdsmiljømæssige fordele ved at skifte til b-hydroxyalkylamid er reelle nok, vurderet ud fra mærkningen af dette stof. Tilsvarende vil reduktion af mængden af farligt affald og emission af chlorforbindelser ved forbrænding af pulvermaling være reel forudsat at alt TGIC substitueres.
Farligt affald kan dog kun betegnes som et miljøproblem i det omfang det ikke håndteres korrekt, ellers er det mere et økonomisk problem.
Derimod er ændringer i ressourceforbrug og drivhuseffekt mere usikker fordi der mangler oplysninger fra råvareleverandørerne. Dvs. det er primært ulemperne der ikke kan dokumenteres fuldt ud endnu.
_________________________
omfatter også energiforbrug ved fremstilling af råmaterialerne naturgas og brint omfatter kun energiforbrug ved fremstilling af urea fra ammoniak og kuldioxid omfatter også energiforbrug ved fremstilling af råmaterialet natriumchlorid omfatter også energiforbrug ved fremstilling af råmaterialerne mineral olie og naturgas Mængderne omfatter ikke ressourceforbruget ved fremstilling af TGIC, epichlorhydrin, hypochlorsyre og cyanursyre samt ressourceforbruget til energi ved fremstillingen Mængderne omfatter ikke emissioner fra fremstilling af TGIC, epichlorhydrin, allylchlorid, hypochlorsyre og cyanursyre samt emissioner fra energiforbrug ved fremstilling af disse stoffer omfatter også energiforbrug ved fremstilling af råmaterialerne naturgas og brint omfattet kun energiforbruget til fremstilling af brint til cyclohexan omfatter kun energiforbruget til fremstilling af b-hydroxyalkylamid ud fra dimethyladipat og diethanolamin Mængderne omfatter ikke ressourceforbruget ved fremstilling af ethylenoxid, cyclohexan, adipinsyre, salpetersyre, dimethyladipat og diethanolamin samt ressourceforbruget til energi ved fremstillingen af disse stoffer Mængderne omfatter ikke emissioner og affald dannet ved fremstilling af ethylenoxid, cyclohexan, adipinsyre, salpetersyre, dimethyladipat og diethanolamin samt ressourceforbruget til energi ved fremstillingen af disse stoffer