Bekæmpelsesmiddelforskning fra Miljøstyrelsen nr. 125, 2009
Transport af bekæmpelsesmidler over moderkagen, analogier til percutan transport og modellering
Indholdsfortegnelse
- 2.1 Præsentation af teststoffer
- 2.2 Delstudie 1. Dermal absorption
- 2.3 Delstudie 2. Transplacental transport
- 2.4 Delstudie 3. Modellering
- 3.1 Delstudie 1. Dermal absorption
- 3.2 Delstudie 2. Transplacental transport
- 3.3 Delstudie 3. modellering
Forord
Erfaringer fra undersøgelse af menneskers udsættelse for visse bekæmpelsesmidler indikerer klare reproduktionstoksiske effekter. Kun ganske få bekæmpelsesmidlers absorption over moderkagen er imidlertid undersøgt. Derimod har man betydelig mere viden om bekæmpelsesmidlers absorption over huden. Absorptionen forventes for både hud og moderkage overvejende at ske ved passiv diffusion. Dette projekt præsenterer parallelle data mellem absorption over moderkage og hud i to forskellige in vitro modeller for en række bekæmpelsesmidler og modelstoffer. Disse data er baggrunden for overvejelser omkring muligheden for at udvikle matematiske modeller for transport over moderkagen baseret på viden om såvel stoffernes hudabsorption som deres specifikke fysisk-kemiske egenskaber.
Forøget viden om bekæmpelsesmidlers muligheder for passage af de for fostre relevante barrierer vil have umiddelbar anvendelighed ved fremtidige fare- og risikovurderinger, ligesom anvendelse af in vitro data kombineret med matematisk modellering forventes at reducere behovet for dyreeksperimentelle undersøgelser af fremmedstoffers reproduktionstoksiske effekter.
Projektet er gennemført på basis af en bevilling fra Miljøstyrelsens midler til bekæmpelsesmiddelforskning til Jesper Bo Nielsen på vegne af forskergrupper ved SDU, KU, samt DHI. Fra disse tre institutioner har en række personers indsats været absolut nødvendig for projektets gennemførelse. Projektledelsen ved Jesper Bo Nielsen, SDU, Lisbeth E. Knudsen, KU, samt Dorthe Nørgaard Andersen og Karl-Heinz Cohr, DHI vil gerne anerkende denne indsats overfor Tina Mose, Mia Birkhøj Kjærstad, Line Mathiesen, Jeanette Kolstrup Søgaard Nielsen, Ann Dyreborg Larsen, og Thit Juul Mørck fra KU samt Flemming Nielsen, Mia Birkhøj Kjærstad, og Franziska Lind fra SDU.
Forfatterne er herudover taknemlige for de konstruktive kommentarer fra en gruppe eksterne eksperter (Grethe Østergaard, Afdeling for Eksperimentel Medicin, Rigshospitalet; Helle Raun Andersen, Institut for Sundhedstjenesteforskning, Syddansk Universitet; Henrik Leffers, Afdeling for Vækst og Reproduktion, Rigshospitalet; Katharina M. Main, Afdeling for Vækst og Reproduktion, Rigshospitalet; Sven Edelfors, Farmakologisk Institut, Københavns Universitet; Karin Sørig Hougaard, Det Nationale Forskningscenter for Arbejdsmiljø; Lise Grupe Larsen, Næstved Sygehus; Mari-Ann Flyvholm, Det Nationale Forskningscenter for Arbejdsmiljø; Ulla Hass, Fødevareinstituttet, Danmarks Tekniske Universitet) samt ansatte ved Miljøstyrelsen (Lærke Ambo Nielsen; Susanne Hougaard; Jørn Kirkegaard)
April 2009
Dorthe Nørgaard Andersen, DHI
Lisbeth E Knudsen, Københavns Universitet
Karl-Heinz Cohr, DHI
Jesper Bo Nielsen, Syddansk Universitet
Sammenfatning
Viden om absorption af bekæmpelsesmidler over den humane placenta er mangelfuld. Ex-vivo perfusion af den humane placenta er en metode til at studere stoffers passage af placenta. Resultater herfra kan indgå i senere risikovurdering omkring reproduktionstoksikologiske problemstillinger. Absorption over huden og placenta afhænger i høj grad af passiv diffusion. I dette studie er resultater fra 9 modelstoffers – heraf 5 pesticider – transport over placentabarrieren og huden anvendt med henblik på matematisk modellering af absorption i forhold til stoffernes fysisk/kemisk egenskaber.
Metoden med et dobbelt recirkulerende perfusionssystem til undersøgelse af absorption over placenta muliggør måling af modelstoffernes koncentration på den maternelle (CM) såvel som føtale (CF)side af placenta. Forholdet mellem CF og CM (FM-ratio) stiger lineært med tiden de første 30-60 minutters af forsøgene. Derefter flader kurven af, idet FM-ratioen nærmer sig en ligevægt. Den initiale hældning af FM-ratioen som funktion af tiden kaldes den indikative permeabilitetskoefficient (IPK). Denne parameter er et udtryk for transportshastigheden over placentabarrieren. Rapporten inddrager data fra nogle stoffer som allerede er undersøgt i et sammenligneligt modelsystem for hudpenetration, hvor parametre for hvert enkelt stof såsom lag-time, huddeposition og hudpenetration (Kρ) er målt. De undersøgte stoffer er benzoesyre, bisphenol A, caffein, samt antipyrin, der er kontrolstof for placentaperfusionerne, og bekæmpelsesmidlerne dimethoat, glyphosat, methiocarb, miconazol og tebuconazol.
Caffein og dimethoat transporteres over den placentale barriere ved passiv diffusion indikeret ved deres FM-ratio. Benzoesyre havde en lavere IPK end caffein, men nåede den samme steady state værdi udtrykt ved FM-ratioen. Transporten af glyphosat, bisphenol A, tebuconazol og methiocarb var begrænset gennem hele transportforløbet udtrykt ved både en lav IPK og FM-ratio. Miconazol blev ikke transporteret over placenta, men blev akkumuleret i placentavævet.
Der findes en sammenhæng mellem et stofs evne til at penetrere placenta / hastigheden, hvormed placenta passeres (IPK og FM-ratio150min) og stoffets lipofilicitet beskrevet ved logKow; jo højere logKow desto lavere permeabilitetskoefficient. Dog ser det ud til, at stoffet glyphosat ikke passer ind i dette mønster. En lineær sammenhæng mellem IPK og logKow med r²=0,96 kan dannes, hvis glyphosat undlades i plottet. Sammenhængen mellem vandopløselighed og IPK kan beskrives ved en logaritmisk funktion, hvor en stigende vandopløselighed betinger stigende IPK-værdier.
I hudabsorptionsmodellen ses ikke en klar sammenhæng mellem molekylevægt og Kρ værdier(permeabilitetskoefficienten for diffusionen over huden). Ved stigende molekylevægt ses en stigende lag-time. Den relative deposition i huden er højest for lipofile modelstoffer.
For LogKow værdier mellem -3,5 og 2 ses en lineær sammenhæng mellem logKow og logKρ.
For flere af modelstofferne ses en betydelig lag-time ved transport over huden (bl.a. dimethoat, bisphenol A, tebuconazol). En sådan lag-time ses ikke i samme grad ved transplacental transport, idet en lille lag-time dog kan anes for stofferne bisphenol A, tebuconazol og methiocarb. Årsagen er sandsynligvis større mulighed for temporær deponering i huden i forhold til placenta.
For hovedparten af modelstofferne ses et sammenligneligt optagelsesmønster over de to barrierer, hvilket indikerer, at de samme fysisk-kemiske parametre har betydning for passagen af stoffer over både hud og placenta. Et stof, antipyrin, adskiller sig dog markant i dets absorption over henholdsvis hud og placenta. For dette stof ses ingen passage af huden, mens absorption over placenta bruges som intern markør for de andre modelstoffer idet antipyrin passerer placenta relativt uhindret. Den manglende absorption over huden skyldes formodentlig stoffets høje vandopløselighed (51,9 g/L). Dette indikerer, at et stofs vandopløselighed har større betydning for dets absorption over huden end for passagen af placenta. For et andet stof, miconazol, ses også en markant anderledes optagelse i forhold til de andre modelstoffer, idet miconazol passerer hverken hud eller placenta.
Projekt har demonstreret paralleller mellem hudoptagelse og placentatransport af fremmedstoffer. For både hud og placenta er vandopløselighed, lipofilicitet, samt størrelse betydende parametre. Disse paralleller kan tænkes anvendt således, at eksisterende viden om enkeltstoffers eller stofgruppers dermale penetration kan ekstrapoleres til en forventning om placentapassage. Der vil eksistere betydende forskelle for enkeltstoffers vedkommende, eksemplificeret også i dette studie, men simple kvalitative ekstrapolationer af dermale absorptionsgrader til placenta vil kunne forventes mulige, men næppe generaliserende og kvantitative.
Generaliserbarhed og validitet af ekstrapolationerne kan videreudvikles gennem flere parallelle datasæt mellem placental og dermal absorption, og sådanne data forventes at kunne indgå i fremtidige struktur/aktivitetsmodeller til prædiktion af stoffers optagelse/transport over barrierer. På lang sigt og med supplerende in vitro tests kan det forventes, at modelresultaterne vil kunne bidrage til en reduktion i anvendelse af forsøgsdyr til undersøgelser af fremmedstoffers absorption over biologiske barrierer.
Data er delvist afrapporteret i videnskabelige artikler og flere er planlagt.
Mose T, Kjaerstad MB, Mathiesen L, Nielsen JB, Edelfors S, Knudsen LE. Placental passage of benzoic acid, caffeine, and glyphosate in an ex vivo human perfusion system. J Toxicol Environ Health A. 2008;71(15):984-91.
Nielsen JB, Sørensen JA, Nielsen F. The usual suspects - influence of physico-chemical properties on lag-time, skin deposition and percutaneous penetration of nine model compounds. J Toxicol Environ Health. 2008b; In press.
Summary
Knowledge on absorption of pesticides across the human placenta is limited. Ex-vivo perfusion of the human term placenta is a method to study placental passage. Results from this model will be an important element in assessment of risk related to reproductive toxicity. Absorption across the human skin as well as placenta depends to a large extent on passive diffusion. This study was designed to provide and use data from 9 substances including 5 pesticides in current use to develop a mathematical model enabling prediction of placental transfer of new compounds.
The placental perfusion method with maternal and fetal recirculating compartments studies transport from the maternal to the fetal compartment by measurements of the concentration of the studied compound in the maternal compartment CM and the fetal compartment CF. The ratio of CF versus CM (FM-ratio) increases linearly for the first 30-60 minutes of the study period and later reach equilibrium. The initial slope of the the FM ratio is named the indicative permeability coefficient (IPK) and this parameter is used as indicator of the initial transport across placenta. The study includes data from skin penetration studies of lag-time, skin deposition and skin penetration (Kρ). The model compounds included were benzoic acid, bisphenol A, caffeine, antipyrine and the pesticides dimethoate, glyphosate, methiocarb, miconazol, tebuconazole.
Caffeine and dimethoate cross the placenta by passive diffusion as indicated by their transfer rates. The initial transfer rate of benzoic acid was more limited in the first part of the perfusion compared to caffeine, but reached the same steady state level by the end of perfusion as measured by the FM-ratio. The placental transfer of glyphosate, bisphenol A, tebuconalzol and methiocarb was restricted throughout perfusion with a lower permeation rate and a lower FM ratio. Miconazol did not pass the placenta, but accumulated in the placental tissue.
In the placenta perfusion model a clear relationship was seen between placental transfer, estimated by the indicative permeability coefficient (IPK) and the (FM-ratio150) and the lipophilicity (logKow). Thus, the higher the logKow, the lower the permeability coefficient (IPK) between foetal and maternal compartments. Glyphosate however does not show this relationship. A linear relationship between IPK and LogKow of r²=0.96 is seen excluding glyphosate from the calculations. In a logarithmic model the IPK values increase by increasing water solubility.
In the skin transport model no clear relationship was observed between molecular weight and Kρ values (Kρ is the permeability coefficient for diffusion across the skin). With increasing molecular weight, the lag-time was increased. The relative deposition in the skin was highest for the lipophilic model compounds. For logKow values between -3.5 and 2 a linear relationship was observed between logKow and logKρ.
For several model substances a considerable lag-time is observed for the skin absorption (dimethoate, bisphenol A, tebuconazol). During placental transfer a lag-time in the same scale is not observed as only a small lag-time is observable for bisphenol A, tebuconazol and methiocarb. The reason is probably a possibility of temporary deposit in the skin compared to the placenta
Our studies demonstrate comparability between dermal and placental transport and common relationships between transport and hydrophilicity of compounds. Antipyrin does not comply with the relations for dermal absorption as antipyrin does not pass the dermal barrier but crosses the placenta and is inscluded as the control substance. The lack of skin penetration is assumed caused by the high water solubility of antipyrine (51.9 g/L) indicating water solubility of importance in skin penetration. Our studies confirm comparability in modelling of the transport across skin and placenta barriers of different origin. The model should be extended with data from more compounds and could potentially be improved through the inclusion of transport data from in vitro transport models using cells resembling placental and dermal tissues.
Our studies demonstrate comparability between dermal and placental passage of chemicals. For both skin- and placental passage of chemicals hydrophilicity, lipophilicity and size is relevant parameters. The observed comparability may be used to extrapolate existing knowledge of the dermal penetration of single substances or groups of substances to an expected placental passage. There will be considerable differences for single substances; also seen in this study, but simple qualitative extrapolation of skin absorption to placenta passage is anticipated. Generally and quantitative extrapolation, however, are not expected.
Reproducibility and validity of the extrapolations should be extended by supplementary placenta- and skin absorption datasets. In the future, such data is expected to be part of QSAR models predicting absorption/passage of specific substances across different barriers. In the long-term and in combination with supplementary in vitro tests the model results are expected to contribute to a reduction in the use of laboratory animals to study the transport of chemicals over biological barriers.
Part of the transport data has already been published and more papers are expected from this project
Mose T, Kjaerstad MB, Mathiesen L, Nielsen JB, Edelfors S, Knudsen LE. Placental passage of benzoic acid, caffeine, and glyphosate in an ex vivo human perfusion system. J Toxicol Environ Health A. 2008;71(15):984-91.
Nielsen JB, Sørensen JA, Nielsen F. The usual suspects - influence of physico-chemical properties on lag-time, skin deposition and percutaneous penetration of nine model compounds. J Toxicol Environ Health. 2008b; In press.
1 Indledning
Akutte forgiftninger med bekæmpelsesmidler ses efterhånden yderst sjældent. Det er lave doser, der er relevante, og det er de særligt sårbare grupper, som fokus i risikovurdering bør rettes imod. Fostre er en særlig sårbar gruppe, idet det ufødte barn har et endnu ufuldstændigt metaboliseringssystem og har vanskeligt ved at eliminere fremmedstoffer, ligesom for eksempel nervesystemet er under fortsat udvikling specielt under den sidste del af graviditeten. Dyreeksperimentelle undersøgelser har vist, at adskillige bekæmpelsesmidler kan påvirke fostrets udvikling (Andersen, 2000). Nogle effekter skyldes en påvirkning af moderen, medens andre effekter er betinget af en transplacental transport og absorption i fostret. Epidemiologiske studier har vist en sammenhæng mellem eksponering for visse bekæmpelsesmidler og forekomst af reproduktionstoksiske effekter (Hanke, 2004). Materialet er dog ikke entydigt og mekanistisk er det svært at skelne mellem følgerne af en toksisk effekt på moderen og en effekt som følge af transplacental transport. Hidtidig human risikovurdering omkring bekæmpelsesmidlers fosterskadelige effekter er primært baseret på dyreeksperimentelle data. Den forskellige struktur og udvikling af placenta i gnavere og mennesker har været et tilbagevendende kritikpunkt ved humane fare- og risikovurderinger baseret på dyreeksperimentelle studier (Carney, 2004; Malassine, 2003).
På grund af forskel i strukturen på placenta fra dyr og mennesker kan overførslen af stoffer være forskellig. Derudover er der forskel i den maternelle-føtale pH-gradient, hvilket kan have betydning for transport af ladede stoffer. Der kan desuden være stor variation i elimination og metabolisme af stoffer i mellem dyr og mennesker, og den aktuelle eksponering af fosteret kan derfor være forskellig. Der foretages ofte en ekstrapolering fra den mest sensitive dyreart til mennesker, men dette kan ofte vise sig at være for konservativt. Mere viden om kinetik og systemisk toksicitet hos mennesker er derfor nødvendig for en mere præcis risikovurdering (Zaretsky, 2004).
Der er derfor et klart og identificeret behov for mere viden om den transplacentale transport, specielt over den humane placenta.
Trofoblast cellelaget i den humane placenta fungerer som en membran og regulerer transporten af stoffer mellem det maternelle og det føtale blod-kammer. Transplacental transport af fremmedstoffer kan ske ved aktiv eller faciliteret transport samt ved passiv diffusion (Carney, 2004). Passiv diffusion anses for den væsentligste transportmekanisme hos både mennesker og gnavere for fremmedstoffer med relativ lille molekylvægt som for eksempel bekæmpelsesmidler (Audus, 1999). På den vis er der klare paralleller til den dermale absorption af fremmedstoffer, hvor den primære barriere for penetration ligger i hornlaget. Der er grund til at antage, at de fysisk-kemiske forhold i form af opløselighed og molekylevægt, der er medbestemmende for hudpenetrationen, har lignende betydning for den passive diffusion over placenta. Det er derfor oplagt at få den mulige analogi belyst gennem sammenlignende studier. Her har man den fordel at kunne anvende allerede eksisterende data fra hudpenetration for bekæmpelsesmidler og fremmedstoffer ((Nielsen, 2004), MST projekt 7041-0334, som omfattede stofferne benzoesyre, caffein, glyphosat, methiocarb, dimethoat). Disse data suppleres med nye stoffer (tebuconazol, bisphenol A, antipyrin og miconazol), således at data på 9 stoffer med et bredt opløseligheds- og molvægtsspektrum opnås.
Det stadigt stigende antal nye stoffer på markedet og ønsket om hurtige og valide metoder til fareidentifikation har øget interessen stærkt for udvikling af (Q)SAR modeller ((Q)SAR – (Quantitative) structure activity relationships – computermodeller, som bruges til forudsigelse af kemiske stoffers egenskaber (Miljøstyrelsen, 2007)). QSAR har også en fremtrædende rolle i EU’s nye kemikalieregulering REACH (Lilienblum, 2008).
Et datasæt indeholdende både percutan og transplacental transport af de samme stoffer giver en oplagt mulighed for udvikling af matematiske modeller for transporten af bekæmpelsesmidler over disse særdeles relevante barrierer. Antallet af stoffer, deres dækning af et bredt opløseligheds- såvel som molekyle størrelsesspektrum vil give særdeles gode muligheder for udvikling af kvantitative modeller, som på sigt vil forventes at reducere behovet for in vivo undersøgelser af fremmedstoffers føtotoksicitet (Hewitt, 2007; Nielsen, 2007).
Den betydeligste pesticideksponering er dermal eller pulmonær med direkte blodtransport til placenta uden forudgående passage gennem leveren og metabolisering i denne. Dog kan der også foregå metabolisering i både hud og lunger inden stofferne transporteres til placenta ligesom metabolisering også kan ske direkte i placenta (Harbison RD, 1995), men denne metabolisering betragtes som begrænset i forhold til metaboliseringen i leveren. Længere tids eksponering kan derfor medføre, at placenta eksponeres for ikke alene udgangsstofferne, men også for metabolitter. Oral eksponering kan i enkelttilfælde efter utilsigtet eksponering være betydende, men denne eksponering vil i givet fald initialt føre til transport til leveren med mulighed for first pass metabolisme før det systemiske kredsløb nås. Metabolisering resulterer oftest i mere hydrofile stoffer med ændret molekylevægt samt ofte tab af funktionelle grupper og detoksificering af stoffet. Dog vil metabolisering i nogle tilfælde netop føre til toksiske stoffer som f.eks. i tilfældet med benz(A)pyren. Dette projekt vil fokusere på generering af generelle data på membranpenetration til anvendelse for modellering, en modellering der også vil forholde sig til penetration af metabolitter med andre fysisk-kemiske karakteristika end udgangsstofferne. Det er imidlertid af analysetekniske årsager ikke muligt at kvantitere alle metabolitterne.
1.1 Projektets målsætning
Projektet har således følgende overordnede mål:
- gennem anvendelse af en række bekæmpelsesmidler/modelstoffer at beskrive betydningen af opløselighed og molekylevægt for den passive absorption over den humane placenta.
- at supplere og komplettere eksisterende viden om bekæmpelsesmidlers dermale penetration ved inkludering af 2 nyere bekæmpelsesmidler af azol-typen.
- at fremkomme med en samlet vurdering af de undersøgte bekæmpelsesmidlers muligheder for passage af de i relation til fostre relevante barrierer, hvilket vil have umiddelbar anvendelse ved fremtidige fare- og risikovurderinger.
- gennem anvendelse af de opnåede data på penetration af såvel huden som placenta at opstille og validere matematiske modeller for percutan og transplacental transport.
De opstillede mål søges nået gennem tre delstudier relateret til henholdsvis transplacental transport, dermal absorption samt modellering af penetrationsdata fra gennemførte dermale og transplacentale eksperimenter.
1.2 Projektets relevans
Til risikovurdering omkring reproduktionstoksikologiske problemstillinger er viden om transport af bekæmpelsesmidler over den humane placenta en mangel. Kun ganske få laboratorier kan gennemføre disse undersøgelser. Ved kobling af erfaring, kendskab til analysekemi, og dermal penetration på SDU med den ved KU etablerede placentamodel, opnås en frugtbar synergi mellem erfaring og innovation. En fungerende matematisk model vil desuden stå stærkt, da den vil bygge på humant materiale og derfor ikke svækkes af usikre dyr-til-menneske ekstrapoleringer. Projektet forventes at generere ny viden omkring faktorer af betydning for transplacental transport, ligesom en bedre udviklet model for absorptionsprocesser på sigt forventes at kunne nedbringe behovet for dyreeksperimentelle undersøgelser. Der er derfor ikke alene et grundvidenskabeligt sigte med dette projekt i forhold til afdækning af faktorer af betydning for bekæmpelsesmidlers passage af membraner og etablering af matematiske modeller herfor, men også klare regulerings- og forebyggelsesmæssige aspekter i forhold til Miljøstyrelsens nuværende rådgivning og regelsætning.
1.3 Internationale samarbejdspartnere
Projektgruppen har via to EU-projekter knyttet tætte forbindelser til en række Europæiske laboratorier, der foretager henholdsvis undersøgelser med humane placenta samt hudpenetrations-undersøgelser. Der er fortsat tæt kontakt til disse laboratorier, og vi vil vedligeholde disse kontakter med henblik på laboratorietekniske erfaringsudvekslinger.
Placentaperfusions-metoden er etableret i Danmark som led i EU-projektet CHILDRENGENONETWORK, hvor Kirsi Vähäkangas i Finland har opbygget metoden og superviseret. Validering af metoden indgår i EU-projektet ReProTect (www.reprotect.com), hvor 4-5 stoffer vil blive testet af såvel den finske som den danske gruppe. Dette samarbejde er videreført i projektet NEWGENERIS (www.newgeneris.org) med risikovurdering af føtal udsættelse for genotoksiske og immunotoksiske fødevarekomponenter.
2 Materialer og metoder
- 2.1 Præsentation af teststoffer
- 2.2 Delstudie 1. Dermal absorption
- 2.3 Delstudie 2. Transplacental transport
- 2.4 Delstudie 3. Modellering
2.1 Præsentation af teststoffer
Teststofferne er valgt ud fra deres opløselighed og molekylevægte idet der ønskes dækning af et bredt opløseligheds- såvel som molekyle størrelsesspektrum for derved at opnå et repræsentativt datasæt med gode muligheder for udvikling af kvantitative modeller.
2.1.1 Antipyrin
| CAS nr.: | 60-80-0 |
| Struktur: | 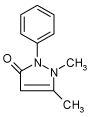 |
| Anvendelse: | Smertestillende middel |
| Molvægt: | 188,1 g/mol |
| Molar volumen: | 162,7 |
| Vand opl.: | 52 g/L |
| LogKow | 0,38 |
| Damptryk: | 4,08 mPa |
| pKa: | 1,4 |
Antipyrin anvendes som intern markør som en del af kvalitetssikringen (positiv kontrol) ved perfusionsforsøgene, idet antipyrin vides at passere placenta relativt uhindret og historiske data eksisterer for sammenligning.
2.1.2 Benzoesyre
| CAS nr.: | 65-85-0 |
| Struktur: | 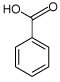 |
| Anvendelse: | Benzoesyre er en svag syre og anvendes til pH-justering og som konserveringsmiddel (fungicid) i føde- og drikkevarer samt i kosmetik industrien |
| Molvægt: | 122 g/mol |
| Molar volumen: | 101,9 |
| Vand opl.: | 3,41 g/L, 25 oC |
| LogKow | 1,87 |
| Damptryk: | 93,3 mPa |
| pKa: | 4,19 |
Benzoesyre optages hurtigt via mave-tarm kanalen og omdannes i leveren til hippursyre. I de aktuelle undersøgelser anvendes radioaktivt mærket ¹4C-Benzoesyre, hvorfor såvel udgangsstoffers som metabolitter detekteres.
2.1.3 Bisphenol A
| CAS nr.: | 80-05-7 |
| Struktur: | 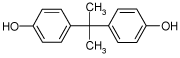 |
| Anvendelse: | Bisphenol A anvendes i en lang række to- eller flerkomponente materialer |
| Molvægt: | 228,28 g/mol |
| Molar volumen: | 199,5 |
| Vand opl.: | 0,12 g/L |
| LogKow | 3,32 |
| Damptryk: | 4 * 10-8 mmHg |
| pKa: | - |
Bisphenol A har stor udbredelse og human eksponering indbefatter såvel oral som dermal eksponering. Målinger fra mennesker viser, at Bisphenol A absorberes hurtigt ved oral eksponering og efterfølgende elimineres via nyrerne i løbet af 24 timer (Volkel, 2002). Den daglige indtagelse af bisphenol A antages at være mellem 0,01-1,18 µg/kg/dag. Serum koncentrationer er målt til 0,2- 20 ng/ml (Ouchi, 2002; Vandenberg, 2007).
Konkret viden om penetrationskinetik over såvel human hud som placenta er sparsom.
Bisphenol A’s størrelse (MW) og opløselighed gør stoffet velvalgt i forhold til allerede testede modelstoffer. Stoffets tilgængelighed som beta-emitter/isotop gør det letanvendeligt i eksperimentelle studier. Samlet set er der ud fra mange prioriteringer tale om et godt modelstof.
I de aktuelle undersøgelser anvendes radioaktivt mærket ¹4C-Bisphenol(A), hvorfor såvel udgangsstoffers som metabolitter detekteres.
2.1.4 Caffein
| CAS nr.: | 58-08-2 |
| Struktur: | 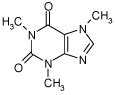 |
| Anvendelse: | Caffein er et trimethylxanthin alkaloid. Caffein er det aktive stof i kaffe, te, cola og energi-drikke |
| Molvægt: | 194,19 g/mol |
| Molar volumen: | 133,3 |
| Vand opl.: | 21,6 g/L, 25 oC |
| LogKow | -0,07 |
| Damptryk: | 2106 mPa |
| pKa: | 10,4 |
Caffein er hydrofilt og optages hurtigt og fuldstændigt over mave-tarm kanalen, kan passere alle organer samt over placenta. Daglig indtagelse af caffein er 4 - 414 mg/person/dag. Ved indtagelse af en kop kaffe opnås f.eks. plasma koncentrationer på 0,25-2,5 mg/ml (Fredholm, 1999; Shapiro, 2007).
I de aktuelle undersøgelser anvendes radioaktivt mærket ¹4C-Caffein, hvorfor såvel udgangsstoffers som metabolitter detekteres.
2.1.5 Dimethoat
| CAS nr.: | 60-51-5 |
| Struktur: | 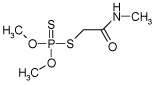 |
| Anvendelse: | Anvendes erhvervsmæssigt til bekæmpelse af fluer, thrips og viklerlarver. Spredes i vandmiljøet og kan muligvis nedvaskes til grundvandet. Er potentielt nedbrydeligt og anses ikke for bioakkumulerende. |
| Molvægt: | 229,26 g/mol |
| Molar volumen: | 175,7 |
| Vand opl.: | 39,8 g/L Farveløse krystaller, der er moderat opløselige i vand |
| LogKow | 0,7 |
| Damptryk: | 0,25 – 1,1 mPa |
| pKa: | - |
Dimethoat optages hurtigt og næsten fuldstændigt over mave-tarm kanalen.
2.1.6 Glyphosat
| CAS nr.: | 1071-83-6 |
| Struktur: | 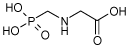 |
| Anvendelse: | Glyphosat er det aktive stof i sprøjtemidlet Roundup. Glyphosat er et non-selektivt ukrudtsmiddel. Stoffet inhiberer enzymet 5-enolpyruvylshikimate-3-phosphatsyntase, hvilket er essentielt for produktionen af chorismat – en intermediær i produktion af aromatiske aminosyrer som phenylalanin, tyrosin og tryptophan. Pattedyr syntetiserer ikke disse aminosyrer og glyphosat virker derfor udelukkende hæmmende for syntesen af disse stoffer i planter. |
| Molvægt: | 169 g/mol |
| Molar volumen: | 100,6 |
| Vand opl.: | 10,5 g/L, 25 oC |
| LogKow | -3,2 |
| Damptryk: | 13,1 mPa |
| pKa: | 2,34 – 10,2 |
Glyphosat optages delvist via mave-tarm kanalen med hurtig udskillelse og akkumuleres ikke. I de aktuelle undersøgelser anvendes radioaktivt mærket ¹4C-Glyphosat, hvorfor såvel udgangsstoffers som metabolitter detekteres.
2.1.7 Methiocarb
| CAS nr.: | 2032-65-7 |
| Struktur: | 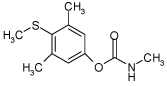 |
| Anvendelse: | Methiocarb anvendes i landbruget til sneglebekæmpelse. |
| Molvægt: | 225,31 g/mol |
| Molar volumen: | 196 |
| Vand opl.: | 0,027 g/L |
| LogKow | 3,34 |
| Damptryk: | 0,036 mPa |
| pKa: | - |
Methiocarb optages næsten fuldstændigt via mave-tarm kanalen med hurtig udskillelse og akkumuleres ikke.
2.1.8 Miconazol
| CAS nr.: | 22916-47-8 |
| Struktur: | 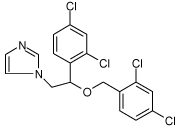 |
| Anvendelse: | Miconazol er et fungicid af azol-typen og anvendes i lægemidler (f.eks. Brentan) til bekæmpelse af svamp. |
| Molvægt: | 416,13 g/mol |
| Molar volumen: | 296 |
| Vand opl.: | Miconazol er praktisk talt uopløseligt i vand; vandopløseligheden er beregnet til 0,000011 g/L |
| LogKow | 5,9 |
| Damptryk: | - |
| pKa: | - |
2.1.9 Tebuconazol
| CAS nr.: | 107534-96-3 |
| Struktur: | 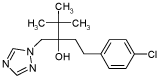 |
| Anvendelse: | Tebuconazol er et fungicid af azol-typen og anvendes som svampemiddel i Danmark |
| Molvægt: | 307,8 g/mol |
| Molar volumen: | 268,1 |
| Vand opl.: | 0,036 g/L, 20 oC |
| LogKow | 3,7 |
| Damptryk: | 0,0017 mPa |
| pKa: | - |
Tebuconazol optages hurtigt og næsten fuldstændigt efter oral administration, og med hurtig udskillelse via fæces (65-80 %) og sekundært via urin (16-35 %). Tebuconazol akkumuleres ikke.
2.2 Delstudie 1. Dermal absorption
2.2.1 Metode
Projektet gennemføres under anvendelse af en in vitro diffusionscellemodel ved anvendelse af human hud (figur 2.2.1). Modellen er beskrevet i OECD´s guidelines for undersøgelse af hudpenetration (OECD, 2003) og er særdeles relevant for denne type undersøgelser (Grandjean, 1990). Modellen tillader kvantitering og sammenligning af både transport igennem og temporær deposition i huden. Modellen har været anvendt på Afdeling for Miljømedicin, SDU i en årrække og laboratoriet har i 2002-2003 deltaget i en EU-finansieret valideringsrunde for hudpenetrationsmodeller. Modellen har vist god overensstemmelse med in vivo resultater fra mennesker (Ramsey, 1994; van de Sandt, 2004b). Modellen er den bedste eksperimentelle mulighed for at tilvejebringe systematisk viden.

Figur 2.2.1. In vitro diffusionscellemodel med anvendelse af human hud som anvendt i dette projekt.
2.2.2 In vitro model
Diffusionscellerne er af håndblæst glas og består af et donorkammer og et receptorkammer. Huden, der stammer fra brystoperationer eller abdominalplastikker foretaget ved læger fra Odense Universitetshospitals plastik-kirurgiske afdeling, monteres mellem de to kamre med hornlaget vendende mod donorkammeret. Udtørring af huden ved fordampning undgås ved at dække donorcellen med parafilm. Receptorvæsken (isotonisk NaCl med 5 % BSA og hexamycin), der fylder receptorkammeret, omrøres konstant (magnetomrøring) for at undgå en koncentrationsgradient mellem top og bund i receptorkammeret. Diffusionscellerne placeres i vandbad (35 oC) for at sikre en temperatur på omkring 32 oC på hudoverfladen, svarende til normal hudtemperatur. Hudens integritet vurderes ved kapacitansmåling før og under forsøg.
2.2.3 Eksperimentelt design
Forsøgene gennemføres med 48 timers eksponering af brugsopløsninger af de valgte stoffer og opsamling af prøver fra receptorvæsken på relevante tidspunkter i dette forløb. Ved afslutning bestemmes den mængde, der resterer i donorkammeret, den i huden deponerede mængde (reservoir-effekt), samt den penetrerede mængde således, at der kan opstilles massebalancer ved forsøgene. Der vil i forsøgene blive anvendt infinite dose for at sikre penetrationskurver med mulighed for bestemmelse af maksimal flux og Kρ. Vi vil anvende 2 bekæmpelsesmidler af azol-typen (miconazol samt tebuconazol). Det er bekæmpelsesmidler, der har fundet stadig stigende anvendelse i Danmark, og for hvilke vi fortsat mangler viden om deres penetrationsegenskaber. Bekæmpelsesmidlerne vil blive appliceret i koncentrationer svarende til de erhvervsmæssigt anvendte.
2.2.4 Variabilitet og statistik og forsøgsplanlægning
Anvendelsen af hud fra forskellige donorer betinger en naturlig heterogenicitet med deraf følgende interindividuel variation, der kan estimeres til omkring 60 %. Med en power på 90 %, et signifikansniveau på 5 % og en standard deviation på 60 % kan den krævede gruppestørrelse anslås til 13-15. Vi kan således opnå valide resultater med gruppestørrelser på 6-8 diffusionsceller per stof (Nielsen, 2000; Nielsen, 2008a) samtidig med, at alle eksperimenter gentages to gange. Tidligere forsøg har vist, at huden opretholder normal barrierefunktion i over 72 timer, hvilket muliggør eksponeringsperioder på 48 timer. Delstudie 1 gennemføres med 2 modelstoffer af azol-typen plus antipyrin og bisphenol A.
2.2.5 Kemiske analyser
Flemming Nielsen (Syddansk Universitet) er ansvarlig for alle kemiske analyser af bekæmpelsesmidler (methiocarb, dimethoate, miconazol og tebuconazol). Udgangspunktet for disse stoffer var analyse ved hjælp af HPLC. Laboratoriet har en betydelig erfaring i analyse af bekæmpelsesmidler fra tidligere projekter (Nielsen, 2000; Nielsen, 2008a). Endvidere er en række modelstoffer anvendt i form af radioaktivt mærkede stoffer (bisphenol A, glyphosat, benzoesyre, caffein), hvilket muliggør anvendelse af ganske lave eksponeringer.
2.3 Delstudie 2. Transplacental transport
2.3.1 Metode
Projektet gennemføres med udgangspunkt i en kendt in-vitro placentaperfusions-model (Miller, 1985; Schneider, 1985). Systemet er siden videreudviklet (Myllynen, 2001; Myllynen, 2003b) og nu etableret på Københavns Universitet (Mose, 2006; Mose, 2007b; Mose, 2007a; Mose, 2008). Der arbejdes med et dobbelt recirkulerende system, hvor moderens og fosterets kredsløb simuleres i en mindre vaskulær enhed, et cotyledon (se figur 2.3.1). I denne forsøgsopstilling kan den føtale og den maternelle side af cotyledonet gennemstrømmes samtidigt, hvilket er forudsætningen for transplacental transport. Den eksperimentelle model medfører, at transporten over placenta, akkumulering i placenta samt metabolisering i placenta, kan bestemmes.
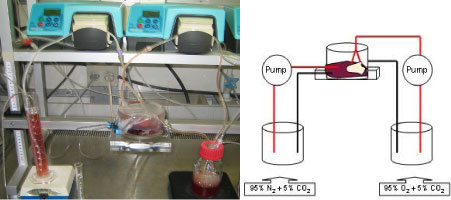
Fig. 2.3.1. Billede samt skematisk fremstilling af det dobbelt recirkulerende perfusionssystem. Det føtale reservoir ses til venstre i opstillingen og det
maternelle til højre. På tegningen er de røde linjer et udtryk for inflow (arterier) til cotyledonet og de sorte et udtryk for outflow (vener).
2.3.2 In vitro model
Placenta og blod indsamles fra ukomplicerede graviditeter og fødsler fra både vaginale fødsler og kejsersnit på Rigshospitalets Fødeafdeling. Placenta afhentes umiddelbart efter fødslen, vejes, navlesnorsblod udtages og næringsvæske tilføres. Fosterets kredsløb simuleres i et enkelt cotyledon ved at kanylere arterie og vene. Cotyledonet isoleres og placeres i perfusionkammer, hvorefter 2 stumpe kanyler tilsluttes det intervilløse rum og derved simulerer det maternelle kredsløb. Flowet på den maternelle og føtale side er henholdsvis 11,5 mL/min og 3,5 mL/min. Perfusionvæsken er en Krebs-Ringer-buffer tilsat heparin, glukose og dextran (føtal 30 g/L, maternalt 8,5 g/L), der i det føtale reservoir mættes med 95 % N2 / 5 % CO2 og i det maternelle med 95 % O2 / 5 % CO2. Væsketab mindskes ved brug af parafilm. Systemet er opsat i en termostateret 37 oC flowbænk, hvor pH, flow, volumentab og pO2 moniteres konstant. Præ-perfusionen gennemføres for at stabilisere placenta inden tilsætning af teststof samt det positive kontrolstof (antipyrin).
Efter præ-perfusion tilsættes 98 ml maternel perfusionsmedie og 1 ml antipyrin sammen med 1 ml af en stamopløsning til opnåelse af valgt slutkoncentration. Stamopløsningerne er enten opløst i vand eller ethanol.
Prøver udtages fra maternel og føtal side inden perfusion og efter 2, 5, 10, 15, 30, 45, 60, 90, 120 og 150 minutter (Mose, 2008).
2.3.3 Eksperimentelt design
Perfusionsforsøgene gennemføres med 2½ timers eksponering. Inden analyse af teststof i de indsamlede prøver, kontrolleres transporten af antipyrin ved hjælp af HPLC-analyse. Teststofferne måles i perfusionsvæskerne efter placental perfusion samt i placentavæv før og efter perfusion. Herved kan stoffernes transportkinetik bestemmes og en sammenhæng fastlægges mellem bekæmpelsesmidlernes opløselighed, størrelse og transportmekanisme. Der anvendes fem teststoffer dækkende et bredt opløseligheds og molvægtsområde (methiocarb, dimethoat, benzoesyre, glyphosat, caffein) for hvilke dermale resultater er tilgængelige fra et tidligere MST-finansieret projekt (MST projekt 7041-0334). Disse er suppleret med to nyere azolforbindelser for hvilke, der ikke findes tilstrækkelig viden om penetrationsevne gennem human hud og placenta, samt stoffet bisphenol A – i alt 8 teststoffer samt antipyrin. Vi tager udgangspunkt i de koncentrationer, der tidligere er målt i receptorkammeret fra hudforsøgene, idet disse koncentrationer er fremkommet efter dermal eksponering for arbejdsmiljørelevante koncentrationer. Der stiles mod bestemmelse af lag-time, FM ratio (CF /CM, der er forholdet mellem koncentrationerne på den føtale side og den maternelle side af cotylidonet), samt den initiale hældning af FM-ratioen som funktion af tiden kaldet den indikative permeabilitetskoefficient (IPK). Denne parameter er et udtryk for transporthastigheden over placentabarrieren. Alle udførte regressioner til beregning af IPK udføres på gennemsnitsværdier. De to valgte azol-forbindelser miconazol samt tebuconazol, er valgt med baggrund i relevans for modellering samt relevant human eksponering.
2.3.4 Etisk godkendelse, tilgængelighed af væv og analyse
Placenta og blod indsamles efter informeret og skriftligt samtykke fra moderen, og data opbevares kodet uden adgang til moderens identitet, jf. godkendelse fra videnskabsetisk komité og datatilsynet. På Rigshospitalet udføres 5-15 planlagte kejsersnit om ugen fordelt på 3 dage, og det tilstræbes at køre forsøg flere dage om ugen. Dette afhænger dog fuldstændig af tilgængelighed og kvalitet af moderkagerne. I flere perioder er det svært at modtage intakte placenta, da iturivning under kejsersnittet hyppigt forekommer. For hvert teststof gennemføres 3-8 perfusioner foruden bestemmelse af baggrundsniveau ved de ikke-radioaktivt mærkede stoffer. De opsamlede prøver analyseres i Odense ved allerede etablerede metoder eller ved radioaktivitetsbestemmelse.
2.4 Delstudie 3. Modellering
2.4.1 Metode
I Delstudie 3 opstilles og afprøves en matematisk model til forudsigelse af hudpenetration og placentatransport. Formålet med modellen er at kunne estimere hudpenetrationens indflydelse på et kemisk stofs (bekæmpelsesmiddels) senere skæbne i kroppen, inklusiv placenta, ud fra dets fysisk-kemiske egenskaber samt en potentiel risiko for fosteret. Der benyttes data fra in vitro undersøgelser af de ni udvalgte modelstoffers transport over henholdsvis human hud og placenta. Disse data er delvis genereret i tidligere undersøgelser (Grandjean, 1990; Nielsen, 2000; Nielsen, 2008a) og dels genereret i dette projekt (Delstudie 1 og Delstudie 2). Modellen baseres på fælles parametre, primært passiv diffusion bestemt af fysisk-kemiske parametre.
Hudens penetration af kemiske stoffer har været modelleret i adskillige år (Borling P, 2001; Engelund EH, 2003; Holmberg RD, 2004). Med udgangspunkt i eksisterende modeller (Berge WF, 2003; Sartorelli, 1998; US EPA, 1992) udvikles en model på baggrund af de data, der genereres i projektet (delstudie 2).
Kendskabet til placentatransport er meget ringe (Frasch, 2002; Myllynen, 2003a). Problemet kompliceres yderligere af, at placenta er et dynamisk organ, der ændrer karakter gennem graviditeten (Gude, 2004). I modelforsøgene anvendes terminale placentaer, som anses for det stadie, hvor placenta er tyndest og dermed det stadie, hvor stoffer må forventes at passere placenta lettest. Som for hudens vedkommende, vil de enkelte stoffers fysisk-kemiske egenskaber og de afledte parametre inddrages i den opstillede model. Der er kendskab til specifikke transportsystemer som f.eks. P2-glycoprotein, ’multidrug resistance proteins’ (MDR, MDP), ’organic anion transporters’ (OAT) og ’organic cation transporters’ (OCT), der kan influere på transporten af modelstofferne (Leazer, 2003; Novotna, 2004; St-Pierre, 2000; St-Pierre, 2004). Der er dog ikke tilstrækkelig viden. Denne del af studiet vil derfor bestå i at opstille en model, der beskriver placentatransport af de uomdannede modelstoffer med forskellige fysisk-kemiske egenskaber. De nødvendige data hertil indhentes fra Delstudie 2.
2.4.2 Eksperimentelt design
For begge organmodellers vedkommende baseres modellen primært på stoffernes fysisk-kemiske egenskaber og de parametre, der kan udledes heraf:
- Molekylvægt (MW)
- Molær volumen
- Lipofilicitet
- Vandopløselighed
- Ionisationsgrad
- Diffusionshastighed
- Lag-time (gennembrudstid)
- Deponeringskapacitet
- Maksimal flux
På grund af den ringe viden vedrørende placentatransport vil den opstillede model i første omgang beskrive placentatransport af de uomdannede bekæmpelsesmidler. Det tilstræbes, at den samme grundmodel kan benyttes til estimering af hudpenetration og placentatransport.
2.4.3 Variabilitet og statistik
Data genereret fra delstudie 1 og 2 (9 forskellige stoffer) anvendes til verificering af modellen til forudsigelse af dermal og placental transport. Verificering af modellen indebærer sammenligninger af kinetikken opnået ud fra de konkrete tal med den computer-estimerede kinetik og ved systematisk at udtrække et stof og undersøge virkningen på modellens statistiske parametre. Verificeringen rummer endvidere sammenligninger med allerede eksisterende humane og dyremodeller. De statistiske bearbejdninger af data foregår med S-PLUS. Fremgangsmåden i verificeringen af modellen vil følge ECVAM’s principper for testvalidering (Hartung, 2004).
3 Resultater
- 3.1 Delstudie 1. Dermal absorption
- 3.2 Delstudie 2. Transplacental transport
- 3.3 Delstudie 3. modellering
3.1 Delstudie 1. Dermal absorption
3.1.1 Antipyrin
Antipyrin er påsat penetrationscellerne i en mængde af 600 µL i en koncentration på 530 µM, svarende til en total antipyrin-mængde på 318 nmol. Antipyrins meget høje vandopløselighed betinger, at der ikke blev set nogen penetration gennem huden under 48 timers observation. Fra huden ekstraheres efter forsøgets afslutning omkring 1 % af den på huden påsatte mængde antipyrin svarende til 3 nmol. Den begrænsede mængde antipyrin deponeret i huden fordeler sig med størstedelen i den mere hydrofile dermis. Den samlede genfinding er ikke højere end godt 80 %. Den resterende mængde må med baggrund i stoffets opløselighedskarakteristika og den manglende penetration forventes at være tabt fra donorkammeret (tabel 3.1.1).
Tabel 3.1.1. Penetrationskarakteristika for dermalt appliceret antipyrin efter 48 timers eksponering for 318 nmol antipyrin. Resultaterne angives som middelværdi ± SD
| Antipyrin | |
| N | 6 |
| Receptor recovery (nmol) | 0,0 ± 0,0 |
| Epidermis deposition (nmol) | 1,1 ± 0,7 |
| Dermis deposition (nmol) | 2,0 ± 1,9 |
| Skin deposition (nmol) | 3,1 ± 2,2 |
| Skin deposition (% of dose) | 1,0 |
| Donor recovery (% of dose) | 80,3 |
| Receptor recovery (% of dose) | 0,0 |
| Overall recovery (% of dose) | 81,3 |
3.1.2 Bisphenol A
Bisphenol A blev påsat i koncentration og mængde på henholdsvis 17,5 mM og 106 µL, svarende til en mængde på 424 µg (1860 nmol).
Over en 48 timers periode genfindes 13 % (242 nmol) af den påsatte mængde bisphenol A i receptorkammeret som udtryk for den dermale penetration. I epidermis og dermis findes henholdsvis 7,4 % (137 nmol) og 17 % (320 nmol) af den påsatte mængde bisphenol A, hvilket er udtryk for den mængde, der er absorberet ind i huden, midlertidigt deponeret og potentielt tilgængelig for efterfølgende penetration. Samlet set vil således mere end en tredjedel af den påsatte mængde bisphenol A i løbet af 48 timer potentielt være tilgængelig for systemiske effekter. Da den samlede genfinding er 82 %, vil dette tal muligvis være lidt større, idet erfaringen viser, at manglende genfinding hyppigst er betinget af tab fra donorkammer under forsøgsafslutning. Modelstoffets opløselighedskarakteristika betinger en større deponering i dermis frem for det mere lipofile epidermis. Betinget af en estimeret lag-time på knap 17 timer sker ovenfor beskrevne dermale penetration med en beregnet maksimal hastighed (flux) på 7,74 nmol/cm²*t (tabel 3.1.2 og figur 3.1.1).
Tabel 3.1.2. Penetrationskarakteristika for dermalt appliceret bisphenol A efter 48 timers eksponering for 1860 nmol. Resultaterne angives som middelværdi ± SD
| Bisphenol A | |
| N | 11 |
| Maximal flux (nmol/cm²*t) | 7,74 ± 3,11 |
| Kρ (µm/t) | 2,1 |
| Lag-time (t) | 16,9 ± 1,1 |
| Donor recovery (nmol) | 826 ± 167 |
| Epidermis deposition (nmol) | 137 ± 30 |
| Dermis deposition (nmol) | 320 ± 120 |
| Skin deposition (nmol) | 457 ± 108 |
| Skin deposition (% of dose) | 24,6 |
| Donor recovery (% of dose) | 44,5 |
| Receptor recovery (% of dose) | 13,0 |
| Overall recovery (% of dose) | 82,1 |
| Skin penetration (nmol/cm²) | |
| T = 0 t | 0,0 ± 0,0 |
| T = 2 t | 0,0 ± 0,0 |
| T = 4 t | 0,0 ± 0,0 |
| T = 6 t | 0,44 ± 0,44 |
| T = 8 t | 1,75 ± 1,31 |
| T = 12 t | 7,89 ± 4,82 |
| T = 24 t | 56,51 ± 27,16 |
| T = 30 t | 101,19 ± 47,31 |
| T = 48 t | 242,25 ± 101,19 |
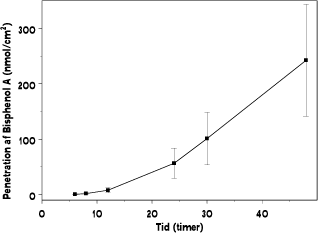
Figur 3.1.1. Dermal penetration af bisphenol A over 48 timer efter initial topikal applicering af 1860 nmol.
3.1.3 Miconazol
Hver celle blev påsat 600 µL miconazol i en koncentration på 4 mM svarende til en mængde på 2400 nmol.
En observationsperiode på 48 timer resulterede ikke i nogen sporbar mængde miconazol i receptorkammeret, og således ingen dermal penetration af miconazol (tabel 3.1.3). Årsagen skal sandsynligvis findes i miconazols meget høje lipofilicitet udtrykt ved en logKow-værdi på omkring 6, der virker bremsende for passage gennem specielt dermis. Miconazol er dog i et vist omfang i stand til at absorberes i huden. Således findes omkring 8 % af den påsatte mængde miconazol i huden ved forsøgsafslutning efter 48 timer. Der er tale om en lidt større mængde miconazol deponeret i dermis i forhold til epidermis.
Tabel 3.1.3. Penetrationskarakteristika for dermalt appliceret miconazol efter 48 timers eksponering for 2400 nmol miconazol. Resultaterne angives som middelværdi ± SD
| Miconazol | |
| N | 6 |
| Receptor recovery (nmol) | 0,0 ± 0,0 |
| Epidermis deposition (nmol) | 83,2 ± 15,3 |
| Dermis deposition (nmol) | 114,6 ± 10,8 |
| Skin deposition (nmol) | 200,9 ± 14,7 |
| Skin deposition (% of dose) | 8,4 |
| Donor recovery (% of dose) | n.d. |
| Receptor recovery (% of dose) | 0,0 |
| Overall recovery (% of dose) | n.d. |
3.1.4 Tebuconazol
Hver celle blev påsat 600 µL Tebuconazol i en koncentration på 200 µM svarende til en mængde på 120 nmol.
Ved forsøgsafslutning efter 48 timer genfindes en fjerdedel af det påsatte tebuconazol i receptorkammeret efter penetration af huden. Tilbage i huden sidder endnu 40 % af den påsatte mængde fordelt med en tredjedel i epidermis og to tredjedele i dermis (tabel 3.1.4 og figur 3.1.2). Det i huden deponerede tebuconazol vil potentielt kunne penetrere huden, således at man samlet vil kunne nå op på at 2/3 af den applicerede dosis efter 48 timers eksponering vil være potentielt tilgængelig for systemisk påvirkning. Den samlede genfinding er 100 % i dette forsøg og de opnåede spredninger er tilfredsstillende lave.
Lag-time estimeres til 14 timer, og ud fra den efterfølgende initiale penetrationsfase bestemmes den maksimale flux til at være 0,6 nmol/cm²*t.
Tabel 3.1.4. Penetrationskarakteristika for dermalt appliceret tebuconazol efter 48 timers eksponering for 120 nmol tebuconazol. Resultaterne angives som middelværdi ± SD
| Tebuconazol | |
| N | 6 |
| Maximal flux (nmol/cm²*t) | 0,57 ± 0,16 |
| Kρ (µm/t) | 28,5 |
| Lag-time (t) | 14,0 ± 0,0 |
| Donor recovery (nmol) | 47,4 ± 8,4 |
| Epidermis deposition (nmol) | 16,5 ± 2,5 |
| Dermis deposition (nmol) | 32,3 ± 8,2 |
| Skin deposition (nmol) | 48,8 ± 7,6 |
| Skin deposition (% of dose) | 40,7 |
| Donor recovery (% of dose) | 39,5 |
| Receptor recovery (% of dose) | 24,7 |
| Overall recovery (% of dose) | 104,9 |
| Skin penetration (nmol/cm²) | |
| T = 0 t | 0,0 ± 0,0 |
| T = 2 t | 0,0 ± 0,0 |
| T = 4 t | 0,0 ± 0,0 |
| T = 6 t | 0,0 ± 0,0 |
| T = 8 t | 0,0 ± 0,0 |
| T = 12 t | 0,0 ± 0,0 |
| T = 24 t | 5,6 ± 1,6 |
| T = 30 t | 9,1 ± 2,6 |
| T = 48 t | 14,0 ± 2,1 |
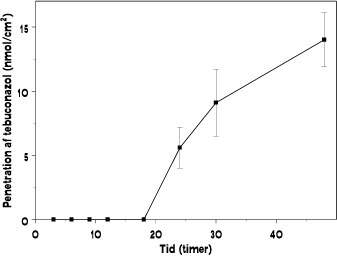
Figur 3.1.2. Dermal penetration af tebuconazol over 48 timer efter initial topikal applicering af 120 nmol.
3.2 Delstudie 2. Transplacental transport
3.2.1 Antipyrin
Antipyrin anvendes som intern markør som en del af kvalitetssikringen (positiv kontrol) ved perfusionsforsøgene, idet antipyrin vides at passere placenta relativt uhindret og historiske data eksisterer for sammenligning. Hvis resultater for antipyrin indikerer en ikke-velfungerende placenta, anvendes data for et givent modelstof opnået med denne perfusion ikke.
Nedenfor er angivet antipyrins perfusion gennem velfungerende placentaer i et udvalgt antal vellykkede forsøg fra dette projekt (fra forsøg med benzoesyre, caffein og glyphosat) (Figur 3.2.1). Figuren viser hvorledes koncentrationen stiger på den føtale side stiger samtidig med et tilsvarende fald i koncentrationen af antipyrin på den maternelle side. Efter godt to timer er der opnået en ligevægt, hvor samme koncentration af antipyrin ses i begge kredsløb, hvilket også illustreres ved, at FM-ratioen er 1 (Figur 3.2.1).
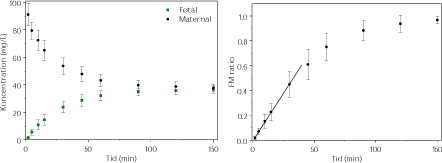
Figur 3.2.1. Perfusion med Antipyrin (100 mg/L og n=19 fra studier med modelstofferne benzoesyre, caffein og benzoesyre). FM-ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM-ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM-ratioen. IPK er beskrevet ved ligningen y = 0,0153x – 0,0069 (r² = 0,9991) og udregnet for tidsrummet 0-30 min.
3.2.2 ¹4C-Benzoesyre
Det første stof, der blev testet var benzoesyre i en koncentration på 32,8 mM, da det er den koncentration, der er testet på huden. Koncentrationen var imidlertid toksisk for placenta-vævet. Benzoesyre er derfor testet i en lavere og ikke-placentatoksisk koncentration på 200 µM. Der er gennemført 5 vellykkede perfusioner, der viser, at benzoesyre transporteres over placenta (Figur 3.2.2). Resultaterne er rapporteret i (Mose, 2008).
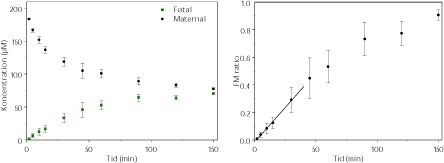
Figur 3.2.2. Perfusion med ¹4C-Benzoesyre (N=5). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0103x – 0,0173 (r² = 0,9985) og udregnet for tidsrummet 0-30 min.
3.2.3 Bisphenol A
Der er gennemført 3 vellykkede perfusioner med 0,5 µM Bisphenol A i Krebs-Ringer-buffer, som viser meget langsom transport (figur 3.2.3). Undersøgelser med humant albumin i mediet pågår i projektet NEWGENERIS og data tyder på carrier effekt af albumin, hvilket øger transporten. Data er ikke publiceret endnu. Data fra to forsøg, som lækkede i slutningen af undersøgelsesperioden, viser samme transportmønster – data ikke vist.
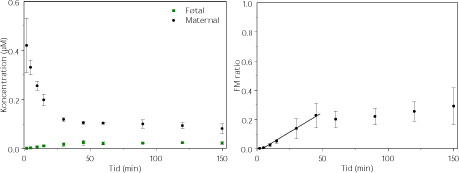
Figur 3.2.3. Perfusion med bisphenol A (N=3). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0054x – 0,022 (r2 = 0,9918) og udregnet for tidsrummet 0-45 min.
3.2.4 ¹4C-Caffein
Caffein er testet ved henholdsvis 10 og 200 µM med i alt 7 vellykkede perfusioner (4 perfusioner med 200µM og tre perfusioner med 10µM). Caffein transporteres over placenta på samme vis som benzoesyre. Dataanalyser viser, at man opnår en udligning af koncentrationsgradienten mellem den maternelle og føtale side i løbet af ca. to timer, hvilket svarer til en hastighed som observeret for antipyrin. (figur 3.2.4 og 3.2.5) (Mose, 2008). Der beregnes samme IPK for eksperimenterne med henholdsvis 10 og 200 µM caffein. Det indikerer, at der er tale om en koncentrationsafhængig passiv diffusion samt, at den anvendte eksperimentelle model er valid.
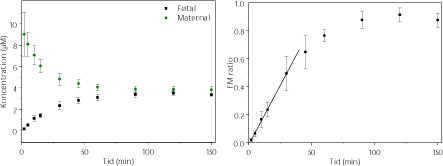
Figur 3.2.4. Perfusion med 14C-Caffein (10 µM og N=3). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0170x – 0,0141 (r2 = 0,9988) og udregnet for tidsrummet 0-30 min.
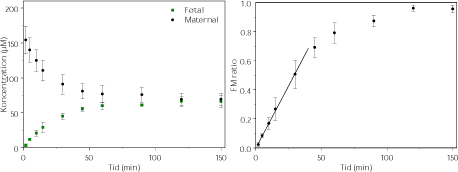
Figur 3.2.5. Perfusion med ¹4C-Caffein (200 µM og N=4). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0171x – 0,0086 (r² = 0,9994) og udregnet for tidsrummet 0-30 min.
3.2.5 Dimethoat
Dimethoat er testet ved 100 µM i 2 vellykkede perfusioner. Dimethoat bliver transporteret over placenta (figur 3.2.6). Dataanalyser viser, at man ikke opnår en udligning af koncentrationsgradienten mellem den maternelle og føtale side i løbet af omkring to timer. Som det ses af figuren, er der store afvigelser i de vellykkede perfusioner, hvilket der ikke umiddelbart findes en forklaring på. Der er data for flere perfusioner, der imidlertid ikke var vellykkede som følge af læk.
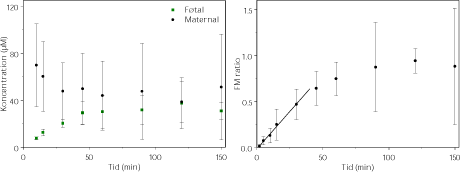
Figur 3.2.6. Perfusion med dimethoat (N=2). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0163x – 0,0157 (r² = 0,9937) og udregnet for tidsrummet 0-30 min.
3.2.6 ¹4C-Glyphosat
Glyphosat er testet ved 200 µM med i alt 7 vellykkede perfusioner. Det ser ud til, at glyphosat transporteres over placenta, men i mindre grad end f.eks. caffein. Glyphosat ophobes ikke i vævet. Resultaterne viser, at man efter 2½ timer fortsat har omkring 3 gange så høj koncentration af glyphosat på den maternelle side i forhold til den føtale (figur 3.2.7) (Mose, 2008).
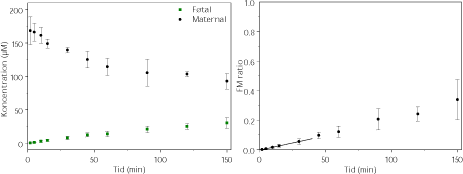
Figur 3.2.7. Perfusion med ¹4C-Glyphosat (N=7). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0019x – 0,0091 (r² = 0,9998) og udregnet for tidsrummet 0-30 min.
3.2.7 Methiocarb
Der er udført et vellykket og et mindre vellykket forsøg, som viser manglende overførsel (figur 3.2.8). Der overføres næsten ikke noget stof til den føtale side, men vævskoncentrationerne er meget høje. Dette kan forklares med ophobning i placentavævet, hvor der måles betydelige koncentrationer mellem 12 og 59 µM i ekstraktioner fra de perfunderede cotyledoner. Den høje FM ratio er i dette tilfælde derfor ikke udtryk for en stor transport over placenta, men bare udtryk for at det forsvinder fra den maternelle side.
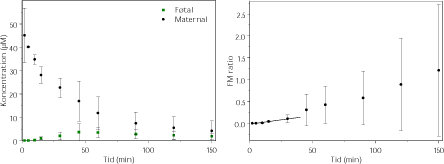
Figur 3.2.8. Perfusion med methiocarb (N=2). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0039x – 0,0179 (r² = 0,9658) og udregnet for tidsrummet 0-30 min.
3.2.8 Miconazol
Der blev først udført et indledende forsøg med miconazol med 60 og 200 µM. Grundet problemer med at opløse miconazol blev 60 µM valgt som testkoncentration i undersøgelserne. Der blev gennemført 4 vellykkede perfusioner med 60 µM. Miconazol bliver tilsyneladende ikke transporteret over placenta, men ophobes i placentavævet. Dette ses ved, at miconazol-koncentrationen mindskes i den maternelle side over tid uden en tilsvarende stigning i koncentrationen af miconazol på den føtale side (figur 3.2.9). Det kan dog også skyldes, at miconazol bindes til materialer i forsøgsopstillingen, men dette er ikke særligt sandsynlig vurderet ud fra en ”slangetest”. I slangetesten uden placentavæv i forsøgsopstillingen fandt vi, at miconazol (100 µM) udfælder og ikke er vandopløseligt. Ved slangetest uden placenta men med blodceller kunne 100 µM opløses og detekteres, idet miconazol bindes til plasmaproteiner.
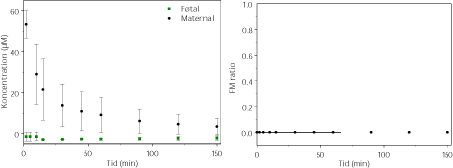
Figur 3.2.9. Perfusion med Miconazol (60 µM og N=2). FM ratioen angiver forholdet CF/CM, men da FM-ratioen ikke kan være negativ sættes det for miconazol til 0.
3.2.9 Tebuconazol
Der er udført 2 perfusioner med 200 µM tebuconazol (figur 3.2.10). Tebuconazol forsvinder fra den maternelle side, men genfindes ikke tilsvarende på den føtale side målt som FM-ratio. Transporten over placenta er begrænset, hvilket sandsynligvis skyldes ophobning af tebuconazol i placentavævet og eventuelt metabolisering. Vi har dog ikke været i stand til at detektere metabolitter.
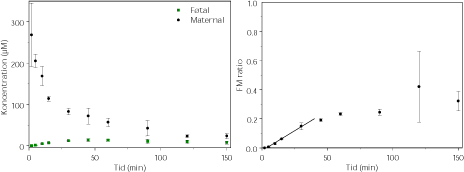
Figur 3.2.10. Perfusion med tebuconazol (N=2). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0055x – 0,0187 (r² = 0,9917) og udregnet for tidsrummet 0-30 min.
3.3 Delstudie 3. modellering
3.3.1 Dermal absorption
3.3.1.1 Faktorer af betydning for dermal absorption
Diffusion gennem hud kan foregå ved passiv diffusion eller som en aktiv transport. Den passive diffusion kan beskrives ved Ficks lov, der siger, at steady-state flux er lig permeabilitetskoefficienten gange koncentrationsforskellen over huden: Jss = Kρ ΔC.
Ved udregning af den dermale absorption er der især tre faktorer, der ses på. Disse er:
- Lag-time (timer)
- Flux (nmol/cm² time)
- Kρ (µm/time)
Lag-time beskriver tiden fra eksponering til gennembrud af huden, og stoffet kan måles i plasma. For lipofile stoffer, der hellere vil befinde sig i det lipofile miljø i hornlaget end i det hydrofile miljø på den anden side af hornlaget, vil man ofte se en lang lag-time. Hydrofile stoffer vil gennembryde hurtigere huden og har derfor en kort lag-time.
Flux’en beskriver den mængde af stof påført huden (i nmol/cm²), der kan gennembryde huden pr tidsenhed. Steady-state flux er en simpel måde til beskrivelse af permeabiliteten af molekyler over huden. For at steady-state kan opnås, må der gå et tidsrum efter den første kontakt med huden til ligevægt kan indstille sig.
Især for lipofile stoffer vil der i den første periode af eksponeringen ske en større transport af stof ind i huden i forhold til transport fra hud til plasma. Der vil altså opbygges et depot i huden. I særlige tilfælde ses det, at der kun sker en begrænset transport fra hud til plasma. I disse tilfælde vil en mætning af hudens depoter virke som en begrænsende faktor på flux’en.
Kρ er permeabilitetskoefficienten er en konstant, som udtrykker den hastighed, hvormed et givet stof kan penetrere huden (µm/time).
Der er mange faktorer, som har betydning for, om der sker en hudpenetration eller ej i et givet tilfælde. Nogle af de i litteraturen nævnte faktorer er:
- Fysisk-kemiske egenskaber for stoffet
- Vehikeleffekter + vehiklens egenskaber
- Hudens tilstand (sygdomme) og dermed hudens barriereegenskab
- Hudområde (arm, inderlår, håndflade, fodsål osv.)
- Hudens fugtighed
- Køn og alder
- Metabolisme i huden
Da mange ting kan influere på hudpenetrationen, vanskeliggør det opbygningen af en model til forudsigelse af hudpenetration.
3.3.1.2 Testdata
Ni kemiske stoffers penetration gennem huden er blevet undersøgt in vitro med human hud. Data om stofferne glyphosat, caffein, dimethoat, benzoesyre og methiocarb stammer fra tidligere undersøgelser (Nielsen, 2000; Nielsen, 2008a; van de Sandt, 2004a), mens bisphenol A, tebuconazol, antipyrin og miconazol er undersøgt indenfor dette projekts rammer.
Modelstofferne er udvalgt således at der indenfor gruppen findes et bredt udvalg af stoffer med forskellig opløselighedsprofil (logKow) samt molekylestørrelse (se tabel 3.3.1).
Tabel 3.3.1. For de undersøgte modelstoffer er de fysisk-kemiske parametre logKow, molekylevægt (MW), molar volumen, vandopløselighed, damptryk (Vp) og ioniseringsgrad (pKa) angivet. Modelstofferne er nævnt rækkefølge med stoffet med laveste logKow værdi
| Stofnavn | logKow | MW (g/mol) |
Molar Volumen | Vandopl. (g/L) |
Vp (mPa) |
pKa |
| Glyphosat | - 3,2 | 169,07 | 100,6 | 10,5 | 13,1 | 2,34 – 10,2 |
| Caffein | - 0,07 | 194,19 | 133,3 | 21,6 | 2106 | 10,4 |
| Antipyrin | 0,38 | 188,25 | 162,7 | 51,9 | 4,08 | 1,4 |
| Dimethoat | 0,7 | 229,26 | 175,7 | 23,8 | 0,25 – 1,1 | - |
| Benzoesyre | 1,87 | 122,13 | 101,9 | 3,41 | 93,3 | 4,19 |
| Bisphenol A | 3,32 | 228,28 | 199,5 | 0,12 | 4x10-8 | - |
| Methiocarb | 3,34 | 225,31 | 196,0 | 0,027 | 0,036 | - |
| Tebuconazol | 3,7 | 307,8 | 268,1 | 0,036 | 0,0017 | - |
| Miconazol | 5,9 | 416,13 | 296 | 0,000011 | - | - |
De målte og udregnede parametre Kρ, lag-time, koncentration målt i hud og receptorkammer (absorberede mængde) samt den maximale hastighed (flux) er angivet i tabel 3.3.2 for de undersøgte modelstoffer.
Som det ses i tabel 3.3.2 er der indenfor gruppen af modelstoffer eksempler på stoffer, der ikke transporteres over den dermale barriere (f.eks. antipyrin og miconazol), mens andre stoffer nærmest uhindret transporteres igennem huden (f.eks. benzoesyre).
Benzoesyre er det stof, som skiller sig mest ud blandt de undersøgte modelstoffer idet dets penetrationskurve adskiller sig væsentlig fra de andre stoffer. Som det ses i figur 3.3.1, opnås der for benzoesyre ligevægt i løbet af den eksperimentelle periode på 48 timer. Benzoesyre er det mindste af de testede stoffer med en molekylevægt på kun 122 g/mol. Derudover har den en logKow på 1,87.
Caffein og bisphenol A har den højeste hudpenetration næstefter benzoesyre af de testede stoffer målt som nmol/cm², mens dimethoat, glyphosat, methiocarb og tebuconazol har et ensartet penetrationsmønster illustreret i figur 3.3.2. Miconazol og antipyrin optages ikke over huden og er derfor ikke medtaget i figur 3.3.2.
Tabel 3.3.2. Parametrene Kρ, lag-time, relativ hud deposit, relativ receptor recovery (absorberet mængde) samt den maksimale flux er opgivet som gennemsnit ± SD. Den eksperimentelle periode var 48 timer
| Stofnavn | Antal studier (N) |
Kρ (µm/t) |
Lag-time (timer) |
Hud deposit (% af dosis) |
Absorberet mængde (% af dosis) |
Maksimal flux (nmol/cm²·t) |
| Glyphosat | 14 | 0,06 | 7,9 ±5,7 | 0,7 ± 0,1 | 0,4 ± 0,1 | 0,14 ± 0,06 |
| Caffein | 17 | 3,8 | 6,9 ± 1,7 | 7,0 ± 4,3 | 18,7 ± 8,5 | 7,78 ± 5,0 |
| Antipyrin | 6 | - | - | 3,2 ± 2,24 | 0 | - |
| Dimethoat | 14 | 4,9 | 22,3 ± 4,4 | 1,9 ± 0,2 | 5,1 ± 0,8 | 0,49 ± 0,26 |
| Benzoesyre | 16 | 50,6 | 1,5 ± 1,0 | 1,5 ± 0,1 | 93,4 ± 0,7 | 165,4 ± 36,0 |
| Bisphenol A | 11 | 2,1 | 16,9 ± 1,1 | 24,6 ± 5,8 | 13,0 ± 5,4 | 7,74 ± 3,11 |
| Methiocarb | 14 | 38,6 | 11,7 ± 6,1 | 26,0 ± 3,6 | 50,9 ± 4,9 | 0,54 ± 0,14 |
| Tebuconazol | 6 | 28,5 | 14,0 ± 0,0 | 40,7 ± 6,3 | 24,7 ± 1,8 | 0,57 ± 0,16 |
| Miconazol | 6 | - | - | 8,4 ± 0,6 | 0 | - |
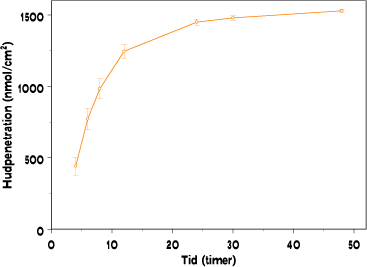
Figur 3.3.1: Hudpenetration som funktion af tiden for modelstoffet benzoesyre.
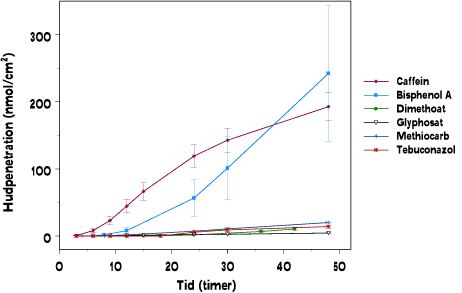
Figur 3.3.2: Hudpenetration som funktion af tiden for 6 af de 7 modelstoffer; Glyphosat, caffein, tebuconazol, bisphenol A, dimethoat og methiocarb. Stofferne Antipyrin og Miconazol er blevet undersøgt, men stofferne blev ikke transporteret over den dermal barriere og derfor ikke medtaget i figuren.
3.3.1.3 Fysisk-kemiske parametre med betydning for transport over huden
Der er gennem de sidste årtier arbejdet med udvikling af både simple modeller baseret på fysisk-kemiske parametre og mere komplicerede farmakokinetiske modeller (PK modeller) til beskrivelse af kemiske stoffers transport over huden (Moss, 2002).
De målte og beregnede hud parametre (Kρ, flux, lag-time, relativ hud-deposit, relativ absorberet mængde og den samlede absorberede mængde inkl. mængden fundet i huden) er afbildet som funktion af en række fysisk-kemiske parametre (figur 3.3.3, 3.3.5 og 3.3.8). Herved kan det vurderes om, der for modelstofferne findes en korrelation mellem nogle af faktorerne (figur 3.3.4, 3.3.6, 3.3.7 og 3.3.9).
Der er en tendens til, at den højeste Kρ findes for stoffer med en logKow i intervallet 1 - 4. Bisphenol A følger dog ikke denne tendens (logKow = 3,32 og Kρ = 2,1 µm/t). Hvis logKρ afbildes som funktion af logKow (figur 3.3.4) ses, at der for stoffer med logKow under 2 er en klar lineær sammenhæng med stigende logKρ værdier ved stigende logKow værdier. For modelstofferne med logKow over to ses en tendens til en konstant til faldende logKρ ved stigende logKow.
Der er ingen sammenhæng mellem den målte maksimale flux og logKow. For de 9 modelstoffer er fluxen =< 10 nmol/cm²·t, undtaget er benzoesyre, der har en meget høj flux på 165 nmol/cm²·t.
Der er en tendens til, at den relative mængde deponeret i huden stiger med en stigende lipofilicitet, dvs. stigende logKow undtagen for meget hydrofile stoffer (glyphosat) og meget lipofile stoffer (miconazol). Statistisk er denne tendens dog ikke robust. Benzoesyre ser ud til at afvige fra denne ”regel”.
Den mængde, som optages gennem huden (både ekskl. og inkl. mængden genfundet i huden) følger samme mønster som Kρ.
![Figur 3.3.3. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af logKow. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]](images/s42.gif)
Figur 3.3.3. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af logKow. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]
![Figur 3.3.4. Lineær regression mellem logKρ og logKow med ligningen Y = 0,5561x + 0,5354 (r² = 0,9822). Kun modelstofferne Glyphosat, Caffeine, Dimethoat og Benzoesyre med en logKow under 2 er medtaget i regression (de andre stoffer er markeret med en ring). Der er ikke målt Kρ værdi for stofferne Antipyrin og Miconazol og disse er derfor udeladt af figuren. [Gly: glyphosat, Caf: caffein, Dim: Dimethoat, Ben: benzoesyre, Met: Methiocarb, Teb:Tebuconazol, Bis: Bisphenol A].](images/s43.gif)
Figur 3.3.4. Lineær regression mellem logKρ og logKow med ligningen Y = 0,5561x + 0,5354 (r² = 0,9822). Kun modelstofferne Glyphosat, Caffeine, Dimethoat og Benzoesyre med en logKow under 2 er medtaget i regression (de andre stoffer er markeret med en ring). Der er ikke målt Kρ værdi for stofferne Antipyrin og Miconazol og disse er derfor udeladt af figuren. [Gly: glyphosat, Caf: caffein, Dim: Dimethoat, Ben: benzoesyre, Met: Methiocarb, Teb:Tebuconazol, Bis: Bisphenol A].
I figur 3.3.5 indikeres en lineær sammenhæng mellem lag-time og stoffernes molekylevægt. Det ser dog ud som om, dimethoat har en væsentlig længere lag-time end trenden i kurven. En regressionsanalyse udført på data viser, at lag-tidens funktion af molekylevægten kan beskrives ved ligningen y = 0,07x – 5,2 (r² = 0,67), når dimethoat udelades, og y = 0,0845x – 6,6483 (r² = 0,4467), når dimethoat medtages i regressionen (figur 3.3.6). Antipyrin og miconazol ikke er medtaget i regressionen, da der ikke er fundet en lag-time for disse to modelstoffer. Deres lag-time må anses for længere end de 48 timer som studierne varer.
Ligeledes kan den relative mængde stof fundet i huden (dermis + epidermis) beskrives ved en lineær sammenhæng (y = 0,2298x – 34,5986; r² = 0,6755), hvor en stigende molekylevægt betinger en stigende mængde stof deponeret i hudlagene (figur 3.3.7). Dette indikerer, at stigende molekylestørrelse gør det sværere at passere den dermale barriere. Det ser dog ud til, at dimethoat ikke følger denne tendens, da stoffet har en væsentlig lavere mængde deponeret i huden (1,9 %) end trenden i dette plot indikerer (y = 0,2493x – 36,294; r² = 0,8527, når dimethoat udelades af regressionen). Miconazol, der er et stort molekyle (416 g/mol), som på mange punkter er et ’yderstof’ i gruppen af modelstoffer. Miconazol følger da heller ikke trenden i regressionen, idet der kun blev fundet 8,4 % i huden.
![Figur 3.3.5. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af molekylevægten. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Mic: Miconazol; Teb: Tebuconazol; Met: Methiocarb]](images/s44a.gif)
Figur 3.3.5. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af molekylevægten. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Mic: Miconazol; Teb: Tebuconazol; Met: Methiocarb]
![Figur 3.3.6. Lineær regression af forholdet mellem lag-time og modelstoffernes molekylevægt med ligningen Y = 0,0845x -6,6483 (r² = 0,4467). Der er ikke målt en lag-time for Antipyrin og Miconazol, hvorfor deres værdig er sat til > 48 timer – disse to stoffer falder derfor udenfor tendensen og er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]](images/s44b.gif)
Figur 3.3.6. Lineær regression af forholdet mellem lag-time og modelstoffernes molekylevægt med ligningen Y = 0,0845x -6,6483 (r² = 0,4467). Der er ikke målt en lag-time for Antipyrin og Miconazol, hvorfor deres værdig er sat til > 48 timer – disse to stoffer falder derfor udenfor tendensen og er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]
![Figur 3.3.7. Lineær regression af forholdet mellem koncentration fundet i huden (epidermis + dermis) og modelstoffernes molekylevægt beskrevet ved ligningen Y = 0,2493x – 36,294 (r² = 0,8527). Dimethoat og miconazol synes at have en lavere mængde stof deponeret i huden i forhold til hvad tendensen i dette plot indikerer hvorfor de er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]](images/s45.gif)
Figur 3.3.7. Lineær regression af forholdet mellem koncentration fundet i huden (epidermis + dermis) og modelstoffernes molekylevægt beskrevet ved ligningen Y = 0,2493x – 36,294 (r² = 0,8527). Dimethoat og miconazol synes at have en lavere mængde stof deponeret i huden i forhold til hvad tendensen i dette plot indikerer hvorfor de er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]
Hudparametrenes sammenhæng med modelstoffernes vandopløselighed er afbilledet i figur 3.3.8
Der er en tendens til at en stigende vandopløselighed medfører en faldende Kρ. Dette blev undersøgt yderligere i figur 6.3.9, hvor logKρ blev afbilledet som funktion af logaritmen til vandopløseligheden. Dog viser figuren at den lineære sammenhæng er meget svag.
Den mængde, som optages gennem huden (både ekskl. og inkl. mængden genfundet i huden) følger samme mønster som Kρ.
![Figur 6.3.8. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af vandopløseligheden. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s46a.gif)
Figur 6.3.8. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af vandopløseligheden. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.9. Forholdet mellem logKρ og modelstoffernes vandopløselighed (Log). Der er ingen Kρ fundet for stofferne antipyrin og miconazol og de er derfor ikke medtaget i plottet. [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].](images/s46b.gif)
Figur 3.3.9. Forholdet mellem logKρ og modelstoffernes vandopløselighed (Log). Der er ingen Kρ fundet for stofferne antipyrin og miconazol og de er derfor ikke medtaget i plottet. [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].
3.3.1.4 Matematiske modeller
Permeabilitetskoefficienten Kρ er som tidligere nævnt den hastighed, hvormed et givet stof kan penetrere huden (cm/time). Der er udviklet en del formler til beregning af Kρ, hvoraf projektgruppen tidligere har afprøvet flere af modellerne (Engelund EH, 2003; Holmberg RD, 2004). Nedenfor er en model til beregning af Kρ beskrevet.
Potts & Guy
Potts og Guy har i 1990’erne udviklet en model til beregning af Kρ, som nok i dag er den mest anvendte simple model (Guy, 1993). Kρ beregnes ved hjælp af følgende formel:
| (målt i cm/time) |
SkinPerm
SkinPerm modellen er udviklet af W.F. ten Berge fra Holland og er primært udviklet til at beskrive hudabsorption og anvendes som risikovurderingsværktøj i forbindelse med eksponering via arbejdsmiljøet (Berge WF, 2003). Modellen er primært baseret på fysisk-kemiske data på det enkelte stof såsom logKow.
Modellen er baseret på en antagelse om, at den drivende kraft ind i huden kun opnås ved den mængde stof, der kan opløses i et vandigt lag på huden (Berge WF, 2003). Yderligere kan modellen kun anvendes for ikke ioniserede stoffer, der ikke virker irriterende på huden, ikke virker affedtende samt kan penetrere huden hurtigere end stoffet er metaboliseret i huden (Berge WF, 2003).
SkinPerm modellen betegner huden som en barriere, der består af følgende komponenter:
- Protein lag i hornlaget
- Lipid lag i hornlag
- Vandigt lag under hornlaget, hvorigennem stofferne skal penetrere for at nå blodbanen
Modellen beskriver hudpenetrationen vha. Kp (permeabilitetskoefficienten) udtrykt som:
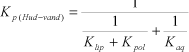 |
(cm/time) |
hvor:
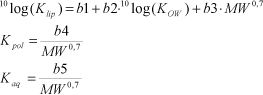
Klip er permeabilitetskoefficienteten i lipidlaget
Kpol er permeabilitetskoefficienteten i proteinlaget
Kaq er permeabilitetskoefficienteten i det vandige lag
KOW er oktanol/vand fordelingskoefficienteten
MW er molekylevægten
b1 (-2,59), b2 (0,7318), b3 (-0,006832), b4 (0,043) og b5 (1,361) er regressionskoefficienter
Skinperm modellen er bygget på Flynn’s datasæt (Flynn, 1990), der i vid udstrækning er blevet brugt til opbygning af modeller til beregning af Kp. De fem anvendte regressionskoefficienter er fundet ud fra Flynn’s datasæt og anvendt i modellen. Flynn’s datasæt er i høj grad koncentreret om stoffer med logKow omkring 0 til 4 og derfor beskrives stoffer med logKow <0 eller >4 ikke godt i modellen.
Modellen beregner en flux vha. følgende formel:
![]()
Hvor Ws er vandopløseligheden, som beregnes vha. formlen:
| (mg/cm³), der beskriver vandopløseligheden. |
Flux’en er begrænset af stoffets vandopløselighed, idet stoffet inden det kan passere ind i blodbanen skal trænge gennem det vandige lag lige under hornlaget.
3.3.1.5 Prædiktive hudabsorptionsværdier
På baggrund af allerede kendte simple matematiske modeller for estimering af transport over den dermale barrierer er prædikterede Kρ-værdier udregnet for modelstofferne (tabel 3.3.3.).
Tabel 3.3.3. Prædikterede Kρ-værdier beregnet vha. modellerne ’Potts & Guy’ og ’SkinPerm’
| Stofnavn | Observerede Kρ (µm/t) |
Prædikterede Kρ (Potts & Guy) (µm/t) |
Prædikterede Kρ (SkinPerm) (µm/t) |
|||
| Kρ | LogKρ | Kρ | LogKρ | Kρ | LogKρ | |
| Glyphosat | 0,06 | -1,22 | 0,0095 | -2,02 | 0,4 | -0,40 |
| Caffein | 3,8 | 0,58 | 1,11 | 0,05 | 1,41 | 0,15 |
| Antipyrin | - | - | 2,52 | 0,40 | 4,19 | 0,62 |
| Dimethoat | 4,9 | 0,69 | 2,39 | 0,38 | 2,53 | 0,40 |
| Benzoesyre | 50,6 | 1,70 | 72,9 | 1,86 | 88,7 | 1,95 |
| Bisphenol A | 2,1 | 0,32 | 175,65 | 2,24 | 191 | 2,28 |
| Methiocarb | 38,6 | 1,59 | 189,24 | 2,28 | 207 | 2,32 |
| Tebuconazol | 28,5 | 1,45 | 107,01 | 2,03 | 104 | 2,02 |
| Miconazol | - | - | 852,33 | 2,93 | 767 | 2,88 |
De i tabel 3.3.3 og figur 3.3.10 anførte prædikterede værdier for Kρ viser store forskelle mellem eksperimentelt bestemte værdier og modellerede værdier (bestemt ved Potts & Guy og SkinPerm). Denne diskrepans gør sig hovedsaglig gældende for stofferne med logKow > ca. 3. En undtagelse er antipyrin, som blev fundet ikke at trænge igennem huden, men som i modellerne synes at kunne trænge igennem huden. Som vist i figur 3.3.10 overestimerer modellerne hovedparten af de predikterede logKρ værdier med 46 % (Potts & Guy) og 35 % (SkinPerm).
![Figur 3.3.10. Observerede logKρ værdier som funktion af prædikterede logKρ værdier. De prædikterede værdier er beregnet ved hhv. modellen Potts & Guy og SkinPerm [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].](images/s49.gif)
Figur 3.3.10. Observerede logKρ værdier som funktion af prædikterede logKρ værdier. De prædikterede værdier er beregnet ved hhv. modellen Potts & Guy og SkinPerm [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].
Som det ses i tabel 3.3.4 og figur 3.3.11 er der en tendens til at modellen SkinPerm overestimerer den beregnede flux. For modelstofferne antipyrin og benzoesyre overestimerer modellen temmelig meget i forhold til den målte værdi. Derimod underestimerer modellen kraftigt stoffernes lag-time i forhold til de observerede (figur 3.3.11). Denne overestimering af Kρ og underestimering af lag-time betyder at modellerne generelt overestimerer den mængde, der kan passere huden En væsentlig årsag til, at vi i dette studie finder lavere flux-værdier og højere lag-time værdier end de tidligere modeller, kan være, at de teoretiske modeller (fx Potts & Guy) anvender et datasæt baseret på forsøg med varierende eksperimentelt setup. For eksempel er der inkluderet forsøg baseret på fuldhud såvel som forsøg baseret på dermatom-hud.
Tabel 3.3.4. Observerede flux- og lag-time værdier og prædikterede flux- og lag-time værdier beregnet vha. modellen ’SkinPerm’
| Stofnavn | Observeret flux (nmol/cm² t) |
Predikteret flux (SkinPerm) (nmol/cm² t) |
Observeret lag-time (timer) |
Predikteret lag-time (timer) |
| Glyphosat | 0,14 | 2,5 | 7,9 | 1,6 |
| Caffein | 7,78 | 15,7 | 6,9 | 1,6 |
| Antipyrin | - | 115,8 | - | 0,8 |
| Dimethoat | 0,49 | 26,3 | 22,3 | 1,9 |
| Benzoesyre | 165,4 | 248,1 | 1,5 | 0,2 |
| Bisphenol A | 7,74 | 10,0 | 16,9 | 0,3 |
| Methiocarb | 0,54 | 2,5 | 11,7 | 0,3 |
| Tebuconazol | 0,57 | 1,2 | 14,0 | 0,9 |
| Miconazol | - | 1,8·10-¹7 | - | 1,08 |
![Figur 3.3.11. Observerede Flux-værdier som funktion af prædiktive flux-værdier og observerede lag-time værdier som funktion af prædiktive lag-time værdier beregnet ved modellen SkinPerm. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]](images/s50.gif)
Figur 3.3.11. Observerede Flux-værdier som funktion af prædiktive flux-værdier og observerede lag-time værdier som funktion af prædiktive lag-time værdier beregnet ved modellen SkinPerm. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]
3.3.2 Transplacental transport
Ved den her anvendte ex vivo metode til undersøgelse af transporten over placenta er benyttet et dobbelt recirkulerende perfusionssystem, hvor koncentrationerne i maternelt (CM) og føtalt (CF) blod er målt i et lukket in vitro system.
Forholdet mellem CF og CM (FM-ratio) stiger lineært med tiden de første 30-60 minutter af forsøgene. Derefter flader kurven af, idet der er tale om et lukket system med en konstant mængde stof. FM-ratioen nærmer sig en ligevægt og FM-ratioen nærmer sig en konstant værdi, jf. figur 3.3.12.
Den initiale hældning af FM-ratioen som funktion af tiden kaldes den indikative permeabilitetskoefficient (IPK). Denne parameter er et mål for transporthastigheden over placentabarrieren (de enkelte regressioner for alle stofferne er angivet i figur 3.1.1 – 3.1.10). FM-ratioen er et mål for ligevægten mellem maternelt og føtalt blod. Undersøgelserne er kørt i 150 minutter. Der er derfor kun få målepunkter på kurvernes flade øverste stykke, som ikke er tilstrækkelige til at udføre robuste regressionsanalyser; for nogle stoffer er ligevægt endog ikke indtrådt. Derfor anvendes FM-ratioen ved 150 min (FM-ratio150min) som det bedst tilnærmede udtryk for ligevægt. Tabel 3.3.5 viser de gennemsnitlige værdier af FM-ratio150min og IPK for de 9 modelstoffer.
Tabel 3.3.5. For de undersøgte modelstoffer er den indikative permeabilitets koefficient (IPK) og FM-ratioen (udtrykt ved forholdet mellem føtalt og maternelt blod, CF hhv. CM) efter 150 minutters testperiode angivet
| Stofnavn | Antal studier (N) | Indikativ permeabilitets koefficient (IPK) (t-¹) | FM-ratio150min |
| Glyphosat | 7 | 0,11 | 0,34 ± 0,14 |
| Caffein | 7 | 1,03 | 0,92 ± 0,05 |
| Antipyrin | 19 | 0,92 | 0,97 ± 0,03 |
| Dimethoat | 2 | 0,98 | 0,9 ± 0,6 |
| Benzoesyre | 5 | 0,62 | 0,91 ± 0,04 |
| Bisphenol A | 3 | 0,32 | 0,29 ± 0,13 |
| Methiocarb | 2 | 0,23 | 1,21 ± 1,5 |
| Tebuconazol | 2 | 0,33 | 0,32 ± 0,07 |
| Miconazol | 2 | 0 | 0 |
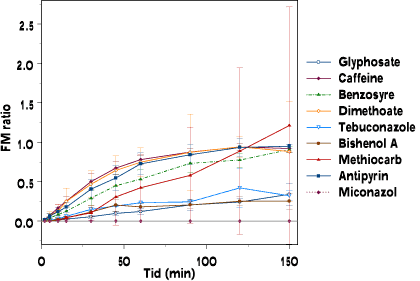
Figur 3.3.12. FM ratio (udtrykt ved forholdet CF/CM) som funktion af tid for de ni modelstoffer. Testperioden var 150 min.
3.3.2.1 Fysisk-kemiske parametre med betydning for transplacental transport
Tidligere undersøgelser af transplacental transport har indikeret, at parametrene molekylestørrelse, lipofilicitet samt hydrogenbindingsevne har betydning for et stofs transport over placenta (Hewitt, 2007).
Da den indikative permeabilitetskoefficient (IPK) er et mål for stoffernes evne til at penetrere placenta, er det undersøgt om, denne parameter har en lineær sammenhæng med ovenstående fysisk-kemiske parametre (figur 3.3.13).
I figur 3.3.13 ses det, at der findes en sammenhæng mellem et stofs evne til at penetrere placenta / hastigheden, hvormed placenta passeres (IPK og FM-ratio150min) og stoffets lipofilicitet beskrevet ved logKow, jo højere logKow desto lavere permeabilitetskoefficient. Dog ser det ud til, at stoffet glyphosat ikke passer ind i dette mønster.
En lineær sammenhæng mellem FM ratio og logKow er beskrevet ved Y = - 0,1767x + 1,0144 (r² = 0,9118), når glyphosat og methiocarb udlades af regressionen (figur 3.3.14.). Ligeledes ses en lineær sammenhæng mellem IPK og logKow beskrevet ved y = -0,2135x + 1,0355 (r² = 0,9629), hvor glyphosat og miconazol er udeladt af regressionen (figur 3.3.15).
Der blev også observeret en sammenhæng mellem modelstoffernes vandopløselighed og IPK. Yderpunkterne for de testede modelstoffer hvad angår logKow falder dog igen udenfor denne sammenhæng (glyphosat og miconazol). Sammenhængen mellem vandopløselighed og IPK viser en lineær sammenhæng (figur 3.3.16), hvor en stigende vandopløselighed betinger stigende IPK-værdier.
![Figur 3.3.13. FM ratioen (forholdet mellem føtalt og maternelt blod – CF/CM) og den indikative permeabilitetskoefficient (IPK) som funktion af molekylevægt, logKow.og vandopløselighed. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s53a.gif)
Figur 3.3.13. FM ratioen (forholdet mellem føtalt og maternelt blod – CF/CM) og den indikative permeabilitetskoefficient (IPK) som funktion af molekylevægt, logKow.og vandopløselighed. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.14. Lineær sammenhæng mellem FM ratio og logKow for 7 af de 9 modelstoffer beskrevet ved ligningen Y = - 0,1767x + 1,0144 (r² = 0,9118). Glyphosat og methiocarb er ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s53b.gif)
Figur 3.3.14. Lineær sammenhæng mellem FM ratio og logKow for 7 af de 9 modelstoffer beskrevet ved ligningen Y = - 0,1767x + 1,0144 (r² = 0,9118). Glyphosat og methiocarb er ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.15. Lineær sammenhæng mellem IPK og logKow for 8 af de 9 modelstoffer udtrykt ved regressionsligningen Y = - 0,1864 + 0,9987 (r² = 0,9537). Glyphosat falder udenfor den lineære sammenhæng og udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s54a.gif)
Figur 3.3.15. Lineær sammenhæng mellem IPK og logKow for 8 af de 9 modelstoffer udtrykt ved regressionsligningen Y = - 0,1864 + 0,9987 (r² = 0,9537). Glyphosat falder udenfor den lineære sammenhæng og udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.16. Lineær sammenhæng mellem IPK og log(Vandopløselighed) for 7 af de 9 modelstoffer udtrykt ved regressionsligningen y = 0,2347x + 0,5985 (r² = 0,9389). Glyphosat falder udenfor den lineære tendens og derfor udeladt af regressionen. Miconazol passer tilsyneladende fint i den lineære regression, men da IPK ikke kan være negativ er miconazol ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s54b.gif)
Figur 3.3.16. Lineær sammenhæng mellem IPK og log(Vandopløselighed) for 7 af de 9 modelstoffer udtrykt ved regressionsligningen y = 0,2347x + 0,5985 (r² = 0,9389). Glyphosat falder udenfor den lineære tendens og derfor udeladt af regressionen. Miconazol passer tilsyneladende fint i den lineære regression, men da IPK ikke kan være negativ er miconazol ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
3.3.2.2 Modeller til beskrivelse af transplacental transport
Kemiske stoffer passerer placenta hovedsagelig ved simpel passiv diffusion (Audus, 1999). Andre mekanismer forekommer dog også, f.eks. faciliteret diffusion, aktiv transport, pinocytose og filtrering (Pacifici, 1995; Reynolds, 1990). Det er anført, at de vigtigste stofegenskaber, som bestemmer passiv diffusion over placenta er molekylevægt, ionisationsgrad (pKa), lipofilicitet og proteinbinding (Audus, 1999; Pacifici, 1995). Det er endvidere fundet, at stoffer med molekylvægt større end ca. 500 Da (g/mol) transporteres dårligt over placenta (Pacifici, 1995). Ikke-ioniserede stoffer passerer placenta lettere end ioniserede (Audus, 1999; Reynolds, 1990), hvilket betyder, at stoffer med syre-/baseegenskaber kun delvis vil passere placenta og i en grad som er proportional med deres ioniseringsgrad. Føtalt blod er mere surt end maternelt blod, hvilket medfører, at svagt basiske stoffer vil ophobes på den føtale side af placenta (”ion trapping”) (Reynolds, 1990). I den i dette projekt anvendte forsøgsopstilling er der dog ikke forskel i pH mellem den føtale og maternelle side (forskel < 0,1 pH-enhed). Indenfor et vist interval af lipofilicitet (logKow) er der en lineær sammenhæng mellem placenta passage og logKow (Akbaraly, 1985; Pacifici, 2005). Plasmabinding i maternelt blod vil medføre, at den del af stoffet, som er bundet til plasmaprotein, ikke vil være tilgængelig for transport over placenta (Corley, 2003).
I de publicerede artikler benyttes 2 forskellige mål for placenta transport: clearance og transfer og data opgives ofte som ”Clearance Index” (CI) og ”Transfer Index” (TI). Disse indices defineres således:
|
Clearance Index | = | Clearance af teststof | |
| Clearance af antipyrin |
|
Transfer Index | = | Transfer af teststof (%) | |
| Transfer af antipyrin (%) |
hvor antipyrin er benyttet som intern kontrol/standard. Clearance er defineret af Schneider et al. 1972 (Schneider, 1972) som
|
Clearance | = | [CV]f – [(CA]f x FFR | |
| [CA]m |
hvor [CV]f er koncentration i føtalt venøst blod, [CA]f er koncentration i føtalt arterielt blod, [CA]m er koncentration i maternelt arterielt blod og FFR er føtalt blod flowrate. Transfer er defineret af bl.a. Heikkinen et al. 2002 (Heikkinen, 2002) som
|
Transfer % | = | [Css]f x FFR x 100 | |
| [CA]m x MFR |
hvor [Css]f er ligevægtskoncentrationen i føtalt venøst blod, [CA]m er koncentrationen i maternelt arterielt blod, FFR er føtalt blod flowrate og MFR er maternelt blod flowrate.
Hewitt et al (Hewitt, 2007)har i et nyligt udarbejdet review over (Q)SAR modellering for transplacental transport lavet metastudier baseret på eksisterende, publicerede in vitro data fra mange kilder. De afprøvede 2 heterogene datasæt, et med CI-data (86 stoffer) og et med TI-data (58 stoffer), samt 3 homogene datasæt som var delmængder af de heterogene datasæt, 1 med CI-data og 2 med TI-data. De homogene datasæt (stoffer som var kemisk beslægtede) viste generelt bedre korrelation (r² = 0,76-0,94) end de heterogene datasæt (r² = 0,62-0,63). En lang række molekylære deskriptorer plus de sædvanlige fysisk-kemiske parametre indenfor grupperne hydrogenbinding, molekylestørrelse og hydrofobicitet blev afprøvet. Men der var ingen fælles deskriptorer for de 5 datasæt. Det ene homogene datasæt (CI-data) for tocolytiske stoffer viste en lineær sammenhæng mellem CI og logKow med regressionsudtrykket:
CI = 0,139 logKow – 0.0605 (n = 8; r² = 0.858)
Akbaraly et al (Akbaraly, 1985) målte den transplacentale transport for en heterogen gruppe stoffer, hovedsagelig lægemidler og fandt følgende sammenhænge mellem TI og logKow:
logTI = 0,223 logKow – 0,250 (n = 17; r² = 0,81)
og
logTI = 0,189 logKow – 0,084 (logKow)² – 0,14 (n = 17; r² = 0,941)
Det ser således ud til, at lipofilicitet er den deskriptor, som giver den bedste korrelation til placentatransport om end de publicerede regressioner afviger en del fra hinanden.
Vi har ikke data på arterielle og venøse koncentrationer og kan derfor ikke applicere disse modeller på vores datasæt.
4 Diskussion
Modellering har stigende fokus i regulatoriske sammenhænge. Således tilstræbes fra EU’s side, at (Q)SAR ((Quantitative) structure activity relationships) anvendes i større udstrækning i forbindelse med registrering af kemiske stoffer under EU’s nye kemikalieregulering REACH til at udfylde datahuller. Der er derfor et behov for at udvikle og validere (Q)SAR modeller. I forbindelse med anvendelse af integrerede teststrategier forventes (Q)SAR modeller at komme til at spille en stigende rolle sammen med in vitro systemer (Combes, 2004; Worth, 2004a; Worth, 2004b).
Der er kun en begrænset viden om bekæmpelsesmidlers transport over placenta. Men det er i litteraturen anført, at placentatransport hovedsaglig sker ved passiv transport (Garland, 1998; Audus, 1999; McDonagh, 2007), ligesom transport over huden, dvs. at transporten følger Fick’s lov. Det har endvidere været anført, at de samme parametre som for hudtransport er bestemmende for transporten over placenta, nemlig stoffets molekylvægt, hydrofobicitet/lipofilicitet, pKa (stoffets ionisation i blodet) og proteinbinding (Bourget, 1995; Pacifici, 1995; Little, 1996; Garland, 1998; Audus, 1999; Garcia-Bournissen, 2003). Der er dog andre mekanismer, som kan influere på placentatransporten for specifikke stoffer, f.eks. lægemidler (Ganapathy, 2000; Gude, 2004; Unadkat, 2004). Lægemidler med molekylevægt større end ca. 500 Da er anført at have nedsat eller ingen transport over placenta, fordi de er for store til at passere porer i placentamembranen (Pacifici, 2005). Da de generelle diffusionsregler øjensynlig gælder for mange stoffer både med hensyn til hudtransport og placentatransport, er det oplagt at undersøge om, det er muligt at opstille en fælles model for hud- og placentatransport.
Ved risikovurdering af kemiske stoffers reproduktionstoksikologiske effekter mangler viden om stoffernes transport over den humane placenta. Der foreligger nogen viden om lægemidlers passage af placenta. I dette studie er transport over placenta og huden undersøgt for 9 kemiske stoffer med henblik på matematisk modellering i forhold til stoffernes fysisk-kemiske egenskaber. Teststofferne blev valgt ud fra et ønske om at dække stor bredde i opløselighed og molekylestørrelse for derved at opnå et repræsentativt datasæt med gode muligheder for modellering.
De testede modelstoffer var caffein, antipyrin, benzoesyre, bisphenol A og de 5 pesticider glyphosat, dimethoat, methiocarb, tebuconazol og miconazol. Heraf forelå der dermale transportdata på stofferne glyphosat, caffein, dimethoat, benzoesyre og methiocarb fra tidligere studier.
For grafisk at sammenligne modelstoffernes passage over henholdsvis hud og placenta er hudpenetrationen (nmol/cm²) og transplacental transport (angivet ved FM-ratioen (CF/CM)) illustreret i tabel 4.1, begge som funktion af tiden.
Tabel 4.1. Transport over hud og placenta for de 9 modelstoffer illustreret som hhv. nmol stof/cm² hud og FM ratio (CF/CM), der beskriver forholdet mellem stofkoncentrationerne i føtalt og maternelt blod. Forsøgsperioderne var hhv. 48 timer for hudstudierne og 150 min for placentaperfusionsstudierne.
| Dermale data | Placenta data |
| Antipyrin | |
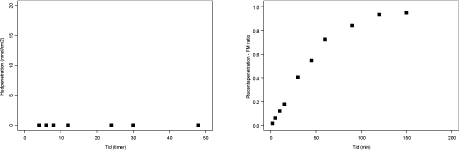 |
|
| Antipyrin passerer ikke den dermale barriere, mens stoffet uhindret passerer placenta. | |
| Benzoesyre | |
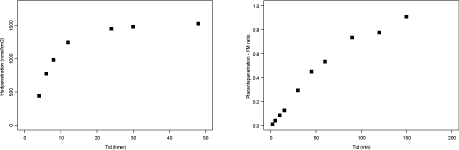 |
|
| Benzoesyre optages meget hurtigt over den dermale barriere og uden lag-time. Transport over placenta går lidt langsommere, men stoffet når over 150 min forsøgsperiode op på samme transport som antipyrin. | |
| Bisphenol A | |
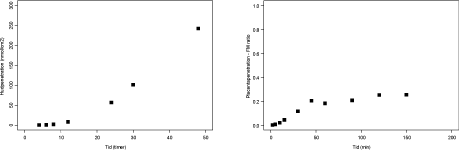 |
|
| Bisphenol A transporteres over den dermale barriere, men en betydelig lag-time ses (17 timer). Bisphenol A transporteres også over placenta, men transporten går betydelig langsommere end for f.eks. antipyrin. | |
| Caffein | |
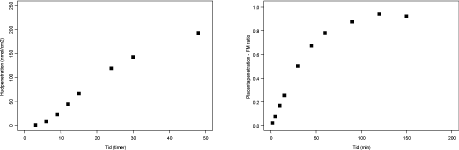 |
|
| Caffein optages relativt hurtigt over både hud og placenta. Transporten over placenta ser ud til at gå hurtigere end transporten over huden. | |
| Dimethoat | |
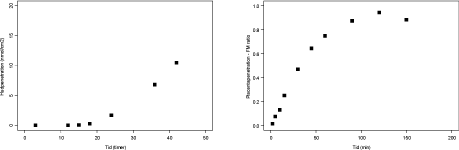 |
|
| For dimethoat ses en betydelig lag-time over den dermale barriere før der sker gennembrud. Derimod ses en hurtig transport over placenta. Der var dog stor spredning på placenta-data | |
| Glyphosat | |
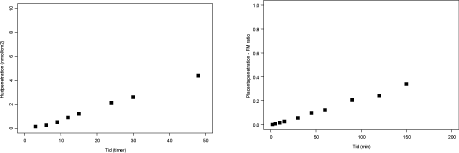 |
|
| Glyphosat optages i nogen grad over både huden og placenta. | |
| Methiocarb | |
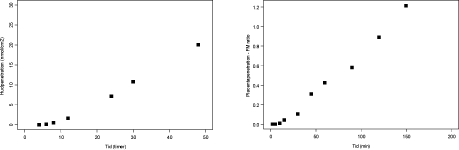 |
|
| Methiocarb transporteres over både hud og placenta. Ved transport over huden ses en lag-time på 12 timer. Der er også en svag tendens til en lag-time ved transport over placenta. Methiocarb når op på en høj FM-ratio (højere end antipyrin). Dog er den høje FM ratio > 1 i dette tilfælde ikke udtryk for en stor transport over placenta idet kun en meget lille koncentration af stoffet blev målt på den føtale side. Det formodes derimod at stoffet ophobes i placentavævet. | |
| Miconazol | |
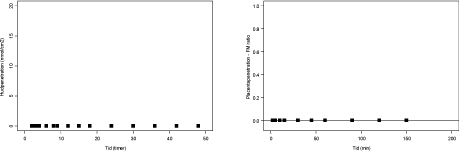 |
|
| Miconazol optages ikke over den dermale barriere – dog findes en lille mængde i huden. Miconazol passerer heller ikke over placenta barrieren. Der blev observeret en ophobning af miconazol i placentavævet | |
| Tebuconazol | |
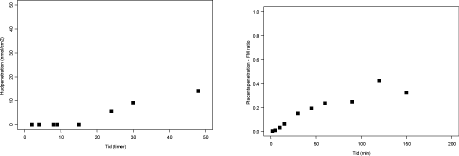 |
|
| Tebuconazol transporteres over både hud og placenta. Ved transport over huden ses en lag-time på 14 timer. Der er også en svag tendens til en lag-time ved transport over placenta og transporten over placenta foregår langsomt. | |
De tidligere unersøgelser af hudtransport har suppleret de data, der er opnået i dette projekt.
Litteraturen beskriver stoffernes logKow som en vigtig faktor for deres transport gennem huden (Cross, 2003). I dette studie observeres en stigende Kρ ved stigende logKow, men kun for stoffer med en logKow mellem -3,5 og ca. 2 (figur 3.3.4). Ved stoffer med en logKow større end 2, så vi ikke denne sammenhæng. For disse stoffer var der en tendens til faldende Kρ ved stigende logKow, men pga. få modelstoffer med en logKow mellem ca. 3 og 5 kan denne tendens ikke præciseres i dette projekt. At den maksimale penetrationsrate findes for stoffer med en logKow omkring 2 er også fundet i andre studier(Cross, 2003; Nielsen, 2008b).
Der blev ikke fundet en klar sammenhæng mellem stoffernes molekylevægt og den målte Kρ. Derimod var der ved stigende molekylevægt en stigende lag-time for passage af huden (figur 3.3.5). Der er en del spredning omkring regressionslinien y = 0,0845x – 6,6483 (r² = 0,45), men to modelstoffer afviger markant fra denne sammenhæng og er ikke medtaget i regressionsudtrykket. Det er antipyrin og miconazol, som ikke passerede huden i løbet af forsøgets varighed (48 timer). Miconazols manglende passage af huden kan forklares med stoffets meget høje lipofilicitet. Antipyrins manglende passage af huden kan ikke umiddelbart forklares. Antipyrin, der anvendes som intern kontrol ved placentaforsøgene, passerer placenta uhindret. Antipyrins fysisk-kemiske karakteristika ligger indenfor det samme interval, som de stoffer, som passerer både hud og placenta. Dog er antipyrin mere vandopløseligt end de øvrige stoffer (51,9 g/L), men kun ca. 2 gange mere vandopløselig end caffein og dimethoat.
Der er en tendens til, at en stigende vandopløselighed medfører en faldende Kρ, men den lineære sammenhæng er meget svag (figur 3.3.8).
I løbet af de 48 timer, som hudforsøgene varer, optages kun et par procent i huden. Der blev observeret en stigende mængde stof deponeret i huden ved stigende molekylevægt (figur 3.3.6). Der opbygges et depot før, stofferne trænger igennem huden og depotets størrelse hænger lineært sammen med molekylevægten, som det kan ses af regressionsudtrykket y = 0,2493x - 36,294 (r² = 0,85). Miconazol falder markant udenfor denne sammenhæng, hvilket kan forklares med stoffets høje lipofilicitet. Der deponeres dog ca. 8 % i huden i løbet af forsøgets varighed (48 timer). Benzosyre afviger også fra denne sammenhæng, formentlig fordi absorptionsprocessen for benzoesyre er afsluttet længe før forsøgsafslutning ved T=48 timer, hvor man måler koncentrationen i huden. For de øvrige modelstoffer var absorptionsprocessen stadig igang ved afslutningen af forsøget. Derfor er det forventeligt, at benzoesyre vil afvige fra de øvrige.
De opnåede resultater for dermal penetration blev testet i to eksisterende matematiske modeller (Berge WF, 2003; Guy, 1993) til beregning af hudpenetration. Modellerne er såkaldte simple modeller til beregning af Kρ. Udregningerne viste at de to modeller begge overestimerer de observerede Kρ-værdier med hhv. 46 % (Potts & Guy) og 35 % (SkinPerm), mens lag-time stærkt underestimeres. Grunden til denne overestimering af Kρ kan skyldes at de eksperimentelle data stammer fra eksperimenter med ’full-thickness’ hud, der vides at resultere i en lavere maksimal fluks og dermed lavere eksperimentelle Kρ-værdier (Nielsen, 2008b).
For 7 af de 9 modelstoffer er der en lineær sammenhæng mellem FM-ratio150min og logKow (figur 3.3.14), og mellem FM-ratio150min og log(vandopløselighed). To stoffer falder udenfor denne sammenhæng, nemlig glyphosat og methiocarb. Glyphosats afvigelse fra disse sammenhænge skyldes sandsynligvis glyphosats stærkt hydrofile phosphorsyregruppe, som medfører, at glyphosat er relativt mindre lipofil end de 8 øvrige modelstoffer, jf. nedenfor og figur 4.1. Som det eneste af de 9 modelstoffer har methiocarb en FM-ratio, som er større end 1. En FM-ratio > 1 kan forklares ved, at methiocarb passerer placenta ved en aktiv transport og ikke blot en passiv diffusion (Reynolds, 1990).
For 8 af de 9 modelstoffer er der en lineær sammenhæng mellem den hastighed, hvormed stofferne passerer placenta (IPK) og stoffets lipofilicitet (logKow), jo højere logKow desto lavere permeabilitetskoefficient (IPK). Glyphosat passer dog ikke ind i dette mønster (figur 3.3.15). Hvis glyphosat udelades fra regressionsudtrykket, er der en lineær sammenhæng mellem IPK og logKow med en pæn korrelation (r²=0,95).
På baggrund af disse data ser det ud til, at grænsen for, hvor lav en logKow stofferne kan have og stadig penetrere placenta, er væsentlig lavere end for den dermale barriere. Glyphosat er det modelstof, som har den laveste logKow (-3,2), og det eneste som har logKow, der er væsentlig lavere end 0. Miconazol har en høj logKow og transporteres ikke over placenta.
Den samme sammenhæng eksisterer mellem IPK og log(vandopløselighed), blot medfører stigende vandopløselighed stigende IPK-værdier (figur 3.3.16).
Miconazol er det eneste af de 9 modelstoffer, som ikke passerer placenta. Det forsvinder imidlertid fra den maternelle side af placenta i testsystemet, sandsynligvis fordi det ophobes i placentavævet. Miconazol er det modelstof, som har den højeste molekylevægt (416 Da) og det mest lipofile (logKow = 5,9). Det er anført i litteraturen, at lægemidler med molekylevægt større end 500 Da kun vanskeligt vil passere placenta (Pacifici, 2005). Vore data tyder på, at denne molekylevægtgrænse snarere ligger ved 400 Da.
![Figur 4.1. Logaritmen til modelstoffernes vandopløselighed som funktion af logKow. En lineær sammenhæng beskrevet ved y = -1,0672x + 2,0614 (n = 8; r² = 0,9454; glyphosat ikke medtaget) beskriver sammenhængen mellem de to parametre. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s63.gif)
Figur 4.1. Logaritmen til modelstoffernes vandopløselighed som funktion af logKow. En lineær sammenhæng beskrevet ved y = -1,0672x + 2,0614 (n = 8; r² = 0,9454; glyphosat ikke medtaget) beskriver sammenhængen mellem de to parametre. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
Glyphosats afvigelse fra ovennævnte sammenhænge skyldes sandsynligvis glyphosats stærkt hydrofile phosphorsyregruppe, som medfører, at glyphosat er relativt mindre lipofil end de 8 øvrige modelstoffer. Hydrofilicitet (vandopløselighed) og lipofilicitet (logKow) er indbyrdes omvendt afhængige parametre således, at høj vandopløselighed (hydrofilicitet) medfører lav lipofilicitet og omvendt. I figur 4.1 er sammenhængen mellem log(vandopløselighed) afbildet som funktion af logKow for de 9 modelstoffer. De 8 af modelstofferne (glyphosat udeladt) ligger på en ret linie med regressionsudtrykket y = -1,0672x + 2,0614 (n = 8; r² = 0,9454), mens glyphosat afviger fra denne lineære sammenhæng på samme måde som i figur 3.3.15 og figur 3.3.16.
Der er ikke en entydig sammenhæng mellem hudpenetration og placentapassage for de 9 modelstoffer. Når dette er sagt viser resultaterne samtidig også områder, hvor der tydeligt kan ses sammenhænge mellem hudoptagelse og placentatransport af stoffer. For både hud og placenta er vandopløselighed, lipofilicitet, samt størrelse betydende parametre.
For flere af modelstofferne ses en betydelig lag-time ved transport over den dermale barriere (bl.a. dimethoat, bisphenol A, tebuconazol). En sådan lag-time ses ikke i samme grad ved transplacental transport. En kort lag-time kan ses for stofferne bisphenol A, tebuconazol og methiocarb. Dette skyldes formentlig at den passive absorption kan foregå langt hurtigere over en membran som placenta i forhold til den mange-cellede (og fortykkede) hornlag, hvor der kan opbygges et depot afhængigt af stoffernes fysisk-kemiske egenskaber.
![Figur 4.2. Lineær sammenhæng mellem IPK og FM-ratio beskrevet ved Y = 0,9897x – 0,0375 (r² = 0,8747). Methiocarb falder udenfor denne sammenhæng og er derfor ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s64.gif)
Figur 4.2. Lineær sammenhæng mellem IPK og FM-ratio beskrevet ved Y = 0,9897x – 0,0375 (r² = 0,8747). Methiocarb falder udenfor denne sammenhæng og er derfor ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
De stoffer, der i dette studie falder udenfor de sammenhænge, der ellers er blevet påvist er bl.a. antipyrin, der anvendes som intern kontrol ved placentaforsøgene. Stoffet optages ikke eller kun ekstremt langsomt gennem huden. I løbet af de 48 timer, som hudforsøgene varer, optages kun et par procent i huden. Der er ikke fundet en forklaring på dette, idet antipyrins fysisk-kemiske karakteristika ikke afviger fra de stoffer, som passerer både hud og placenta om end stoffet dog har en højere vandopløselighed end de andre stoffer (51,9 g/L), dog ikke væsentligt højere end caffein og dimethoat. Et andet stof er miconazol, der hverken optages gennem huden eller passerer placenta, men ophobes langsomt i såvel hud som placentavæv. Benzoesyre opfører sig også specielt, idet stoffet transporteres næsten uhindret over den dermale barriere og opnår ligevægt i løbet af 48 timer. En sammenlignelig hurtig transport over placenta ville derfor være forventelig. Benzoesyre ses dog at have en lavere IPK end forventet i forhold til andre stoffer, som optages hurtigt (figur 4.2).
Sammenhængen mellem data fra placentamodel og hudmodel ses i bl.a. hydrofilicitet af stofferne, men der ses dog ikke umiddelbart nogen sammenhæng mellem de to hastigheder, der beskriver transporten over huden (Kρ) hhv. transporten over placenta (IPK)(figur 4.3).
![Figur 4.3. IPK som funktion af logKρ. Da der ikke er målt en Kρ for stofferne antipyrin og miconazol er disse udeladt af plottet. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s65.gif)
Figur 4.3. IPK som funktion af logKρ. Da der ikke er målt en Kρ for stofferne antipyrin og miconazol er disse udeladt af plottet. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
Undersøgelserne af placentatransport blev gennemført i den treårige projektperiode af forskellige medarbejdere ved KU og en række metodologiske fremskridt er sket undervejs. En mere effektiv rekruttering af donorer af moderkager efter en lang periode med manglende adgang til moderkager er sat i system med dedikeret samarbejde med fødselsafdelingen. Ved anskaffelse af ABL måler (automatisk blodgasmåler fra Radiometer) kan der udføres mere avanceret og sikker overvågning af pH og ilttensioner i væv. Vi har også indført en mere kontinuert overvågning af tab af væske som mål for succes’en af perfusionen, idet vi i et samarbejdsprojekt med Rigshospitalets blodbank har fundet en klar sammenhæng mellem lækage i systemet målt ved IgG overførsel og tab af væske fra den føtale side af cotyledonet til den maternelle. På denne måde har vi bedre kontrol med den enkelte perfusion og kan derfor tidligere i forløbet afgøre om, den er succesfuld. Ofte vil de initiale data fra perfusioner, som senere viser sig at have tabt for megen væske, alligevel kunne bruges, f.eks. til beregning af IPK. Vi har derfor undervejs i projektet udviklet succeskriterier og 2-3 perfusioner er i mange tilfælde tilstrækkelige til at genere brugbare data. Validering af modellen kan ske ved analyser af andre stoffer og/eller analyse af transporten af stofferne i andre modelsystemer. I EU projekterne ReProTect og Nanotest arbejder vi med trophoblastcellelinien BeWo til transportstudier af de samme stoffer og en række andre stoffer. Foreløbige data tyder på korrelation mellem transport i in vitro cellesystemet og ex vivo placentaperfusion.
Forudsætningen for modellering baseret på Ficks lov er proportionalitet mellem påsat koncentration og efterfølgende penetrationshastighed. Den eksperimentelle models validitet i forhold til forudsætningen er tidligere vist i forhold til hudmodellen, og i nærværende studie er opnåelsen af identiske IPK-værdier ved to forskellige koncentrationer af modelstof en styrkelse af også den placentale models validitet (Når man ved to forskellige koncentrationer af modelstof appliceret på donorsiden opnår samme permeabilitetskoefficienter er det udtryk for at Ficks lov holder i vores eksperimentelle set-up, hvilket er forudsætningen for videre anvendelse af data). Baseret på disse to eksperimentelle modeller er en række modelstoffers penetrationsegenskaber undersøgt og sammenholdt med deres fysisk-kemiske karakteristika. Her er fundet en række sammenhænge, men også påpeget en række forskelle og ikke umiddelbart forklarlige observationer for enkeltstoffer forekommer ligeledes. Disse afvigelser mellem modeller og teoretiske forventninger kan naturligvis være betinget af eksperimentelle forhold. Her kan eksempelvis nævnes, at der er anvendt fuldhud i vore studier, medens megen af litteraturen som danner basis for teoretiske modeller har anvendt dermatomhud, der er markant tyndere. Konsekvensen er lavere lag-times og ofte en højere penetrationsrate. Der er faktorer, der taler for og imod begge hudtyper, og OECD anerkender anvendelsen af begge hudtyper, og resultater fra begge typer giver typisk alene kvantitative forskelle. Der er derfor grund til at antage, at størstedelen af de observerede afvigelser fra det forventede har grund i faktorer, der ikke domineres af eksperimentelle forhold. Konsekvensen er derfor en erkendelse af, at ikke alle stoffer opfører sig som forventet, idet man ikke modelmæssigt har medinddraget den faktor, der for et specifikt stof er afgørende. Der vil altid være enkeltstoffer, der afviger fra flertallet, hvilket er en konstant udfordring i ethvert modelleringsarbejde. Reguleringsmæssigt betyder det, at man ved anvendelse af data baseret alene eller overvejende på modelberegninger skal være meget opmærksom på, at specifikke fysisk-kemiske forhold, fx ioniserbare grupper, større funktionelle grupper med deraf følgende steriske karakteristika, kan resultere i klare afvigelser fra det forventede. Der vil i princippet kunne være tale om både over- og underestimerede penetrationshastigheder.
5 Konklusion
Projektet har opfyldt sit hovedformål og leveret viden af både grundvidenskabelig og anvendelsesorienteret værdi.
Ni modelstoffers – heraf 5 pesticider - transport over hhv. den dermale og den placentale barriere er blevet undersøgt med henblik på matematisk modellering af transport i forhold til stoffernes fysisk/kemisk egenskaber. De undersøgte modelstoffer var benzoesyre, bisphenol A, caffein samt antipyrin og bekæmpelsesmidlerne dimethoat, glyphosat, methiocarb, miconazol og tebuconazol.
Der er blevet gennemført undersøgelser af transport over placenta for i alt 9 stoffer med gode resultater. Dermale studier blev gennemført for 4 af de 9 stoffer og hudpenetrationsdata for de resterende stoffer blev benyttet fra tidligere undersøgelser.
Betydningen af forskellige fysisk-kemiske egenskaber for transporten over de to barrierer blev beskrevet for de ni stoffer ligesom sammenhængen mellem transport over hud kontra transport over placenta blev belyst. Ligheder og forskelle i transport for de testede 9 modelstoffer blev illustreret.
For transport over huden kan en række konklusioner drages af projektet:
- Der var en lineær sammenhæng mellem logKow og log Kρ for stoffer med logKow < ca. 2-3. Denne sammenhæng er dog kun baseret på 4 modelstoffer
- Studierne indikerer at stoffer med logKow > ca. 2-3 deponeres i større mængde i huden (25-40 %) end stoffer med en logKow < 2-3
- Der indikeres en lineær sammenhæng mellem molekylevægt og lag-time for hudpenetration, og mellem molekylevægt og deponering i huden
- To stoffer penetrerer ikke huden, og deponeres endvidere kun i nogen grad i huden: antipyrin (3,2 % deponering) og miconazol (8,4 % deponering). Det kan ikke forklares umiddelbart ud fra molekylevægte, logKow eller vandopløseligheder (188 Da, 0,38 og 52 g/L hhv. 416 Da, 5,9 og 0,00001 g/L)
For transport over placenta kan følgende konklusioner drages af projektet:
- Der var en lineær sammenhæng mellem forholdet mellem koncentrationerne på den føtale og maternelle side af placenta (FM-ratio) og logKow, og mellem den initiale transporthastighed (IPK) og logKow
- Tre stoffer passer ikke ind i den generelle sammenhæng: glyphosat (ioniseret ved fysiologisk pH); miconazol passerer ikke over placenta, men deponeres sandsynligvis i placentavævet; methiocarb passerer kun i begrænset mængde placenta, og ophobes tilsyneladende ligeledes i placentavævet
- Studierne indikerer at der ikke er en sammenhæng mellem molekylevægt og FM-ratio, og mellem molekylevægt og IPK
I modelforsøgene blev der anvendt terminale placentaer, som anses for det stadie, hvor placenta er tyndest og dermed det stadie, hvor stoffer må forventes at passere placenta lettest. Transporten af stoffer over placenta varierer med tiden gennem graviditeten på samme vis som også fostrets sårbarhed gør. Dette bør tages med i betragtning ved vurdering af risici forbundet med eksponering af fosteret.
For sammenligning mellem transport over placenta og hud kan følgende konklusioner drages af projektet:
- For flere af modelstofferne ses en betydelig lag-time ved transport over huden (bl.a. dimethoat, bisphenol A, tebuconazol). En sådan lag-time ses ikke i samme grad ved transplacental transport, idet en lille lag-time dog kan anes for stofferne bisphenol A, tebuconazol og methiocarb. Årsagen er sandsynligvis større mulighed for temporær deponering i huden i forhold til placenta
- For hovedparten af modelstofferne ses et sammenligneligt optagelsesmønster over den dermale og placentale barriere, hvilket indikerer, at de samme fysisk-kemiske parametre har betydning for transporten af stoffer over både hud og moderkage
- Der er dog stoffer blandt de undersøgte, som ikke passer ind i de sammenhænge, som kan beskrives for størsteparten af stofferne. Disse stoffer afviger i forhold til forskellige parametre, dvs. at der ikke er et ensartet mønster for afvigelserne. Ligeledes ved man at der kan forekomme en grad af metabolisering i både hud og placenta, der kan ændre på det billede som er belyst i dette projekt. Metabolisering resulterer oftest i mere hydrofile stoffer med ændret molekylevægt samt ofte tab af funktionelle grupper og detoksificering af stoffet. Dog vil metabolisering i nogle tilfælde netop føre til toksiske stoffer som f.eks. i tilfældet med benz(A)pyren.
- Årsagen til afvigelser bør undersøges nærmere. Data fra yderligere stoffer kan belyse disse forhold og bidrage til forståelse for sammenhængene, og dermed til at forbedre modellen ved at beskrive dens anvendelsesområde (’domæne’) mere præcist
Overordnede konklusioner af projektet er, at der er ligheder mellem percutan og transplacental absorption, idet der ved såvel transport over huden som transport over placenta er sammenhæng med stoffernes fysisk/kemiske egenskaber.
6 Perspektivering
Med vores projekt har vi vist sammenhænge mellem hudoptagelse og placentatransport af stoffer. For både hud og placenta er vandopløselighed, lipofilicitet, samt molekylestørrelse betydende parametre. Disse paralleller kan tænkes anvendt således, at eksisterende viden om enkeltstoffers eller stofgruppers dermale penetration kan ekstrapoleres til en forventning om placentapassage. Der vil eksistere betydende forskelle for enkeltstoffers vedkommende, eksemplificeret også i dette studie, men simple kvalitative ekstrapolationer af dermale absorptionsgrader til placenta vil kunne forventes mulige, men næppe generaliserende og kvantitative.
Matematisk modellering kan udover data for flere stoffer også forbedres ved en øget forståelse af, hvorfor nogle stoffer afviger fra de generelle sammenhænge, som beskrives af andre stoffer. I den proces vil en vurdering af de eksperimentelle modellers begrænsninger i forhold til specifikke stoffer eller stofgrupper kunne indgå.
Modellen kan således videreudvikles ved generering af flere parallelle datasæt mellem placental og dermal absorption, og forventes at kunne indgå i fremtidige struktur/aktivitetsmodeller til prædiktion af stoffers optagelse/transport over barrierer. På lang sigt og med introduktion af supplerende in vitro test kan det endvidere forventes, at anvendelsen af validerede matematiske modeller vil kunne bidrage til en reduktion i anvendelse af forsøgsdyr til undersøgelser af transport af stoffer over biologiske barrierer.
Referencer
- Akbaraly JP, Leng JJ, Bozler G, Seydel JK. Quantitative relationship between trans-placental transfer physicochemical properties of a series of heterogenous drugs. In: Seydel JK, editor. QSAR and Strategies in the Design of Bioactive Compounds: Proceedings of the Fifth European Symposium on Quantitative Structure-Activity Relationships Bad Segeberg 1984. Weinheim: VCH Verlagsgesellschaft; 1985. p. 313-7. (.
- Andersen HR, Nielsen JB, Grandjean P. Toxicologic evidence of developmental neurotoxicity of environmental chemicals. Toxicology. 2000;144(1-3):121-7.
- Audus KL. Controlling drug delivery across the placenta. Eur J Pharm Sci. 1999;8:161-5.
- Berge WF. Modelling dermal exposure and absorption through the skin 2003.
- Borling P, Cohr K-H. Testing/evaluation of DEREK for windows. Hørsholm: Dansk Toksikologi Center; 2001.
- Bourget P, Roulet C, Fernandez H. Models for placental transfer studies of drugs. Clin Pharmacokinet. 1995;28(2):161-80.
- Carney EW, Scialli AR, Watson RE, DeSesso JM. Mechanisms regulating toxicant disposition to the embryo during early pregnancy: an interspecies comparison. Birth Defects Res C Embryo Today. 2004;72(4):345-60.
- Combes R, Gaunt I, Balles M. ATLA. 2004;32:163.
- Corley RA, Mast TJ, Carney EW, Rogers JM, Daston GP. Evaluation of physiologically based models of pregnancy and lactation for their application in children's health risk assessment. CRC Crit Rev Toxicol. 2003;33(2):137-211.
- Cross SE, Magnusson BM, Winckle G, Anissimov Y, Roberts MS. Determination of the effect of lipophilicity on the in vitro permeability and tissue reservoir characteristics of topically applied solutes in human skin layers. J Invest Dermatol. 2003;120(5):759-64.
- Engelund EH, Andersen DN, Nielsen AK, Larsen JR, Cohr K-H. Skin penetration. Hørsholm: Dansk Toksikologi Center; 2003.
- Flynn GL. Physiochemical determinants of skin absorption. In: Gerrity TR, Henry CJ, editors. Prinicples of route-to-route extrapolation for risk assessment : proceedings of the workshops of route-to-route extrapolation for risk assessment, Hilton Head, S.C. 1990 and Durham, N.C. 1990. New York, N.Y. : Elsevier: 1990. p. 93-127. (.
- Frasch HF, Landsittel DP. Regarding the sources of data analyzed with quantitative structure-skin permeability relationship methods (commentary on 'Investigation of the mechanism of flux across human skin in vitro by quantitative structure-permeability relationship'). European journal of pharmaceutical sciences. 2002;15(5):399-403.
- Fredholm BB, Battig K, Holmen J, Nehlig A, Zvartau EE. Actions of caffeine in the brain with special reference to factors that contribute to its widespread use. Pharmacol Rev. 1999;51(1):83-133.
- Ganapathy V, Prasad PD, Ganapathy ME, Leibach FH. Placental transporters relvant to drug distribution across the maternal-fetal interface. J Pharmacol Exp Ther. 2000;294(2):413-20.
- Garcia-Bournissen F, Feig DS, Koren G. Maternal-fetal transport of hypoglycaemic drugs. Clin Pharmacokinet. 2003;42(4):303-13.
- Garland M. Pharmacology of drug transfer across the placenta. Obstet Gynecol Clin. 1998;25(1):21-43.
- Grandjean P. Skin penetration. In: Grandjean P, editor. Hazardous chemicals at work. London: Taylor & Francis; 1990. p. 1-187. (.
- Gude NM, Roberts CT, Kalionis B, King RB. Growth and function of the normal human placenta. Thrombosis Res. 2004;114:397-407.
- Guy RH, Potts RO. Penetration of industrial chemicals across the skin: a predictive model. Am J Ind Med. 1993;23(5):711-9.
- Hanke W, Jurewicz J. The risk of adverse reproductive and developmental disorders due to occupational pesticide exposure: an overview of current epidemiological evidence. Int J Occup Med Environ Health. 2004;17(2):223-43.
- Harbison RD, Borgert CJ, Teaf CM. Placental metabolism of xenobiotics. In: Sastry BVR, editor. Placental Toxicology. Boca Raton: CRC Press; 1995.(.
- Hartung T, Bremer S, Casati S, Coecke S, Corvi R, Fortaner S, et al. A modular approach to the ECVAM principles on test validity. Altern Lab Anim. 2004;32(5):467-72.
- Heikkinen T, Ekblad U, Laine K. Placental transfer of citalopram, fluoxetine and their primary demethylated metabolites in isolated perfused human placenta. Br J Obstet Gynaecol. 2002;109:1003-8.
- Hewitt M, Madden JC, Rowe PH, Cronin MT. Structure-based modelling in reproductive toxicology: (Q)SARs for the placental barrier. SAR QSAR Environ Res. 2007;18(1-2):57-76.
- Holmberg RD, Andersen DN. Validering af modeller til forudsigelse af dermal absorption. Hørsholm: Dansk Toksikologi Center; 2004.
- Leazer TM, Klaassen CD. The presence of xenobiotic transporters in rat placenta. Drug Metab Dispos. 2003;31(2):153-67.
- Lilienblum W, Dekant W, Foth H, Gebel T, Hengstler JG, Kahl R, et al. Alternative methods to safety studies in experimental animals: role in the risk assessment of chemicals under the new European Chemicals Legislation (REACH). Arch Toxicol. 2008;82(4):211-36.
- Little BB, VanBeveren TT. Placental transfer of selected substances of abuse. Sem Perinatol. 1996;20(2):147-55.
- Malassine A, Frendo JL, Evain-Brion D. A comparison of placental development and endocrine functions between the human and mouse model. Hum Reprod Update. 2003;9(6):531-9.
- McDonagh AF. Movement of bilirubin and bilirubin conjugates across the placenta. Pediatrics. 2007;119:1032-3.
- Miljøstyrelsen. (Q)SAR-modeller. Miljøstyrelsen, København [updated 2007]. Available from: http://www.mst.dk/Kemikalier/Klassificering+og+risikovurdering/QSAR-modeller/.
- Miller RK, Wier PJ, Maulik D, di Sant'Agnese PA. Human placenta in vitro: characterization during 12 h of dual perfusion. Contrib Gynecol Obstet. 1985;13:77-84.
- Mose T, Kjaerstad MB, Mathiesen L, Nielsen JB, Edelfors S, Knudsen LE. Placental passage of benzoic acid, caffeine, and glyphosate in an ex vivo human perfusion system. J Toxicol Environ Health A. 2008;71(15):984-91.
- Mose T, Knudsen LE. Placental perfusion - A human alternative. Altex. 2006;23:358-63.
- Mose T, Knudsen LE, Hedegaard M, Mortensen GK. Transplacental transfer of monomethyl phthalate and mono(2-ethylhexyl) phthalate in a human placenta perfusion system. Int J Toxicol. 2007a;26(3):221-9.
- Mose T, Mortensen GK, Hedegaard M, Knudsen LE. Phthalate monoesters in perfusate from a dual placenta perfusion system, the placenta and umbilical cord blood. Reprod Toxicol. 2007b;23:83-91.
- Moss GP, Dearden JC, Patel H, Cronin MT. Quantitative structure-permeability relationships (QSPRs) for percutaneous absorption. Toxicol in Vitro. 2002;16(3):299-317.
- Myllynen P. In search of model for hepatic and placental pharmacokinetics [thesis]. Oulu, Finland: University of Oulu; 2003a.
- Myllynen P, Pienimaki P, Jouppila P, Vahakangas K. Transplacental passage of oxcarbazepine and its metabolites in vivo. Epilepsia. 2001;42(11):1482-5.
- Myllynen PK, Pienimaki PK, Vahakangas KH. Transplacental passage of lamotrigine in a human placental perfusion system in vitro and in maternal and cord blood in vivo. Eur J Clin Pharmacol. 2003b;58(10):677-82.
- Nielsen JB. Hudpenetration af pesticider - en undersøgelse af effekten af hjælpestoffer, kombinationseffekter, handsker, samt lettere beskadiget hud Miljøstyrelsen; 2008a. 90.
- Nielsen JB, Nielsen F. Dermal in vitro penetration of methiocarb, paclobutrazol, and pirimicarb. Occup Environ Med. 2000;57(11):734-7.
- Nielsen JB, Nielsen F, Sorensen JA. In vitro percutaneous penetration of five pesticides--effects of molecular weight and solubility characteristics. Ann Occup Hyg. 2004;48(8):697-705.
- Nielsen JB, Nielsen F, Sorensen JA. Defense against dermal exposures is only skin deep: significantly increased penetration through slightly damaged skin. Arch Dermatol Res. 2007;299(9):423-31.
- Nielsen JB, Sørensen JA, Nielsen F. The usual suspects - influence of physico-chemical properties on lag-time, skin deposition and percutaneous penetration of nine model compounds. J Toxicol Environ Health. 2008b;In press.
- Novotna M, Libra A, Kopecky M, Pavek P, Fendrich Z, Semecky V, et al. P-glycoprotein expression and distribution in the rat placenta during pregnancy. Reprod Toxicol. 2004;18(6):785-92.
- OECD. Guideline for testing of chemicals, No. 428: Skin Absorption: In vitro Method2003.
- Ouchi K, Watanabe S. Measurement of bisphenol A in human urine using liquid chromatography with multi-channel coulometric electrochemical detection. J Chromatogr B Analyt Technol Biomed Life Sci. 2002;780(2):365-70.
- Pacifici GM. Transfer of antivirals across the human placenta. Early Human Development. 2005;81:647-54.
- Pacifici GM, Nottoli R. Placental transfer of drugs administered to the mother. Clinical Pharmacokinetic Concepts. 1995;28(3):235-69.
- Ramsey JD, Woollen BH, Auton TR, Scott RC. The predictive accuracy of in vitro measurements for the dermal absorption of a lipophilic penetrant (fluazifop-butyl) through rat and human skin. Fundam Appl Toxicol. 1994;23(2):230-6.
- Reynolds F, Knott C. Pharmacokinetics in pregnancy and placental drug transfer. Oxf Rev Reprod Biol. 1990;11:389-449.
- Sartorelli P, Aprea C, Cenni A, Novelli MT, Orsi D, Palmi S, et al. Prediction of percutaneous absorption from physicochemical data: a model based on data of in vitro experiments. Ann Occup Hyg. 1998;42(4):267-76.
- Schneider H, Panigel M, Dancis J. Transfer across the perfused human placenta of antipyrine, sodium, and leucine. Am J Obstet Gynecol. 1972;114(6):822-8.
- Schneider H, Huch A. Dual in vitro perfusion of an isolated lobe of human placenta: method and instrumentation. Contrib Gynecol Obstet. 1985;13:40-7.
- Shapiro RE. Caffeine and headaches. Neurol Sci. 2007;28 Suppl 2:S179-S183.
- St-Pierre MV, Serrano MA, Macias RI, Dubs U, Hoechli M, Lauper U, et al. Expression of members of the multidrug resistance protein family in human term placenta. Am J Physiol Regul Integr Comp Physiol. 2000;279(4):R1495-R1503.
- St-Pierre MV, Stallmach T, Freimoser GA, Dufour JF, Serrano MA, Marin JJ, et al. Temporal expression profiles of organic anion transport proteins in placenta and fetal liver of the rat. Am J Physiol Regul Integr Comp Physiol. 2004;287(6):R1505-R1516.
- Unadkat JD, Dahlin A, Viyay S. Placental Drug Transfer. Current Drug Metabolism. 2004;5:125-31.
- US EPA. Dermal Exposure Assessment: Principles and Applications. Washington DC: US EPA; 1992. (Available from: http://www.epa.gov/opptintr/exposure/presentations/efast/usepa_1992d_dermalea.pdf)
- van de Sandt JJ, van Burgsteden JA, Cage S, Carmichael PL, Dick I, Kenyon S, et al. In vitro predictions of skin absorption of caffeine, testosterone, and benzoic acid: a multi-centre comparison study. Regul Toxicol Pharmacol. 2004b;39(3):271-81.
- van de Sandt JJ, van Burgsteden JA, Cage S, Carmichael PL, Dick I, Kenyon S, et al. In vitro predictions of skin absorption of caffeine, testosterone, and benzoic acid: a multi-centre comparison study. Regul Toxicol Pharmacol. 2004a;39(3):271-81.
- Vandenberg LN, Hauser R, Marcus M, Olea N, Welshons WV. Human exposure to bisphenol A (BPA). Reprod Toxicol. 2007;24(2):139-77.
- Volkel W, Colnot T, Csanady GA, Filser JG, Dekant W. Metabolism and kinetics of bisphenol a in humans at low doses following oral administration. Chem Res Toxicol. 2002;15(10):1281-7.
- Worth AP, van Leeuwen CJ, Hartung T. The prospects for using (Q)SARs in a changing political environment - high expectations and a key role the European Commission's Joint Research Centre. SAR QSAR Environ Res. 2004a;15(5-6):331-43.
- Worth AP, Cronin MTD. Report of the workshop on the validation of QSARs and other computational prediction models. ATLA. 2004b;32(Suppl.1):703-6.
- Zaretsky MV, Alexander JM, Byrd W, Bawdon RE. Transfer of inflammatory cytokines across the placenta. Am J Obstet Gynecol. 2004;103(3):546-50.
Version 1.0 Juli 2009 • © Miljøstyrelsen.