Transport af bekæmpelsesmidler over moderkagen, analogier til percutan transport og modellering
3 Resultater
- 3.1 Delstudie 1. Dermal absorption
- 3.2 Delstudie 2. Transplacental transport
- 3.3 Delstudie 3. modellering
3.1 Delstudie 1. Dermal absorption
3.1.1 Antipyrin
Antipyrin er påsat penetrationscellerne i en mængde af 600 µL i en koncentration på 530 µM, svarende til en total antipyrin-mængde på 318 nmol. Antipyrins meget høje vandopløselighed betinger, at der ikke blev set nogen penetration gennem huden under 48 timers observation. Fra huden ekstraheres efter forsøgets afslutning omkring 1 % af den på huden påsatte mængde antipyrin svarende til 3 nmol. Den begrænsede mængde antipyrin deponeret i huden fordeler sig med størstedelen i den mere hydrofile dermis. Den samlede genfinding er ikke højere end godt 80 %. Den resterende mængde må med baggrund i stoffets opløselighedskarakteristika og den manglende penetration forventes at være tabt fra donorkammeret (tabel 3.1.1).
Tabel 3.1.1. Penetrationskarakteristika for dermalt appliceret antipyrin efter 48 timers eksponering for 318 nmol antipyrin. Resultaterne angives som middelværdi ± SD
| Antipyrin | |
| N | 6 |
| Receptor recovery (nmol) | 0,0 ± 0,0 |
| Epidermis deposition (nmol) | 1,1 ± 0,7 |
| Dermis deposition (nmol) | 2,0 ± 1,9 |
| Skin deposition (nmol) | 3,1 ± 2,2 |
| Skin deposition (% of dose) | 1,0 |
| Donor recovery (% of dose) | 80,3 |
| Receptor recovery (% of dose) | 0,0 |
| Overall recovery (% of dose) | 81,3 |
3.1.2 Bisphenol A
Bisphenol A blev påsat i koncentration og mængde på henholdsvis 17,5 mM og 106 µL, svarende til en mængde på 424 µg (1860 nmol).
Over en 48 timers periode genfindes 13 % (242 nmol) af den påsatte mængde bisphenol A i receptorkammeret som udtryk for den dermale penetration. I epidermis og dermis findes henholdsvis 7,4 % (137 nmol) og 17 % (320 nmol) af den påsatte mængde bisphenol A, hvilket er udtryk for den mængde, der er absorberet ind i huden, midlertidigt deponeret og potentielt tilgængelig for efterfølgende penetration. Samlet set vil således mere end en tredjedel af den påsatte mængde bisphenol A i løbet af 48 timer potentielt være tilgængelig for systemiske effekter. Da den samlede genfinding er 82 %, vil dette tal muligvis være lidt større, idet erfaringen viser, at manglende genfinding hyppigst er betinget af tab fra donorkammer under forsøgsafslutning. Modelstoffets opløselighedskarakteristika betinger en større deponering i dermis frem for det mere lipofile epidermis. Betinget af en estimeret lag-time på knap 17 timer sker ovenfor beskrevne dermale penetration med en beregnet maksimal hastighed (flux) på 7,74 nmol/cm²*t (tabel 3.1.2 og figur 3.1.1).
Tabel 3.1.2. Penetrationskarakteristika for dermalt appliceret bisphenol A efter 48 timers eksponering for 1860 nmol. Resultaterne angives som middelværdi ± SD
| Bisphenol A | |
| N | 11 |
| Maximal flux (nmol/cm²*t) | 7,74 ± 3,11 |
| Kρ (µm/t) | 2,1 |
| Lag-time (t) | 16,9 ± 1,1 |
| Donor recovery (nmol) | 826 ± 167 |
| Epidermis deposition (nmol) | 137 ± 30 |
| Dermis deposition (nmol) | 320 ± 120 |
| Skin deposition (nmol) | 457 ± 108 |
| Skin deposition (% of dose) | 24,6 |
| Donor recovery (% of dose) | 44,5 |
| Receptor recovery (% of dose) | 13,0 |
| Overall recovery (% of dose) | 82,1 |
| Skin penetration (nmol/cm²) | |
| T = 0 t | 0,0 ± 0,0 |
| T = 2 t | 0,0 ± 0,0 |
| T = 4 t | 0,0 ± 0,0 |
| T = 6 t | 0,44 ± 0,44 |
| T = 8 t | 1,75 ± 1,31 |
| T = 12 t | 7,89 ± 4,82 |
| T = 24 t | 56,51 ± 27,16 |
| T = 30 t | 101,19 ± 47,31 |
| T = 48 t | 242,25 ± 101,19 |
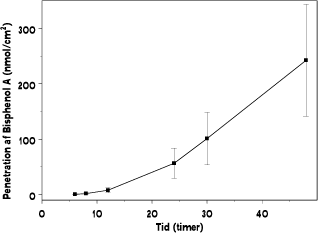
Figur 3.1.1. Dermal penetration af bisphenol A over 48 timer efter initial topikal applicering af 1860 nmol.
3.1.3 Miconazol
Hver celle blev påsat 600 µL miconazol i en koncentration på 4 mM svarende til en mængde på 2400 nmol.
En observationsperiode på 48 timer resulterede ikke i nogen sporbar mængde miconazol i receptorkammeret, og således ingen dermal penetration af miconazol (tabel 3.1.3). Årsagen skal sandsynligvis findes i miconazols meget høje lipofilicitet udtrykt ved en logKow-værdi på omkring 6, der virker bremsende for passage gennem specielt dermis. Miconazol er dog i et vist omfang i stand til at absorberes i huden. Således findes omkring 8 % af den påsatte mængde miconazol i huden ved forsøgsafslutning efter 48 timer. Der er tale om en lidt større mængde miconazol deponeret i dermis i forhold til epidermis.
Tabel 3.1.3. Penetrationskarakteristika for dermalt appliceret miconazol efter 48 timers eksponering for 2400 nmol miconazol. Resultaterne angives som middelværdi ± SD
| Miconazol | |
| N | 6 |
| Receptor recovery (nmol) | 0,0 ± 0,0 |
| Epidermis deposition (nmol) | 83,2 ± 15,3 |
| Dermis deposition (nmol) | 114,6 ± 10,8 |
| Skin deposition (nmol) | 200,9 ± 14,7 |
| Skin deposition (% of dose) | 8,4 |
| Donor recovery (% of dose) | n.d. |
| Receptor recovery (% of dose) | 0,0 |
| Overall recovery (% of dose) | n.d. |
3.1.4 Tebuconazol
Hver celle blev påsat 600 µL Tebuconazol i en koncentration på 200 µM svarende til en mængde på 120 nmol.
Ved forsøgsafslutning efter 48 timer genfindes en fjerdedel af det påsatte tebuconazol i receptorkammeret efter penetration af huden. Tilbage i huden sidder endnu 40 % af den påsatte mængde fordelt med en tredjedel i epidermis og to tredjedele i dermis (tabel 3.1.4 og figur 3.1.2). Det i huden deponerede tebuconazol vil potentielt kunne penetrere huden, således at man samlet vil kunne nå op på at 2/3 af den applicerede dosis efter 48 timers eksponering vil være potentielt tilgængelig for systemisk påvirkning. Den samlede genfinding er 100 % i dette forsøg og de opnåede spredninger er tilfredsstillende lave.
Lag-time estimeres til 14 timer, og ud fra den efterfølgende initiale penetrationsfase bestemmes den maksimale flux til at være 0,6 nmol/cm²*t.
Tabel 3.1.4. Penetrationskarakteristika for dermalt appliceret tebuconazol efter 48 timers eksponering for 120 nmol tebuconazol. Resultaterne angives som middelværdi ± SD
| Tebuconazol | |
| N | 6 |
| Maximal flux (nmol/cm²*t) | 0,57 ± 0,16 |
| Kρ (µm/t) | 28,5 |
| Lag-time (t) | 14,0 ± 0,0 |
| Donor recovery (nmol) | 47,4 ± 8,4 |
| Epidermis deposition (nmol) | 16,5 ± 2,5 |
| Dermis deposition (nmol) | 32,3 ± 8,2 |
| Skin deposition (nmol) | 48,8 ± 7,6 |
| Skin deposition (% of dose) | 40,7 |
| Donor recovery (% of dose) | 39,5 |
| Receptor recovery (% of dose) | 24,7 |
| Overall recovery (% of dose) | 104,9 |
| Skin penetration (nmol/cm²) | |
| T = 0 t | 0,0 ± 0,0 |
| T = 2 t | 0,0 ± 0,0 |
| T = 4 t | 0,0 ± 0,0 |
| T = 6 t | 0,0 ± 0,0 |
| T = 8 t | 0,0 ± 0,0 |
| T = 12 t | 0,0 ± 0,0 |
| T = 24 t | 5,6 ± 1,6 |
| T = 30 t | 9,1 ± 2,6 |
| T = 48 t | 14,0 ± 2,1 |
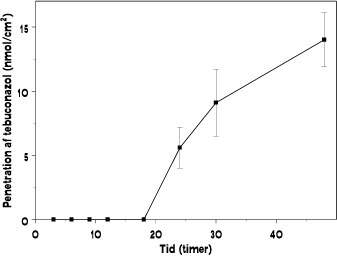
Figur 3.1.2. Dermal penetration af tebuconazol over 48 timer efter initial topikal applicering af 120 nmol.
3.2 Delstudie 2. Transplacental transport
3.2.1 Antipyrin
Antipyrin anvendes som intern markør som en del af kvalitetssikringen (positiv kontrol) ved perfusionsforsøgene, idet antipyrin vides at passere placenta relativt uhindret og historiske data eksisterer for sammenligning. Hvis resultater for antipyrin indikerer en ikke-velfungerende placenta, anvendes data for et givent modelstof opnået med denne perfusion ikke.
Nedenfor er angivet antipyrins perfusion gennem velfungerende placentaer i et udvalgt antal vellykkede forsøg fra dette projekt (fra forsøg med benzoesyre, caffein og glyphosat) (Figur 3.2.1). Figuren viser hvorledes koncentrationen stiger på den føtale side stiger samtidig med et tilsvarende fald i koncentrationen af antipyrin på den maternelle side. Efter godt to timer er der opnået en ligevægt, hvor samme koncentration af antipyrin ses i begge kredsløb, hvilket også illustreres ved, at FM-ratioen er 1 (Figur 3.2.1).
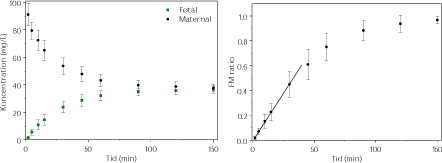
Figur 3.2.1. Perfusion med Antipyrin (100 mg/L og n=19 fra studier med modelstofferne benzoesyre, caffein og benzoesyre). FM-ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM-ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM-ratioen. IPK er beskrevet ved ligningen y = 0,0153x – 0,0069 (r² = 0,9991) og udregnet for tidsrummet 0-30 min.
3.2.2 ¹4C-Benzoesyre
Det første stof, der blev testet var benzoesyre i en koncentration på 32,8 mM, da det er den koncentration, der er testet på huden. Koncentrationen var imidlertid toksisk for placenta-vævet. Benzoesyre er derfor testet i en lavere og ikke-placentatoksisk koncentration på 200 µM. Der er gennemført 5 vellykkede perfusioner, der viser, at benzoesyre transporteres over placenta (Figur 3.2.2). Resultaterne er rapporteret i (Mose, 2008).
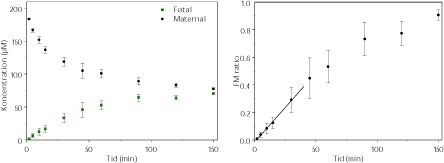
Figur 3.2.2. Perfusion med ¹4C-Benzoesyre (N=5). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0103x – 0,0173 (r² = 0,9985) og udregnet for tidsrummet 0-30 min.
3.2.3 Bisphenol A
Der er gennemført 3 vellykkede perfusioner med 0,5 µM Bisphenol A i Krebs-Ringer-buffer, som viser meget langsom transport (figur 3.2.3). Undersøgelser med humant albumin i mediet pågår i projektet NEWGENERIS og data tyder på carrier effekt af albumin, hvilket øger transporten. Data er ikke publiceret endnu. Data fra to forsøg, som lækkede i slutningen af undersøgelsesperioden, viser samme transportmønster – data ikke vist.
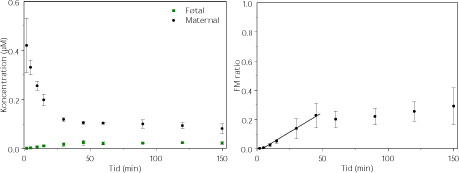
Figur 3.2.3. Perfusion med bisphenol A (N=3). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0054x – 0,022 (r2 = 0,9918) og udregnet for tidsrummet 0-45 min.
3.2.4 ¹4C-Caffein
Caffein er testet ved henholdsvis 10 og 200 µM med i alt 7 vellykkede perfusioner (4 perfusioner med 200µM og tre perfusioner med 10µM). Caffein transporteres over placenta på samme vis som benzoesyre. Dataanalyser viser, at man opnår en udligning af koncentrationsgradienten mellem den maternelle og føtale side i løbet af ca. to timer, hvilket svarer til en hastighed som observeret for antipyrin. (figur 3.2.4 og 3.2.5) (Mose, 2008). Der beregnes samme IPK for eksperimenterne med henholdsvis 10 og 200 µM caffein. Det indikerer, at der er tale om en koncentrationsafhængig passiv diffusion samt, at den anvendte eksperimentelle model er valid.
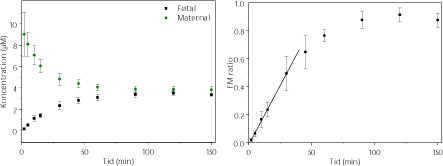
Figur 3.2.4. Perfusion med 14C-Caffein (10 µM og N=3). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0170x – 0,0141 (r2 = 0,9988) og udregnet for tidsrummet 0-30 min.
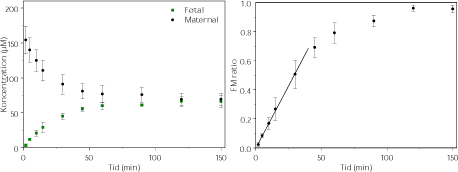
Figur 3.2.5. Perfusion med ¹4C-Caffein (200 µM og N=4). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0171x – 0,0086 (r² = 0,9994) og udregnet for tidsrummet 0-30 min.
3.2.5 Dimethoat
Dimethoat er testet ved 100 µM i 2 vellykkede perfusioner. Dimethoat bliver transporteret over placenta (figur 3.2.6). Dataanalyser viser, at man ikke opnår en udligning af koncentrationsgradienten mellem den maternelle og føtale side i løbet af omkring to timer. Som det ses af figuren, er der store afvigelser i de vellykkede perfusioner, hvilket der ikke umiddelbart findes en forklaring på. Der er data for flere perfusioner, der imidlertid ikke var vellykkede som følge af læk.
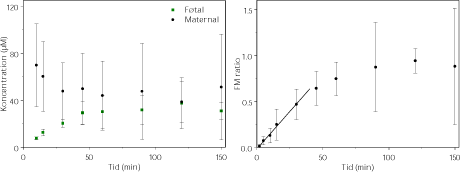
Figur 3.2.6. Perfusion med dimethoat (N=2). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0163x – 0,0157 (r² = 0,9937) og udregnet for tidsrummet 0-30 min.
3.2.6 ¹4C-Glyphosat
Glyphosat er testet ved 200 µM med i alt 7 vellykkede perfusioner. Det ser ud til, at glyphosat transporteres over placenta, men i mindre grad end f.eks. caffein. Glyphosat ophobes ikke i vævet. Resultaterne viser, at man efter 2½ timer fortsat har omkring 3 gange så høj koncentration af glyphosat på den maternelle side i forhold til den føtale (figur 3.2.7) (Mose, 2008).
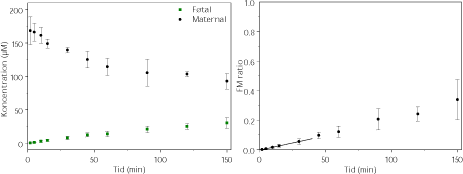
Figur 3.2.7. Perfusion med ¹4C-Glyphosat (N=7). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0019x – 0,0091 (r² = 0,9998) og udregnet for tidsrummet 0-30 min.
3.2.7 Methiocarb
Der er udført et vellykket og et mindre vellykket forsøg, som viser manglende overførsel (figur 3.2.8). Der overføres næsten ikke noget stof til den føtale side, men vævskoncentrationerne er meget høje. Dette kan forklares med ophobning i placentavævet, hvor der måles betydelige koncentrationer mellem 12 og 59 µM i ekstraktioner fra de perfunderede cotyledoner. Den høje FM ratio er i dette tilfælde derfor ikke udtryk for en stor transport over placenta, men bare udtryk for at det forsvinder fra den maternelle side.
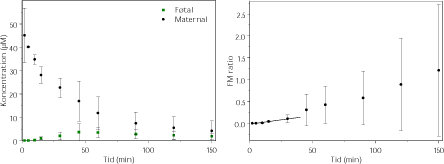
Figur 3.2.8. Perfusion med methiocarb (N=2). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0039x – 0,0179 (r² = 0,9658) og udregnet for tidsrummet 0-30 min.
3.2.8 Miconazol
Der blev først udført et indledende forsøg med miconazol med 60 og 200 µM. Grundet problemer med at opløse miconazol blev 60 µM valgt som testkoncentration i undersøgelserne. Der blev gennemført 4 vellykkede perfusioner med 60 µM. Miconazol bliver tilsyneladende ikke transporteret over placenta, men ophobes i placentavævet. Dette ses ved, at miconazol-koncentrationen mindskes i den maternelle side over tid uden en tilsvarende stigning i koncentrationen af miconazol på den føtale side (figur 3.2.9). Det kan dog også skyldes, at miconazol bindes til materialer i forsøgsopstillingen, men dette er ikke særligt sandsynlig vurderet ud fra en ”slangetest”. I slangetesten uden placentavæv i forsøgsopstillingen fandt vi, at miconazol (100 µM) udfælder og ikke er vandopløseligt. Ved slangetest uden placenta men med blodceller kunne 100 µM opløses og detekteres, idet miconazol bindes til plasmaproteiner.
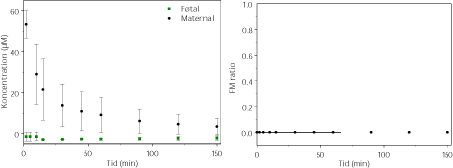
Figur 3.2.9. Perfusion med Miconazol (60 µM og N=2). FM ratioen angiver forholdet CF/CM, men da FM-ratioen ikke kan være negativ sættes det for miconazol til 0.
3.2.9 Tebuconazol
Der er udført 2 perfusioner med 200 µM tebuconazol (figur 3.2.10). Tebuconazol forsvinder fra den maternelle side, men genfindes ikke tilsvarende på den føtale side målt som FM-ratio. Transporten over placenta er begrænset, hvilket sandsynligvis skyldes ophobning af tebuconazol i placentavævet og eventuelt metabolisering. Vi har dog ikke været i stand til at detektere metabolitter.
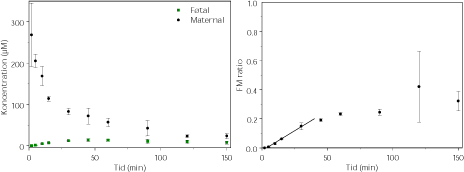
Figur 3.2.10. Perfusion med tebuconazol (N=2). FM ratioen angiver forholdet CF/CM. Regressionen angiver den initiale hældning af FM ratioen også kaldet den indikative permeabilitetskoefficient (IPK) beregnet for et gennemsnit af FM ratioen. IPK er beskrevet ved ligningen y = 0,0055x – 0,0187 (r² = 0,9917) og udregnet for tidsrummet 0-30 min.
3.3 Delstudie 3. modellering
3.3.1 Dermal absorption
3.3.1.1 Faktorer af betydning for dermal absorption
Diffusion gennem hud kan foregå ved passiv diffusion eller som en aktiv transport. Den passive diffusion kan beskrives ved Ficks lov, der siger, at steady-state flux er lig permeabilitetskoefficienten gange koncentrationsforskellen over huden: Jss = Kρ ΔC.
Ved udregning af den dermale absorption er der især tre faktorer, der ses på. Disse er:
- Lag-time (timer)
- Flux (nmol/cm² time)
- Kρ (µm/time)
Lag-time beskriver tiden fra eksponering til gennembrud af huden, og stoffet kan måles i plasma. For lipofile stoffer, der hellere vil befinde sig i det lipofile miljø i hornlaget end i det hydrofile miljø på den anden side af hornlaget, vil man ofte se en lang lag-time. Hydrofile stoffer vil gennembryde hurtigere huden og har derfor en kort lag-time.
Flux’en beskriver den mængde af stof påført huden (i nmol/cm²), der kan gennembryde huden pr tidsenhed. Steady-state flux er en simpel måde til beskrivelse af permeabiliteten af molekyler over huden. For at steady-state kan opnås, må der gå et tidsrum efter den første kontakt med huden til ligevægt kan indstille sig.
Især for lipofile stoffer vil der i den første periode af eksponeringen ske en større transport af stof ind i huden i forhold til transport fra hud til plasma. Der vil altså opbygges et depot i huden. I særlige tilfælde ses det, at der kun sker en begrænset transport fra hud til plasma. I disse tilfælde vil en mætning af hudens depoter virke som en begrænsende faktor på flux’en.
Kρ er permeabilitetskoefficienten er en konstant, som udtrykker den hastighed, hvormed et givet stof kan penetrere huden (µm/time).
Der er mange faktorer, som har betydning for, om der sker en hudpenetration eller ej i et givet tilfælde. Nogle af de i litteraturen nævnte faktorer er:
- Fysisk-kemiske egenskaber for stoffet
- Vehikeleffekter + vehiklens egenskaber
- Hudens tilstand (sygdomme) og dermed hudens barriereegenskab
- Hudområde (arm, inderlår, håndflade, fodsål osv.)
- Hudens fugtighed
- Køn og alder
- Metabolisme i huden
Da mange ting kan influere på hudpenetrationen, vanskeliggør det opbygningen af en model til forudsigelse af hudpenetration.
3.3.1.2 Testdata
Ni kemiske stoffers penetration gennem huden er blevet undersøgt in vitro med human hud. Data om stofferne glyphosat, caffein, dimethoat, benzoesyre og methiocarb stammer fra tidligere undersøgelser (Nielsen, 2000; Nielsen, 2008a; van de Sandt, 2004a), mens bisphenol A, tebuconazol, antipyrin og miconazol er undersøgt indenfor dette projekts rammer.
Modelstofferne er udvalgt således at der indenfor gruppen findes et bredt udvalg af stoffer med forskellig opløselighedsprofil (logKow) samt molekylestørrelse (se tabel 3.3.1).
Tabel 3.3.1. For de undersøgte modelstoffer er de fysisk-kemiske parametre logKow, molekylevægt (MW), molar volumen, vandopløselighed, damptryk (Vp) og ioniseringsgrad (pKa) angivet. Modelstofferne er nævnt rækkefølge med stoffet med laveste logKow værdi
| Stofnavn | logKow | MW (g/mol) |
Molar Volumen | Vandopl. (g/L) |
Vp (mPa) |
pKa |
| Glyphosat | - 3,2 | 169,07 | 100,6 | 10,5 | 13,1 | 2,34 – 10,2 |
| Caffein | - 0,07 | 194,19 | 133,3 | 21,6 | 2106 | 10,4 |
| Antipyrin | 0,38 | 188,25 | 162,7 | 51,9 | 4,08 | 1,4 |
| Dimethoat | 0,7 | 229,26 | 175,7 | 23,8 | 0,25 – 1,1 | - |
| Benzoesyre | 1,87 | 122,13 | 101,9 | 3,41 | 93,3 | 4,19 |
| Bisphenol A | 3,32 | 228,28 | 199,5 | 0,12 | 4x10-8 | - |
| Methiocarb | 3,34 | 225,31 | 196,0 | 0,027 | 0,036 | - |
| Tebuconazol | 3,7 | 307,8 | 268,1 | 0,036 | 0,0017 | - |
| Miconazol | 5,9 | 416,13 | 296 | 0,000011 | - | - |
De målte og udregnede parametre Kρ, lag-time, koncentration målt i hud og receptorkammer (absorberede mængde) samt den maximale hastighed (flux) er angivet i tabel 3.3.2 for de undersøgte modelstoffer.
Som det ses i tabel 3.3.2 er der indenfor gruppen af modelstoffer eksempler på stoffer, der ikke transporteres over den dermale barriere (f.eks. antipyrin og miconazol), mens andre stoffer nærmest uhindret transporteres igennem huden (f.eks. benzoesyre).
Benzoesyre er det stof, som skiller sig mest ud blandt de undersøgte modelstoffer idet dets penetrationskurve adskiller sig væsentlig fra de andre stoffer. Som det ses i figur 3.3.1, opnås der for benzoesyre ligevægt i løbet af den eksperimentelle periode på 48 timer. Benzoesyre er det mindste af de testede stoffer med en molekylevægt på kun 122 g/mol. Derudover har den en logKow på 1,87.
Caffein og bisphenol A har den højeste hudpenetration næstefter benzoesyre af de testede stoffer målt som nmol/cm², mens dimethoat, glyphosat, methiocarb og tebuconazol har et ensartet penetrationsmønster illustreret i figur 3.3.2. Miconazol og antipyrin optages ikke over huden og er derfor ikke medtaget i figur 3.3.2.
Tabel 3.3.2. Parametrene Kρ, lag-time, relativ hud deposit, relativ receptor recovery (absorberet mængde) samt den maksimale flux er opgivet som gennemsnit ± SD. Den eksperimentelle periode var 48 timer
| Stofnavn | Antal studier (N) |
Kρ (µm/t) |
Lag-time (timer) |
Hud deposit (% af dosis) |
Absorberet mængde (% af dosis) |
Maksimal flux (nmol/cm²·t) |
| Glyphosat | 14 | 0,06 | 7,9 ±5,7 | 0,7 ± 0,1 | 0,4 ± 0,1 | 0,14 ± 0,06 |
| Caffein | 17 | 3,8 | 6,9 ± 1,7 | 7,0 ± 4,3 | 18,7 ± 8,5 | 7,78 ± 5,0 |
| Antipyrin | 6 | - | - | 3,2 ± 2,24 | 0 | - |
| Dimethoat | 14 | 4,9 | 22,3 ± 4,4 | 1,9 ± 0,2 | 5,1 ± 0,8 | 0,49 ± 0,26 |
| Benzoesyre | 16 | 50,6 | 1,5 ± 1,0 | 1,5 ± 0,1 | 93,4 ± 0,7 | 165,4 ± 36,0 |
| Bisphenol A | 11 | 2,1 | 16,9 ± 1,1 | 24,6 ± 5,8 | 13,0 ± 5,4 | 7,74 ± 3,11 |
| Methiocarb | 14 | 38,6 | 11,7 ± 6,1 | 26,0 ± 3,6 | 50,9 ± 4,9 | 0,54 ± 0,14 |
| Tebuconazol | 6 | 28,5 | 14,0 ± 0,0 | 40,7 ± 6,3 | 24,7 ± 1,8 | 0,57 ± 0,16 |
| Miconazol | 6 | - | - | 8,4 ± 0,6 | 0 | - |
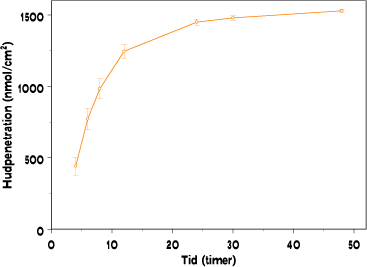
Figur 3.3.1: Hudpenetration som funktion af tiden for modelstoffet benzoesyre.
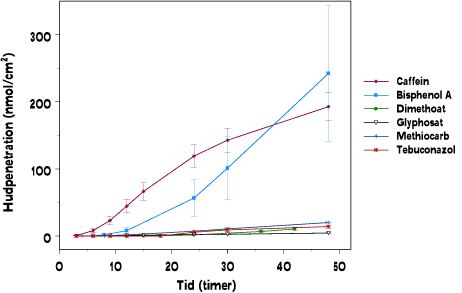
Figur 3.3.2: Hudpenetration som funktion af tiden for 6 af de 7 modelstoffer; Glyphosat, caffein, tebuconazol, bisphenol A, dimethoat og methiocarb. Stofferne Antipyrin og Miconazol er blevet undersøgt, men stofferne blev ikke transporteret over den dermal barriere og derfor ikke medtaget i figuren.
3.3.1.3 Fysisk-kemiske parametre med betydning for transport over huden
Der er gennem de sidste årtier arbejdet med udvikling af både simple modeller baseret på fysisk-kemiske parametre og mere komplicerede farmakokinetiske modeller (PK modeller) til beskrivelse af kemiske stoffers transport over huden (Moss, 2002).
De målte og beregnede hud parametre (Kρ, flux, lag-time, relativ hud-deposit, relativ absorberet mængde og den samlede absorberede mængde inkl. mængden fundet i huden) er afbildet som funktion af en række fysisk-kemiske parametre (figur 3.3.3, 3.3.5 og 3.3.8). Herved kan det vurderes om, der for modelstofferne findes en korrelation mellem nogle af faktorerne (figur 3.3.4, 3.3.6, 3.3.7 og 3.3.9).
Der er en tendens til, at den højeste Kρ findes for stoffer med en logKow i intervallet 1 - 4. Bisphenol A følger dog ikke denne tendens (logKow = 3,32 og Kρ = 2,1 µm/t). Hvis logKρ afbildes som funktion af logKow (figur 3.3.4) ses, at der for stoffer med logKow under 2 er en klar lineær sammenhæng med stigende logKρ værdier ved stigende logKow værdier. For modelstofferne med logKow over to ses en tendens til en konstant til faldende logKρ ved stigende logKow.
Der er ingen sammenhæng mellem den målte maksimale flux og logKow. For de 9 modelstoffer er fluxen =< 10 nmol/cm²·t, undtaget er benzoesyre, der har en meget høj flux på 165 nmol/cm²·t.
Der er en tendens til, at den relative mængde deponeret i huden stiger med en stigende lipofilicitet, dvs. stigende logKow undtagen for meget hydrofile stoffer (glyphosat) og meget lipofile stoffer (miconazol). Statistisk er denne tendens dog ikke robust. Benzoesyre ser ud til at afvige fra denne ”regel”.
Den mængde, som optages gennem huden (både ekskl. og inkl. mængden genfundet i huden) følger samme mønster som Kρ.
![Figur 3.3.3. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af logKow. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]](images/s42.gif)
Figur 3.3.3. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af logKow. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]
![Figur 3.3.4. Lineær regression mellem logKρ og logKow med ligningen Y = 0,5561x + 0,5354 (r² = 0,9822). Kun modelstofferne Glyphosat, Caffeine, Dimethoat og Benzoesyre med en logKow under 2 er medtaget i regression (de andre stoffer er markeret med en ring). Der er ikke målt Kρ værdi for stofferne Antipyrin og Miconazol og disse er derfor udeladt af figuren. [Gly: glyphosat, Caf: caffein, Dim: Dimethoat, Ben: benzoesyre, Met: Methiocarb, Teb:Tebuconazol, Bis: Bisphenol A].](images/s43.gif)
Figur 3.3.4. Lineær regression mellem logKρ og logKow med ligningen Y = 0,5561x + 0,5354 (r² = 0,9822). Kun modelstofferne Glyphosat, Caffeine, Dimethoat og Benzoesyre med en logKow under 2 er medtaget i regression (de andre stoffer er markeret med en ring). Der er ikke målt Kρ værdi for stofferne Antipyrin og Miconazol og disse er derfor udeladt af figuren. [Gly: glyphosat, Caf: caffein, Dim: Dimethoat, Ben: benzoesyre, Met: Methiocarb, Teb:Tebuconazol, Bis: Bisphenol A].
I figur 3.3.5 indikeres en lineær sammenhæng mellem lag-time og stoffernes molekylevægt. Det ser dog ud som om, dimethoat har en væsentlig længere lag-time end trenden i kurven. En regressionsanalyse udført på data viser, at lag-tidens funktion af molekylevægten kan beskrives ved ligningen y = 0,07x – 5,2 (r² = 0,67), når dimethoat udelades, og y = 0,0845x – 6,6483 (r² = 0,4467), når dimethoat medtages i regressionen (figur 3.3.6). Antipyrin og miconazol ikke er medtaget i regressionen, da der ikke er fundet en lag-time for disse to modelstoffer. Deres lag-time må anses for længere end de 48 timer som studierne varer.
Ligeledes kan den relative mængde stof fundet i huden (dermis + epidermis) beskrives ved en lineær sammenhæng (y = 0,2298x – 34,5986; r² = 0,6755), hvor en stigende molekylevægt betinger en stigende mængde stof deponeret i hudlagene (figur 3.3.7). Dette indikerer, at stigende molekylestørrelse gør det sværere at passere den dermale barriere. Det ser dog ud til, at dimethoat ikke følger denne tendens, da stoffet har en væsentlig lavere mængde deponeret i huden (1,9 %) end trenden i dette plot indikerer (y = 0,2493x – 36,294; r² = 0,8527, når dimethoat udelades af regressionen). Miconazol, der er et stort molekyle (416 g/mol), som på mange punkter er et ’yderstof’ i gruppen af modelstoffer. Miconazol følger da heller ikke trenden i regressionen, idet der kun blev fundet 8,4 % i huden.
![Figur 3.3.5. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af molekylevægten. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Mic: Miconazol; Teb: Tebuconazol; Met: Methiocarb]](images/s44a.gif)
Figur 3.3.5. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af molekylevægten. For de stoffer hvor en parameter ikke er målt i forsøgsperioden (f.eks. Kρ pga. manglende optagelse) er disse stoffer udeladt af figuren. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Mic: Miconazol; Teb: Tebuconazol; Met: Methiocarb]
![Figur 3.3.6. Lineær regression af forholdet mellem lag-time og modelstoffernes molekylevægt med ligningen Y = 0,0845x -6,6483 (r² = 0,4467). Der er ikke målt en lag-time for Antipyrin og Miconazol, hvorfor deres værdig er sat til > 48 timer – disse to stoffer falder derfor udenfor tendensen og er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]](images/s44b.gif)
Figur 3.3.6. Lineær regression af forholdet mellem lag-time og modelstoffernes molekylevægt med ligningen Y = 0,0845x -6,6483 (r² = 0,4467). Der er ikke målt en lag-time for Antipyrin og Miconazol, hvorfor deres værdig er sat til > 48 timer – disse to stoffer falder derfor udenfor tendensen og er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]
![Figur 3.3.7. Lineær regression af forholdet mellem koncentration fundet i huden (epidermis + dermis) og modelstoffernes molekylevægt beskrevet ved ligningen Y = 0,2493x – 36,294 (r² = 0,8527). Dimethoat og miconazol synes at have en lavere mængde stof deponeret i huden i forhold til hvad tendensen i dette plot indikerer hvorfor de er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]](images/s45.gif)
Figur 3.3.7. Lineær regression af forholdet mellem koncentration fundet i huden (epidermis + dermis) og modelstoffernes molekylevægt beskrevet ved ligningen Y = 0,2493x – 36,294 (r² = 0,8527). Dimethoat og miconazol synes at have en lavere mængde stof deponeret i huden i forhold til hvad tendensen i dette plot indikerer hvorfor de er udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Teb: Tebuconazol; Met: Methiocarb; Mic: Miconazol]
Hudparametrenes sammenhæng med modelstoffernes vandopløselighed er afbilledet i figur 3.3.8
Der er en tendens til at en stigende vandopløselighed medfører en faldende Kρ. Dette blev undersøgt yderligere i figur 6.3.9, hvor logKρ blev afbilledet som funktion af logaritmen til vandopløseligheden. Dog viser figuren at den lineære sammenhæng er meget svag.
Den mængde, som optages gennem huden (både ekskl. og inkl. mængden genfundet i huden) følger samme mønster som Kρ.
![Figur 6.3.8. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af vandopløseligheden. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s46a.gif)
Figur 6.3.8. Forskellige parametre (Kρ, flux, lag-time, konc. i hud, konc. optaget) målt eller udregnet på baggrund af modelstoffernes optagelse over den dermale barriere som funktion af vandopløseligheden. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.9. Forholdet mellem logKρ og modelstoffernes vandopløselighed (Log). Der er ingen Kρ fundet for stofferne antipyrin og miconazol og de er derfor ikke medtaget i plottet. [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].](images/s46b.gif)
Figur 3.3.9. Forholdet mellem logKρ og modelstoffernes vandopløselighed (Log). Der er ingen Kρ fundet for stofferne antipyrin og miconazol og de er derfor ikke medtaget i plottet. [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].
3.3.1.4 Matematiske modeller
Permeabilitetskoefficienten Kρ er som tidligere nævnt den hastighed, hvormed et givet stof kan penetrere huden (cm/time). Der er udviklet en del formler til beregning af Kρ, hvoraf projektgruppen tidligere har afprøvet flere af modellerne (Engelund EH, 2003; Holmberg RD, 2004). Nedenfor er en model til beregning af Kρ beskrevet.
Potts & Guy
Potts og Guy har i 1990’erne udviklet en model til beregning af Kρ, som nok i dag er den mest anvendte simple model (Guy, 1993). Kρ beregnes ved hjælp af følgende formel:
| (målt i cm/time) |
SkinPerm
SkinPerm modellen er udviklet af W.F. ten Berge fra Holland og er primært udviklet til at beskrive hudabsorption og anvendes som risikovurderingsværktøj i forbindelse med eksponering via arbejdsmiljøet (Berge WF, 2003). Modellen er primært baseret på fysisk-kemiske data på det enkelte stof såsom logKow.
Modellen er baseret på en antagelse om, at den drivende kraft ind i huden kun opnås ved den mængde stof, der kan opløses i et vandigt lag på huden (Berge WF, 2003). Yderligere kan modellen kun anvendes for ikke ioniserede stoffer, der ikke virker irriterende på huden, ikke virker affedtende samt kan penetrere huden hurtigere end stoffet er metaboliseret i huden (Berge WF, 2003).
SkinPerm modellen betegner huden som en barriere, der består af følgende komponenter:
- Protein lag i hornlaget
- Lipid lag i hornlag
- Vandigt lag under hornlaget, hvorigennem stofferne skal penetrere for at nå blodbanen
Modellen beskriver hudpenetrationen vha. Kp (permeabilitetskoefficienten) udtrykt som:
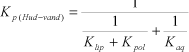 |
(cm/time) |
hvor:
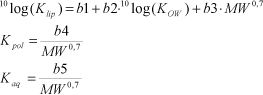
Klip er permeabilitetskoefficienteten i lipidlaget
Kpol er permeabilitetskoefficienteten i proteinlaget
Kaq er permeabilitetskoefficienteten i det vandige lag
KOW er oktanol/vand fordelingskoefficienteten
MW er molekylevægten
b1 (-2,59), b2 (0,7318), b3 (-0,006832), b4 (0,043) og b5 (1,361) er regressionskoefficienter
Skinperm modellen er bygget på Flynn’s datasæt (Flynn, 1990), der i vid udstrækning er blevet brugt til opbygning af modeller til beregning af Kp. De fem anvendte regressionskoefficienter er fundet ud fra Flynn’s datasæt og anvendt i modellen. Flynn’s datasæt er i høj grad koncentreret om stoffer med logKow omkring 0 til 4 og derfor beskrives stoffer med logKow <0 eller >4 ikke godt i modellen.
Modellen beregner en flux vha. følgende formel:
![]()
Hvor Ws er vandopløseligheden, som beregnes vha. formlen:
| (mg/cm³), der beskriver vandopløseligheden. |
Flux’en er begrænset af stoffets vandopløselighed, idet stoffet inden det kan passere ind i blodbanen skal trænge gennem det vandige lag lige under hornlaget.
3.3.1.5 Prædiktive hudabsorptionsværdier
På baggrund af allerede kendte simple matematiske modeller for estimering af transport over den dermale barrierer er prædikterede Kρ-værdier udregnet for modelstofferne (tabel 3.3.3.).
Tabel 3.3.3. Prædikterede Kρ-værdier beregnet vha. modellerne ’Potts & Guy’ og ’SkinPerm’
| Stofnavn | Observerede Kρ (µm/t) |
Prædikterede Kρ (Potts & Guy) (µm/t) |
Prædikterede Kρ (SkinPerm) (µm/t) |
|||
| Kρ | LogKρ | Kρ | LogKρ | Kρ | LogKρ | |
| Glyphosat | 0,06 | -1,22 | 0,0095 | -2,02 | 0,4 | -0,40 |
| Caffein | 3,8 | 0,58 | 1,11 | 0,05 | 1,41 | 0,15 |
| Antipyrin | - | - | 2,52 | 0,40 | 4,19 | 0,62 |
| Dimethoat | 4,9 | 0,69 | 2,39 | 0,38 | 2,53 | 0,40 |
| Benzoesyre | 50,6 | 1,70 | 72,9 | 1,86 | 88,7 | 1,95 |
| Bisphenol A | 2,1 | 0,32 | 175,65 | 2,24 | 191 | 2,28 |
| Methiocarb | 38,6 | 1,59 | 189,24 | 2,28 | 207 | 2,32 |
| Tebuconazol | 28,5 | 1,45 | 107,01 | 2,03 | 104 | 2,02 |
| Miconazol | - | - | 852,33 | 2,93 | 767 | 2,88 |
De i tabel 3.3.3 og figur 3.3.10 anførte prædikterede værdier for Kρ viser store forskelle mellem eksperimentelt bestemte værdier og modellerede værdier (bestemt ved Potts & Guy og SkinPerm). Denne diskrepans gør sig hovedsaglig gældende for stofferne med logKow > ca. 3. En undtagelse er antipyrin, som blev fundet ikke at trænge igennem huden, men som i modellerne synes at kunne trænge igennem huden. Som vist i figur 3.3.10 overestimerer modellerne hovedparten af de predikterede logKρ værdier med 46 % (Potts & Guy) og 35 % (SkinPerm).
![Figur 3.3.10. Observerede logKρ værdier som funktion af prædikterede logKρ værdier. De prædikterede værdier er beregnet ved hhv. modellen Potts & Guy og SkinPerm [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].](images/s49.gif)
Figur 3.3.10. Observerede logKρ værdier som funktion af prædikterede logKρ værdier. De prædikterede værdier er beregnet ved hhv. modellen Potts & Guy og SkinPerm [Gly: Glyphosat, Caf: Caffein; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol].
Som det ses i tabel 3.3.4 og figur 3.3.11 er der en tendens til at modellen SkinPerm overestimerer den beregnede flux. For modelstofferne antipyrin og benzoesyre overestimerer modellen temmelig meget i forhold til den målte værdi. Derimod underestimerer modellen kraftigt stoffernes lag-time i forhold til de observerede (figur 3.3.11). Denne overestimering af Kρ og underestimering af lag-time betyder at modellerne generelt overestimerer den mængde, der kan passere huden En væsentlig årsag til, at vi i dette studie finder lavere flux-værdier og højere lag-time værdier end de tidligere modeller, kan være, at de teoretiske modeller (fx Potts & Guy) anvender et datasæt baseret på forsøg med varierende eksperimentelt setup. For eksempel er der inkluderet forsøg baseret på fuldhud såvel som forsøg baseret på dermatom-hud.
Tabel 3.3.4. Observerede flux- og lag-time værdier og prædikterede flux- og lag-time værdier beregnet vha. modellen ’SkinPerm’
| Stofnavn | Observeret flux (nmol/cm² t) |
Predikteret flux (SkinPerm) (nmol/cm² t) |
Observeret lag-time (timer) |
Predikteret lag-time (timer) |
| Glyphosat | 0,14 | 2,5 | 7,9 | 1,6 |
| Caffein | 7,78 | 15,7 | 6,9 | 1,6 |
| Antipyrin | - | 115,8 | - | 0,8 |
| Dimethoat | 0,49 | 26,3 | 22,3 | 1,9 |
| Benzoesyre | 165,4 | 248,1 | 1,5 | 0,2 |
| Bisphenol A | 7,74 | 10,0 | 16,9 | 0,3 |
| Methiocarb | 0,54 | 2,5 | 11,7 | 0,3 |
| Tebuconazol | 0,57 | 1,2 | 14,0 | 0,9 |
| Miconazol | - | 1,8·10-¹7 | - | 1,08 |
![Figur 3.3.11. Observerede Flux-værdier som funktion af prædiktive flux-værdier og observerede lag-time værdier som funktion af prædiktive lag-time værdier beregnet ved modellen SkinPerm. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]](images/s50.gif)
Figur 3.3.11. Observerede Flux-værdier som funktion af prædiktive flux-værdier og observerede lag-time værdier som funktion af prædiktive lag-time værdier beregnet ved modellen SkinPerm. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol]
3.3.2 Transplacental transport
Ved den her anvendte ex vivo metode til undersøgelse af transporten over placenta er benyttet et dobbelt recirkulerende perfusionssystem, hvor koncentrationerne i maternelt (CM) og føtalt (CF) blod er målt i et lukket in vitro system.
Forholdet mellem CF og CM (FM-ratio) stiger lineært med tiden de første 30-60 minutter af forsøgene. Derefter flader kurven af, idet der er tale om et lukket system med en konstant mængde stof. FM-ratioen nærmer sig en ligevægt og FM-ratioen nærmer sig en konstant værdi, jf. figur 3.3.12.
Den initiale hældning af FM-ratioen som funktion af tiden kaldes den indikative permeabilitetskoefficient (IPK). Denne parameter er et mål for transporthastigheden over placentabarrieren (de enkelte regressioner for alle stofferne er angivet i figur 3.1.1 – 3.1.10). FM-ratioen er et mål for ligevægten mellem maternelt og føtalt blod. Undersøgelserne er kørt i 150 minutter. Der er derfor kun få målepunkter på kurvernes flade øverste stykke, som ikke er tilstrækkelige til at udføre robuste regressionsanalyser; for nogle stoffer er ligevægt endog ikke indtrådt. Derfor anvendes FM-ratioen ved 150 min (FM-ratio150min) som det bedst tilnærmede udtryk for ligevægt. Tabel 3.3.5 viser de gennemsnitlige værdier af FM-ratio150min og IPK for de 9 modelstoffer.
Tabel 3.3.5. For de undersøgte modelstoffer er den indikative permeabilitets koefficient (IPK) og FM-ratioen (udtrykt ved forholdet mellem føtalt og maternelt blod, CF hhv. CM) efter 150 minutters testperiode angivet
| Stofnavn | Antal studier (N) | Indikativ permeabilitets koefficient (IPK) (t-¹) | FM-ratio150min |
| Glyphosat | 7 | 0,11 | 0,34 ± 0,14 |
| Caffein | 7 | 1,03 | 0,92 ± 0,05 |
| Antipyrin | 19 | 0,92 | 0,97 ± 0,03 |
| Dimethoat | 2 | 0,98 | 0,9 ± 0,6 |
| Benzoesyre | 5 | 0,62 | 0,91 ± 0,04 |
| Bisphenol A | 3 | 0,32 | 0,29 ± 0,13 |
| Methiocarb | 2 | 0,23 | 1,21 ± 1,5 |
| Tebuconazol | 2 | 0,33 | 0,32 ± 0,07 |
| Miconazol | 2 | 0 | 0 |
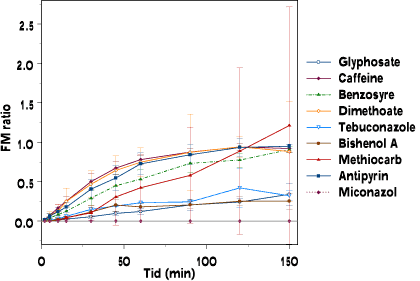
Figur 3.3.12. FM ratio (udtrykt ved forholdet CF/CM) som funktion af tid for de ni modelstoffer. Testperioden var 150 min.
3.3.2.1 Fysisk-kemiske parametre med betydning for transplacental transport
Tidligere undersøgelser af transplacental transport har indikeret, at parametrene molekylestørrelse, lipofilicitet samt hydrogenbindingsevne har betydning for et stofs transport over placenta (Hewitt, 2007).
Da den indikative permeabilitetskoefficient (IPK) er et mål for stoffernes evne til at penetrere placenta, er det undersøgt om, denne parameter har en lineær sammenhæng med ovenstående fysisk-kemiske parametre (figur 3.3.13).
I figur 3.3.13 ses det, at der findes en sammenhæng mellem et stofs evne til at penetrere placenta / hastigheden, hvormed placenta passeres (IPK og FM-ratio150min) og stoffets lipofilicitet beskrevet ved logKow, jo højere logKow desto lavere permeabilitetskoefficient. Dog ser det ud til, at stoffet glyphosat ikke passer ind i dette mønster.
En lineær sammenhæng mellem FM ratio og logKow er beskrevet ved Y = - 0,1767x + 1,0144 (r² = 0,9118), når glyphosat og methiocarb udlades af regressionen (figur 3.3.14.). Ligeledes ses en lineær sammenhæng mellem IPK og logKow beskrevet ved y = -0,2135x + 1,0355 (r² = 0,9629), hvor glyphosat og miconazol er udeladt af regressionen (figur 3.3.15).
Der blev også observeret en sammenhæng mellem modelstoffernes vandopløselighed og IPK. Yderpunkterne for de testede modelstoffer hvad angår logKow falder dog igen udenfor denne sammenhæng (glyphosat og miconazol). Sammenhængen mellem vandopløselighed og IPK viser en lineær sammenhæng (figur 3.3.16), hvor en stigende vandopløselighed betinger stigende IPK-værdier.
![Figur 3.3.13. FM ratioen (forholdet mellem føtalt og maternelt blod – CF/CM) og den indikative permeabilitetskoefficient (IPK) som funktion af molekylevægt, logKow.og vandopløselighed. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s53a.gif)
Figur 3.3.13. FM ratioen (forholdet mellem føtalt og maternelt blod – CF/CM) og den indikative permeabilitetskoefficient (IPK) som funktion af molekylevægt, logKow.og vandopløselighed. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.14. Lineær sammenhæng mellem FM ratio og logKow for 7 af de 9 modelstoffer beskrevet ved ligningen Y = - 0,1767x + 1,0144 (r² = 0,9118). Glyphosat og methiocarb er ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s53b.gif)
Figur 3.3.14. Lineær sammenhæng mellem FM ratio og logKow for 7 af de 9 modelstoffer beskrevet ved ligningen Y = - 0,1767x + 1,0144 (r² = 0,9118). Glyphosat og methiocarb er ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.15. Lineær sammenhæng mellem IPK og logKow for 8 af de 9 modelstoffer udtrykt ved regressionsligningen Y = - 0,1864 + 0,9987 (r² = 0,9537). Glyphosat falder udenfor den lineære sammenhæng og udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s54a.gif)
Figur 3.3.15. Lineær sammenhæng mellem IPK og logKow for 8 af de 9 modelstoffer udtrykt ved regressionsligningen Y = - 0,1864 + 0,9987 (r² = 0,9537). Glyphosat falder udenfor den lineære sammenhæng og udeladt af regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
![Figur 3.3.16. Lineær sammenhæng mellem IPK og log(Vandopløselighed) for 7 af de 9 modelstoffer udtrykt ved regressionsligningen y = 0,2347x + 0,5985 (r² = 0,9389). Glyphosat falder udenfor den lineære tendens og derfor udeladt af regressionen. Miconazol passer tilsyneladende fint i den lineære regression, men da IPK ikke kan være negativ er miconazol ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].](images/s54b.gif)
Figur 3.3.16. Lineær sammenhæng mellem IPK og log(Vandopløselighed) for 7 af de 9 modelstoffer udtrykt ved regressionsligningen y = 0,2347x + 0,5985 (r² = 0,9389). Glyphosat falder udenfor den lineære tendens og derfor udeladt af regressionen. Miconazol passer tilsyneladende fint i den lineære regression, men da IPK ikke kan være negativ er miconazol ikke medtaget i regressionen. [Gly: Glyphosat, Caf: Caffein; Ant: Antipyrin; Dim: Dimethoat; Ben: Benzoesyre; Bis: Bisphenol A; Met: Methiocarb; Teb: Tebuconazol; Mic: Miconazol].
3.3.2.2 Modeller til beskrivelse af transplacental transport
Kemiske stoffer passerer placenta hovedsagelig ved simpel passiv diffusion (Audus, 1999). Andre mekanismer forekommer dog også, f.eks. faciliteret diffusion, aktiv transport, pinocytose og filtrering (Pacifici, 1995; Reynolds, 1990). Det er anført, at de vigtigste stofegenskaber, som bestemmer passiv diffusion over placenta er molekylevægt, ionisationsgrad (pKa), lipofilicitet og proteinbinding (Audus, 1999; Pacifici, 1995). Det er endvidere fundet, at stoffer med molekylvægt større end ca. 500 Da (g/mol) transporteres dårligt over placenta (Pacifici, 1995). Ikke-ioniserede stoffer passerer placenta lettere end ioniserede (Audus, 1999; Reynolds, 1990), hvilket betyder, at stoffer med syre-/baseegenskaber kun delvis vil passere placenta og i en grad som er proportional med deres ioniseringsgrad. Føtalt blod er mere surt end maternelt blod, hvilket medfører, at svagt basiske stoffer vil ophobes på den føtale side af placenta (”ion trapping”) (Reynolds, 1990). I den i dette projekt anvendte forsøgsopstilling er der dog ikke forskel i pH mellem den føtale og maternelle side (forskel < 0,1 pH-enhed). Indenfor et vist interval af lipofilicitet (logKow) er der en lineær sammenhæng mellem placenta passage og logKow (Akbaraly, 1985; Pacifici, 2005). Plasmabinding i maternelt blod vil medføre, at den del af stoffet, som er bundet til plasmaprotein, ikke vil være tilgængelig for transport over placenta (Corley, 2003).
I de publicerede artikler benyttes 2 forskellige mål for placenta transport: clearance og transfer og data opgives ofte som ”Clearance Index” (CI) og ”Transfer Index” (TI). Disse indices defineres således:
|
Clearance Index | = | Clearance af teststof | |
| Clearance af antipyrin |
|
Transfer Index | = | Transfer af teststof (%) | |
| Transfer af antipyrin (%) |
hvor antipyrin er benyttet som intern kontrol/standard. Clearance er defineret af Schneider et al. 1972 (Schneider, 1972) som
|
Clearance | = | [CV]f – [(CA]f x FFR | |
| [CA]m |
hvor [CV]f er koncentration i føtalt venøst blod, [CA]f er koncentration i føtalt arterielt blod, [CA]m er koncentration i maternelt arterielt blod og FFR er føtalt blod flowrate. Transfer er defineret af bl.a. Heikkinen et al. 2002 (Heikkinen, 2002) som
|
Transfer % | = | [Css]f x FFR x 100 | |
| [CA]m x MFR |
hvor [Css]f er ligevægtskoncentrationen i føtalt venøst blod, [CA]m er koncentrationen i maternelt arterielt blod, FFR er føtalt blod flowrate og MFR er maternelt blod flowrate.
Hewitt et al (Hewitt, 2007)har i et nyligt udarbejdet review over (Q)SAR modellering for transplacental transport lavet metastudier baseret på eksisterende, publicerede in vitro data fra mange kilder. De afprøvede 2 heterogene datasæt, et med CI-data (86 stoffer) og et med TI-data (58 stoffer), samt 3 homogene datasæt som var delmængder af de heterogene datasæt, 1 med CI-data og 2 med TI-data. De homogene datasæt (stoffer som var kemisk beslægtede) viste generelt bedre korrelation (r² = 0,76-0,94) end de heterogene datasæt (r² = 0,62-0,63). En lang række molekylære deskriptorer plus de sædvanlige fysisk-kemiske parametre indenfor grupperne hydrogenbinding, molekylestørrelse og hydrofobicitet blev afprøvet. Men der var ingen fælles deskriptorer for de 5 datasæt. Det ene homogene datasæt (CI-data) for tocolytiske stoffer viste en lineær sammenhæng mellem CI og logKow med regressionsudtrykket:
CI = 0,139 logKow – 0.0605 (n = 8; r² = 0.858)
Akbaraly et al (Akbaraly, 1985) målte den transplacentale transport for en heterogen gruppe stoffer, hovedsagelig lægemidler og fandt følgende sammenhænge mellem TI og logKow:
logTI = 0,223 logKow – 0,250 (n = 17; r² = 0,81)
og
logTI = 0,189 logKow – 0,084 (logKow)² – 0,14 (n = 17; r² = 0,941)
Det ser således ud til, at lipofilicitet er den deskriptor, som giver den bedste korrelation til placentatransport om end de publicerede regressioner afviger en del fra hinanden.
Vi har ikke data på arterielle og venøse koncentrationer og kan derfor ikke applicere disse modeller på vores datasæt.
Version 1.0 Juli 2009, © Miljøstyrelsen.