Miljøprojekt nr. 1306, 2009
Dermal absorption af bekæmpelsesmidler - Evaluering af årsager til variation samt forebyggelsesmuligheder
Indholdsfortegnelse
3 Metoder til at studere hudpenetration
4 Biologiske faktorer med indflydelse på hudpenetration
6 Betydning af opløselighed og molekylstørrelse
7 Hjælpestoffers effekt på hudintegriteten og hudpenetrationen
8 Penetration af pesticider gennem beskadiget hud
9 Afvaskning af huden og midlertidig huddeponering
10 Forebyggelse af dermal absorption ved brug af personlige værnemidler
- 10.1 Personlige værnemidler
- 10.2 Typer af handsker og penetration af pesticider
- 10.3 Brug og genbrug af handsker
- 10.4 Genbrugshandsker
11 Konklusioner og perspektiver
Forord
Flere projekter er gennem årene blevet udgivet af Miljøstyrelsen og beskriver betydningen af en række relevante faktorer for variationen mellem individer i hudabsorption af bekæmpelsesmidler. For at give en samlet fremstilling af disse projekter og den nyere tilgængelige litteratur er der udarbejdet en større, mere omfangsrig, og detaljeret engelsksproget rapport (Dermal absorption of pesticides – evaluation of variability and prevention). Nærværende danske udgave af rapporten resumerer hovedkonklusionerne fra den engelsksprogede rapport.
Rapporten har til mål at forbedre og tilgængeliggøre den faglige og evidensbaserede baggrund for regulatoriske tiltag til forebyggelse af hudoptagelse af bekæmpelsesmidler. Rapporten afsluttes med en opsummering af den reguleringsmæssige betydning i forhold til forebyggelse samt et afsnit om fortsatte ubesvarede forskningsspørgsmål. Rapporten er tænkt som baggrundsinformation for arbejdsmiljøprofessionelle, faglige organisationer, regulatoriske myndigheder samt Arbejds- og Miljømedicinske klinikker.
Forfatterne er taknemlige for de konstruktive, skriftlige kommentarer fra en gruppe af eksterne eksperter (Flemming Lander, Mari-Ann Flyvholm, Svend Edelfors) samt ansatte ved Miljøstyrelsen (Lærke Ambo Nielsen, Susanne Hougaard, Jørn Kirkegaard).
December 2008
Rikke Holmgaard, MD
Jesper Bo Nielsen, PhD
Sammenfatning
Flere projekter er gennem årene blevet udgivet af Miljøstyrelsen med beskrivelse af faktorer af betydning for variationer i hudoptagelsen af bekæmpelsesmidler. For at give en samlet fremstilling af disse projekter og den nyere tilgængelige litteratur er der udarbejdet en detaljeret engelsksproget rapport (Dermal absorption of pesticides – evaluation of variability and prevention). Den rapport er suppleret med en kortere dansk udgave (Dermal absorption af bekæmpelsesmidler – evaluering af årsager til variation samt forebyggelsesmuligheder), der resumerer hovedkonklusionerne fra den engelsksprogede rapport.
Variation i hudoptagelsen efter udsættelse for bekæmpelsesmidler afhænger af personens egen sårbarhed, anvendelse af forebyggelsestiltag, samt af bekæmpelsesmidlernes kemiske egenskaber.
Der er således stor forskel på, hvor godt kemiske stoffer trænger over huden fra forskellige steder på kroppen, ligesom man optager klart større mængder fremmedstoffer over huden, hvis huden er beskadiget med rifter, hudafskrabninger, eksem eller er opblødt efter længere tids vådt arbejde. Det skyldes at hudens beskyttelsesevne i meget høj grad afhænger af det yderste meget tynde lag af huden (stratum corneum). Men der findes heldigvis måder at beskytte sig på. Bruger man for eksempel handsker, vil man være godt beskyttet mod at få noget på hænderne. Her er det imidlertid meget vigtigt at man anvender de rigtige handsker, der passer til de kemiske stoffer, man arbejder med, ligesom engangshandsker kun skal tages på én gang og altså ikke genbruges.. Endvidere vises det, at det virkelig betyder noget at vaske hænder efter at man har haft kontakt til bekæmpelsesmidler.
En række egenskaber ved kemiske stoffer har også betydning for deres evne til at trænge gennem huden. Rapporten dokumenterer, hvorledes store molekyler generelt er længere tid om at passere huden, ligesom rapporten beskriver, hvorledes stofferne opløselighed har stor indflydelse på, hvor hurtigt stofferne passerer huden. Denne viden kan bruges til at opstille simple modeller til forudsigelse af andre fremmedstoffers evne til at trænge gennem huden.
Rapporten har til mål at forbedre og tilgængeliggøre den faglige baggrund for regulatoriske tiltag til forebyggelse af hudoptagelse af bekæmpelsesmidler. Rapporten er tænkt som baggrundsinformation for arbejdsmiljøprofessionelle, faglige organisationer, regulatoriske myndigheder samt Arbejds- og Miljømedicinske klinikker.
Summary
Several projects describing factors of relevance to variations in dermal absorption of pesticides have during recent years been published by the Danish EPA. To summarize these projects and update them with the most recent literature, a detailed report (Dermal absorption of pesticides – evaluation of variability and prevention) was made. This report was supplemented with a shorter Danish version (Dermal absorption af bekæmpelsesmidler – evaluering af årsager til variation samt forebyggelsesmuligheder) focusing on the main conclusions from the English report.
Variability in dermal absorption following exposure to pesticides depends on individual susceptibility, use of preventive measures, and chemical characteristics of the pesticides.
There are large differences between penetration rates of a chemical through skin from different parts of the body. Likewise, dermal absorption of chemicals is significantly enhanced through skin compromised by minor scrapes, atopic dermatitis, eczema, or by hydrated skin due to wet work. The reason is that protection against dermal absorption of chemicals mainly depends on the condition of the upper very thin layer on the skin (stratum corneum). Fortunately, personal protective equipment such as gloves exists that will prevent or reduce dermal exposure of the hands. It is, however, of immense importance to use the type of gloves suitable for the pesticide in question, and not use disposable gloves more than once. Further, evidence is presented that hand wash following dermal exposure to pesticides significantly reduces absorption.
Different chemical characteristics of pesticides affect their ability to penetrate human skin. This report presents evidence that large molecules (high molecular weight) generally require more time to be absorbed through the skin. Likewise, solubility characteristics of the pesticides will affect penetration rates. This knowledge may be used for establishing mathematic models that can be used to predict dermal penetration characteristics of other chemicals.
This report is aimed at improving the scientific background and the accessibility of knowledge on regulatory measures to prevent or reduce dermal absorption of pesticides. The report is intended to be used as background information by occupational health professionals, labour organizations, and regulatory agencies.
Indledning
Bekæmpelsesmidler (pesticider) er blandt de få produkter, der fremstilles med det mål at skade planter og dyr. Antallet og anvendelsesområderne for pesticider er stort og varierer, og mange af de steder og måder, hvor produkterne anvendes, sker med potentiel mulighed for direkte eller indirekte påvirkning af mennesker.
Den dominerende eksponeringsvej for pesticider i landbrug, gartnerier og i eget hjem er dermal (Archibald et al., 1994; Benford et al., 1999). Eksponeringen sker hyppigst under re-entry aktiviteter, hvor planter håndteres kort tid efter, at de er blevet behandlet med pesticider. Her er der direkte kontakt til blade, stængler og jord, på hvis overflade pesticiderne stadig befinder sig. Behandlingshyppigheder er afhængig af de dyrkede kulturer og varierer meget. Undersøgelser fra fynske gartnerier viser, at behandlingshyppigheden i visse perioder kan være 3-5 gange om ugen. Afhængig af pesticidtype vil aktivstoffet kunne genfindes på overflader i kortere eller længere tid efter udbringning. Den hyppige behandling med flere forskellige midler, fx svampemidler og retarderingsmidler, gør, at samtidig dermal eksponering for flere stoffer kan være hyppig.
Formålet med rapporten er ikke at afdække nye forhold relateret til hudpenetration af pesticider, men at beskrive og opsummere den eksisterende viden inden for området. Rapporten vil indeholde en diskussion af potentielle konsekvenser for regulatoriske guidelines, der er implementeret og brugt af myndighederne.
Rapporten er tænkt som baggrundsinformation for arbejdsmiljøprofessionelle, faglige organisationer, regulatoriske myndigheder samt Arbejds- og Miljømedicinske klinikker til brug ved vurdering af risici og forebyggelse af eksponering ved brug af bekæmpelsesmidler. Brugerne kan i rapporten finde information om risici ved at bruge disse produkter, forhold af betydning for den enkeltes absorption, samt om vigtigheden af at bruge egnede personlige værnemidler.
1 Hudens struktur og funktion
Huden er kroppens største organ og er en yderst kompliceret struktur, som konstant udsættes for kemikalier, mekanisk påvirkning, mikroorganismer, UV-lys, temperaturændringer og væsketab. Den vigtigste funktion for huden som organ er at minimere utilsigtet væsketab og opretholde en normal væskebalance samt at virke som barriere mod ovenstående eksponeringer.
Huden består af forskellige lag (figur 1) samt hårfollikler og kirtler. Lagene inddeles i en ydre del (epidermis) samt en indre del (dermis). Kroppens forskellige regioner har forskellig hudtykkelse. Den levedygtige epidermis kan nedbryde kemikalier, som infiltrerer det yderste cellelag - stratum corneum. Dermis yder fysiologisk støtte til epidermis og giver næring til denne del af huden, der ikke har egen blodforsyning.
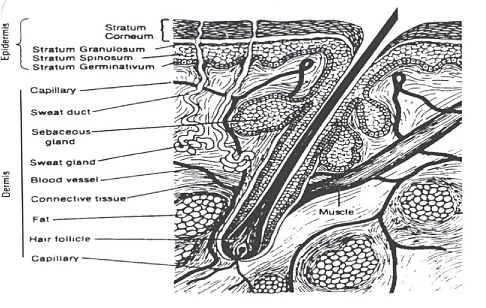
Figur 1: Hudens struktur
Stratum corneum består af en heterogen struktur af celler (40% protein, 40% vand, og ca. 20% lipider) (Michales AS et al., 1975). Lipiderne findes overvejende i extracellulærfasen, og denne struktur af celler omgivet af lipider er beskrevet som ”Brick and mortar” – mursten i mørtel (Elias, 1983). Fordi extracellularfasen indeholder lipider, har den en lav gennemtrængelighed for mange hydrofobe stoffer og en beskyttende effekt over for individet. Murstenene (keratinocytterne) virker som en hydrofil membran og er næsten uigennemtrængelig for vand og er derfor med i reguleringen af væsketabet fra huden.
Et tidligere studie har påvist, at såvel meget lipofile som meget hydrofile stoffer penetrerer huden dårligt (Nielsen JB, 2004).
2 Hudpenetration
Hudpenetration som følge af hudeksponering er af stor vigtighed både klinisk, erhvervsmæssigt og miljømæssigt. Mange mennesker har og bliver stadig utilsigtet eksponeret for toksiske stoffer enten i hjemmet eller på jobbet. Det drejer sig om støv, pesticider, opløsningsmidler etc.. Hudpenetration er imidlertid vanskelig at kvantificere (såfremt den ikke er massiv) og bliver derfor sjældent regnet for en væsentlig eksponeringsvej, selvom folk oplever problemer, efter at deres hud har været eksponeret for farlige stoffer. Det er derfor vigtigt, at sætte fokus på disse problemer og forbedre procedurer omkring arbejdsforhold med mulig hudkontakt til pesticider.
For at et stof kan passere huden må følgende finde sted (Guy et al., 1987; Kao et al., 1988; Clark NWE, 1992):
- Stoffet kommer i kontakt med stratum corneum
- Passiv diffusion af stoffet gennem stratum corneum
- Passage fra det lipofile stratum corneum til det mere hydrofile epidermis
- Fortsat passage fra det avaskulære epidermis til det velvaskulariserede dermis
- Fra dermis optages stoffet via mikrocirkulationen i den systemiske cirkulation
Permeabilitetskoefficienten stiger i takt med, at lipofiliciteten stiger (Roy & Flynn, 1989). Et lipofilt stof vil nemmere passere gennem stratum corneum, men penetrationsraten vil falde, når stoffet når det hydrofile epidermis. Ficks lov om diffusion gælder alene under meget specifikke forhold, men giver et fingerpeg om penetrationshastigheden (fluxen) (Grandjean P, 1990).
JSS = kP * ΔC
JSS = flux af det penetrerende molekyle under steady-state forhold (absorption rate; udtrykt som µg/cm²*time); kP = permeabilitetskoefficienten gennem huden (cm/time) og ΔC = koncentrationsgradienten over huden (ug/cm³)
Permeabilitetskoefficienten kan også udregnes ud fra eksperimentelle data :
kP = JSS /A * ΔC = K * D /h
JSS = flux af det penetrerende molekyle (µg/time); A = applikationsarealet (fx arealet i en Franz diffusionscelle, cm²); K = hud/vehikel partition koefficienten i opløsningen. D = diffusionskoefficienten. h = længden af diffusionsvejen (cm).
Lag-time er den tid, det tager, fra et stof påføres hudoverfladen, til stoffet kan påvises på den anden side af huden. Det er vigtigt at kende lag-time for de stoffer, der arbejdes med, da flux (penetrationsraten) og lag-time influerer på den mængde stof, der optages over huden i løbet af fx en arbejdsdag (figur 2).
Manglende kendskab til lag-time for forskellige stoffer vanskeliggør risikovurdering.
Når et stof ophobes i huden i stedet for at passere direkte gennem til blodet, beskrives det som et reservoir. Reservoiret kan forefindes i stratum corneum, dybere epidermis eller i dermis (Roberts et al., 2004). Stoffet i reservoiret bliver ofte frigivet med en hvis forsinkelse til blodet eller måske tilbage til hudoverfladen. Absorptionen af stoffet til blodet fortsætter fra applikationsområdet med en dalende hastighed, hvilket vil give indtryk af en forlænget udskillende (Cnubben et al., 2002).

Figur 2: Teoretisk penetrations kurve for to stoffer A og B med identisk total penetration efter 6 timer, men med forskellig lag-time og flux.
3 Metoder til at studere hudpenetration
Gennem de seneste årtier har metoder til at standardisere og validere eksperimentelle modeller for hudpenetration fået meget opmærksomhed. Der eksisterer både in vitro- og in vivo-metoder, og hver metode har fordele og ulemper. Derfor accepterer OECD også flere forskellige metoder i deres guidelines.
I 2004 lavede OECD guidelines for testning af kemikalier via in vitro-metoder. Standardprincipperne blev beskrevet ved brugen af enten statiske diffusionsceller eller flow-through celler. I begge metoder påføres teststoffet til hudoverfladen – som adskiller donorkammer fra receptorkammer – og mængden af penetreret stof måles i receptorkammeret over tid (OECD, 2004).
3.1 In vitro modeller
3.1.1 Statisk diffusionscelle
I 1975 udviklede Franz den statiske diffusionscelle (figur 3), som nu er en af de mest brugte in vitro-modeller, når det gælder forskning inden for hudpenetration. Modellen har et simpelt design og er billig i drift. Der kan bruges human- eller dyrehud samt fuldhud eller delhud. Teststoffet tilsættes donorkammeret. Stoffet passerer gennem huden, der ligger på et metalgitter mellem donor- og receptorkammer. I receptorkammeret optages stoffet i en receptorvæske, hvor man vha. magnetomrøring undgår koncentrationsgradienter i væsken. Receptorkammeret står i et 37º grader varmt vandbad, der sikrer en temperatur på hudens overflade svarende til de omkring 32º på normal hud.

Figur 3: Statisk diffusionscelle.
3.1.2 Flow-through-celle
En anden in vitro-model er ”flow-through cellen” (figur 4), der ligesom den statiske diffusionscelle kan bruges med både human hud, dyrehud, fuldhud og delhud. Cellen er specielt velegnet til at bestemme reservoireffekten (Bronaugh & Stewart, 1985a). Den består af et donorkammer, hvori teststoffet tilsættes. Derefter passerer stoffet gennem huden til receptorkammeret. I receptorkammeret løber en opsamlingsvæske med konstant hastighed. Denne væske kan sammenlignes med blodstrømmen i en blodåre.
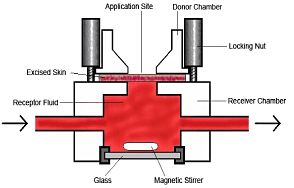
Figur 4: Flow-through cellen (Tilladelse til brug af skitsen fra Dr. Wilkinson SC, University of Newcastle).
3.2 In vivo modeller
In vivo studier er baserede på fysiologisk og metabolisk intakte systemer. Der er to slags in vivo studier: 1) dyre studier eller 2) humane studier. Det mest anvendte dyr er rotten, selvom studier har vist, at man ved brug af dette dyr ofte overestimerer human hudabsorption, men valget af et andet forsøgsdyr forøger omkostningen ved forsøget (ECETOC, 1993).
I 2004 vedtog OECD guidelines for afprøvning af kemikalier via in vivo-metoder. Standardprincipperne blev beskrevet som applikation af teststoffet på huden i den korrekte applikationsform og det rette tidsrum. Endvidere beskriver guidelines prøvetagning af forskellige kropsvæsker eller væv med specifikke intervaller samt kvantificering af teststofferne eller deres metabolitter med en tilpas sensitiv analysemetode.
3.2.1 Traditionel metode
Ved den traditionelle metode appliceres teststoffet til huden af raske frivillige forsøgspersoner, hvorefter blod og/eller urin opsamles og analyseres. Mængden af teststof, der findes i blodet/urinen, giver en god indikation af den mængde stof, der er absorberet gennem huden til den systemiske cirkulation. Denne metode har været brugt, før alle andre teknikker blev udviklet, og bruges stadig, hvor der ikke er væsentlig risiko for de frivillige forsøgspersoner (Lammers JHCM et al., 2005; Nohynek et al., 2006; Hueber-Becker et al., 2007). Ofte er risici dog ukendt, hvilket i forsøgsøjemed gør det etisk bekymrende at bruge forsøgspersoner.
3.2.2 Microdialyse
Microdialyseteknikken er brugt klinisk i mange år til kontinuerlig måling af fx ilttension i transplanteret væv såvel som i forskning, hvor fremmedstoffers kinetik kan følges. Det er den eneste teknik, der kan opsamle endogene/eksogene substanser i det ekstracellulære rum i levende væv, og den er derfor vigtig ved undersøgelser af farmakologiske og biokemiske processer i væv. Denne type data kan give vigtig information i bestemmelsen af farmakokinetiske samt farmakodynamiske forhold for forskellige stoffer og kan derigennem give en bedre beskrivelse af eksponeringsrisici (Chaurasia et al., 2007).
Principperne ved microdialyse er, at proben imiterer et blodkar i dermis (figur 5). Teststoffet tilføres hudoverfladen, hvorefter det penetrerer til dermis, hvor proben ligger. Proben består af en semi-permeabel struktur, hvorigennem molekyler kan passere til perfusatet, der løber igennem proben til et opsamlingsglas. Molekylerne diffunderer over membranen grundet koncentrationsgradienten, der opstår, når perfusatet pumpes gennem proben med en konstant og meget præcis hastighed. Perfusatet indeholdende molekyler af teststof kaldes nu for dialysatet. Dialysatet opsamles til videre analyse. Teknikken har været brugt i såvel humane undersøgelser som i dyreforsøg (Groth, 1996; Benfeldt & Serup, 1999; Benfeldt et al., 2007).
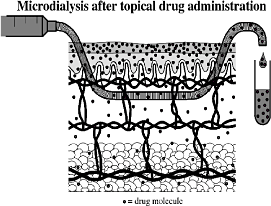
Figur 5: Microdialyse. Proben beliggende i dermis. (Benfeldt & Serup, 1999)
3.2.3 Tape-stripping
Tape-stripping er en velkendt in vivo-metode, som også bruges in vitro. Teststoffet (ofte radioaktivt mærket) penetrerer et forudbestemt område af huden over et bestemt tidsinterval. Derefter vaskes huden skånsomt for at fjerne eventuelle uabsorberede rester på hudoverfladen. Endeligt fjernes hudens tynde lag af eksponeret stratum corneum ved gentagne påsætninger og fjernelser af tapestykker. De fjernede celler på tapen kan derefter analyseres med en egnet analysemetode. Metoden er billig at anvende og minimal invasiv, såfremt kun døde hudceller fjernes, men har også visse metodemæssige begrænsninger.
I dermato-farmakologien bruges tape-stripping til at fremskaffe information om lægemidler appliceret på huden. Tape-stripping er en speciel nyttig teknik, når det gælder studier om lokal biotilgængelighed af præparater med effekt i hudens øverste lag, som fx antibiotika (Lboutounne et al., 2002) , svampemidler (Alberti et al., 2001) eller UVA/UVB filtre (Fernandez et al., 2002; Wissing & Muller, 2002; Jacobi et al., 2004; Sarveiya et al., 2004).
De forskellige metoder har hver deres fordele og ulemper (uddybet i den engelsksprogede rapport) og bør benyttes alt efter formål.
4 Biologiske faktorer med indflydelse på hudpenetration
Flere biologiske faktorer påvirker hudabsorptionen. Primært har området, hvor huden eksponeres, meget stor indflydelse på, hvor godt et stof trænger over hudbarrieren. Desuden har individets alder også en vis indflydelse på hudens gennemtrængelighed.
4.1 Applikationsområde
Området, der eksponeres, er væsentligt for penetrationshastigheden af mange stoffer. Det har været vist, at for lægemidlet hydrocortison har huden på scrotum den største permeabilitet og huden på fodsålerne den laveste. Permeabiliteten varierer over 40 gange (Feldmann & Maibach, 1967). Der forventes således også at være forskel på penetrationsraten mellem den ubeskadigede håndflade og underarm. Der er dog endnu ikke lavet et generelt kort over kroppens permeabilitet, der passer på alle stoffer, og grunden til forskellen kan skyldes både antallet af follikler, tykkelsen af stratum corneum, sebum-kompositionen samt strukturen af kapillærerne (Rougier et al., 1999).
4.2 Alder
Alderen indvirker på hudstrukturen og på hudens permeabilitet. Strukturen ændrer sig med alderen – stratum corneum bliver mere tør og overfladelipiderne færre. Generelt bliver huden mere rynket og vandindholdet i huden forskubbes til i mindre grad at være proteinbundet (Waller & Maibach, 2006). Ændringen i overfladelipider og vandindhold har vist sig at have den største effekt på hydrofile stoffers hudgennemtrængelighed, da lipofile stoffer let opløses i stratum corneum på trods af de færre lipider (Roskos et al., 1989).
4.3 Hudbarrieren
Hudens barrierefunktion bestemmes hovedsagelig af, hvorvidt stratum corneum er intakt eller ej. Ændringer eller skade på hudstrukturen øger permeabiliteten. Denne ændring kan være kemisk eller fysisk betinget eller skyldes sygdom. Flere opløsningsmidler har vist sig at ændre hudbarrieren, og der er udført talrige studier, der påviser dette (Nielsen & Nielsen, 2000; Kezic et al., 2001; Rosado & Rodrigues, 2003; Dias et al., 2008). Hudsygdomme som atopisk dermatitis ændrer hudbarrieren pga. et reduceret lipidindhold i stratum corneum (Imokawa et al., 1991; Yamamoto et al., 1991), ligesom det nu er påvist, at 10 % af den europæiske befolkning har en mutation i filaggrin-genet (Palmer et al., 2006), der gør filaggrin funktionsløst. Filaggrin er nøgleprotein i opbygningen af hudens barriere, og manglende funktion giver udtørring af huden (Kezic et al., 2008) med potentielt store penetrationshastighed til følge.
4.4 Metabolisme
Kroppens primære metaboliske organ er leveren, men også huden har en vis metabolisk kapacitet (Denyer S.P et al., 1985). Målet er at omdanne stofferne, så de bliver lettere for kroppen at udskille. Men metabolismen kan også føre til mere toksiske metabolitter (Liu et al., 2002; Liu & Kim, 2003)..
4.5 Hydrering
For at huden skal virke som en god barriere er det vigtigt, at den indeholder tilstrækkelig fugt, om end også for meget fugt øger absorptionen. Dette kan ses ved brugen af gummihandsker samt hos opvaskere, rengøringspersonale, frisører mm. Disse fag er forbundet med en øget forekomst af kontakteksem, som skyldes et øget optag af hudirritanter. Da vand- og lufttæthed (gummihandsker) har vist sig at være den faktor, der øger hudens penetration mest, er det vigtigt, at man undgår kemikalier inden i handskerne.
5 Pesticider
5.1 Definition
Bekæmpelsesmidler (pesticider) er produkter eller blandinger af produkter, der bruges for at forebygge, kontrollere og mindske effekten af skadedyr, svampe, eller ukrudt. Pesticider inddeles i kategorier alt efter formål, for eksempel insekticider, herbicider, rodenticider eller fungicider.
5.2 Brug
Brugen af pesticider er faldet gennem det sidste årti. Data fra Miljøstyrelsen viser, at pesticidsalget er faldet fra 19.400 ton i 1995 (6.600 ton aktivt stof) (Miljøstyrelsen, 1998) til 12.234 ton i 2006 (3.200 ton aktivt stof) (Miljøstyrelsen, 2007). Pesticider er i dag designet til at forblive i miljøet i kortere tid end tidligere og skulle på den måde være mindre skadelige for miljøet end førhen. Der er dog noget, der tyder på, at alternativer til pesticider faktisk er mere effektive end kemikalier, da man i Sverige har halveret brugen af pesticider uden nævneværdigt fald i produktion af afgrøder. I Indonesien har man reduceret brugen af pesticider i risproduktionen med 65 % og samtidig set en stigning i produktionen på 15 % (Miller, 2004). Alternativer til pesticider kan være mekanisk (fx radrensning af markafgrøder) eller biologisk bekæmpelse i væksthuse (fx snyltehvepse). Endelig er der arbejdet en del med udvikling af genmodificerede planter, der er modstandsdygtige overfor specifikke skadevoldere. Udvikling af mere potente pesticider vil dog også i statistiske oversigter af denne art fremstå som en reduktion i mængden af aktivstof.
5.3 Toksicitet
Toksiciteten kan inddeles i øjeblikkelig eller forsinket toksicitet samt reversible eller irreversible effekter.
Øjeblikkelige toksiske effekter kan defineres som effekter, der udvikler sig hurtigt efter en enkelt udsættelse for et stof, hvor forsinkede toksiske effekter er dem, der opstår lang tid efter eksponeringen. Hvorvidt en effekt er reversibel eller irreversibel afhænger ofte af, hvilket væv der er beskadiget, da nogle væv er bedre til at regenerere end andre (Klaassen CD, 1996).
De utilsigtede pesticideffekter kan også inddeles efter pesticidernes effekt:
| Effekt | Forklaring |
| Carcinogent | er evnen til at danne cancerceller. |
| Mutagent | er evnen til at skabe genetiske forandringer. |
| Leverskadeligt | kan føre til gulsot (ofte reversibel), skrumpelever og celledød. |
| Reproduktionsforstyrrelser | som reduceret sædkvalitet, sterilitet og abort. |
| Neurotoksicitet | skader på hjerne- og/eller nervevæv. |
| Allergi-sensibilitet | udvikling af allergi over for pesticider eller kemikalier brugt i fremstillingen eller formuleringen af disse. |
5.4 Symptomer
Symptomer på baggrund af toksicitet kan vise sig som akut toksicitet – kvalme, brystsmerter og opkastning eller som kroniske skade på lever, nyrer og lunger. De kan også vise sig langsomt uden nogen forudgående kliniske tegn på akut intoksikation fx vejrtrækningsbesvær eller hudsensibilisering (allergi) efter gentagen eksponering. Man kan også se forsinkede symptomer fx neurotoksicitet (med ugers forsinkelse) eller udvikling af cancer (med års forsinkelse) efter eksponering over for fx organofosfater.
6 Betydning af opløselighed og molekylstørrelse
Et stofs opløselighed kan udtrykkes som den mængde, der kan opløses i et givet medium ved en given temperatur, men generelt anvendes ofte stoffets lipofilicitet (forkærlighed for en fedtfase) eller stoffets hydrofilicitet (forkærlighed for en vandfase). Som samlet værdi anvendes da ofte ratioen mellem hvorledes stoffet ville fordele sig mellem en oktanolfase og en vandfase, en ratio der kendes som fordelingskoefficienten mellem oktanol og vand – Pow, og ofte beskrives i den logaritmiserede form logPow. Jo mere lipofilt et stof er, jo højere logPow-værdi.
Hudpenetration påvirkes af stoffets opløselighed Et meget lipofilt såvel som et meget hydrofilt stof har således begge en nedsat hudpenetrationen (McDougal & Boeniger, 2002). Denne viden er vigtig, når man fremstiller kosmetik eller medicinske produkter til brug på huden. Men også når man designer pesticider, der skal kunne penetrere fx en plantes overflade for at opnå den ønskede effekt. Et kendskab til penetrationshastighed er endvidere vigtigt i vurderingen af humane risici og muligheden for forebyggelse.
Stoffer, der skal penetrere huden, skal have en molekylær vægt under 1000 daltons. Vægten i sig selv er muligvis ikke den begrænsende faktor, men når molekylet bliver større, bliver den kemiske struktur også mere kompleks, og derfor reduceres penetrationen.
Nielsen et al. har testet glyphosat, benzosyre, malathion, koffein, pirimicarb, methiocarb, paclobutrazol, dimethoat og prochloraz og karakteriseret dem ved deres opløselighed, logPow, molekylevægt, Kp og lag-time (Nielsen et al., 2004; Nielsen JB et al., 2006). Studierne viser at den laveste Kp findes for det mest hydrofile stof (glyphosat), og Kp stiger med stigende lipofilicitet. Maksimal Kp er set for benzosyre (1000 gange højere end Glyphosat). Forskellen i Pow er mere end 3000. Der ses en klar relation mellem logKp og logPow for logPow værdier under 2 (figur 6). Dette stemmer overens med tidligere studier, som beskriver en optimal penetration gennem huden for stoffer med en logPow omkring 2 (Morgan et al., 2003; Cross et al., 2003).
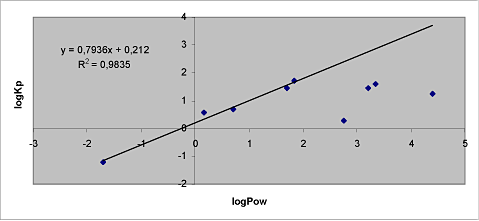
Figur 6. Korrelationen mellem logPow og logKp for de 9 stoffer testet af Nielsen et al. Linjen er baseret på kemikalier med logPow under 2.
Den mest effektive absorption får man ved at kombinere en hurtig penetrationshastighed (høj Kp) med en kort lag-time.
Mængden af stof fundet i huden er også vigtig, da denne mængde muligvis optages over tid. Hvis et stof foretrækker huden frem for receptorvæsken, er en større koncentrationsgradient nødvendig, for at stoffet kan optages i receptorvæsken, og hvis denne gradient ikke foreligger, opstår der et reservoir. Lag-time bliver herved også påvirket af et reservoir i huden samt af afstanden stoffet skal penetrere, altså hudens tykkelse, ligesom den også påvirkes af stoffets størrelse. Figur 7 viser hvordan lag-time er associeret med stoffets opløselighed. En kort lag-time kan forventes af stoffer med en vandopløselighed mellem 3g/L - 20g/L.
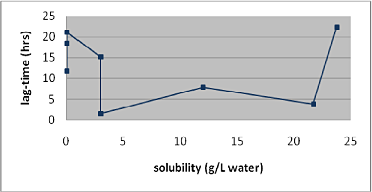
Figur 7: Association mellem opløselighed i vand og lag-time.
Ved risikovurdering efter hudeksponering bruges ofte alene flux eller relativ absorption. Det er dog ikke alene nok for at kunne evaluere et stofs toksiske profil efter hud eksponering, da det viser sig, at eksponering til to stoffer med forskellig maksimal penetrationshastighed (og derfor også forskellig Kp) kan medføre identiske penetrerede stofmængder, hvis deres lag-time også er forskellige (figur 2).
Der er en klar relation mellem den molekylvægten og lag-time for de fleste stoffer (figur 8) – eksemplificeret ved at lag-time stiger med stigende molekylvægt i de fleste stoffer testet af Nielsen et al. (Nielsen JB et al., 2006). Både dimethoat og malathion burde ud fra deres opløseligheder og molekylevægte udvise andre penetrationsegenskaber end, hvad tilfældet er (figur 8). Der findes ingen simpel forklaring for dette, men observationen tydeliggør vanskeligheden ved anvendelse af generaliserende matematiske modeller for penetrationskarakteristika.

Figur 8: Relationen mellem molekylær vægt og lag-time for 9 modelstoffer. Der er to stoffer, der afviger fra den generelle sammenhæng: Malathion (nederst) og dimethoat (øverst) er markedet med stjerne.
6.1 Eksponering i relation til erhvervsrisikovurdering
For at imitere en realistisk erhvervseksponering har Nielsen et al. udført penetrationsstudier, som forløb over 6 timer (Nielsen et al., 2004). En vigtig observation var, at den dermale penetration fortsætter længe efter eksponeringen er slut grundet midlertidig deponering i huden. Derfor vil den egentlige mængde stof, som optages, være underestimeret, såfremt denne vurderes ud fra for eksempel en blodprøve taget efter endt arbejdsdag/eksponering. Dette er væsentligt i relation til overvejelser omkring eksponeringsvurdering baseret på biologisk monitering.
7 Hjælpestoffers effekt på hudintegriteten og hudpenetrationen
7.1 Hjælpestoffer
Hjælpestoffer herunder detergenter tilhører en stor gruppe kemikalier, som karakteriseres ved deres evne til at reducere overfladespændingen i hydrofile opløsninger. De gør det muligt for lipofile og hydrofile stoffer at blande sig og lader hydrofile stoffer penetrere lipofile membraner – på den måde kan de i pesticider øge disses absorption i fx planter. Studier har vist, at hjælpestoffer også i sig selv kan have en skadelig effekt på hudens integritet og på den måde også potentielt øge absorptionen af pesticider i mennesker. Brugen af specifikke hjælpestoffer i pesticider afhænger ofte alene af tekniske karakteristika, men stoffer med identiske tekniske kvaliteter kan have forskellige toksiske karakteristika. Det betyder, at valg af hjælpestoffer også har indflydelse på det formulerede salgsprodukts toksikologiske egenskaber. Der er dog ikke fundet overbevisende publikationer, der viser nogen simpel og direkte sammenhæng mellem evnen til at reducere overfladespændingen og evnen til at skade hudoverfladen.
Flere studier har vist, at der til en risikovurdering hører en evaluering, ikke kun af det aktive pesticid, men også salgsproduktet, der ofte er tilsat hjælpestoffer og derfor har ændrede penetrations-karakteristika (fx lag-time) (Baynes & Riviere, 1998; Baynes et al., 2002; Nielsen JB, 2004). Godkendelse af produkter og anbefalinger i forhold til beskyttelsesudstyr er ofte baseret på data fra studier, der alene har undersøgt penetrationskarakteristika for det aktive stof og ikke salgsproduktet. Disse data kan derfor være misvisende og give forkerte indtryk af den absorberede mængde stof, en arbejder udsættes for dagligt. Denne viden er implementeret i forhold til fx Miljøstyrelsens godkendelsesprocedurer, der foreskriver test ikke alene af aktivstof, men også af salgsprodukt. Der er imidlertid ikke samme afklaring i forbindelse med udskiftning af hjælpestoffer i allerede godkendte produkter.
Under arbejdet med pesticider sker det ofte at flere produkter blandes sammen, når de fyldes på sprøjten, for at reducere antallet af arbejdsgange. Nogle produkter har vist sig at øge penetrationen af andre produkter ikke kun på det ønskede område nemlig planter eller skadedyr, men også gennem den humane hud (Nielsen JB, 2004), lige som også lag-time kan nedsættes (Griffin et al., 2000; Brand & Mueller, 2002)
Det har også vist sig, at cremer, som huden behandles med inden eksponeringen for pesticiderne, kan ændre hudens barriereegenskaber. Et studie har således vist, at 3 ud af 4 fugtighedscremer enten øgede penetrationen af et bestemt bekæmpelsesmiddel eller nedsatte lag-time (Brand et al., 2007). Det nuværende vidensgrundlag tillader endnu ingen generelle udmeldinger i forhold til vejledninger omkring anvendelse af cremer idet disse cremer også virker beskyttende i forhold til anden beskadigelse af hudens integritet (barriereegenskaber). Ovenstående er vigtig information for såvel brugere af pesticider fx arbejdere i drivhuse, landmænd eller haveejere, som for rådgivere der med den viden kan vurdere forholdsregler og eventuel anvendelse af handsker og andre personlige værnemidler.
8 Penetration af pesticider gennem beskadiget hud
Jo mere vi ved om den ideelle tilstand, desto vigtigere bliver vores viden om den knap så ideelle tilstand. Hovedparten af de studier, hvor der er lavet undersøgelser omkring hudpenetration, er lavet på rask, ubeskadiget hud. I det virkelige liv er hudens tilstand dog knap så ideel, som den der oftest bruges i forsøg (Kezic & Nielsen JB, 2008). Det er derfor relevant at studere, hvilken effekt beskadiget hud har på forskellige stoffers penetrationskarakteristika.
8.1 Arbejdsrelaterede hudproblemer
Hudproblemer er i mange lande blandt de hyppigste grunde til fravær fra arbejde i udsatte erhverv (Elsner, 2007; Korinth et al., 2007b; Suuronen et al., 2007). En dansk undersøgelse af hospitalsansatte viste, at ca. 23 % af de ansatte rapporterede problemer med håndeksem inden for de seneste 12 måneder (Flyvholm et al., 2007). I forhold til gartnerierhvervet, så optræder håndeksem (såvel allergisk som toksisk) med større hyppighed i end i den almindelige befolkning.
De ovennævnte undersøgelser beskriver problemets omfang i højrisiko-erhverv, hvor huden er eksponeret for opløsningsmidler, vand og detergenter. Påvirket hudbarriere pga. gentagende vådt arbejde, småskader, hudirritation, eksem mm. har vist sig at øge den dermale penetration (Ilyin et al., 1975; Bronaugh & Stewart, 1985b; Scott & Dugard, 1986; Grandjean P, 1990). Forskere inden for dette område har i årevis rådgivet arbejdere om, at en beskadiget hudbarriere kunne betyde en øget hudoptagelse af kemikalier (Grandjean P, 1990; Levang et al., 1999).
Flere studier indikerer, at en lettere beskadiget hud resulterer i en generel forøget penetrationshastighed for alle testede stoffer, at forøgelsen er marginal for de stoffer, der allerede ved den intakte hud har gode penetrationsegenskaber, at forøgelsen er signifikant for de mere lipofile stoffer, men at den klart største effekt observeres ved eksponering for hydrofile stoffer (Nielsen, 2005; Nielsen JB et al., 2006; Nielsen et al., 2007).
En anden væsentlig pointe er, at hos atopikere og andre med hudlidelser der varierer i intensitet, er hudens barriereegenskaber nedsatte selv når huden er uden eksematøse forandringer og ser normal og ubeskadiget ud (Kezic & Nielsen JB, 2008). Det betyder at disse grupper er mere sårbare også i perioder uden synlige hudforandringer.
Denne viden omkring øget sårbarhed hos specifikke grupper samt den forøgede hudpenetration gennem lettere beskadiget hud er vanskelig at håndtere regulatorisk med mindre man forebyggelsesstrategisk søger at sikre denne store og mere sårbare gruppe. Indtil da bør denne viden få klare implikationer for den generelle såvel som den individorienterede rådgivning af folk med potentiel hudeksponering og eksisterende hudlidelser og/eller lettere beskadiget hud.
9 Afvaskning af huden og midlertidig huddeponering
Reservoireffekten har tidligere været beskrevet og defineres ved at et stof forbliver og ophobes i huden i stedet for at passere direkte gennem til blodstrømmen. Huden vil derefter afgive stoffer til blodstrømmen med en hvis forsinkelse og med en stadig faldende hastighed (Cnubben et al., 2002). En anden mulighed er, at den del af stoffet bliver i det øverste hudlag og kan vaskes af ved håndvask.
Fjernelse af deponeret stof gennem afvaskning er undersøgt i forsøg, hvor man efter 6 timers eksponering har foretaget en reel afvaskning af huden med en svag sæbeopløsning. Da mange stoffer har lag-times under 6 timer, vil disse være trængt ind i huden i løbet af den tid. Resultaterne viser entydigt, at en afvaskning efter 6 timer fjerner den altovervejende del af den administrerede mængde teststof og derved nedsætter muligheden for senere huddeponering, således at man ved forsøgsafslutning ser en signifikant reduceret huddeponering i de grupper, hvor der er gennemført afvaskning efter 6 timer. Samlet kan det konkluderes, at en afvaskning efter endt eksponering signifikant nedsætter den samlede absorption af modelstofferne. For de mest vandopløselige stoffer er denne reduktion omkring 67 % og for de mere lipofile modelstoffer lidt mindre (Nielsen JB et al., 2006). Det er ligeledes muligt ved almindelig let afvaskning at fjerne en del af den stofmængde, der er trængt ind i huden. Denne observation har klare forebyggelsesmæssige implikationer og dokumenterer betydningen af håndvask med vand og sæbe efter hudkontakt til pesticider.
Den nuværende regelsætning omkring vurdering af penetrationsforsøg følger gældende OECD guidelines, der foreskriver at man skal henregne alt stof, der ikke er genfundet i donordelen som absorberet og dermed potentielt tilgængeligt for systemisk toksicitet. Dette gælder således også den fraktion af den administrerede dosis, der er ophobet i huden. Undersøgelsen viser, at absorption fra huden og ud i receptordelen fortsætter efter endt eksponering (Nielsen JB et al., 2006). For visse stoffer fortsætter absorptionen i over et døgn efter endt eksponering (Nielsen JB et al., 2006). Der er derfor ingen tvivl om, at en vis del af den i huden deponerede mængde modelstof senere vil absorberes. Det er imidlertid uafklaret, hvor stor en fraktion af den i huden midlertidigt deponerede mængde modelstof, der vil fjernes uden at nå systemisk cirkulation, det vil sige ovenud af huden, men omfanget må forventes at afhænge af blandt andet håndvask, andre aktiviteter samt hudens almene tilstand.
10 Forebyggelse af dermal absorption ved brug af personlige værnemidler
- 10.1 Personlige værnemidler
- 10.2 Typer af handsker og penetration af pesticider
- 10.3 Brug og genbrug af handsker
- 10.4 Genbrugshandsker
Målet ved at bruge handsker og andre værnemidler er at ændre en uacceptabel eksponering til en acceptabel risiko. Risiko er defineret som sandsynligheden for, at en person eller miljøet skades ved en speciel proces. Et bekæmpelsesmiddels potentiale for at udøve skadelig effekt kan ikke ændres, men risikoen ved håndtering af stoffet kan nedsættes ved at bruge de rigtige værnemidler på korrekt vis.
Eksponering for pesticider sker gennem arbejdet med planter, frugter, blomster mm. Graden af eksponering afhænger af flere ting og kan ske i produktion, ved blanding, distribution, re-entry aktivitet eller i ved udbringning af stoffet. Studier har vist at landmænd, der arbejder med udtynding af afgrøder, er specielt udsat for eksponering i forhold til dem, der fx høster (de Cock et al., 1998b; de Cock et al., 1998a; Simcox et al., 1999). Selv i husstøvet hos disse arbejdere samt i disses børns urin er der fundet højere koncentrationer bekæmpelsesmidler end hos andre ueksponerede (Coronado et al., 2004; Coronado et al., 2006). Sidstnævnte illustrerer at optagelse sker uden egen deltagelse i udbringning og i visse tilfælde kan eksponering optræde fjernt fra udbringningsstedet.
10.1 Personlige værnemidler
Det vigtigste, når man potentielt kan komme i kontakt med pesticider, hvad enten det er under blanding, distribution, eller når man arbejder med afgrøderne efter behandling med pesticider, er at bruge personlige værnemidler – handsker især.
Handsker nedsætter signifikant hudoptagelsen af pesticider, men gennembrudstiden såvel som den hastighed hvormed pesticiderne passerer handsken er forskellig og nogle handsker er bedre end andre til specifikke stoffer.
Et stort problem, som også kan have indflydelse på valget og brugen af handsker er ubehag fra handsken. Ofte er de mest behagelige handsker måske ikke resistente nok over for de stoffer, der arbejdes med, eller de optimale handsker er for dyre i forhold til mindre gode handsker.
Grundene til, handsker ofte ikke giver en effektiv beskyttelse, kan være betinget af forkert brug, beskadiget handske, eller kemisk nedbrydning af handskematerialet. I mange situationer vil det være en kombination af disse 3 årsager der gør, at brugeren eksponeres til uden måske at være klar over det (Packham, 2006).
Gennembrudstiden vil ikke nødvendigvis sige noget om mængden af bekæmpelsesmiddel, som bryder gennem handsken, eller penetrationsraten efter eksponering, men det er stadig en vigtig parameter, da to typer handsker kan have identisk penetration efter 6 timer, men meget forskellig gennembrudstid og penetrationsrate (Figur 9).
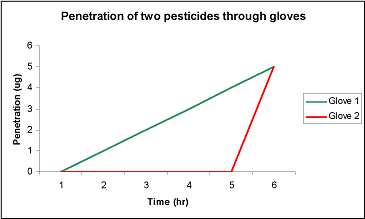
Figur 9: Penetration af to typer af pesticider (1 and 2) gennem handsker. Penetration af 1 og 2 er identisk, men gennembrudstiden og penetrationsraten er forskellig (Nielsen JB, 2005).
Vigtigt i brugen af engangshandsker er:
- Viden om, hvornår handskerne skal skiftes for at undgå at overskride gennembrudstiden.
- Viden om at engangshandsker er engangshandsker og ikke må genbruges.
- Viden om, at handskernes barriere kan forringes ved håndens bevægelse i handsken idet handskematerialet bøjes og strækkes under brug (Phalen & Hee, 2008).
10.2 Typer af handsker og penetration af pesticider
Data fra forskellige studier omhandlende penetration af pesticider gennem forskellige typer handsker har vist en variation i penetrationskarakteristika selv inden for den samme gruppe pesticider. Generelt er nitril handsker, butyl gummihandsker og SilverShield handsker de mest resistente (Guo et al., 2002; Kirknel E & Sjelborg P, 2003). Der er dog ingen garanti for beskyttelse over for alle de testede pesticider inden for én type handsker.
Latex/naturgummihandsker bør ikke bruges ved længerevarende arbejde med pesticider, hvis der findes alternativer, og slet ikke ved håndtering af salgsopløsninger. Ved korttidseksponering (< 2 timer) til brugsopløsninger af pesticider vil latexhandsker på baggrund af den nuværende viden yde en tilnærmelsesvis lige så god beskyttelse som nitrilhandsker.
10.3 Brug og genbrug af handsker
Når man genbruger handsker som værnemiddel mod pesticider, er det vigtigt, at man kender til den rette måde at opbevare dem på før og efter brug. Som de fleste ved af erfaring, ændres handskers struktur/integritet over tid (Raheel & Dai, 2002). Men der er ikke mange, der har sat sig ind i, hvordan penetrationskarakteristika ændrer sig. Ofte er opbevaringsinformationen slet ikke tilgængelig for brugerne af handskerne. Som udgangspunkt kan genbrug ikke anbefales medmindre handskerne er lavet med det formål (se nedenfor).
10.4 Genbrugshandsker
Genbrugshandsker bruges ofte i arbejdet med pesticider. Det kan betyde en øget risiko for sekundær eksponering. I forsøget på at rengøre handskerne kan handskematerialet ødelægges og integriteten ændres (Gao et al., 2005). Noget materiale kan slet ikke rengøres, ligesom der ofte findes bekæmpelsesmiddel på indersiden af handsken efter rengøring (Guo et al., 2002). Det er påvist, at en stor mængde af det bekæmpelsesmiddel, en arbejder udsættes for, sker i forbindelse med handskeskifte (Garrod et al., 2001; Kirknel E & Sjelborg P, 2003; Edwards et al., 2007), ligesom handsken kan være ligeså forurenet på indersiden som på ydersiden (Creely & Cherrie, 2001; Garrod et al., 2001; Machera et al., 2003).
Endelig viser helt nye resultater fra eget laboratorium, at visse pesticider ophobes i handskematerialet. Såfremt en del af genbrugshandskers beskyttelsesevne ligger i at pesticidet bindes til handskematerialet, vil der muligvis alene være tale om en midlertidig beskyttelse. Når handskematerialets bindingskapacitet overskrides vil beskyttelsesgraden i givet fald mindskes markant. Denne problemstilling er ny, og bør belyses nærmere, især da genbrugshandsker oftest anvendes i forbindelse med håndtering af koncentrerede salgsopløsninger.
Hvis hænderne forurenes inden i handskens tillukkede miljø, forekommer der en øget risiko for penetration af stoffet gennem huden (Wester & Maibach, 1983).
Da den interindividuelle variation ved denne form for eksponering kan være udtalt og i betydelig grad afhængig af relevant personlig hygiejne, er det vigtigt, at handskebrugerne er klar over deres risiko og bliver undervist for at undgå unødig eksponering.
Det har også vist sig, at engangshandsker ofte genbruges. Når en arbejder tror, han/hun er beskyttet af handskerne mod eksponering, er situationen faktisk værre, end når en arbejder helt undlader at bruge handsker, men er bevidst om sine risici.
Med udgangspunkt i de ovennævnte problemer er vigtige elementer i forebyggelsesstrategien at reducere eksponeringen ved at undervise, træne og supervisere arbejderne i brugen af værnemidler. Hvis problemet med genbrug af handsker (engangs- såvel som flergangshandsker) ikke udforskes yderligere, er rådet at bruge engangshandsker 1 gang og derefter smide dem væk.
11 Konklusioner og perspektiver
11.1 Regulatoriske aspekter
- Viden om dermal penetration kan opnås ved såvel in vitro som in vivo eksperimenter samt på basis af undersøgelser af mennesker under og efter eksponering. Kvantitative forskelle er forventelige og primært betinget af den naturlige forskellighed, der eksisterer mellem mennesker – og dermed også mellem donorer til in vitro forsøg.
- Resultater baseret på in vitro metoder udført i henhold til OECD guidelines på human hud svarer udmærket overens med in vivo erfaringer fra mennesker. Kvalitativt er der således gentagne gange vist god overensstemmelse mellem in vitro og in vivo.
- Normalt vil in vitro forsøg udført på human hud efter OECD guidelines være mere prædiktive end klassiske studier i mus eller rotter.
- Evaluering af dermal absorption og lokal såvel som systemisk toksicitet fra stoffer som man ved metaboliseres i huden kræver særlig opmærksomhed.
- Den nuværende regelsætning omkring vurdering af penetrationsforsøg følger gældende OECD guidelines, der foreskriver, at man skal henregne alt stof, der ikke er genfundet i donordelen som absorberet og dermed potentielt tilgængeligt for systemisk toksicitet. Dette gælder således også den fraktion af den administrerede dosis, der er ophobet i huden. Undersøgelser viser, at absorption fra huden og ud i receptordelen fortsætter efter endt eksponering - for visse stoffer fortsætter absorptionen i over et døgn efter endt eksponering. Det er uafklaret, hvor stor en fraktion af den i huden midlertidigt deponerede mængde stof der vil fjernes uden at nå systemisk cirkulation, det vil sige ovenud af huden.
- For lipofile stoffer vil den nuværende regelsætning for dermal absorption i en vis grad overestimere den reelle absorberbare mængde fremmedstof. Overestimatet er dog ikke voldsomt stort for de lipofile stoffers vedkommende, og den hidtil anvendte regulering synes pragmatisk anvendelig.
- For de mere vandopløselige stoffer er data endnu ikke tilstrækkelige for valide tolkninger.
- Den fortsatte absorption efter endt eksponering betyder, at blod- eller urinprøver opsamlet umiddelbart efter endt eksponering potentielt vil undervurdere pesticidbelastningen.
- Hudabsorption afhænger i høj grad af stoffernes opløselighed (fx udtrykt ved logPow) og størrelse (fx udtrykt ved molvægt). Der er udviklet matematiske modeller for hudabsorption baseret på data fra mere end 100 kemiske stoffer.
- For stoffer med logPow værdier mellem -2 og 2, synes der at være en positiv korrelation mellem logPow og Kp (et udtryk for penetrationshastigheden).
- Såfremt et stof ikke indeholder specielle kemiske substituenter/grupper eller har affinitet for proteinbinding i huden, vil disse modeller indenfor et forholdsvist bredt opløselighedsinterval give en udmærket indikation for en forventet dermal penetration.
- Anvendelse af matematiske modeller i regulatorisk øjemed kræver betydelig faglig indsigt og erfaring idet adskillige studier har vist at en del enkeltstoffer af umiddelbart uforklarlige grunde ikke opfører sig som forventet efter de givne modeller.
- Det kan på basis af flere studier konkluderes, at en afvaskning af huden efter endt eksponering signifikant nedsætter den samlede dermale absorption. Effekten er størst for de mest vandopløselige stoffer, hvor absorptionen kan nedsættes til en tredjedel.
- Der er således solid evidens for at god hygiejne såsom håndvask efter kontakt til sprøjtede overflader reducerer absorption af pesticider.
- Denne viden har klare forebyggelsesmæssige perspektiver og vil med fordel kunne anvendes i forbindelse med oplæring og instruktion omkring håndtering og af sprøjtemidler og kontakt med sprøjtede overflader.
- En lettere beskadiget hud resulterer i en generel forøget penetrationshastighed for alle stoffer.
- En kraftigt forøgede penetration gennem lettere beskadiget hud ses specielt for de mere vandopløselige stoffer.
- Man bør reguleringsmæssigt forholde sig til, at en stor del af ansatte med dermal eksponering og ikke-intakt hud absorberer ganske meget mere gennem huden end traditionelle in vitro-guideline-forsøg indikerer.
- Man må her være opmærksom på, at det ikke alene drejer sig om personer med rifter eller lignende på huden, men også har relevans for den store del af befolkningen med mere eller mindre kroniske hudproblemer af varierende intensitet.
- Handsker har vist sig at nedsætte eksponering og efterfølgende absorption af pesticider, men gennembrudstiden er forskellig og nogle handsker er bedre end andre til specifikke stoffer.
- Ved korttidseksponering (< 2 timer) til brugsopløsninger af pesticider vil latexhandsker på baggrund af den nuværende viden yde en tilnærmelsesvis lige så god beskyttelse som nitrilhandsker.
- Genbrug af engangshandsker bør undgås.
- Anvendelse af handsker beregnet til gentagen brug kræver betydelig opmærksomhed omkring oplæring og personlig hygiejne.
- Penetration gennem handsker og hud afhænger af mængde såvel som koncentration af pesticid. Undersøgelser viser at pesticider kan ophobes i handskemateriale.
- Ved udsættelse for salgsopløsninger af pesticider (typisk høje koncentrationer) er beskyttelsesgraden fra engangshandsker af såvel latex som nitril stærkt reduceret, hvorfor andet/kraftigere handskemateriale må tilrådes.
- Såfremt der sker ophobning af pesticid i handskematerialet vil det kunne reducere genanvendeligheden af handskerne betydeligt.
11.2 Forskningsaspekter
- Der er behov for undersøgelse af reservoireffekten i relation til stoffets opløselighed og molekylvægt.
- Der er behov for en grundig analyse af, hvor stor en mængde stof der forbliver i huden efter endt eksponering.
- Der er behov for en kvantificering af hvor stor en mængde stof der penetrerer til den systemiske cirkulation efter eksponeringen.
- Der er behov for en vurdering af hvilken fraktion der kan fjernes ved afvaskning.
- Det er påvist, at man foruden at undersøge hudabsorptionen af det aktive stof i et bekæmpelsesmiddel også må rette fokus mod salgsproduktet, som ofte indeholder div. detergenter og hjælpestoffer, som vides at påvirke lag-time og penetrationsrate.
- Det er væsentligt at man fortsætter forskning omkring effekt af detergenter og andre hjælpestoffer på absorption af aktivstoffer.
- Man bør ved reevaluering af allerede godkendte produkter anerkende, at evidensen for den ofte brugte ekstrapolering mellem produkter ikke nødvendigvis er tilstrækkelig i risikovurderingen af produktet, hvorfor en vidensopbygning på dette område er nødvendig.
- Pesticider bruges ofte i kombination, hvilket kan bevirke stigende eller faldende penetrationsrate afhængig af produkt.
- Undersøgelser af kombinationseffekter bør derfor vises fortsat opmærksomhed.
- Nyere resultater der viser en betydelig ophobning af pesticid i handskemateriale har potentielt klare implikationer for gentagen anvendelse af handsker. Hvorvidt og hvilket omfang det ophobede pesticid senere kan frigives og efterfølgende absorberes er ikke kendt.
- Forskning på dette område bør klart prioriteres idet det typisk drejer sig om eksponering til koncentrerede salgsopløsninger med en koncentration af pesticid flere størrelsesordner over brugsopløsningerne, og en situation hvor brugerne måske fejlagtigt tror sig velbeskyttede.
Referencer
Alberti I, Kalia YN, Naik A, Bonny J, & Guy RH (2001). Effect of ethanol and isopropyl myristate on the availability of topical terbinafine in human stratum corneum, in vivo. Int J Pharm 219, 11-19.
Archibald BA, Solomon KR, & Stephenson GR (1994). Estimating pirimicarb exposure to greenhouse workers using video imaging. Arch Environ Contam Toxicol 27, 126-129.
Baynes RE, Brooks JD, Mumtaz M, & Riviere JE (2002). Effect of chemical interactions in pentachlorophenol mixtures on skin and membrane transport. Toxicol Sci 69, 295-305.
Baynes RE & Riviere JE (1998). Influence of inert ingredients in pesticide formulations on dermal absorption of carbaryl. American Journal of Veterinary Research 59, 168-175.
Benfeldt E, Hansen SH, Volund A, Menne T, & Shah VP (2007). Bioequivalence of topical formulations in humans: evaluation by dermal microdialysis sampling and the dermatopharmacokinetic method. J Invest Dermatol 127, 170-178.
Benfeldt E & Serup J (1999). Effect of barrier perturbation on cutaneous penetration of salicylic acid in hairless rats: in vivo pharmacokinetics using microdialysis and non-invasive quantification of barrier function. Arch Dermatol Res 291, 517-526.
Benford DJ, Cocker J, Sartorelli P, Schneider T, van HJ, & Firth JG (1999). Dermal route in systemic exposure. Scand J Work Environ Health 25, 511-520.
Brand RM, Charron AR, Sandler VL, & Jendrzejewski JL (2007). Moisturizing lotions can increase transdermal absorption of the herbicide 2,4-dichlorophenoxacetic acid across hairless mouse skin. Cutan Ocul Toxicol 26, 15-23.
Brand RM & Mueller C (2002). Transdermal penetration of atrazine, alachlor, and trifluralin: effect of formulation. Toxicol Sci 68, 18-23.
Bronaugh RL & Stewart RF (1985a). Methods for in vitro percutaneous absorption studies IV: The flow-through diffusion cell. J Pharm Sci 74, 64-67.
Bronaugh RL & Stewart RF (1985b). Methods for in vitro percutaneous absorption studies V: Permeation through damaged skin. J Pharm Sci 74, 1062-1066.
Chaurasia CS, Muller M, Bashaw ED, Benfeldt E, Bolinder J, Bullock R, Bungay PM, DeLange EC, Derendorf H, Elmquist WF, Hammarlund-Udenaes M, Joukhadar C, Kellogg DL, Jr., Lunte CE, Nordstrom CH, Rollema H, Sawchuk RJ, Cheung BW, Shah VP, Stahle L, Ungerstedt U, Welty DF, & Yeo H (2007). AAPS-FDA workshop white paper: microdialysis principles, application and regulatory perspectives. Pharm Res 24, 1014-1025.
Clark NWE (1992). Cutaneous xenobiotic metabolism and its role in percutaneous absorption, pp. 56-77.
Cnubben NH, Elliott GR, Hakkert BC, Meuling WJ, & van de Sandt JJ (2002). Comparative in vitro-in vivo percutaneous penetration of the fungicide ortho-phenylphenol. Regul Toxicol Pharmacol 35, 198-208.
Coronado GD, Thompson B, Strong L, Griffith WC, & Islas I (2004). Agricultural task and exposure to organophosphate pesticides among farmworkers. Environmental Health Perspectives 112, 142-147.
Coronado GD, Vigoren EM, Thompson B, Griffith WC, & Faustman EM (2006). Organophosphate pesticide exposure and work in pome fruit: Evidence for the take-home pesticide pathway. Environmental Health Perspectives 114, 999-1006.
Creely KS & Cherrie JW (2001). A novel method of assessing the effectiveness of protective gloves--results from a pilot study. Ann Occup Hyg 45, 137-143.
Cross SE, Magnusson BM, Winckle G, Anissimov Y, & Roberts MS (2003). Determination of the effect of lipophilicity on the in vitro permeability and tissue reservoir characteristics of topically applied solutes in human skin layers. J Invest Dermatol 120, 759-764.
de Cock J, Heederik D, Kromhout H, Boleij JSM, Hoek F, Wegh H, & Ny ET (1998a). Determinants of exposure to captan in fruit growing. American Industrial Hygiene Association Journal 59, 166-172.
de Cock J, Heederik D, Kromhout H, Boleij JSM, Hoek F, Wegh H, & Ny ET (1998b). Exposure to captan in fruit growing. American Industrial Hygiene Association Journal 59, 158-165.
Denyer S.P, Guy RH, Hadgraft J, & Hugo W.B (1985). The microbial degradation of topically applied drugs. Int J Pharm 26, 89-97.
Dias M, Naik A, Guy RH, Hadgraft J, & Lane ME (2008). In vivo infrared spectroscopy studies of alkanol effects on human skin. Eur J Pharm Biopharm69, 1171-1175.
ECETOC. ECETOC 1993 Percutaneous abosrption. 20, 1-80. 1993. Brussels, European Centre for Ecotoxicology and Toxicology of Chemicals.
Edwards JW, Lee SG, Heath LM, & Pisaniello DL (2007). Worker exposure and a risk assessment of Malathion and Fenthion used in the control of Mediterranean fruit fly in South Australia. Environmental Research 103, 38-45.
Elias PM (1983). Epidermal lipids, barrier function, and desquamation. J Invest Dermatol 80 Suppl, 44s-49s.
Elsner P (2007). Skin protection in the prevention of skin diseases. Curr Probl Dermatol 34, 1-10.
Feldmann RJ & Maibach HI (1967). Regional variation in percutaneous penetration of 14C cortisol in man. J Invest Dermatol 48, 181-183.
Fernandez C, Nielloud F, Fortune R, Vian L, & Marti-Mestres G (2002). Benzophenone-3: rapid prediction and evaluation using non-invasive methods of in vivo human penetration. J Pharm Biomed Anal 28, 57-63.
Flyvholm MA, Bach B, Rose M, & Jepsen KF (2007). Self-reported hand eczema in a hospital population. Contact Dermatitis 57, 110-115.
Gao P, El-Ayouby N, & Wassell JT (2005). Change in permeation parameters and the decontamination efficacy of three chemical protective gloves after repeated exposures to solvents and thermal decontaminations. Am J Ind Med 47, 131-143.
Garrod AN, Phillips AM, & Pemberton JA (2001). Potential exposure of hands inside protective gloves-a summary of data from non-agricultural pesticide surveys. Ann Occup Hyg 45, 55-60.
Grandjean P (1990). Skin Penetration - Hazardous Chemicals at Work Taylor and Francis.
Griffin P, Payne M, Mason H, Freedlander E, Curran AD, & Cocker J (2000). The in vitro percutaneous penetration of chlorpyrifos. Hum Exp Toxicol 19, 104-107.
Groth L (1996). Cutaneous microdialysis. Methodology and validation. Acta Derm Venereol Suppl (Stockh) 197, 1-61.
Guo C, Stone J, Stahr HM, & Shelley M (2002). Cleanup of gloves contaminated with granular terbufos and tefluthrin. Arch Environ Contam Toxicol 42, 383-388.
Guy RH, Hadgraft J, & Bucks DA (1987). Transdermal drug delivery and cutaneous metabolism. Xenobiotica 17, 325-343.
Hueber-Becker F, Nohynek GJ, Dufour EK, Meuling WJA, De Bie ATHJ, Toutain H, & Bolt HM (2007). Occupational exposure of hairdressers to [C-14]-para-phenylenediamine-containing oxidative hair dyes: A mass balance study. Food and Chemical Toxicology 45, 160-169.
Ilyin LA, Ivannikov AT, Parfenov YD, & Stolyarov VP (1975). Strontium absorption through damaged and undamaged human skin. Health Phys 29, 75-80.
Imokawa G, Abe A, Jin K, Higaki Y, Kawashima M, & Hidano A (1991). Decreased level of ceramides in stratum corneum of atopic dermatitis: an etiologic factor in atopic dry skin? J Invest Dermatol 96, 523-526.
Jacobi U, Weigmann HJ, Baumann M, Reiche AI, Sterry W, & Lademann J (2004). Lateral spreading of topically applied UV filter substances investigated by tape stripping. Skin Pharmacol Physiol 17, 17-22.
Kao J, Hall J, & Helman G (1988). In vitro percutaneous absorption in mouse skin: influence of skin appendages. Toxicol Appl Pharmacol 94, 93-103.
Kezic S, Kemperman PM, Koster ES, de Jongh CM, Thio HB, Campbell LE, Irvine AD, McLean IW, Puppels GJ, & Caspers PJ (2008). Loss-of-Function Mutations in the Filaggrin Gene Lead to Reduced Level of Natural Moisturizing Factor in the Stratum Corneum. J Invest Dermatol,128, 2117-2119.
Kezic S, Monster AC, van dG, I, Kruse J, Opdam JJ, & Verberk MM (2001). Dermal absorption of neat liquid solvents on brief exposures in volunteers. AIHAJ 62, 12-18.
Kezic S & Nielsen JB (2008). Absorption of chemicals through compromised skin. International Archives of Occupational and Environmental Health, in press.
Kirknel E & Sjelborg P. Handskers beskyttelsesevne ved arbejde med pesticider i jordbrugene, samt modeller for håndeksponering. 73. 2003. Danish Environment Protection Agency, Copenhagen, Denmark.
Korinth G, Goen T, Schaller KH, & Drexler H (2007a). Discrepancies between different rat models for the assessment of percutaneous penetration of hazardous substances. Archives of Toxicology 81, 833-840.
Korinth G, Weiss T, Penkert S, Schaller KH, Angerer J, & Drexler H (2007b). Percutaneous absorption of aromatic amines in rubber industry workers: impact of impaired skin and skin barrier creams. Occup Environ Med 64, 366-372.
Lammers JHCM, Meuling WJ, Muijser H, Freidig AP, & Bessems JGM (2005). Neurobehavioural evaluation and kinetics of inhalation of constant or fluctuating toluene concentrations in human volunteers. Environ Toxicol Pharmacol 20, 431-442.
Lboutounne H, Chaulet JF, Ploton C, Falson F, & Pirot F (2002). Sustained ex vivo skin antiseptic activity of chlorhexidine in poly(epsilon-caprolactone) nanocapsule encapsulated form and as a digluconate. J Control Release 82, 319-334.
Levang AK, Zhao K, & Singh J (1999). Effect of ethanol/propylene glycol on the in vitro percutaneous absorption of aspirin, biophysical changes and macroscopic barrier properties of the skin. Int J Pharm 181, 255-263.
Liu KH & Kim JH (2003). In vitro dermal penetration study of carbofuran, carbosulfan, and furathiocarb. Arch Toxicol 77, 255-260.
Liu KH, Sung HJ, Lee HK, Song BH, Ihm YB, Kim K, Lee HS, & Kim JH (2002). Dermal pharmacokinetics of the insecticide furathiocarb in rats. Pest Manag Sci 58, 57-62.
Machera K, Goumenou M, Kapetanakis E, Kalamarakis A, & Glass CR (2003). Determination of potential dermal and inhalation operator exposure to malathion in greenhouses with the whole body dosimetry method. Annals of Occupational Hygiene 47, 61-70.
McDougal JN & Boeniger MF (2002). Methods for assessing risks of dermal exposures in the workplace. Critical Reviews in Toxicology 32, 291-327.
Michales AS, Chandrasekaran SK, & Shaw JE (1975). Drug permeation through human skin: Theory and in vitro experimental measurement. AIChE Journal 21, 985-996.
Miljøstyrelsen. Bekæmpelsesmiddelstatistik 1997. 1998. Miljøstyrelsen, 221 Miljøstyrelsen. 6-1-2008.
Miljøstyrelsen. Bekæmpelsesmiddelstatistik 2006. Orientering fra Miljøstyrelsen Nr. 5 2007. 2007. Miljøstyrelsen. 6-1-2008.
Miller G (2004). Sustaining the Earth. pp. 211-216. Thompson Learning, Inc., Pacific Grove, CA.
Morgan CJ, Renwick AG, & Friedmann PS (2003). The role of stratum corneum and dermal microvascular perfusion in penetration and tissue levels of water-soluble drugs investigated by microdialysis. Br J Dermatol 148, 434-443.
Nielsen JB. Hudpenetration af pesticider - en undersøgelse af effekten af hjælpestoffer, kombinationseffekter, handsker, samt lettere beskadiget hud. [90], 1-62. 2004. Bekæmpelsesmiddelforskning fra Miljøstyrelsen, Miljøstyrelsen.
Nielsen JB (2005). The selection and use of gloves against pesticides. In Protective gloves for occupational use, eds. Boman A, Estlander T, Wahlberg JE, & Maibach HI, pp. 321-334. CRC Press.
Nielsen JB, Nielsen F, & Sørensen JA. Hudoptagelse af pesticider - betydning af lag-time og reservoir effekt. 2006. Miljøstyrelsen. Bekæmpelsesmiddelforskning fra Miljøstyrelsen.
Nielsen JB (2005). Percutaneous penetration through slightly damaged skin. Arch Dermatol Res 296, 560-567.
Nielsen JB & Nielsen F (2000). Dermal in vitro penetration of methiocarb, paclobutrazol, and pirimicarb. Occup Environ Med 57, 734-737.
Nielsen JB, Nielsen F, & Sorensen JA (2004). In vitro percutaneous penetration of five pesticides--effects of molecular weight and solubility characteristics. Ann Occup Hyg 48, 697-705.
Nielsen JB, Nielsen F, & Sorensen JA (2007). Defense against dermal exposures is only skin deep: significantly increased penetration through slightly damaged skin. Arch Dermatol Res 299, 423-431.
Nohynek GJ, Meuling WJ, Vaes WH, Lawrence RS, Shapiro S, Schulte S, Steiling W, Bausch J, Gerber E, Sasa H, & Nau H (2006). Repeated topical treatment, in contrast to single oral doses, with Vitamin A-containing preparations does not affect plasma concentrations of retinol, retinyl esters or retinoic acids in female subjects of child-bearing age. Toxicol Lett 163, 65-76.
OECD. OECD (2004a) Guidance document for the conduct of skin absorption studies. Paris. 28, 1-31. 2004.
Packham C (2006). Gloves as chemical protection - Can they really work? Annals of Occupational Hygiene 50, 545-548.
Palmer CN, Irvine AD, Terron-Kwiatkowski A, Zhao Y, Liao H, Lee SP, Goudie DR, Sandilands A, Campbell LE, Smith FJ, O'Regan GM, Watson RM, Cecil JE, Bale SJ, Compton JG, DiGiovanna JJ, Fleckman P, Lewis-Jones S, Arseculeratne G, Sergeant A, Munro CS, El HB, McElreavey K, Halkjaer LB, Bisgaard H, Mukhopadhyay S, & McLean WH (2006). Common loss-of-function variants of the epidermal barrier protein filaggrin are a major predisposing factor for atopic dermatitis. Nat Genet 38, 441-446.
Phalen R & Hee SQ (2008). A moving robotic hand system for whole-glove permeation and penetration: Captan and nitrile gloves. Journal of Occupational and Environmental Hygiene 5, 258-270.
Raheel M & Dai GX (2002). Viability of textile systems for hand and body protection: effects of chemical interaction, wear, and storage conditions. Bull Environ Contam Toxicol 69, 164-172.
Roberts MS, Cross SE, & Anissimov YG (2004). Factors affecting the formation of a skin reservoir for topically applied solutes. Skin Pharmacol Physiol 17, 3-16.
Rosado C & Rodrigues LM (2003). Solvent effects in permeation assessed in vivo by skin surface biopsy. BMC Dermatol 3, 5.
Roskos KV, Maibach HI, & Guy RH (1989). The effect of aging on percutaneous absorption in man. J Pharmacokinet Biopharm 17, 617-630.
Rougier A, Dupuis D, Lotte C, & Maibach HI (1999). Stripping method for measuring percutaneous absorption in vivo. In Percutaneous absorption: drugs-cosmetics-mechanisms-methodology pp. 375-393. Marcel Dekker, New York.
Roy SD & Flynn GL (1989). Transdermal delivery of narcotic analgesics: comparative permeabilities of narcotic analgesics through human cadaver skin. Pharm Res 6, 825-832.
Sarveiya V, Risk S, & Benson HA (2004). Liquid chromatographic assay for common sunscreen agents: application to in vivo assessment of skin penetration and systemic absorption in human volunteers. J Chromatogr B Analyt Technol Biomed Life Sci 803, 225-231.
Scott RC & Dugard PH (1986). A model for quantifying absorption through abnormal skin. J Invest Dermatol 86, 208-212.
Simcox NJ, Camp J, Kalman D, Stebbins A, Bellamy G, Lee IC, & Fenske R (1999). Farmworker exposure to organophosphorus pesticide residues during apple thinning in Central Washington State. American Industrial Hygiene Association Journal 60, 752-761.
Suuronen K, alto-Korte K, Piipari R, Tuomi T, & Jolanki R (2007). Occupational dermatitis and allergic respiratory diseases in Finnish metalworking machinists. Occupational Medicine-Oxford 57, 277-283.
Waller JM & Maibach HI (2006). Age and skin structure and function, a quantitative approach (II): protein, glycosaminoglycan, water, and lipid content and structure. Skin Res Technol 12, 145-154.
Walters KA & Roberts MS (1993). Veterinary applications of skin penetration enhancers. In Pharmaceutical skin penetration enhancement pp. 345-364. Marcel Dekker, New York.
Wester RC & Maibach HI (1983). Cutaneous pharmacokinetics: 10 steps to percutaneous absorption. Drug Metab Rev 14, 169-205.
Wissing SA & Muller RH (2002). Solid lipid nanoparticles as carrier for sunscreens: in vitro release and in vivo skin penetration. J Control Release 81, 225-233.
Yamamoto A, Serizawa S, Ito M, & Sato Y (1991). Stratum corneum lipid abnormalities in atopic dermatitis. Arch Dermatol Res 283, 219-223.
Version 1.0 Maj 2009 • © Miljøstyrelsen.